离子色谱法同时测定新鲜蔬菜中的三种阴离子
2021-05-18吴丹亚席杰君
吴丹亚,席杰君
(宁波市农业技术推广总站,浙江 宁波 315012)
氟化物、硝酸盐与亚硝酸盐是自然界中普遍存在的化合物。氟是人体必需的微量元素,但过量摄入也会对人体健康造成危害。硝酸盐在细菌的作用下能被还原成亚硝酸盐,过量的亚硝酸盐进入体内后,可与胺类物质生成强致癌物亚硝胺,严重危害人类健康。但随着工业的发展和化肥特别是含氮化肥的广泛使用,各种含氮化合物和氟化物进入土壤、水体和空气并富集于蔬菜中,使得蔬菜中的氟离子、硝酸盐与亚硝酸盐含量偏高。研究表明,蔬菜是一类极易富集硝酸盐的作物[1],这就更容易造成蔬菜中普遍存在不同程度的硝酸盐污染现象[2-3]。因此,对蔬菜中的这3种物质进行快速有效的检测具有重要意义。
目前蔬菜中硝酸盐和亚硝酸盐的测定方法有离子色谱法和分光光度法[4],氟离子的测定方法有氟试剂比色法、氟离子选择电极法[5]和离子色谱法[6-8]。本文建立了超声提取、离子色谱检测新鲜蔬菜中氟离子、硝酸盐与亚硝酸盐3种阴离子的方法,并利用该方法对辖区基地内的蔬菜进行检测。
1 材料与方法
1.1 仪器与试剂
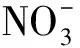
Dionex Aquion RFIC离子色谱仪(热电公司,配淋洗液自动发生器),抑制型电导检测器,超声波清洗器(YJ25-12DTD),数显恒温水浴锅(HH-4,国华)。
1.2 方法
1.2.1 样品前处理
将一定量的新鲜蔬菜的可食部位放入组织粉碎机中粉碎后,称取5.00 g粉碎样品于锥形瓶中,加入80 mL水,超声提取30 min,每隔5 min振摇1次,保持固相完全分散。于75 ℃水浴中放置5 min,取出放置于室温,完全转移至100 mL容量瓶,加水稀释至刻度并混匀。溶液经布氏漏斗抽滤后,取部分滤液过0.45 μm滤膜,待测。
1.2.2 色谱分离条件
分离柱为Dionex IonPac AS 19分析柱(4 mm×250 mm),流速1 mL·min-1,进样体积25 μL,柱温30 ℃,抑制器电流50 mA,淋洗液浓度20 mmol·L-1。
1.2.3 标准曲线绘制
准确吸取10.00 mL的氟离子、亚硝酸盐、硝酸盐标准品,用水定容至100.0 mL,配制成100 μg·mL-1的单一标准储备液。准确吸取一定量的各标准储备液,配制成混合标准工作溶液。
2 结果与分析
2.1 前处理中净化方式的选择
蔬菜提取液中通常含有色素等大分子有机物,如果上机前不进行净化,对色谱柱有影响。试验中,比较过0.45 μm滤膜、弗罗里硅土柱与C18固体萃取小柱的净化效果。结果表明,对常见的蔬菜样品,过滤膜与过弗罗里硅土柱及过C18固体萃取小柱就色素的去除并无太大差异,过0.45 μm滤膜也能得到较为澄清的待测液,对测定结果基本无影响。因此,采用最常见的过0.45 μm滤膜的净化方式。
2.2 色谱条件的确定
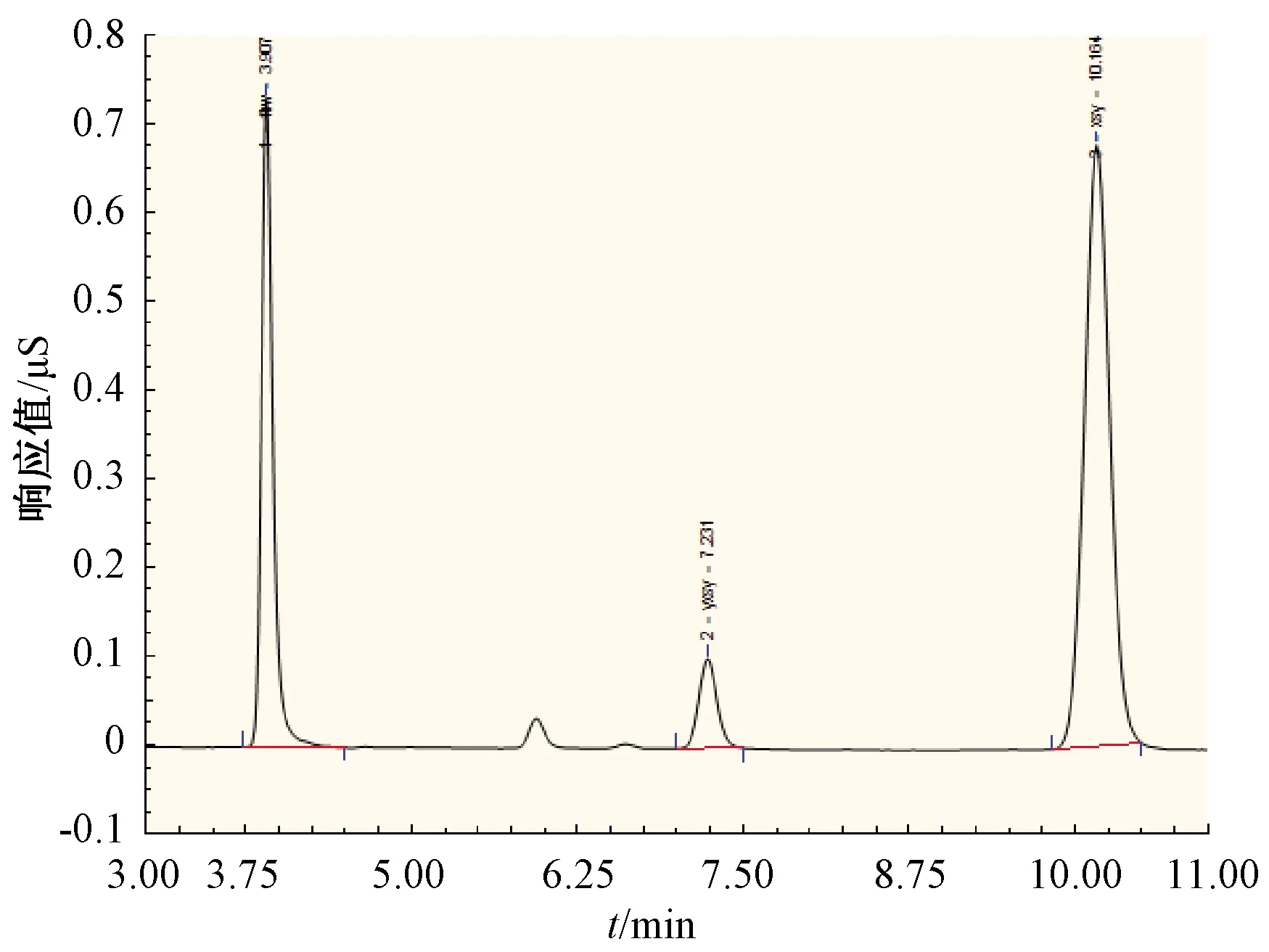
试验表明,当流速为1 mL·min-1、淋洗液浓度为20 mmol·L-1时,等度洗脱,11 min内3种物质能完全分离。图1为3种阴离子混合溶液的色谱图。
2.3 线性及最低检出限

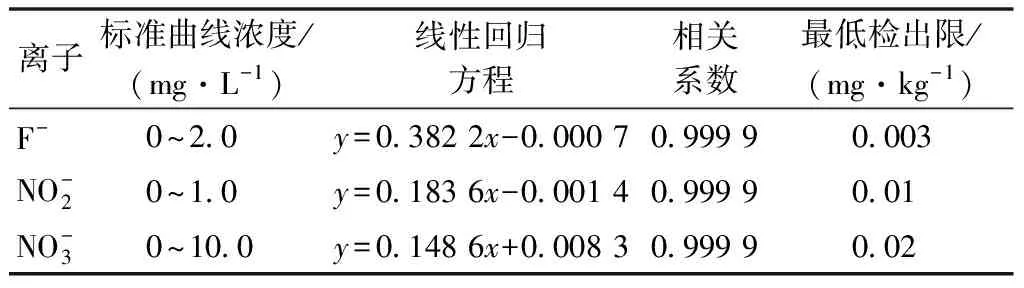
表1 3种阴离子的标准曲线
2.4 回收率与精密度
采用在番茄样品中加入一定体积的标准溶液进行回收率试验,即将一定体积的氟离子、亚硝酸盐与硝酸盐的混合标准溶液加入5 g番茄样品中,按照上述样品前处理方法进行处理,用离子色谱仪进行定量检测,同时进行空白试验。由表2可知,3种离子的回收率89.6%~103.2%,RSD均小于10%,样品加标回收率良好,精密度符合方法学要求。

表2 番茄中3种阴离子的回收率和精密度
2.5 实际样品的测定
对辖区内蔬菜基地中7类蔬菜共24个样品进行检测。结果(表3)表明,24份分析样品中,氟离子、亚硝酸盐与硝酸盐的检出率分别为8.3%、58.3%与100.0%。不同类别的蔬菜中硝酸盐的含量具有一定的规律性。其中,叶菜类与葱蒜类中硝酸盐的含量相对较高,茄果类与瓜类的硝酸盐含量较低,各类别蔬菜中硝酸盐含量从大到小依次为叶菜类>葱蒜类>甘蓝类>根茎类>豆类>瓜类>茄果类,这与国内其他研究基本一致[2-3,9]。

表3 不同蔬菜类别中3种阴离子含量
3 小结
采用超声提取、离子色谱法,同时测定蔬菜中的氟离子、亚硝酸盐与硝酸盐,一次进样11 min内,3种离子完全分离。该方法操作简单,精密度与准确度都符合方法学要求。值得注意的是蔬菜中不同成分阴离子之间的浓度差异很大,有时需对样品进行稀释后再测定。
