超高效液相色谱法测定甲基磺酸电镀锡液中硫酸根
2021-05-17周桂海王德智
周桂海,王德智
(上海梅山钢铁股份有限公司技术中心,江苏南京210039)
随着环保要求越来越高,传统电镀锡工艺已逐步被新型环保的甲基磺酸(MSA)电镀锡工艺取代。甲基磺酸镀锡具有毒性低、导电性好、运行速度快等优点[1],已在梅钢、沙钢、首钢等大型钢厂成功应用。电镀锡液是镀锡工艺最重要介质,镀液成分波动会影响镀锡产品稳定生产及镀锡板表面质量,因此需对镀液中的组分进行快速的检测监控。其中硫酸根含量是电镀锡液的重要指标之一,硫酸根含量一般需控制在2~4 g/L范围,过高或过低均会直接影响到电镀锡生产过程中锡泥量及锡泥尺寸,因此检测监控电镀锡液中硫酸根含量对电镀锡稳定生产意义十分重要。
硫酸根检测方法有硫酸钡重量法[2‐3]、比浊光度法[4‐5]、离子色谱法[6‐7]、电感耦合等离子发射光谱法[8‐9]等,但传统硫酸钡重量法、比浊光度法虽然检测准确较高,但操作繁琐,自动化程度差,很难满足现代化钢铁企业高效生产检测要求。离子色谱法、电感耦合等离子发射光谱法,虽然操作简便,但由于甲基磺酸电镀锡液组成体系复杂,很难快速准确将镀液中硫酸根分离并检测。本文利用超高效液相色谱具有小颗粒填料、低系统体积等优点并利用蒸发光散射检测器特点,提出了超高效液相色谱‐蒸发光散射法测定甲基磺酸电镀锡液中硫酸根含量,具有操作简便,检测数据准确度高,自动化程度高等优点,满足镀锡生产对电镀锡液中硫酸根检测监控要求。
1 实验部分
1.1 实验仪器
色谱仪选用美国Waters 公司生产的Waters AC‐QUITY UPLC 超高效液相色谱,并配有蒸发光散射检测器;离心机为上海安亭科学仪器厂的飞鸽TDL‐5‐A型离心机。
1.2 实验试剂与标准溶液
使用1000 mg/L 硫酸根标准溶液(国家标准物质认证中心),使用时准确稀释100倍;分析纯氨水;色谱纯乙腈(Fisher公司)。
1.3 实验方法
1.3.1 样品处理
准确移取5.00 mL 甲基磺酸电镀锡液样品置于50 mL 容量瓶中,加20 mL 去离子水稀释后,用氨水(1+1)调节溶液到pH 5.5‐6.5,去离子水稀释到刻度,摇匀。取部分液体置于离心分离管内,设定转速2000 r/min,离心分离15 min后,将离心分离管取出,取上层清液色谱分析。
1.3.2 色谱分析条件
亚乙基桥杂化颗粒BEH Amide 色谱柱(美国Waters 公司):规格为 3.0×150 mm、1.7 μm;柱温45 ℃;流动相为乙腈溶液和水(体积比80∶20),流速0.3 mL/min;强洗溶液为20%乙腈+80%水溶液;弱洗溶液为10% 乙腈+90% 水溶液;蒸发管温度55 ℃;氮气流速3.0 L/min;增益80;样品进样量5 μL。
1.3.3 硫酸根标准溶液色谱峰
按照1.3.2 色谱分析条件分析硫酸根标准溶液(10 mg/L),色谱峰见图1。由图1可知,硫酸根保留时间为6.2 min。

图1 硫酸根标准溶液的色谱图Fig.1 Chromatogram of SO42‐standard solution
2 结果与讨论
2.1 样品前处理
甲基磺酸电镀锡液具有较强酸性,且有大量锡离子,若直接色谱分离不仅效果较差,同时大量锡离子易水解,可能堵塞色谱柱和沉积在检测器蒸发管壁上,严重缩短色谱柱和检测器使用寿命。二价锡和四价锡氢氧化物均为难溶物质,可通过调节溶液pH 值去除锡离子。Sn(OH)2溶度积常数KSP=1.4×10‐28,Sn(OH)4溶度积常数KSP=1.0×10‐56,“沉淀完全”的标准浓度为 10‐5mol/L,计算得出 Sn(OH)2和 Sn(OH)4完全沉淀溶液的pH 值分别为2.6 和1.25。同时考虑色谱柱最佳使用条件,电镀液样品用氨水(1+1)调节到pH 5.5‐6.5,即可保证溶液中锡离子沉淀完全,又得到较好的色谱分离效果。
2.2 色谱柱选择
选择合适色谱柱是电镀液组分高效分离关键。实验选择HSS C18 和BEH Amide 色谱柱对电镀锡液分离,结果见图2 所示。由图可知,采用HSS C18色谱柱,电镀锡液中组分间分离效果较差,其中硫酸根未达到基本分离要求。而采用BEH Amide 色谱柱,共出现6个色谱峰,电镀锡液组分达到基本分离要求,其中硫酸根也达到完全分离要求。因此本实验选用型号为BEH Amide色谱柱。
2.3 色谱柱柱温
柱温是影响色谱分离效果重要因素。本次实验了柱温分别为 25 ℃、30 ℃、35 ℃、40 ℃、45 ℃、50 ℃、55 ℃、60 ℃对分离效果的影响,实验结果见表1 所示。由表1 可知,当柱温在 25 ℃~35 ℃时,由于传质速率较低,分析时间拉长,峰型也较差。当柱温在50 ℃~60 ℃时,出峰变快,分析时间缩短,半峰宽变窄,峰高变高,但分离度减小,组分间分离效果不理想,同时发现有杂峰现象,可能由于电镀液组分分解导致。柱温在40 ℃~45 ℃时,电镀液出峰时间适中且组分分离效果理想,色谱峰峰型较好,本实验选择柱温为45 ℃。

图2 电镀溶液两种色谱柱的色谱图Fig 2 Chromatograms of two chromatographic columns for electroplating solution
2.4 蒸发管温度
蒸发管温度是对分离后目标组分准确检测的关键参数。本次实验了蒸发管温度分别为30 ℃、35 ℃、40 ℃、45 ℃、50 ℃、55 ℃、60 ℃、65 ℃、70 ℃对目标组分检测的影响,实验结果见表2。由表2可知,当蒸发管温度低于50 ℃时,检测基线不稳定,噪音相对较大;当温度高于65 ℃时,电镀液部分组分无法检测,这是由于电镀锡液某些组分沸点较低引起。兼顾到电镀锡液中其它组分检测,本次实验确定蒸发管温度为55 ℃。
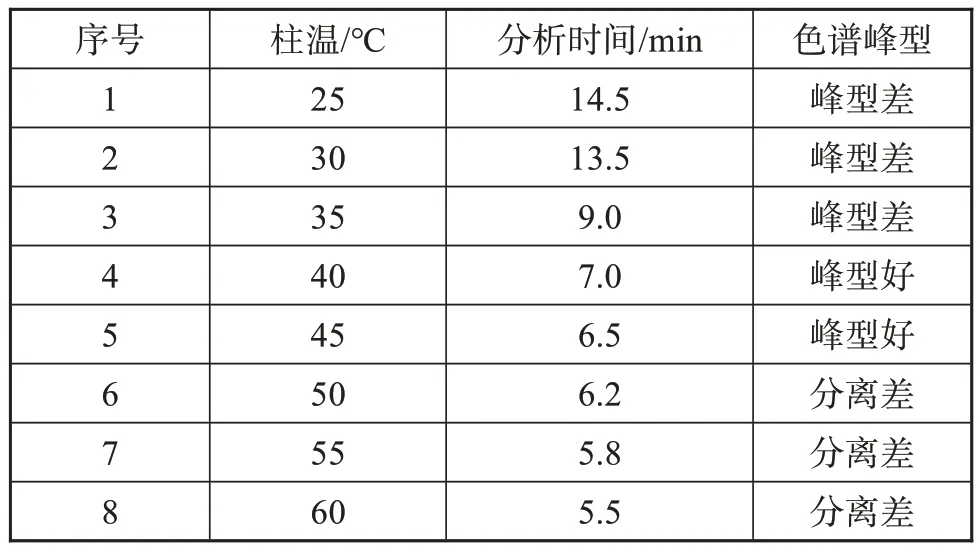
表1 色谱柱柱温实验结果Table 1 Column temperature experiment results

表2 蒸发管温度实验结果Table 2 Evaporation tube temperature test results
2.5 线性范围与检出限
根据电镀锡液中硫酸根含量控制范围,配制一列硫酸根浓度的标准溶液,按照1.3.2 实验条件测定硫酸根色谱峰面积,结果见表3 所示。对峰面积Y的对数及相应硫酸根浓度X的对数进行线性回归计算,结果表明,硫酸根质量浓度在100.00~1000.00 mg/L 范围内,其硫酸根峰面积对数与硫酸根浓度对数呈现良好线性关系,线性回归方程为:
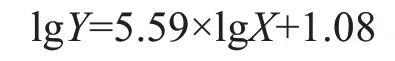
线性相关系数r为0.9997,计算检出限(3S/N)为15.2 mg/L。

表3 不同硫酸根浓度测定的色谱峰面积Table 3 Chromatographic peak areas determined by different sulfate concentrations
2.6 精密度实验
采用实验方法对6 组甲基磺酸电镀锡液样品中硫酸根进行测定,实验结果见表4 所示。由实验结果可知,采用本文方法测定电镀锡液样品中硫酸根含量,相对标准偏差在0.74% ~1.73%范围内,相对标准偏差RSD 小于3%,满足电镀锡生产对电镀液组分检测监控要求。

表4 精密度实验结果Table 4 Precision test results
2.7 加标回收实验
按照实验方法,分别在1#和2#电镀锡液样品中加入硫酸根标准溶液进行加标回收实验,结果见表5 所示。由实验结果可知,采用本文方法测定电镀锡液样品加标回收率在99.3% ~101.0%之间,回收率较高,满足电镀锡液组分检测监控要求。

表5 加标回收实验结果Table 5 Result of spike recovery experiment
2.8 比对实验
分别采用超高效液相色谱法和硫酸钡重量法检测甲基磺酸电镀锡液中硫酸根含量,结果见表6。按照F‐检验法和t‐检验法计算F和t值,结果为F8,8=3.44、t0.05,16=2.12,均小于规定值,说明两种分析方法之间无显著性差异。

表6 两种检测方法的实验结果Table 6 Experimental results of two detection methods
3 样品分析
目前暂无电镀锡液标准样品,根据甲基磺酸电镀锡液组成,配制不同硫酸根含量的电镀液合成样品。按照实验方法对合成电镀锡液样品测定,结果见表7。由分析结果可知,采用本文方法测定合成电镀锡液样品中硫酸根含量,相对误差在‐1.00% ~+1.00%范围内,测得值与理论值吻合。
4 结论
(1)建立了超高效液相色谱法测定甲基磺酸电镀锡液中硫酸根含量的方法,具有前处理简便快速、分离效果好,分析时间短等优点。
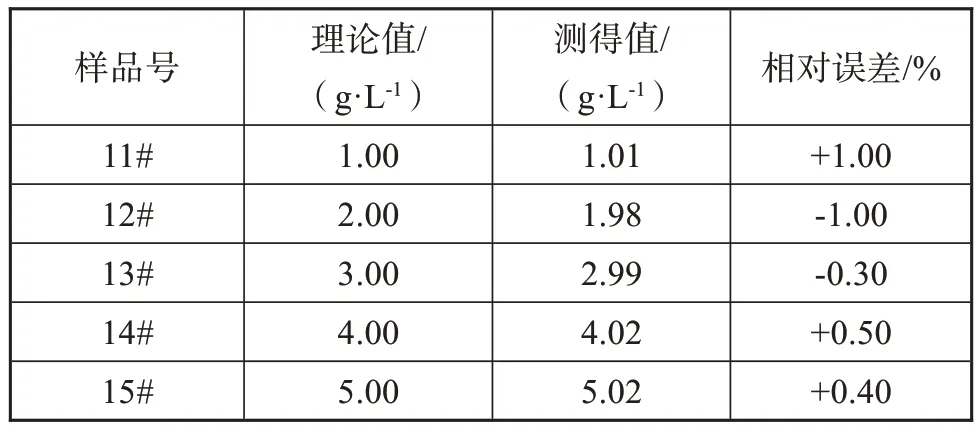
表7 电镀锡液合成样品中硫酸根测定结果Table43 Determination results of SO42‐in synthetic sam‐ples of tin plating bath
(2)建立的硫酸根分析方法检测数据精密度好,加标回收、对比实验均能满足电镀锡生产对电镀液中硫酸根监控检测要求,同时该方法可应用到电镀洗液中其它组分的检测。
