高效液相色谱-串联质谱法同时测定鸡肉和鸡蛋中10种硝基咪唑类药物及代谢物
2021-05-14高玉时马丽娜陆俊贤唐修君杨星星
张 静,高玉时,周 倩,马丽娜,陆俊贤,唐修君,万 玉,杨星星,赵 敏
(江苏省家禽科学研究所,江苏扬州 225125)
硝基咪唑类药物(Nitromidazoles,NMZs)是一类具有5-硝基取代咪唑杂环结构的化合物,主要包括甲硝唑(Metronidazole,MNZ)、二甲硝唑(Dimetridazole,DMZ)、洛硝哒唑(Ronidazole,RNZ)、塞克硝唑(Secnidazole,SNZ)、异丙硝唑(Ipronidazole,IPZ)和奥硝唑(Ornidazole,ORN)等。因该类药物具有抗菌和抗原虫作用且疗效快,曾广泛用于杀灭及预防厌氧菌和病原虫,同时它们还有促生长和提高饲料利用率[1]的作用。研究发现,硝基咪唑类药物具有动物致癌性和细胞诱变毒性,欧盟、美国和日本已禁止在食源性动物中使用[2];我国国家标准(GB 31650-2019)明确规定MNZ和DMZ允许作治疗用,但在动物源性食品中不得检出。硝基咪唑类药物代谢迅速,主要是咪唑环上的取代基甲基被氧化成羟甲基,MNZ形成羟基甲硝唑(Metronidzole-OH,MNZOH),DMZ和RNZ都代谢成羟基二甲硝咪唑(2-Hydroxymethyl-1-methyl-5-nitroimidazole,HMMNI),IPZ代谢成羟基异丙硝唑(Ipronidazole-OH,IPZOH)[3]。有研究表明硝基咪唑类代谢产物在动物体内的维持时间比原药长,并且具有和原药类似的毒性[4]。目前兽医中常用的有MNZ、RNZ和DMZ,但SNZ、ORN、TNZ和IPZ是继上述三种之后疗效更高,耐受性更好,不良反应较少的药物。但未见各国对这5种药物在动物组织中使用和残留量作出规定,其实际应用中它们有可能替代MNZ和DMZ等应用于临床兽医,且它们也具有硝基咪唑类药物的毒副作用。所以建立这7种硝基咪唑类药物及其相应的3种代谢物残留的检测方法对食品安全监管是完全有必要的。
目前用于硝基咪唑类药物及其代谢物的研究方法主要有液相色谱法(HPLC)[5,6]、气相色谱法(GC/MS)[7 - 9]、毛细管电泳法[10,11]和液相色谱-质谱法(LC/MS)[12 - 18]。本文采用同位素内标稀释法,利用乙酸乙酯提取,SCX固相萃取柱净化,高效液相色谱-串联质谱法(HPLC-MS/MS)同时测定鸡肉和鸡蛋中10种硝基咪唑类药物及代谢物。方法简单,灵敏度高,特异性强,回收率高,能够满足日常检测和监督的需求。
1 实验方法
1.1 仪器与试剂
Thermo TSQ MAX型液相色谱-三重四极杆质谱仪(美国,塞默飞公司);固相萃取装置(美国,Supelco公司);N-EVAP 112氮吹仪(美国,Organomation公司)。SCX固相萃取柱(500 mg/6mL,上海安谱实验科技股份有限公司)。
标准品:甲硝唑(MNZ)、地美硝唑(DMZ)、洛硝哒唑(RNZ)、奥硝唑(ORN)、塞克硝唑(SNZ)、羟基甲硝唑(MNZOH)、羟基二甲硝咪唑(HMMNI)、异丙硝唑(IPZ)、羟基异丙硝唑(IPZOH)、甲硝唑-D4(MNZ-D4)、地美硝唑-D3(DMZ-D3)、洛硝哒唑-D3(RNZ-D3)、奥硝唑-D3(ORN-D3)、塞克硝唑-D6(SNZ-D6)、羟基甲硝唑-D2(MNZOH-D2)、羟基二甲硝咪唑-D3(HMMNI-D3)、异丙硝唑-D3(IPZ-D3)、羟基异丙硝唑-D3(IPZOH-D3),均购于德国Dr.Ehrenstorfer公司,纯度均≥98%。标准品溶液:分别准确称取适量MNZ、DMZ、RNZ、ORN、SNZ、IPZ、IPZOH、MNZOH和HMMNI(精确到0.01 mg),用甲醇溶解,配制成浓度为1 mg/mL的标准储备溶液,于-20 ℃保存;内标标准溶液分别准确称取适量MNZ-D4、DMZ-D3、RNZ-D3、ORN-D3、SNZ-D6、IPZ-D3、IPZOH-D3、MNZOH-D2和HMMNI-D3(精确到0.01mg),用甲醇溶解,配制成浓度为1 mg/mL的内标储备溶液,于-20 ℃保存。乙腈、甲醇、丙酮、乙酸乙酯(色谱纯,德国Merck公司);其他试剂均为分析纯。水为Milli-Q系统制备的超纯水(18.2 MΩ·cm)。
1.2 样品的制备
空白样品为经检验不含上述硝基咪唑类化合物,搅碎使均匀,-20 ℃保存备用。实际样品来源于超市、养殖场和农贸市场。
1.3 样品前处理
准确称取样品2 g(精确到0.01 g),加入100 μL 100 ng/mL硝基咪唑混合内标工作溶液,采用10 mL乙酸乙酯提取,涡旋混匀,振荡10 min,10 000 r/min离心5 min,取上清液。重复提取一次,合并上清液。上清液中加入5 mL乙睛饱和的正己烷,涡旋混匀后振荡10 min,5 000 r/min离心5 min后,弃去正己烷。40 ℃氮气浓缩仪吹干。加入5 mL乙酸-乙酸乙酯(5+95)混匀后备用。
净化采用SCX固相萃取柱,5 mL乙酸-乙酸乙酯(5+95)活化,将提取液全部过柱,分别用2.5 mL丙酮,5 mL甲醇,5 mL乙睛淋洗。真空抽干,5 mL氨水-乙睛(5+95)洗脱后,45 ℃氮气浓缩仪吹干,准确加入1.0 mL 0.1%甲酸溶液-乙睛(体积比9∶1)溶解残渣,过0.45 μm膜,备用。
1.4 液相色谱-质谱条件
色谱条件:色谱柱:Waters C18柱(100 mm×2.1 mm,1.8 μm);流动相:A为0.1%甲酸溶液,B为0.1%甲酸甲醇溶液。梯度洗脱条件为:0~1.0 min,90%A;1.0~5.0 min,90~10%A;5.0~6.0 min,10%A;6.0~6.1 min,10%~90%A;6.1~8.0 min,90%A。柱温:30 ℃;流速:0.3 mL/min;进样量:10 μL。
质谱条件:离子源:电喷雾离子源,正离子扫描(ESI+);检测方式:多反应监测(MRM)模式;离子源温度:350 ℃;电喷雾电压:3 500 V;雾化气压力:35 Arb;辅助气压力:10 Arb;离子传输管温度:350 ℃;碰撞气:氩气。目标分析物的定性定量离子对、碰撞电压、离子透镜电压等信息见表1。

表1 硝基咪唑类药物的信息及质谱参数优化条件
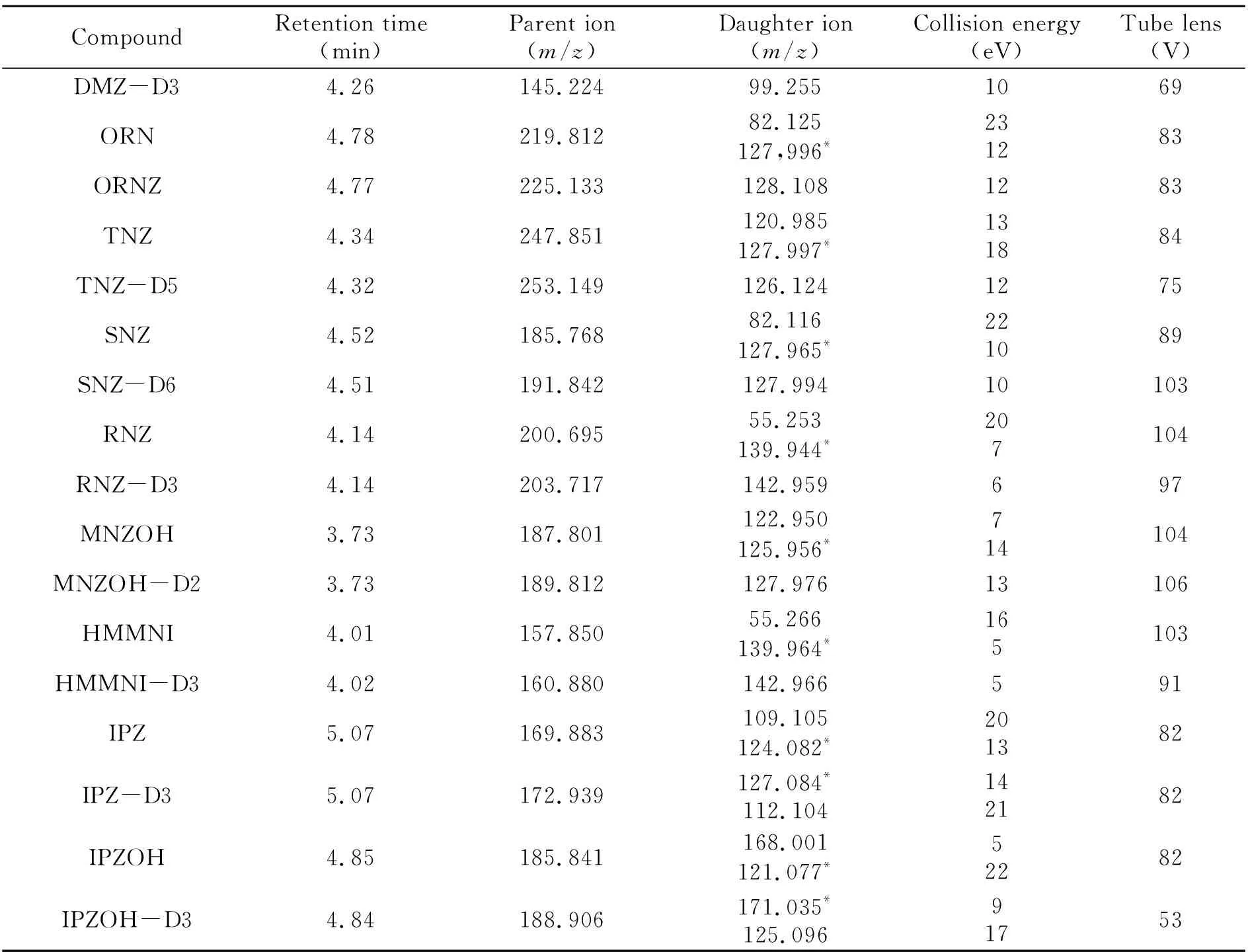
(续表1)
2 结果与讨论
2.1 质谱条件和色谱条件的优化
采用直接进样的方式将500 ng/mL的10种硝基咪唑类化合物的标准溶液,以及对应的氘代内标标准溶液注入到离子源中,在正离子模式下进行母离子全扫描,通过优化离子透镜电压得到最佳强度的各待测目标物的分子离子峰。以确定的分子离子峰为母离子进行二级质谱碎片离子扫描,获得碎片离子信息,得到二级质谱图。选取丰度高的为定量离子,另一种化合物为定性离子。内标化合物选取丰度高的为定性离子,不需定量离子。
2.2 样品前处理方法的选择
2.2.1 提取溶剂的选择硝基咪唑类化合物的提取溶剂一般为乙腈、乙酸乙酯、二氯甲烷、甲醇等单一溶剂或混合溶剂。本文比较了乙腈、甲醇、二氯甲烷-乙腈(1∶1,V/V)和乙酸乙酯等溶剂的提取效率,结果见图1。由图可以看出,提取溶剂对MNZOH和HMMNI的回收率影响最大,乙酸乙酯提取效率最高,分别为98.1%和80.5%。提取溶剂对其他化合物的影响不是很大,且采用乙酸乙酯提取可去除大部分亲水性杂质,降低后续净化的难度,因此选用乙酸乙酯作为提取溶剂。
2.2.2 固相萃取柱的优化本文比较了C18、HLB和SCX三种固相萃取柱对硝基咪唑化合物回收率的影响。由图2可以看出,C18和HLB小柱对9种硝基咪唑化合物的回收率均偏低,而SCX小柱对目标化合物的回收率均在70%~115%之间,因此选用SCX固相萃取柱净化。
2.3 基质效应(ME)评价
本研究按(空白基质匹配标准曲线斜率/纯溶剂标准曲线斜率-1)×100%计算基质效应(ME)(表2)。当ME为负值时表示存在基质抑制效应,ME为正值时表示存在基质增强效应;绝对值越大基质效应越强。由表2可知,硝基咪唑类药物及其代谢物在各基质溶液中呈现一定的基质抑制作用,其中MNZOH和HMMNI基质抑制效应较大。经过本方法净化处理后目标化合物的基质效应均可在接受范围内,且本文采用内标法测定实际样品也可在一定程度上补偿基质效应的影响。
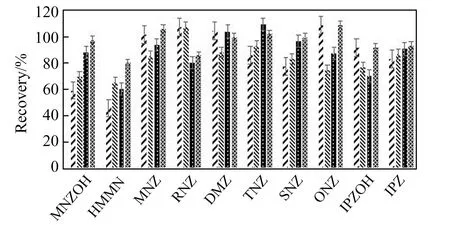
图1 提取溶剂对硝基咪唑化合物回收率的影响Fig.1 Effects of extraction solvents on the recoveries of the NIMs
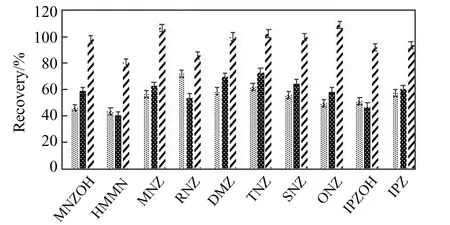
图2 不同固相萃取柱对硝基咪唑化合物回收率的影响Fig.2 Effects of SPE cartridges on the recoveries of the NIMs

表2 不同基质中硝基咪唑类药物及其代谢基质效应评价
2.4 线性范围、相关系数(R2)、检出限(LOD)和定量限(LOQ)
取一系列硝基咪唑类的标准工作溶液,在选定的色谱-质谱条件下进行测定。以外标内标峰面积之比Y和对应的质量浓度X(ng/mL)绘制标准曲线。结果表明,在0.5~40.0 ng/mL范围内具有良好的线性关系,其线性方程和相关系数见表3。在空白样品中添加标准溶液,按信噪比(S/N)等于10和3计算,本方法的定量限和检测限见表3。
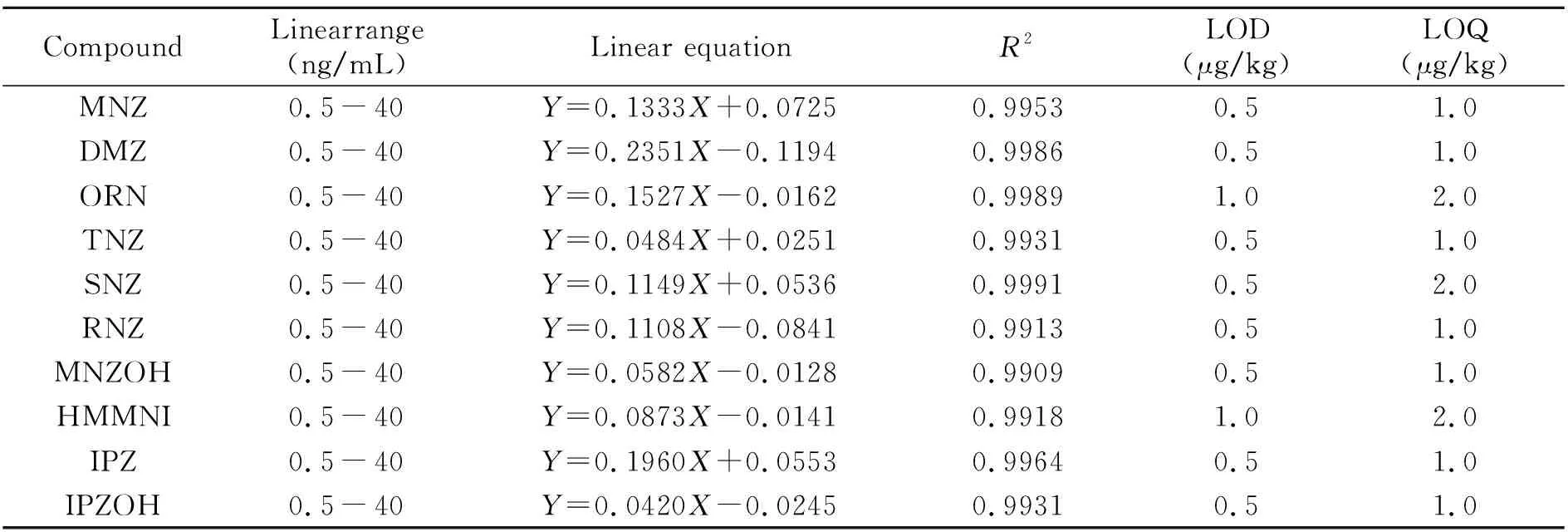
表3 硝基咪唑药物线性范围、线性方程、相关系数(R2)、检测限(LOD)和定量限(LOQ)
2.5 准确度和精密度
在空白组织中添加1.0、2.0、10.0 μg/kg水平的目标分析物,每个样品按上述方法重复测定6次,求日内精密度(RSD);再每天测定一次,连续测定6天,求日间RSD,结果见表4。结果表明日内加标回收率在73.8%~112%之间,RSD为3.21%~11.8%;日间加标回收率在70.5%~106%之间,RSD为4.67%~14.6%。准确度和精密度能满足相关标准[19]的要求。
2.6 实际样品分析
应用本法测定了当地及周边地区市场鸡肉、鸡蛋等60批次样品,鸡肉中无检出;鸡蛋有2份检出MNZ、DMZ、TNZ和MNZOH,含量分别为5.7 μg/kg、3.7~423.5 μg/kg、5.2 μg/kg和3.2 μg/kg。其余样品未检出上述硝基咪唑类药物。说明在鸡养殖过程中,硝基咪唑类药物存在着一定的使用率。
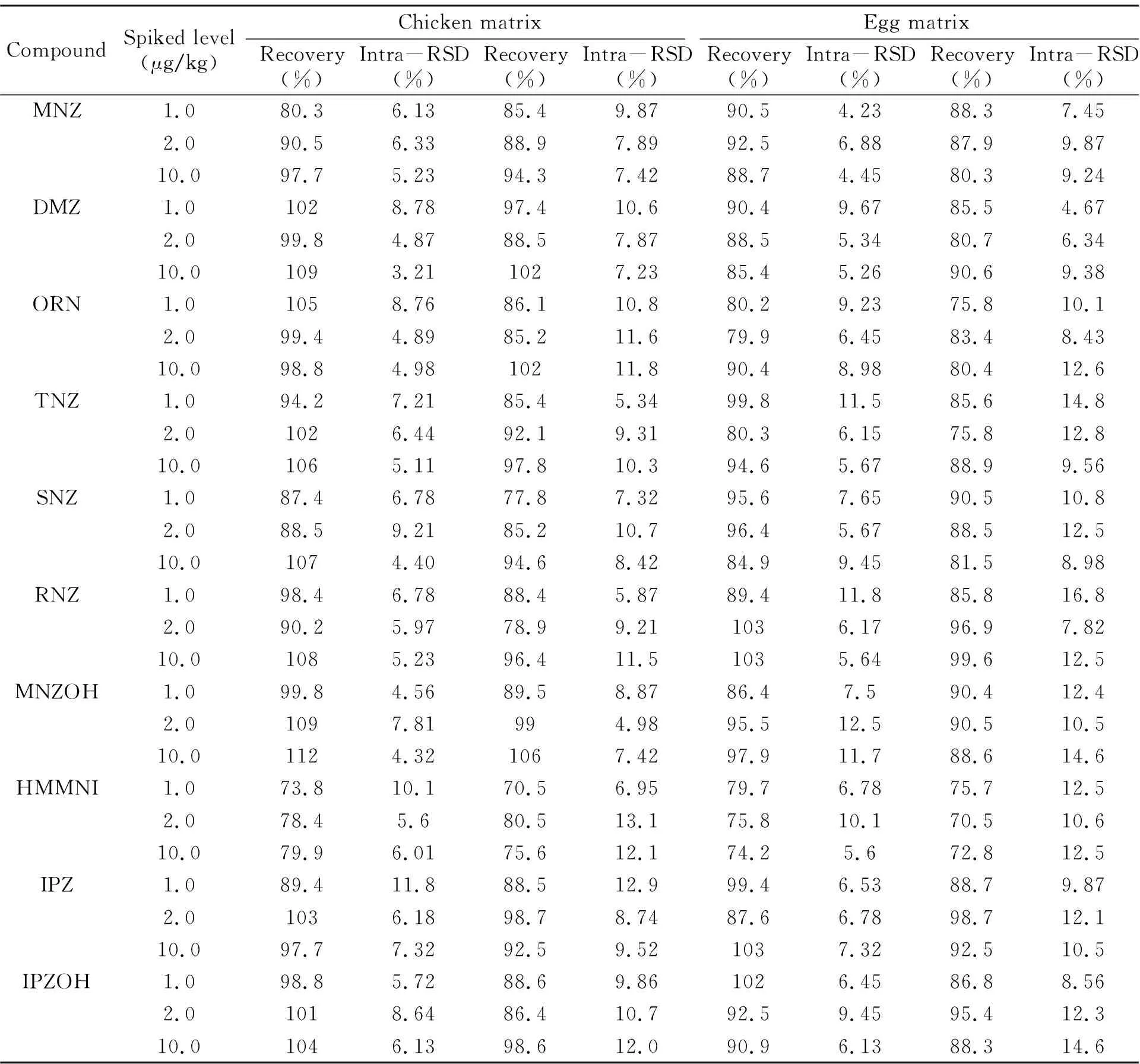
表4 方法的加标回收率和精密度
3 结论
本研究建立了高效液相色谱-串联质谱法同时测定鸡肉和鸡蛋中7种硝基咪唑类药物及其对应的3种羟基代谢物残留。硝基咪唑类化合物及代谢物在0.5~40 ng/mL范围内线性良好,方法的检测限0.5~1.0 μg/kg。该方法简单、准确、快速、重复性好、灵敏度高,且方法的回收率、灵敏度和定量限均能满足目前日常监控和检测的要求。
