高盐基度聚氯化铝对控制饮用水中铝的应用
2021-05-12狄春华施学峰
狄春华,施学峰
(江苏中法水务股份有限公司,江苏常熟 215500)
铝是自然界中的丰量元素,在地壳中分布广泛,含量高达8.8%,仅次于氧和硅,位居第三。铝在食物、饮用水和抗酸制剂中普遍存在,研究表明,铝和老年性痴呆有关[1]。铝在饮用水中的浓度主要取决于原水中的浓度以及是否使用铝絮凝剂。我国《生活饮用水卫生标准》(GB 5749—2006)[2]中,规定铝的限值为0.20 mg/L;《江苏省城市自来水厂关键水质指标控制标准》(DB 32/T 3701—2019)[3]中,规定铝的控制标准限值为0.15 mg/L;某公司将出厂水铝的内控标准定为0.10 mg/L。
该公司有2个自来水厂,生产工艺基本类似,且均以长江为水源,以液体聚氯化铝(PAC)为净水剂。经过对2个水厂出厂水水质数据分析,发现夏季(6月—9月)其铝含量不能稳定控制在内控标准之内,通过进一步分析,发现2个水厂使用的PAC来自不同的供应商,盐基度与出厂水铝含量呈反比。
研究表明,当使用铝盐作为絮凝剂时,pH和水温是影响饮用水中铝的重要因素[4-5]。李润生等[7-8]研究还发现,高盐基度PAC有助于降低饮用水中残留铝,盐基度也是影响混凝效果的最重要因素,铝离子3种水解形态中,Alc占比又与盐基度呈现正相关。降低原水pH对铝的影响可采取的手段有3种。一是原水直接加盐酸[5]等强酸,2015年开始该公司第二水厂(以湖泊水为原水,制水能力为7.5万t/d)采用此工艺。其优点是投加工艺简单,缺点是盐酸类强酸属于易制毒化学品,且一般情况下无涉水产品卫生批件,采购、储存和使用管理等各环节要求较高,较适用于制水能力不超过10万t/d的小型水厂。二是原水直接加二氧化碳来降低pH[9-10],原理与加强酸相同,缺点是投加工艺相对复杂、实际应用较少。三是使用降pH能力较强的净水剂,如硫酸铝或酸化聚氯化铝等降低原水pH[11-12],2018年该公司2个长江水厂采用了此工艺。其优点是无需更改现有工艺,缺点是投加量较大、成本较高,且不能稳定地将出厂水铝含量控制在内控标准内。
本文从PAC的盐基度对铝的影响角度开展研究,通过测定不同盐基度PAC中铝盐水解3种形态占比,开展出厂水铝含量影响因素分析和高盐基度PAC控制铝效果等试验,提出夏季净水剂选型建议,并在实际中加以运用,从而实现控铝降费的双重效果。
1 铝盐水解形态分析
为研究验证PAC的盐基度与其水解形态的关系,收集6种不同盐基度的PAC,对其水解形态进行分析。常用的铝盐水解形态分析方法有Al-Ferron逐时络合比色法(简称Ferron法)和A1-NMR核磁共振法[13-14]。本文采用Ferron法对不同盐基度的PAC产品的水解形态进行分析[15]。
1.1 方法原理
Ferron法研究铝的水解聚合形态的原理是基于显色剂Ferron与铝水解态络合反应速度的差异,将水解铝溶液中的各种形态划分为3类,即:Ala(单体形态,与Ferron瞬时反应部分,反应时间为0~1 min)、Alb(中等聚合形态,与Ferron缓慢反应的部分,且反应动力学表现为准一级反应,反应时间<120 min)、A1c(一般指水解聚合大分子或溶胶聚合物,与Ferron反应十分缓慢或基本不反应,反应时间>120 min)。
1.2 仪器及试剂
可见光分光光度计,T6,北京普析通用;微量注射器,1 μL;铝标准使用液:采用铝有证标准物质[中国计量科学研究院,GBW(E)080219-18216]配制,浓度为0.001 mol/L-1;Ferron比色液:将A、B、C这3种试剂按2.5∶2∶1(A最后加)混合后即得,溶液配制后的pH值约为5.2,置于冰箱中保存,可使用3个月。
试剂A[0.2%(m/v)Ferron水溶液]:在1 000 mL煮沸并冷却至室温的纯水中加入2.0 g分析纯Ferron试剂,用磁力搅拌使之溶解,过滤后用纯水定容至1 000 mL,冰箱保存。试剂B[20%(m/v)的NaAc溶液]:将50 g分析纯无水NaAc溶解后,用纯水定容至250 mL。试剂C(1∶9盐酸):将100 mL分析纯盐酸溶于适量纯水中,定容至1 000 mL。
1.3 待测样品
6种不同盐基度PAC,其中,氧化铝的质量分数为10%~11%,盐基度为1%~90%。
1.4 分析步骤
(1)标准曲线制备
分别准确移取1、2、3、4、5 mL铝标准使用液于25 mL具塞比色管中,并加入5.5 mL Ferron比色液,纯水定容至25.0 mL,摇匀。显色5 min后,用10 mm比色皿,以水为参比,在366 nm处测量吸光度。以铝浓度为横坐标,经过空白校正的吸光度为纵坐标,得到标准曲线和方程式(图1)。
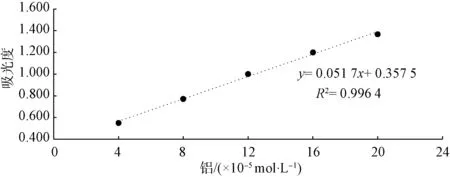
图1 标准曲线及方程式Fig.1 Standard Curve and Equation
(2)总铝分析
取1 μL待测样品置于25.0 mL比色管中,加入(1∶9)盐酸0.5 mL,再加入少量纯水(使管內溶液总体积少于10 mL),加塞后在沸水浴中加热15 min。冷却后加入Ferron比色液,定容至25.0 mL,显色5 min后,10 mm比色皿在366 nm处测量吸光度。由图1中方程式可计算出总铝含量Alt。
(3)铝水解形态分析
取Ferron比色液5.5 mL加到25.0 mL比色管中,纯水定容至25 mL,然后加入1 μL待测样品,计时,迅速摇匀,将盛有样品的10 mm比色皿在366 nm处,分别在1 min及120 min时测量其吸光度。由图1中方程式计算得到Ala和Ala+Alb含量。
根据Alt=Ala+Alb+Alc能够计算得到不同铝水解形态所占比例。
1.5 结果讨论
试验结果如表1和图2所示。试验结果表明,PAC的3种铝盐水解形态中,Alb占比与盐基度基本不相关(r=0.195),Ala占比与盐基度呈负相关(r=-0.995),Alc占比与盐基度呈正相关(r=0.951),与李凯等[6]的研究结论类似。

表1 PAC中铝水解形态测定结果Tab.1 Determination Results of Aluminum Hydrolysis Forms in PAC

图2 PAC中铝水解形态与PAC盐基度的关系Fig.2 Relationship between Aluminum Hydrolysis Forms and PAC Basicity
2 影响出厂水铝的因素分析试验
选用2种盐基度较高(分别为73%和89%)的PAC进行试验,开展出厂水铝含量的影响因素分析。
2.1 仪器与试验条件
混凝试验搅拌机,R4-6,深圳中润;浊度仪,2100P,美国哈希;可见光光度计,T6,北京普析通用;搅拌试验条件:快混、转速为200 r/min、3 min,慢混、转速为50 r/min、17 min,沉淀20 min;残余铝浓度的检测:试验水样经0.45 μm滤膜过滤后,采用铬天青S分光光度法测定。
2.2 结果与讨论
(1)沉淀时间的影响
PAC投加量为15 mg/L,沉淀时间设定为20、40、60 min,试验用水水质如表2所示,试验结果如图3所示。

表2 试验用水水质Tab.2 Water Quality in Experiment

图3 沉降时间与残余铝浓度的关系Fig.3 Relationship between Settling Time and Residual Aluminum Concentration
由图3可知,高盐基度(89%)的PAC出水铝浓度仅为73%盐基度PAC的一半,控铝效果明显;不同沉淀时间(20、40、60 min)对出水铝浓度的影响不大,因此,以下工艺试验的沉淀时间均设定为20 min。
(2)pH对铝的影响
pH是影响出厂水铝含量的主要因素[5,16]。铝盐的水解产物Al(OH)3是典型的两性物质,pH过低会生成铝离子,过高则生成偏铝酸根离子,均会造成出厂水铝含量的升高。
本试验主要考查高盐基度(89%)PAC,在不同pH下控铝的效果。试验投加量为35 mg/L,试验用水水质如表3所示。试验结果:1#水样铝为0.053 mg/L,2#水样铝为0.132 mg/L。表明当长江原水pH值为8.0左右时,高盐基度PAC控铝效果显著;原水pH过高时,其控铝效果也有一定的局限性。
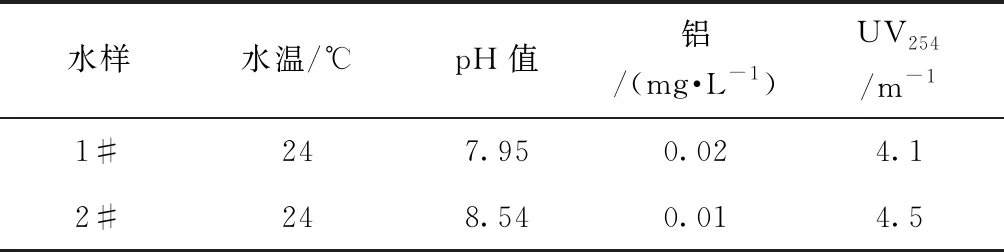
表3 试验用水水质Tab.3 Water Quality in Experiment
(3)水温对铝的影响
选用盐基度为89%的PAC,投加量分别为15、25、35 mg/L,试验用水水质如表4所示,试验结果如图4所示。水温越高,沉淀水铝浓度越高,这与生产实际情况是一致的。当水温在32 ℃以下时,15 mg/L的投加量即可获得满意结果。

表4 试验用水水质Tab.4 Water Quality in Experiment
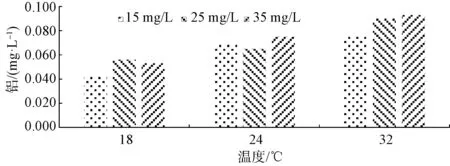
图4 水温与残余铝浓度的关系Fig.4 Relationship between Water Temperature and Residual Aluminum Concentration
(4)PAC的盐基度和投加量对出水铝和浑浊度的影响
选用不同盐基度的PAC,投加量分别为15、25、35 mg/L,试验用水水质如表5所示,试验结果如图5和图6所示。由图5可知,6种PAC在投加为15 mg/L时,沉淀水浑浊度均低于2 NTU,可完全满足沉淀池出水要求,且盐基度越高,沉淀水浑浊度越低,混凝效果越好。由图6可知,高盐基度PAC控制铝效果明显优于低盐基度PAC。在试验条件下,投加15 mg/L的高盐基度(>80%)PAC,可将沉淀水铝浓度控制在0.10 mg/L以下。

表5 试验用水水质Tab.5 Water Quality in Experiment

图5 PAC盐基度与浑浊度的关系Fig.5 Relationship between PAC Basicity and Turbidity Concentration

图6 PAC盐基度与残余铝浓度的关系Fig.6 Relationship between PAC Basicity and Residual Aluminum
3 实际运用情况分析
2018年夏季, 2个长江水厂为应对出厂水铝超过内控值(0.10 mg/L)的问题,用硫酸铝(AS,氧化铝含量为7%左右)代替PAC作为净水剂,利用其较强的降pH能力来降低水的pH,以控制出厂水铝含量。从实际情况来看,尚不能稳定地将出厂水铝控制在内控标准以内,且AS投加量较大,成本增加明显。
2019年,在工艺试验的基础上,采用高盐基度PAC(盐基度>80%)代替AS作为净水剂。就实际运用情况及效果进行对比分析。
3.1 长江原水水质分析
选取2018年和2019年高峰供水期间相关原水水质指标(水温、pH和耗氧量)进行对比,如图7~图9所示。与2018年相比,2019年长江原水水质总体变化不大。其中,水温有所降低,幅度在0.6~1.2 ℃;8月、9月这2个月pH有所升高;耗氧量有所下降,降幅在0.1~0.6 mg/L。

图7 水温对比Fig.7 Comparison of Water Temperature
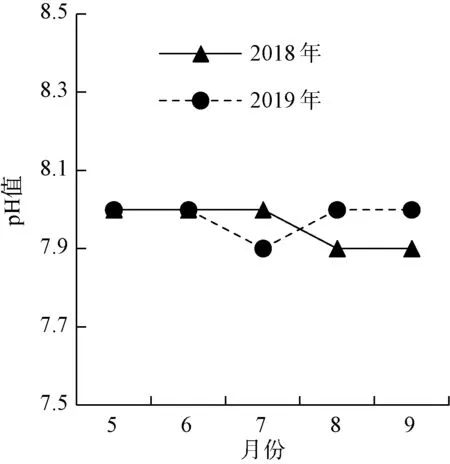
图8 pH对比Fig.8 Comparison of pH Value

图9 耗氧量对比Fig.9 Comparison of CODMn
3.2 净水剂成本分析
分别收集了2018年和2019年高峰供水期间千吨水净水剂投加量及相关数据,如表6所示;统计对比了净水剂投加量(均以净水剂原液计)变化情况,如图10所示。2019年,高峰供水期间净水剂投加量同比下降62.1%;千吨水净水剂成本下降58.8%;以2019年制水量计,可节约净水剂费用约161万元。

图10 净水剂投加量对比Fig.10 Comparison of Dosages of Water Purification Chemicals
3.3 出厂水水质分析
以滨江水厂为例,选取2018年和2019年高峰供水期间出厂水的pH、铝、浑浊度和耗氧量进行了对比,如图11~图14所示。2019年滨江水厂出厂水水质稳定,总体优于2018年,特别是铝稳定低于0.10 mg/L内控标准。
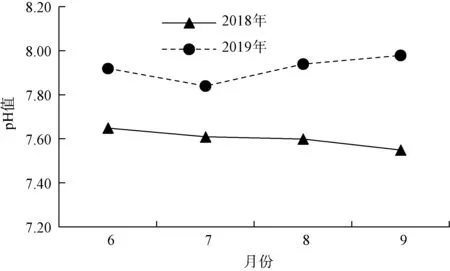
图11 pH对比Fig.11 Comparison of pH Value

图12 铝对比Fig.12 Comparison of Aluminum
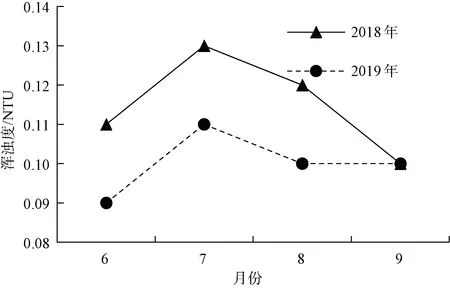
图13 浑浊度对比Fig.13 Comparison of Turbidity
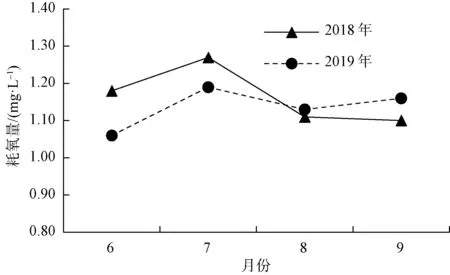
图14 耗氧量对比Fig.14 Comparison of CODMn
4 总结
(1)原水pH和水温是影响水中铝含量的重要因素。当pH值基本稳定在8.0时,由于铝盐的水解反应是吸热反应,水温越高,铝含量也越高,导致夏季出厂水铝含量不能稳定达到内控标准。
(2)高盐基度(>80%)PAC对水中铝的控制效果明显优于低盐基度PAC或AS,且所需投加量较低,其原因可能是高盐基度PAC水解后以Alc(惰性态的聚合大分子或溶胶聚合物)为主,有利于提高混凝效果;另外,由于单核形态的Ala占比很少,水中残余铝降低。
(3)经水厂实际使用,高峰供水期间千吨水投加15~20 kg的高盐基度(>80%)PAC,可稳定控制出厂水铝低于0.10 mg/L,同比下降约12%;千吨水净水剂成本下降58.8%,取得了很好的效果,适合本地以长江为原水的水厂使用。