不同剂量伊曲康唑制剂对犬血常规及肝肾功能的影响
2021-05-12关桐旭金圣子李婉莹
雷 磊,牟 婧,关桐旭,金圣子,李婉莹,刘 云
(东北农业大学动物医学学院/黑龙江省实验动物与比较医学重点实验室,哈尔滨150030)
伊曲康唑(itraconazole,ITZ)是一种具有广谱抗真菌活性的三唑类抗真菌药,被广泛应用于浅表及系统真菌感染的治疗。在兽医临床上,ITZ被用来治疗多种动物皮肤癣菌病、念珠菌病、马拉色菌病、隐球菌病、组织浆胞菌病[1]、曲霉菌病、芽生菌病和其他真菌感染,疗效显著。ITZ通过与真菌CYP底物结合位点相互作用,阻断羊毛甾醇14α-去甲基化,导致羊毛甾醇和其他14α-甲基甾醇在细胞膜上积累,真菌细胞膜的渗透性、膜结合酶活性和几丁质合成异常,最终真菌细胞死亡[2]。ITZ是一种弱碱性药物,水溶性极差,只能酸性条件下发生电离,这对剂型的开发和应用带来了不少的困难。其血浆蛋白结合率高达99%以上,具有亲脂性和亲角质性,相较于血浆,皮肤角质层、毛发、皮脂和组织器官中ITZ浓度更高,局部的高浓度药物更有利于皮肤浅表和肺部真菌感染的治疗。
羟丙基-β-环糊精(HP-β-CD)是一种淀粉经浸麻芽孢杆菌和其他细菌代谢的副产物,其分子具有内部疏水、外部亲水性的“筒状结构”;由于这种特殊结构和良好的安全性,许多药物制剂使用HP-β-CD作为药物搭载系统,如糖皮质激素、雌二醇、多肽、蛋白质和其他难溶性药物;其分子内部产生的脂溶性微环境,在适当的比例下,可以稳定搭载ITZ,复合物具有良好的水溶性,很大程度上解决了ITZ吸收度差的问题。
目前国内尚无兽用商品化伊曲康唑制剂,兽医临床应用大多为人用伊曲康唑或由兽医师配置的复方伊曲康唑。但人用伊曲康唑成本过高,复方伊曲康唑吸收度极差、生物利用度极低[3-4],不足以达到目标治疗浓度。因此,亟需开发一种适合兽医临床应用的伊曲康唑制剂。ITZ的给药方式主要有口服和静脉注射两种。但ITZ胶囊吸收不稳定,生物利用度低;口服液与胶囊相比,虽然在生物利用度方面有所提升,但两种口服药都会受到饮食、胃肠运动和肝肠首过效应的影响,产生较大的个体差异[5-6];静脉注射液虽然能在人体内达到良好的血药浓度和临床疗效,但对于兽医临床来说,成本过高且操作复杂,动物依从性差。皮下注射途径具有稳定的吸收特性、较高的生物利用度,且便于管理,适合兽医临床应用。
本试验对伊曲康唑环糊精制剂皮下注射途径给药的安全性进行探索,设置3个不同剂量(2.5 mg/kg、7.5 mg/kg和12.5 mg/kg)多次给药,对犬临床表现、血常规、血液生化、尿常规等进行评价,为开发简单、高效的兽用伊曲康唑制剂提供安全性依据。
1 材料与方法
1.1 材料
1.1.1 实验动物 健康成年比格犬32只,体重±10 kg,雄性,未去势,已免疫驱虫,由哈尔滨医科大学附属二院实验动物中心提供。饲料为全价日粮,不添加任何药物,自由饮水,饲养于东北农业大学动物医学学院临床教学医院。
1.1.2 主要试剂 伊曲康唑注射液(10 mg/mL),四川鼎尖动物药业有限责任公司产品。
1.1.3 主要仪器 动物型生化分析仪(D240V型),南京神州英诺华医疗科技有限公司产品;全自动血常规分析仪(MEK-7222K型),日本光电工业株式会社公司产品;尿液分析仪(VetLab UA型),美国IDEXX公司产品。
1.2 方法
1.2.1 剂量与分组 试验犬建立稳定,科学的生活制度。在标准实验条件下喂养14天适应环境并评价其健康状况。将健康犬进行称重、编号,随机分为4组,每组8只,体重大致相等。给药组分别按照2.5 mg/kg、7.5 mg/kg和12.5 mg/kg剂量,背部皮下多点注射,每点不超过0.25 mL,3日1次,连续注射7次。对照组注射等体积的生理盐水。于试验过程中第0、5、10、15、19天进行相关指标的观察和测定。
1.2.2 临床观察 试验期间观察动物的体温、体重、呼吸、行为、排粪、精神状态、运动、被毛、皮肤状态及饲料消耗量等是否有异常变化。
1.2.3 血常规检查 于试验过程中第0、5、10、15、19天,所有受试犬采血5 mL,使用肝素钠抗凝管抗凝。采血部位为前肢头静脉和后肢隐静脉,采血速度适当,采样结束后立刻用全自动血常规分析仪进行检查。
检测的血液学参数包括:白细胞计数,淋巴细胞计数,单核细胞计数,淋巴细胞百分比,单核细胞百分比;红细胞计数,血红蛋白浓度,平均红细胞血红蛋白浓度,红细胞压积,平均红细胞体积,红细胞分布宽度,平均红细胞血红蛋白量;血小板计数,平均血小板体积,血小板分布宽度和血小板压积。
1.2.4 血液生化检查 血常规检查后,立即对采集的血液进行离心(3 000 r/min,10 min),取上层血浆于-20℃保存备用。4℃融化后,使用动物生化分析仪进行血液生化检查。
检查的项目有谷草转氨酶(AST)、谷丙转氨酶(ALT)、碱性磷酸酶(ALP)、谷酰氨转移酶(GGT)、总蛋白(TP)、白蛋白(ALB)、总胆红素(DBIL)、直接胆红素(TBIL)、尿素(BUN)和肌酐(Cre)。
1.2.5 尿常规检查 于试验过程中第0、5、10、15、19天,以自然采集和导尿的形式采集部分受试犬的尿液,检测pH、比重、尿蛋白、尿糖、尿胆红素和尿酮。
1.2.6 数据分析 使用IBM SPSS Statistics 21,对组内和组间数据进行单因素方差分析(one-way ANOVA),比较差异性。
2 结果
2.1 临床观察
试验过程中所有受试犬体温、体重、呼吸、行为、精神、排便及饲料消耗量等无异常变化。中高剂量组部分注射部位肿胀、僵硬、痛疼,但无皮肤损伤和感染。在试验结束后2周内,该症状完全消失。
2.2 血常规检查
2.2.1 对红细胞相关指标的影响 低剂量组犬在第10天和第19天红细胞计数出现一过性降低;中剂量组犬在第15天红细胞压积轻度降低;高剂量组犬在第19天红细胞计数轻度降低。其他红细胞相关指标无明显变化。虽然给药组部分指标轻度变化,但均在正常范围内,无剂量和时间依赖性,结果见表1。

表1 伊曲康唑注射液对犬红细胞相关指标的影响
2.2.2 对白细胞相关指标的影响 低剂量组在试验第5天、第10天和第19天,中剂量组在第5天和第19天,高剂量组在第15天和第19天,白细胞计数升高,部分指标超出正常范围,试验过程中给药组部分单核细胞指标和淋巴细胞指标均有一定的变化,但无剂量和时间依赖性,且在停药后第5天相关异常指标均恢复正常。结果见表2。
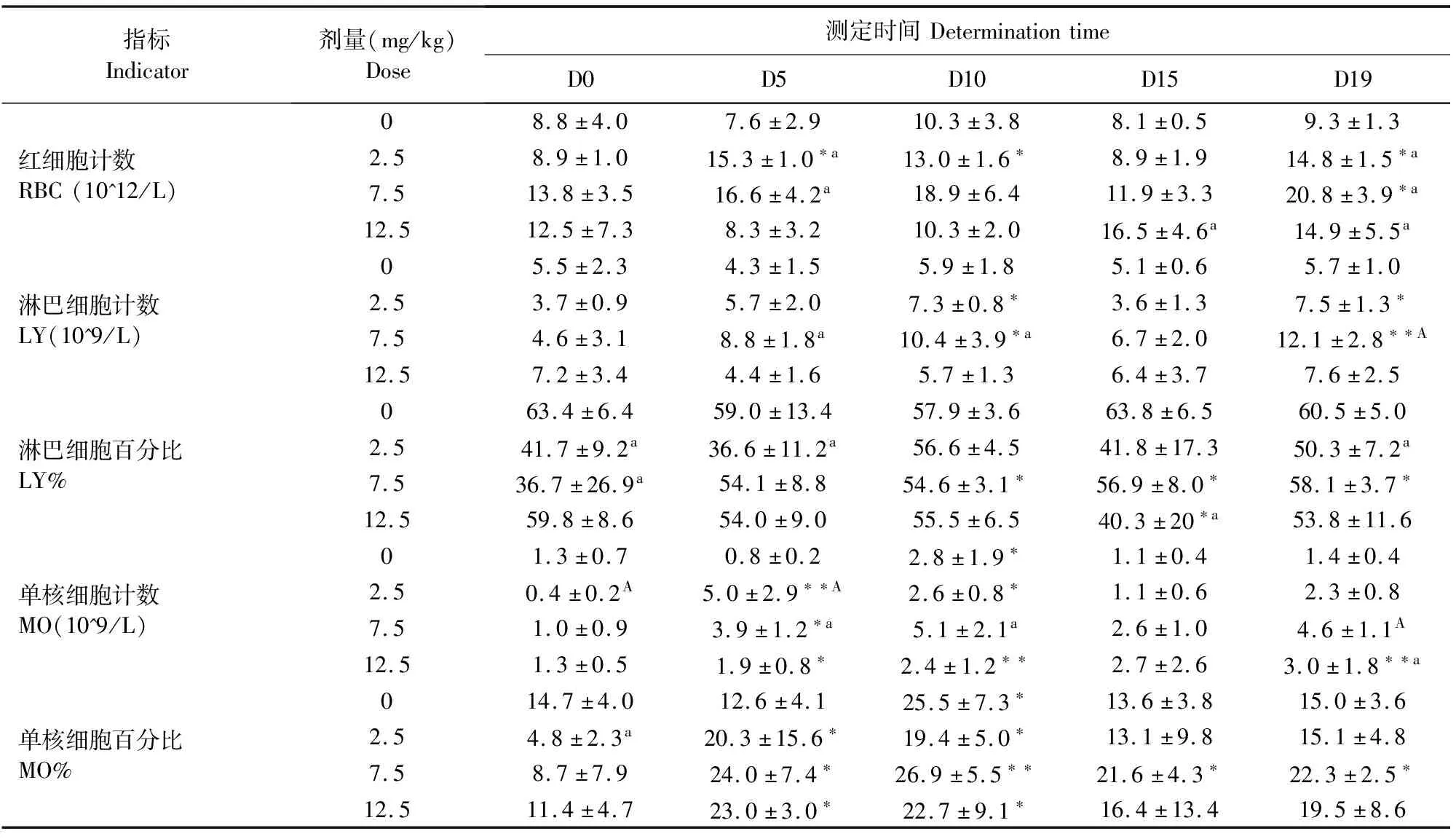
表2 伊曲康唑注射液对犬白细胞相关指标的影响
2.2.3 对血小板相关指标的影响 低剂量组和高剂量组犬血小板计数出现一过性升高,中高剂量组犬血小板平均体积出现一过性升高,但均在正常范围内,其他血小板相关指标无明显变化,无剂量和时间依赖性。结果见表3。

表3 伊曲康唑注射液对犬血小板相关指标的影响
2.3 血浆生化指标检查
2.3.1 对肝功能的影响 中高剂量组谷草转氨酶出现一过性升高或降低,虽然给药组总胆红素和直接胆红素出现较大幅度的变化,但与对照组相比并无明显异常,无剂量依赖性或时间依赖性,且都在正常生理范围内,无病理损伤意义。其他相关指标无明显变化。结果见表4。

表4 伊曲康唑注射液对犬肝功能指标的影响
2.3.2 对肾功能的影响 低高剂量组尿素出现一过性升高或降低,虽然3个给药组肌酐出现较大幅度的变化,但与对照组相比并无明显异常,无剂量依赖性或时间依赖性,且都在正常生理范围内,无病理损伤意义。结果见表5。

表5 伊曲康唑注射液对犬肾功能指标的影响
2.4 尿液检查
各组犬在试验过程中尿液颜色正常。3个给药组尿液pH出现一过性升高或降低,但均在正常范围内。尿比重无明显变化,PRO、GLU、BIL、KET呈阴性。结果见表6。

表6 伊曲康唑注射液对犬尿常规指标的影响
3 讨论
目前国内尚无批准使用的ITZ兽用制剂。虽然兽医临床上经常使用ITZ治疗犬猫浅表真菌感染,但其应用制剂多为人用胶囊或口服液,无法对其安全性进行统计与分析,在此之前,尚无系统、全面、客观的评价。
ITZ在肝脏广泛代谢,肝功能的变化是伊曲康唑毒性的一项重要的评价[7-8]。肝毒性通常定义为AST大于正常上限的3倍,ALP大于正常范围上限的2倍,或总胆红素大于正常范围上限的2倍[9]。具体毒性机制尚不清楚,但通常认为ITZ的肝毒性与长期、持续使用以及延长脉冲治疗有关[10-11]。本实验对犬进行临床检查及肝功能相关生化指标的检测,虽然给药组部分指标出现一过性升高或降低,但未发现这种变化具有剂量依赖性和时间依赖性,且均在正常范围之内,说明在试验设置的3个剂量下,犬肝脏具有良好的耐受性。
临床观察未发现犬出现尿液和肾功能相关指标异常,部分轻度的变化均在正常范围内。虽然有报道称皮下注射高剂量环糊精制剂导致试验鼠肾毒性增加[12],但在本试验中并未发现该变化,这可能与皮下注射剂量有关。临床常用的环糊精搭载的皮下注射药物如双氯芬酸钠和孕酮等显示出良好的安全性和耐受性[13],也可以说明环糊精作为皮下注射剂型的增溶剂,在注射剂量较低的情况下具有良好的安全性。普遍认为,ITZ的毒性与血药浓度有关。一项关于伊曲康唑浓度和毒性关系的研究中,阐明了伊曲康唑的血药浓度与不良反应的发生概率密切相关[14]。但这些不良反应的的症状都不威胁生命,且在停药或减少剂量后有所好转。
尽管该制剂对犬肝肾功能无影响,但在给药组均发现白细胞升高现象。在触诊过程中发现中高剂量组注射部位肿胀、僵硬、疼痛,但未发生坏死和血液循环障碍,这种症状在试验结束后两周内完全消失。剖检时发现,该部位皮下组织充血、增生、变硬,但皮肤结构无病理变化。剖检观察皮下注射部位无药物沉淀。低剂量组肿胀程度明显低于其他两组,无明显痛觉。这种现象可能与中高剂量组注射药物体积过大有关。由于该制剂比较黏稠,其辅料可能不容易吸收,持续刺激注射部位产生炎症反应。但在后续试验中发现,这种现象对ITZ成分的吸收并无影响。在停药后,肿胀症状明显好转,未产生不可逆的损伤。
伊曲康唑环糊精制剂皮下注射具有良好的吸收性,相较于口服制剂,不受食物和pH的影响,避免了肝肠首过效应,减小个体差异,便于达到稳定的目标药物浓度,胃肠耐受性好;与静脉注射液相比,操作简单,方便快捷,适合兽医临床应用。但该制剂也存在一定的缺点:①注射部位可能会发生无菌性炎症,注射液黏稠,体积相对较大;②在注射过程中,伴随一定的疼痛。为了解决以上两个问题,未来的研究中可以考虑开发更好的伊曲康唑增溶剂,提高药物浓度,减小注射体积;除此之外,可以考虑在制剂中添加局部麻醉药,减少注射操作中的痛疼,要注意添加的局麻药与环糊精之间的相互作用,确保局麻药能够正常发挥麻醉效果[15]。
总而言之,本试验对犬伊曲康唑-环糊精皮下注射液的安全性进行了系统的评价,结果表明该注射液具有良好的耐受性和安全性。相比于口服制剂和静脉注射液,该剂型具有稳定、方便、安全等优点,更适合兽医临床使用。由于本实验动物数量有限,其安全性和有效性还需在后续大规模动物临床试验中进行研究和验证。
