84消毒液与医用酒精的反应原理探究
2021-05-11翁雪香吴朝辉徐彦博王盈懿
翁雪香 吴朝辉 徐彦博 王盈懿

摘要: 围绕84消毒液和医用酒精混用能否引起氯气中毒的争论,从考察两者混合反应有无碱和氯气生成入手,设计系列实验进行求证;结合理论计算,讨论分析影响氯气逸出浓度的关键因素。实验结果发现,在84消毒液与医用酒精混合的初始阶段有少量氯气逸出,而体系中存在的酸性物质会促进Cl2的生成和逸出;当C2H5OH的氧化产物CH3CHO积累到一定浓度,CH3CHO与Cl2、 NaClO在强碱催化下可发生卤仿反应。
关键词: 84消毒液; 医用酒精; 反应原理; 实验探究
文章编号: 1005-6629(2021)03-0074-06
中图分类号: G633.8
文献标识码: B
1 问题提出
2019年底暴发的新型冠状病毒性肺炎对生产生活带来了巨大冲击。为消灭病毒、战胜疫情,卫生防疫部门要求用医用酒精、84消毒液等做好个人与环境的消杀。关于两种消毒剂使用的注意事项,一些自媒体给出了以下两种说法。
说法一: 84消毒液与医用酒精混合可产生Cl2。人吸入Cl2后易感染呼吸道和肺部,导致支气管炎和肺水肿,吸入Cl2量过大会导致心脏骤停。所以84消毒液和医用酒精切不可混用。
说法二: 不会产生氯气。为稳定ClO-,84消毒液中添加了少量NaOH。强碱性条件抑制Cl2逸出。酒精和84消毒液混合,可能发生反应: NaClO+C2H5OHNaCl+CH3CHO+H2O,生成没有杀菌能力的乙醛。幸好这个反应速率很慢。另外,乙醛可能会被NaClO氧化成乙酸或者发生卤仿反应。
我们还发现,浙江某市的高三适应性试卷根据第一种说法命制了一道模拟试题[1]。
某兴趣小组为了探究84消毒液(主要成分是NaClO)与酒精混合是否存在安全隐患,利用图1所示装置进行实验。
请回答:
(1) 三颈烧瓶中出现黄绿色气体,请写出相应的化学方程式 。(乙醇氧化为乙醛)
试题以下部分省略。
参考答案: (1) 2NaClO+CH3CH2OHCH3CHO+2NaOH+Cl2↑(式①)。
参考答案公布后,立即引发了学生的质疑与讨论,形成了多种不同的观点。
观点一 如果考虑Cl2与NaOH的后續反应,可得:
ClO-+C2H5OHCl-+CH3CHO+H2O(式②);
式②即上文说法二中提及的反应原理。
观点二 CH3CHO可能被Cl2氧化:
CH3CHO+Cl2+H2OCH3COOH+2H++2Cl-(式③);
生成的HCl再与体系中的NaOH反应,与式①、 ③耦合可得:
2ClO-+CH3CH2OHCH3COOH+2Cl-+H2O(式④);
强氧化性的NaClO也可能将CH3CHO氧化:
CH3CHO+ClO-CH3COOH+Cl-;
与式②耦合,同样得式④。
观点三 CH3COOH与ClO-之间能发生复分解反应,与式④耦合可得:
3ClO-+CH3CH2OHCH3COO-+2Cl-+HClO+H2O(式⑤)。
观点四 在CH3COOH作用下,Cl-、 ClO-会生成Cl2,与式④耦合可得:
2CH3CH2OH+5NaClOCl2↑+2CH3COONa+3NaCl+3H2O(式⑥)。
也有赞同参考答案的:“Cl2生成后脱离溶液,与NaOH不能充分接触,Cl2与NaOH就同时生成了”。
84消毒液和医用酒精混用会不会造成Cl2中毒?模拟试题是实验结果的投射还是命题者的主观判断?学生对参考答案的质疑合不合理?为解答这些疑问,我们设计如下系列实验以一探究竟。
2 实验探究
2.1 试剂与仪器
试剂: 84消毒液(有效氯含量8~10.5g/L)、医用酒精(酒精含量70%~77%)、氢氧化钠固体、2mol/L盐酸、40 wt%乙醛
仪器: PHS-3C型pH计、E-201-C型pH复合电极、恒温磁力搅拌器
2.2 实验过程与分析
梳理各个方程式的产物后,决定围绕式①设计实验: 用pH计实时检测混合液的pH变化,用湿润的KI-淀粉试纸检验有无Cl2生成。试剂用量控制为84消毒液10mL[经计算c(NaClO)为0.22~0.30mol·L-1]、医用酒精5mL[经计算c(C2H5OH)≈12.2~13.4mol·L-1]。酒精过量的目的是提高式①的比例。
每个实验均平行三次,实验数据取平均值。为了减少反应热效应对实验的影响,溶液混合采用缓慢滴加方式: 10min左右将所滴加液体全部加完。除已指明反应温度的实验外,均恒温27℃。
2.2.1 溶液pH变化的探究
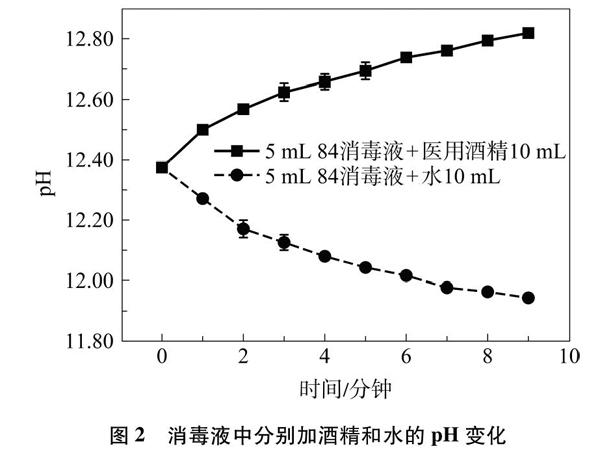
[实验1]取2份5mL 84消毒液,缓慢滴加医用酒精或蒸馏水各10mL,用pH计检测pH变化(每分钟记录一次数据),结果见图2。滴加完成后,停止测pH,装置加盖密封,盖子内侧贴KI-淀粉试纸,观察试纸颜色变化。试纸颜色变化情况见下文。
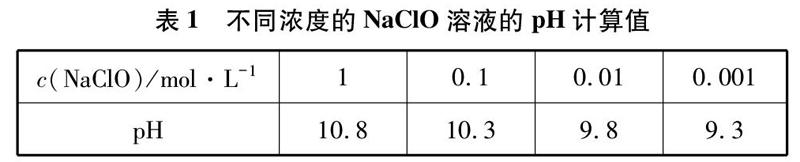
84消毒液的有效成分是NaClO,其浓度为0.22~0.30mol·L-1。NaClO会水解,由Ka(HClO)=2.8×10-8得Kh(NaClO)=KwKa=3.6×10-7,计算不同浓度的NaClO溶液的理论pH,如表1所示。由表1推测,84消毒液的pH应小于10.8,而实验1测得pH初始值为12.37(见图2),这就证实了“说法二”中的“为稳定ClO-,84消毒液中添加了少量NaOH”的说法。
用NaOH固体吸收酒精中溶解的CO2。调pH至8是防止乙醇中c(OH-)过高抑制Cl2生成。试纸在50s时变蓝,41min时褪色。
对比实验4、实验5的褪色时间,说明医用酒精与84消毒液混合会生成Cl2、乙醇中溶解的CO2会促进Cl2生成。从褪色时间以及在10min、 20min时闻容器内气体的气味,无明显刺激性,说明生成Cl2的速率與浓度并不大。
2.2.3 消毒液与乙醛、乙酸的反应
[实验6]取2份10mL质量分数为40%的乙醛溶液与5mL 84消毒液,分别缓慢地相互滴加,用pH计检测溶液pH变化(每隔一分钟记录一次数据),结果见图5。持续观察溶液颜色变化,结果见表2。滴加完成后,将装置密封,盖子内侧贴KI-淀粉试纸,观察试纸变色情况。
实验6的结果有: (1)无论是消毒液中加入乙醛,还是乙醛中加入消毒液,溶液皆是逐渐变黄色,最后都有黄色油状液滴析出,只是产生这些变化的时间不同(见表2);(2)容器中的KI-淀粉试纸始终未见变色。甚至取黄色溶液直接滴在湿润的试纸上,试纸也不变色;(3)两份溶液的最终pH相差不大(见图5)。由上述实验现象,可得出如下推论:
第一,CH3CHO在NaClO的碱溶液作用下发生卤仿反应,油状液体应是CHCl3。在碱的催化下,当乙醛的一个α-H被氯原子取代后,由于氯原子的吸电子作用,使得CH3CHO的α-H的酸性增强,更易被氯原子取代。所以在碱的催化下,乙醛的三个α-H会全部被氯原子取代生成三氯乙醛。三氯乙醛在碱溶液中不稳定,与NaOH反应生成氯仿和甲酸钠。方程式如下[5,6]:
CH3CHO+3NaClOCCl3CHO+3NaOH
CCl3CHO+NaOHCHCl3+HCOONa
第二,两种滴加方式的差异主要是试纸变色的时间(见表2)。参照碱性条件下丙酮的碘代反应,乙醛的氯代反应的速率与Cl2浓度无关,而与乙醛、碱的浓度成正比,即v=kc(CH3CHO)c(OH-)[7]。分析pH曲线与所用试剂的浓度,在混合的前几分钟,CH3CHO与NaClO的反应速率主要由c(OH-)决定,所以消毒液中缓慢加入乙醛,c(OH-)大,反应速率相对较快,溶液更早出现黄色。
[实验7] 取10mL 84消毒液于锥形瓶,滴加稀CH3COOH溶液(配制方法: 取冰醋酸1mL,加水稀释至10mL),每加完1滴管就加塞子密封,持续振荡1min,闻气体的气味(实验时室温为35℃)。
溶液中无明显气泡产生,锥形瓶内气体未显黄绿色。加至4滴管,刺激性气味明显加重。将锥形瓶密封放置10min,气体的气味很刺鼻。说明在CH3COOH作用下,消毒液释放出的Cl2足以被感官辨识。
Cl2(g)+2OH-(aq)Cl-(aq)+ClO-(aq)+H2O(l) Kθ1=7.7×1015(25℃)
CH3COOHCH3COO-+H+ Ka=1.8×10-5(25℃)
式⑥的平衡常数K2=K2a×K2w/Kθ1=421,反应能自发进行。实验7也反向证实实验6中没有CH3COOH生成。虽然从理论上看,碱性条件下NaClO[φθB(ClO-/Cl-)=0.81V]可以氧化CH3CHO[φθB(CH3COOH/CH3CHO)=-1.22V],但可能这个反应的活化能比较大。
3 结论与反思
综合上述实验探究及理论计算的结果,我们得出以下结论:
(1) 84消毒液与医用酒精混合会有Cl2逸出。NaClO氧化C2H5OH时,会生成Cl2,而NaOH溶液吸收Cl2的速率不快[8],所以有Cl2从混合液中逸出。
(2) 消毒液与医用酒精反应生成的Cl2的浓度较低。一是随着C2H5OH和NaClO反应的进行,产物NaOH浓度增大,吸收Cl2的能力增强。二是在碱催化下,Cl2会与CH3CHO发生卤仿反应。三是碱性条件下,CH3CHO不会被NaClO氧化成CH3COOH(上述“说法二”中的相关叙述不正确),也就没有出现CH3COOH促进Cl2生成的情形。Cl2只是在两种溶液刚混合时有少量生成,所以模拟试题中“三颈烧瓶中出现黄绿色气体”的说法值得商榷。
(3) 空气中的CO2、乙醇中溶解的CO2均会增大Cl2的浓度,导致Cl2浓度超出安全限度。需提醒的是,使用84消毒液进行室内消毒时,因水膜表面积大,与空气接触充分,生成Cl2的速率与浓度都明显增大,所以消毒后不久就可闻到较刺鼻的刺激性气味。从安全角度考虑,在一个较封闭的室内使用84消毒液时,一是要对84消毒液原液按要求比例进行稀释(1∶100);二是消毒结束后要用清水重新擦拭消毒区域,并保持通风以降低室内的Cl2浓度。上述“说法一”虽然说消毒液与酒精混合有Cl2生成,但归因有误。
(4) 卤仿反应是影响Cl2逸出量的关键因素。CH3CHO与Cl2在碱催化下较快地进行卤仿反应,而且发生卤仿反应时消耗的Cl2量大于C2H5OH氧化阶段生成的Cl2量,需要NaClO作为氯原子的补充来源。所以当CH3CHO的浓度积累到足以发生卤仿反应时,混合液就不再有Cl2逸出。所以消毒液与酒精混合的主要反应如下(不考虑其他副反应):
2NaClO+CH3CH2OHCH3CHO+2NaOH+Cl2↑
CH3CHO+3Cl2+3NaOHCCl3CHO+3NaCl+3H2O
CH3CHO+3NaClOCCl3CHO+3NaOH
CCl3CHO在碱性条件下水解,故总反应式可表示为:
C2H5OH+4NaClOCHCl3+HCOONa+2NaOH+NaCl+H2O
工业上可用乙醇代替乙醛或丙酮制取氯仿[9],证实了上述过程的可能性。在本文选择的实验条件下,因氧化反应与卤仿反应的速率慢,生成的CHCl3少,CHCl3溶解在过量C2H5OH中,所以实验1、实验3均未观察到分层现象。
此次求证过程让我们感受到了化学反应的复杂性: 既有遵从化学原理和规律的共性的一面,又有具体问题具体分析的个性的一面。中学教师若欲利用陌生情境命制试题时,有必要从物质个性的角度进行实验求证,以获得第一手资料,在实验事实的指导下命制试题,从而提高试题的科学性。日常教学碰到疑难问题不足为怪,但需要我们激活好奇心以一探究竟,在探索中提升自己的化学学科专业素养。
参考文献:
[1]浙江省选考科目考试绍兴市适应性试卷(2020年4月)[EB/OL]. https://wenku.baidu.com/view/64e2aa3833b765ce0508763231126edb6e1a7665.html. [2020-4-21].
[2]王祖浩主编. 普通高中课程标准实验教科书·实验化学(选修)(第二版)[M]. 南京: 江苏教育出版社, 2009: 57.
[3]杜强. 氯气[EB/OL]. https://baike.baidu.com/item/%E6%B0%AF%E6%B0%94/1759805?fr=aladdin. [2016-1-16].
[4]周金汉, 王成羽. 二氧化碳在乙醇水溶液中的溶解度[J]. 化学工程, 1996, (1): 63~67.
[5]邢其毅, 裴伟伟, 徐瑞秋等. 基础有机化学(第4版)[M]. 北京: 北京大学出版社, 2016: 481.
[6]姚映钦. 有机化学[M]. 北京: 化学工业出版社, 2008: 238.
[7][9]王积涛, 王永梅, 张宝申等. 有机化学(第三版)[M]. 天津: 南开大学出版社, 2009: 372, 373.
[8]张红卫. 用氨水吸收氯气尾气[J]. 化学教学, 2013, (9): 44~45.
