医用外科口罩和防护口罩生物气溶胶过滤效率的评价
2021-05-08刘克洋刘思敏黄永富岳卫华
刘克洋,刘思敏,王 丹,张 娟,黄永富,李 鹏,岳卫华*
(1.北京市医疗器械检验所材料一室,北京101111;2.北京化工大学有机无机复合材料国家重点实验室,北京100029)
0 引言
2020 年3 月11 日,世界卫生组织(World Health Organization,WHO)宣布新型冠状病毒肺炎疫情构成全球大流行[1]。根据WHO 官方报告,截至2020 年9 月9 日,全球共有确诊患者27 486 960 例,死亡894 983 例[2]。疫情的暴发导致医用口罩、防护服等防疫物资的全球性供应短缺。口罩作为不可或缺的个人防护用品,在疫情防控中发挥了重要作用。保持社交距离和佩戴口罩也是中国在短时间内取得抗疫胜利的重要经验[3]。北京市医疗器械检验所作为医用生物防护产品标准化技术归口单位,自非典型肺炎疫情之后先后制订了有关医用防护口罩和外科口罩检测的国家和行业标准。本研究主要对医用外科口罩、防护口罩的颗粒过滤效率(particle filtration efficiency,PFE)、细菌过滤效率(bacterial filtration efficiency,BFE)和病毒过滤效率(viral filtration efficiency,VFE)进行评价,以期为医用外科口罩、防护口罩的科学使用和标准的修订提供数据支撑。
1 材料与方法
1.1 材料
1.1.1 菌株
金黄色葡萄球菌(ATCC 6538)、大肠杆菌(ATCC 13706)和大肠杆菌噬菌体Phi-X174(ATCC 13706-B1),均购自美国Microbiologics 公司。
1.1.2 主要试剂、仪器
试剂:1%蛋白胨溶液(每升水含蛋白胨10 g、氯化钠5 g,pH 值为7.0~7.5),胰蛋白胨大豆琼脂(tryptonesoyagar,TSA)(90mm 平板含27~30 mL 培养基),噬菌体营养肉汤、上层和下层营养琼脂培养基[4]。
仪器:TSI 8130A 自动滤料分析仪(美国TSI 公司),ZR-1000 细菌过滤效率实验系统、Anderson 6级采样器、ZR-C01 型和ZR-C01A 型气溶胶发生器(青岛众瑞智能仪器有限公司),HRH-WAG6 型6 孔液体气溶胶发生器(北京慧荣和科技有限公司)。
1.2 实验方法
1.2.1 医用外科口罩对不同粒径细菌气溶胶的过滤效率研究
选取5 种不同品牌的医用外科口罩(品牌A、B、C、D、E),每种品牌口罩至少选取3 个。利用TSI 8130A自动滤料分析仪测试PFE,实验方法参照行业标准YY 0469—2011《医用外科口罩》中5.6.2 部分[5]。同一个口罩测试PFE 后,再进行BFE 检测。BFE 实验方法参照YY 0469—2011 中的附录B,分别选择ZRC01A 型气溶胶发生器和HRH-WAG6 型6 孔液体气溶胶发生器,用于产生2 种不同平均颗粒直径(mean particle size,MPS)的细菌气溶胶。喷雾液选择1%蛋白胨溶液,调整喷雾液中细菌浓度使阳性对照菌数控制在1 700~3 000 cfu;Anderson 6 级采样器收集到的细菌数目只校正3~6 级,根据各级菌数计算MPS,计算方法参考EN14683—2019[6]。
1.2.2 医用外科口罩PFE 与BFE 的相关性研究
1.2.2.1 不同测试流量下医用外科口罩PFE 的变化
选取3 种不同品牌(A、B、C)医用外科口罩,每种品牌口罩至少选取3 个,每个口罩分别在30、85和95 L/min 流量条件下检测PFE,实验方法参照YY 0469—2011 的5.6.2 部分。
1.2.2.2 PFE 与BFE 的相关性
分别选择不同品牌的新医用外科口罩和经实际佩戴过一段时间的医用外科口罩,检测PFE 和BFE,测试方法同1.2.1 章节。所选择口罩具有3 层结构(内外侧为2 层无纺布、中间过滤层为熔喷布),PFE 为25%~90%且在不同品牌之间存在梯度差异。
1.2.3 医用外科口罩BFE 与VFE 的差异研究
选择3 种经检测合格的不同品牌(品牌A、B、C)医用外科口罩(BFE>95%),每种品牌口罩同批次至少选取3 个,同一个口罩检测PFE 后,再进行BFE或者VFE 的检测。BFE 测试方法同1.2.1 章节,VFE测试方法同BFE 测试方法。均采用HRH-WAG6 型6 孔液体气溶胶发生器,喷雾液均选择1%蛋白胨溶液,并采用含有同等厚度TSA 培养基的平板进行细菌和病毒气溶胶采样。大肠杆菌噬菌体Phi-X174扩增方法参考标准YY/T 1497—2016[4],用1%蛋白胨溶液稀释至合适浓度使阳性对照噬菌斑数控制在1 700~3 000 pfu。
VFE 测试中大肠杆菌噬菌体检测方法:(1)Anderson 6 级采样器采样完成后,将平板取出,标记各级编号;(2)准备无菌试管,向其中加入约200 μL 对数期宿主大肠杆菌,再加入约5 mL 45 ℃左右0.7%上层营养琼脂培养基混合均匀后,迅速倒入已编号的各层平板;(3)(36±1)℃培养约8 h,在噬菌斑混合前计数,各级噬菌斑数目校正方法同BFE 实验。
1.2.4 防护口罩的PFE 与VFE 研究
选择市面上3 种不同品牌型号的防护口罩(2 种颗粒防护口罩、1 种医用防护口罩),每种口罩至少选择3 个,采用TSI 8130A 自动滤料分析仪在85 L/min 流量条件下检测PFE,方法参照GB 19083—2010[7]。VFE 检测方法参照YY/T 1497—2016,气溶胶发生器为ZR-C01 型,采用1%蛋白胨溶液作为喷雾液,将大肠杆菌噬菌体悬液稀释至合适浓度使阳性对照大肠杆菌噬菌体数目至少达到106pfu。阳性对照组选用AGI-30 采样器,样品组分别选择AGI-30 采样器和Anderson 6 级采样器收集过滤后的病毒气溶胶颗粒。采用噬菌体营养肉汤作为采样液,采样流量为14 L/min,为减少起泡,AGI-30采样器装液量为15 mL。
阳性对照收集完成后,测量采样液体积,采用双层平板法测试大肠杆菌噬菌体滴度。当样品组采样器为AGI-30时,采样结束后测量采样液体积。取500 μL 采样液与200 μL 对数期宿主大肠杆菌混合,加入约5 mL 45 ℃左右0.7%上层营养琼脂培养基混合均匀后,迅速倒入已含下层营养琼脂的培养基中。样品组采样器为Anderson 6 级采样器时,大肠杆菌噬菌体检测方法同1.2.3 章节。
1.2.5 实际佩戴+热水浸泡处理后医用外科口罩PFE 和BFE 的变化研究
1.2.5.1 热水浸泡对医用外科口罩的消毒效果
选择A 品牌无菌级医用外科口罩,由6 名北京市医疗器械检验所工作人员(3 名男性、3 名女性)分别正常佩戴该品牌口罩8 h。佩戴结束后,按照YY 0469—2011 中要求分别用营养琼脂和沙氏琼脂培养基检测细菌和真菌菌落总数。次日,由同样6 人佩戴同一品牌口罩8 h。提前准备6 个干净的烧杯,加入蒸馏水,放入恒温水浴锅中,设置温度并用热电偶测试确保烧杯中水温达到65 ℃。将佩戴后的口罩分别放入各烧杯中,浸入65 ℃水中作用30 min。结束后,将口罩取出,按照相同的方法检测细菌和真菌菌落总数。取烧杯中水样,检测细菌和真菌数目,作为阴性对照。
1.2.5.2 重复使用处理后医用外科口罩PFE 和BFE的变化
实验流程如图1 所示。选择A 品牌无菌级医用外科口罩,由6 名北京市医疗器械检验所工作人员(3 名男性、3 名女性)分别正常佩戴该品牌口罩8 h。佩戴结束后,在30 L/min 流量条件下检测每个口罩的PFE,然后放入65 ℃热水中作用30 min 后取出自然晾干。晾干后再测试每个口罩的PFE,观察PFE的变化。

图1 医用外科口罩重复使用处理及检测示意图
重新取6 个新口罩,由同样6 人分别佩戴8 h后,按使用者姓名编号,放入65 ℃热水中作用30 min后取出自然晾干。次日,6 人按各自标号继续佩戴对应的6 个口罩8 h。结束后,在30 L/min 流量条件下检测每个口罩的PFE,之后放入65 ℃热水中作用30 min 后取出自然晾干。晾干后再测试每个口罩的PFE 和BFE,观察过滤效率变化。
重新取6 个新口罩,由同样6 人分别按照佩戴8 h—热水浸泡处理—晾干—继续佩戴8 h—热水浸泡处理—晾干—继续佩戴8 h 的顺序进行实验。结束后,在30 L/min 流量条件下检测每个口罩的PFE,之后放入65 ℃热水中作用30 min 后取出自然晾干。晾干后再测试每个口罩的PFE 和BFE,观察过滤效率变化。
采用新医用外科口罩作为阳性对照,未经实际佩戴,分别做1 次、2 次和3 次热水浸泡处理,并检测过滤效率变化。
PFE 和BFE 检测方法同1.2.1 章节,BFE 实验选择HRH-WAG6 型6 孔液体气溶胶发生器。
1.3 统计学方法
采用SAS 8.2 软件进行统计学分析,P<0.05 表示有统计学差异。医用外科口罩的PFE 与BFE 相关性采用两变量简单线性相关分析法,BFE 与VFE 的差异采用单因素定量资料成组设计t检验进行统计分析。
2 结果
2.1 医用外科口罩对不同粒径细菌气溶胶的过滤效率研究结果
HRH-WAG6 型6 孔液体气溶胶发生器和ZRC01A 型气溶胶发生器在ZR-1000 型细菌过滤效率实验系统中分别能产生MPS 约为2 μm(2.07~2.21 μm)和约为3 μm(2.81~2.92 μm)的细菌气溶胶颗粒。实验结果如图2 所示。从选取的5 种品牌的医用外科口罩BFE 差异结果来看,口罩对于MPS 约为3 μm 的BFE 比MPS 约为2 μm 的BFE 高1%~5%,口罩的PFE 越高,2 种MPS 下的BFE 差距越小。取几组采样数据,利用累积概率法估算空气动力学中值直径(median aerodynamic diameter,MAD)和几何标准偏差(geometric standard deviation,GSD)[8],并与MPS 进行比较,结果详见表1,可知MAD 比MPS 低0.5~1.0 μm。
2.2 医用外科口罩PFE 与BFE 的相关性研究结果
2.2.1 不同流量下医用外科口罩PFE 的变化
在3 种不同流量条件下医用外科口罩的PFE结果详见表2。由表2 可知,流量越高,PFE 越低,不同品牌口罩随流量的增高,PFE 的降低值不同。
2.2.2 医用外科口罩PFE 与BFE 的相关性
医用外科口罩PEE 与BFE 的检测结果与相关性分析结果如图3、4 所示。
采用HRH-WAG6 型6 孔液体气溶胶发生器产生MPS 约为2 μm 的细菌气溶胶,选取8 种不同过滤能力的新口罩检测,实验结果如图3(a)所示。结果表明,在PFE<60%的29 个口罩中,27 个口罩的BFE<95%,占比93%。两变量简单线性相关分析结果表明,BFE 与PFE 存在相关性(r=0.819 64,P<0.000 1),相关系数R2=0.671 8,如图4(a)所示。

图2 5 种不同品牌医用外科口罩在2 种MPS 检测条件下的BFE 差异
用ZR-C01A 型气溶胶发生器产生MPS 约为3 μm 的细菌气溶胶,选取5 种不同过滤能力的新口罩检测,实验结果如图3(b)所示。结果表明,PFE<60%的口罩,BFE 均小于98%。两变量简单线性相关分析结果表明,BFE 与PFE 存在相关性(r=0.881 19,P<0.000 1),相关系数R2=0.776 5,如图4(b)所示。
收集实际佩戴过一段时间或佩戴后经热水处理的医用外科口罩,研究其对MPS 约为2 μm 的细菌气溶胶的BFE,结果如图3(c)所示。结果表明,PFE<80%的16 个口罩,BFE 均小于95%。两变量简单线性相关分析结果呈现出较好的相关性(r=0.955 22,P<0.000 1),相关系数R2=0.912 4,如图4(c)所示。

表1 MPS 与MAD 及GSD 的比较

表2 医用外科口罩在不同流量下PFE 的实验结果(x¯±s)单位:%

图3 医用外科口罩的PFE 与BFE 检测结果
2.3 医用外科口罩BFE 与VFE 的差异研究结果
实验结果表明,对于MPS 约2 μm 的生物气溶胶颗粒,医用外科口罩的VFE 略低于BFE,相差0.6%~1.7%,如图5 所示。单因素定量资料成组设计t检验结果显示,2 种数值差异具有统计学意义(品牌A:t=10.72,P=0.007 8<0.05;品牌B:t=5.98,P=0.0039<0.05;品牌C:t=6.87,P=0.002 3<0.05)。虽然BFE 与VFE 实验采用同一种发生器,生物气溶胶MPS 均在2 μm 左右,但在Anderson 6 级采样器上分布不同,VFE 实验中大肠杆菌噬菌体气溶胶颗粒在第6 级的数目百分比高于BFE 实验上的第6 级百分比,相差5%~9%,详见表3。

图4 医用外科口罩的PFE 与BFE 的相关性分析

图5 医用外科口罩的BFE 与VFE 差异
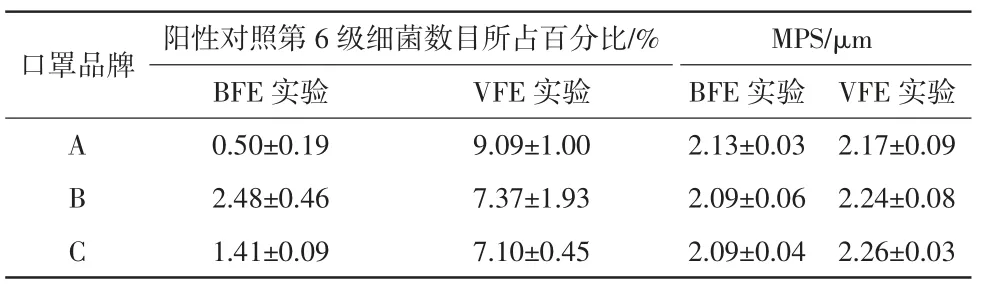
表3 不同品牌医用外科口罩的BFE 与VFE 实验结果(x¯±s)
2.4 防护口罩的PFE 与VFE 研究结果
3 种防护口罩的PFE 结果详见表4。3 种防护口罩对大肠杆菌噬菌体Phi-X174 气溶胶的VFE 均大于99.98%,其中3M 1860>3M 9501>纳通MC。3 种不同防护口罩的VFE 结果详见表5。由表5 可知,PFE越高,VFE 越高。
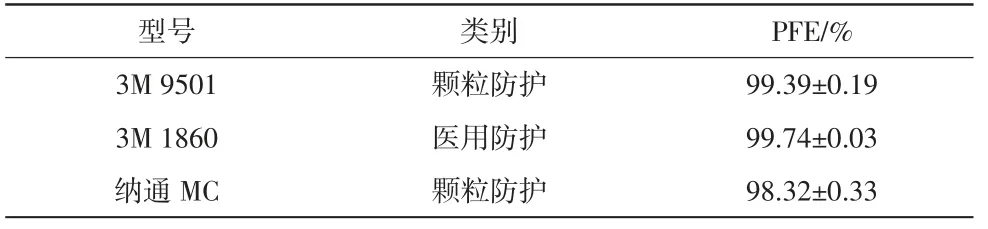
表4 3 种不同型号防护口罩的PFE 检测结果(x¯±s)
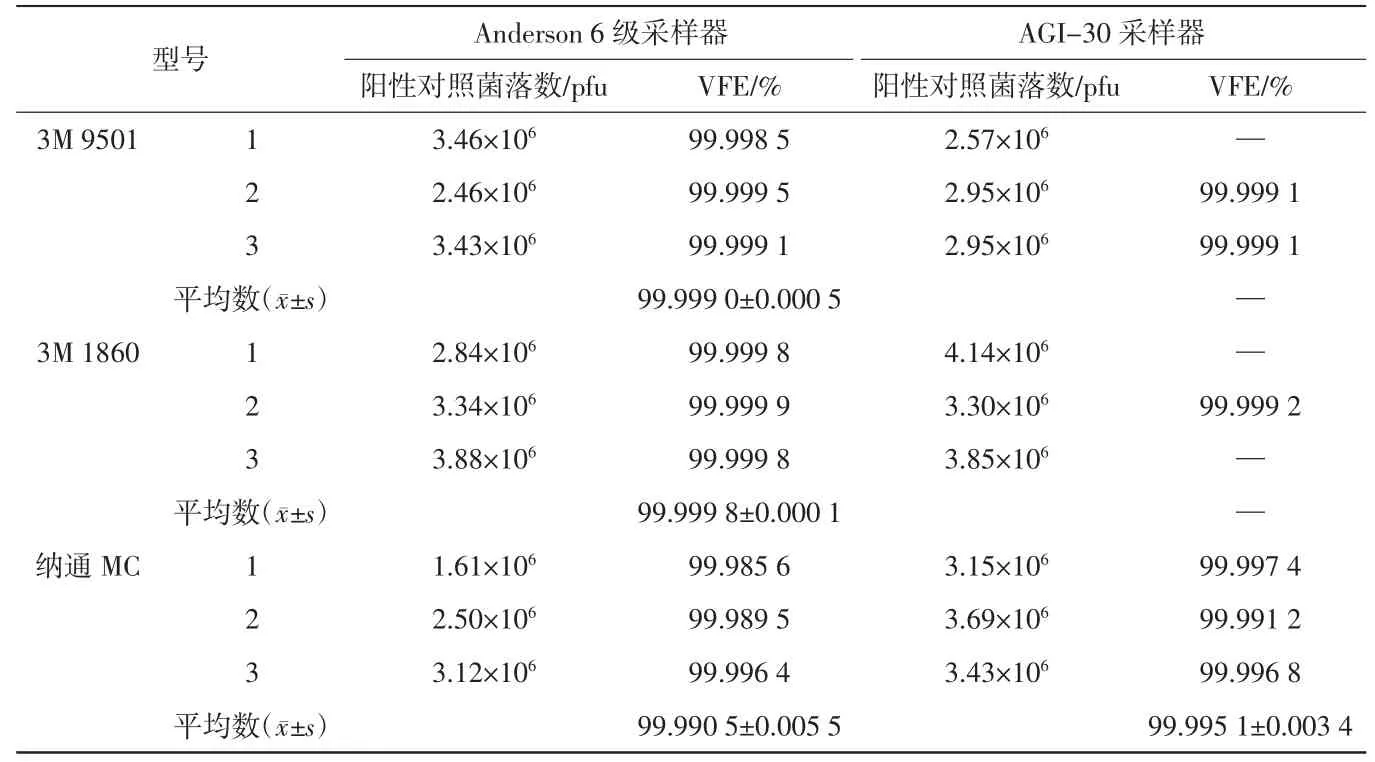
表5 3 种不同型号防护口罩的VFE 检测结果
2.5 实际佩戴+热水浸泡处理后医用外科口罩PFE和BFE 的变化研究结果
2.5.1 热水浸泡对医用外科口罩的消毒效果
实际佩戴8 h 后,口罩上的微生物数目因人而异,实验结果详见表6。由表6 可知,细菌数目可达1.42×104~5.56×104cfu/g,真菌数目为0.80×102~1.33×104cfu/g。经65 ℃热水浸泡30 min后,细菌数目降低至0~50 cfu/g,减少了至少3 个数量级,真菌数目降低至0~20 cfu/g,细菌和真菌总数降低至0~60 cfu/g。阴性对照组无微生物检出。
2.5.2 重复使用处理后医用外科口罩PFE 和BFE 的变化
对医用外科口罩进行实际佩戴和热水浸泡处理后,PFE 和BFE 的变化详见表7。口罩佩戴8 h 后,热水浸泡处理前除一个人的口罩PFE 降低至85%外,其余与新口罩PFE 相比均无明显变化(新口罩PFE 约为93%)。热水浸泡处理后,与处理前相比,PFE 降低9%~22%。经过2 个循环的佩戴8 h+热水浸泡处理后,口罩PFE 降低至60.24%~86.81%,BFE 为90.90%~97.97%。经过3 个循环的佩戴8 h+热水浸泡处理,PFE 降低至49.06%~76.11%,BFE 为86.12%~94.15%。新口罩未经佩戴,但经过3次热水消毒程序后,PFE 仍大于90%。
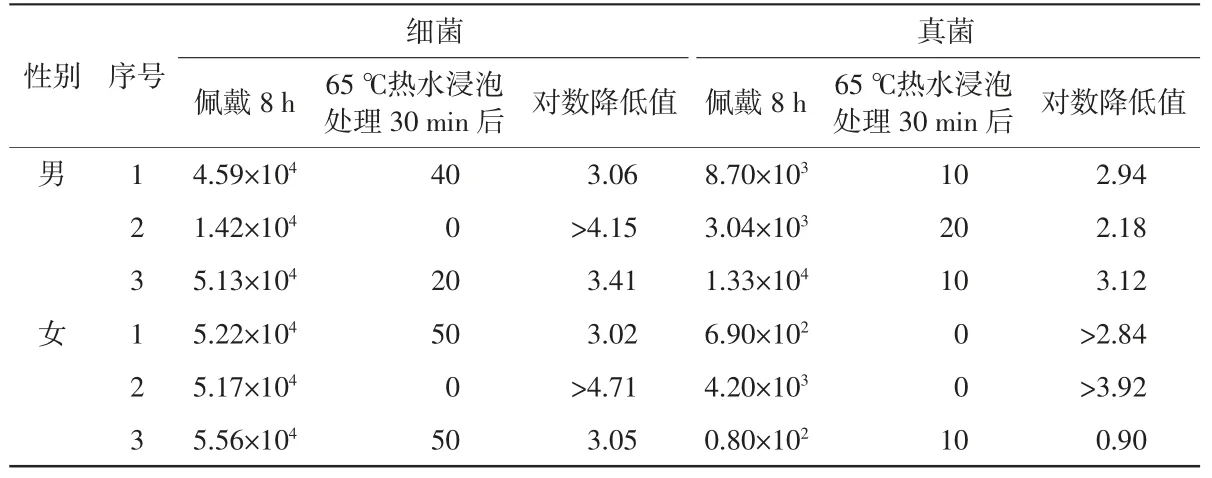
表6 热水浸泡处理对医用外科口罩的消毒效果单位:cfu/g
3 讨论
我国医用外科口罩标准YY 0469—2011、欧洲医用外科口罩标准EN 14683—2019 和美国口罩材料标准ASTM F2101-19[9]均要求进行BFE 测试时细菌气溶胶MPS 应为(3±0.3)μm。MPS 反映的空气动力学属性与PFE 测试时常用的空气动力学MAD(约0.3 μm)不同。根据MPS 计算公式,其实质上为Anderson 6 级采样器各级有效截留直径与各级数目所占百分比的乘积之和,是根据Anderson 采样器的截留能力来间接反映粒子的大小。而MAD和GSD 更适合描述气溶胶粒子的空气动力学属性和分布特点,不依赖于某个特定的采样器。在假定粒子符合对数正态分布的条件下,可根据Anderson 采样器的采样结果估算MAD 和GSD。表1结果表明,MAD 小于MPS。多数情况下,气溶胶粒子的MAD 越大,对应的Anderson 采样器MPS 越大。医用外科口罩标准将MPS 定为3 μm,主要是由医用外科口罩用于防喷溅、近距离飞沫传播的特点决定的。本研究通过使用不同的气溶胶发生器来改变MPS,结果表明MPS 越大,口罩的BFE 越高。MPS 为3 μm 条件下的BFE 与2 μm 条件下的BFE 差值随着口罩PFE 的提高而缩小。

表7 医用外科口罩经佩戴和热水浸泡处理前后过滤效率的变化
PFE 是针对最易穿透直径进行检测,是评价口罩滤材性能的核心指标。欧洲标准EN 14683—2019对BFE 有要求,对PFE 无要求,而美国标准ASTM 2100-19[10]要求医用外科口罩所用材料对0.1 μm 乳胶球的PFE 应大于95%。我国标准YY 0469—2011规定,PFE 应大于30%。口罩滤材的PFE 越高,BFE越高。PFE 检测比BFE 检测省时省力,能帮助检验机构或制造商快速鉴别材料优劣,但无法根据PFE值对BFE 进行准确预测,二者差异因口罩品牌、型号或批号等不同而呈现不同的规律,与电荷载量、存储条件等因素有关。本研究对医用外科口罩的PFE和BFE 进行相关性分析,同时为呈现较好的相关性,选取PFE 较低的样本进行研究。随着PFE 的升高,BFE 的增幅会逐渐减少而失去相关性。在实际医用外科口罩的注册或委托检测工作中,经检验合格的大多数口罩PFE 大于80%。2020 年2—5 月,北京市医疗器械检验所承检的41 批合格医用外科口罩中,PFE 均大于88%,其中大于90%的占比93%;63批合格的医用外科口罩和一次性使用医用口罩,BFE 均大于99%。有研究指出,人体在除咳嗽、喷嚏外的正常呼吸情况下也能产生大量气溶胶颗粒,粒径多在1 μm 以下[11-13]。0.1~0.5 μm 气溶胶颗粒能在空气中传播较长时间,不会发生沉降或被截留等情况,也是常用滤材的最易穿透粒径范围。我国科研人员在2020 年4 月发表在Nature杂志的一篇研究中指出[14],通过在武汉方舱医院空气中采集新型冠状病毒、数字聚合酶链式反应(polymerase chain reaction,PCR)检测病毒RNA 的方法,发现在防护服更换区的空气中,在0.25~0.5 μm 区间的病毒浓度为40个拷贝数/m3,在0.5~1 μm 区间的病毒浓度为9 个拷贝数/m3。另外有研究发现,佩戴医用外科口罩的患者呼出的空气中依然能检测到流感病毒,并指出医用外科口罩能降低空气中呼出的病毒数量,但并不能完全阻断它们在空气中的传播[15-16]。医用外科口罩是平面型,缺乏面部密合性,因而不具备呼吸防护功能,但其仍能在阻挡气溶胶粒子传播方面发挥一定作用。综合来看,我国目前现行医用外科口罩行业标准对PFE 要求较低,可进行适当提高。
通过对比医用外科口罩的BFE 和VFE 发现,VFE 略低于BFE。分析原因是,在相同MPS 条件下,细菌和大肠杆菌噬菌体在Anderson 6 级采样器各级分布规律不同。VFE 实验中采样器在第6 级收集到的大肠杆菌噬菌体数目百分比高于BFE 实验,而口罩对粒径越小、越接近最易穿透直径的粒子过滤效率越差,使得透过口罩的大肠杆菌噬菌体颗粒增加,过滤效率降低。本研究测试了3 种防护口罩的VFE,包括2 种颗粒防护口罩(N95 和N99 级)和1 种医用防护口罩(N99 级),结果均大于99.98%。选择Anderson 固体采样的方式收集过滤后的大肠杆菌噬菌体,结果优于AGI-30 液体冲击式采样。当选择AGI-30采样器收集过滤后的大肠杆菌噬菌体颗粒时,会出现采集不到任何大肠杆菌噬菌体的结果,原因是液体冲击采样过程使噬菌体活性丧失,该采样方式对低浓度的气溶胶颗粒采样效率偏低。实验结果还表明,当大肠杆菌噬菌体气溶胶颗粒浓度为4~7×104pfu/L时,经PFE 为98%的N95 级颗粒防护口罩过滤后,仍能检测到100~300 个活性病毒颗粒。Nikitin 等[17]的研究表明,吸入300~3 000 个病毒粒子便可能引起流感病毒感染。但防护口罩在实际佩戴中不会与面部完全密合,因此在存在高致病性病原体气溶胶暴露风险的场景下,应佩戴N95 级别以上防护口罩或者采取更高等级的防护措施。
通过研究医用外科口罩经过佩戴和热水浸泡处理后PFE 和BFE 的变化,发现新口罩经过3 次65 ℃热水浸泡30 min 处理后,PFE 基本不降低,但当口罩经过佩戴后再进行热水浸泡处理,PFE 和BFE 都出现不同程度的降低。医用外科口罩经佩戴和热水浸泡后,PFE 与BFE 呈现较好的相关性,但与新口罩2个指标的相关性不同。如图3(c)所示,当对MPS 约为2 μm 的细菌气溶胶过滤效率为95%时,PFE 需大于80%。分析原因可能是佩戴过程中的盐分、油脂等成分部分损坏了熔喷层结构,导致BFE降低;也可能与佩戴过程中截留或吸附在口罩内部的微生物等颗粒有关,加载更多细菌时导致BFE 降低。医用防护口罩在经过高压蒸汽灭菌(121 ℃30 min)处理后,过滤效率未受影响,但密合性降低。国外有研究发现N95 级口罩经过50 个循环的85 ℃20 min 干热处理后,过滤效率基本未受到影响[18]。医用防护口罩的使用场景风险相对较高,重复处理可能导致密合性降低等风险,但本研究未对防护口罩的重复处理方法进行深入研究。
本研究主要对实际佩戴前后医用外科口罩的气溶胶过滤效率进行了评价,但关于医用外科口罩和防护口罩对空气微生物的过滤、阻隔能力,还需在更加真实的环境或使用场景下进行研究。
