油气管道的CO2腐蚀及防护研究进展
2021-05-08李佳航王丹谢飞王月陈一鸣杨海燕
李佳航,王丹,谢飞,王月,陈一鸣,杨海燕
油气管道的CO2腐蚀及防护研究进展
李佳航1,王丹1,谢飞1,王月1,陈一鸣1,杨海燕2
(1.辽宁石油化工大学 石油天然气工程学院,辽宁 抚顺 113001;2.中石油辽河油田油气集输公司,辽宁 盘锦 124010)
腐蚀控制是石油天然气管输过程中的一个重要问题。CO2是石油天然气管道中最常见的腐蚀介质,研究CO2腐蚀机制和防护措施具有重要科学意义和经济价值。综述了CO2的腐蚀机理,包括化学反应、电化学反应和传质过程。对现有的腐蚀理论进行了深入讨论,发现阴极反应对CO2腐蚀具有重要影响,CO2对阳极过程的影响尚未明确。在腐蚀机理的基础上,考虑管道实际工况,结合电化学实验结果阐述了各影响因素对CO2腐蚀行为的影响,并结合CO2腐蚀的影响因素讨论了常用管道防护措施的缺陷:阴极保护系统受电位影响较大,应确立新的阴极保护电位,以保证在杂散电流作用下的阴极保护效果;防护涂层容易在杂散电流干扰下发生降解,失去保护性;多数缓蚀剂对环境有害。最后,展望了未来CO2腐蚀和防护的发展方向:为进一步了解CO2腐蚀机理,需要对CO2的电化学腐蚀行为进行系统地实验测试。研究不同缓蚀剂的协同效应,使用环境友好型绿色缓蚀剂,利用新材料开发智能涂层和新型阴极保护系统,也是未来的研究方向之一。
油气管道;内腐蚀;CO2腐蚀机理;影响因素;防护技术
腐蚀问题是石油天然气工业中的常见问题,其中内腐蚀占腐蚀事故的50%以上,是油气管道最常见的失效形式[1]。在油气开采的过程中,CO2几乎总是作为副产物存在,而当管道中有积水存在时,CO2会对管道造成严重腐蚀[2]。有研究表明,由于管道中存在CO2而造成的腐蚀速率最高可达20 mm/a[3]。自20世纪70年代以来,国内外学者对CO2腐蚀展开了深入研究[4-7],近年来对CO2腐蚀的研究有了新的进展[8-10]。
目前,我国的管道多为低碳钢制成。虽然相比于不锈钢和合金钢,低碳钢的抗腐蚀性能较差,但是由于成本低廉、力学性能良好,因而被广泛应用[2]。尽管腐蚀是一个不可避免的问题,但是采用适当的防护措施可以降低腐蚀速率,延长管道的使用寿命[11-12]。目前常用的防护措施主要包括:电化学防护、涂层防护和添加缓蚀剂[13]。随着近年来科技的进步,关于太阳能阴极保护系统、新的涂层材料和新型缓蚀剂的研究逐渐成为腐蚀界的热门领域[14-15],这些研究对于合理保护管材、延长管道使用寿命和减少灾害事故的发生具有重要意义。
本文归纳了包括化学反应、电化学反应和传质过程的CO2腐蚀机理,并讨论了CO2腐蚀的影响因素及作用机制。分析了腐蚀防护技术的最新进展,针对现行研究的缺陷和不足进行了讨论,并对未来的研究方向进行了展望。
1 CO2腐蚀机理
CO2腐蚀,又称甜腐蚀,是油气管道发生内腐蚀的重要原因之一。为了更好地理解管道的CO2腐蚀,首先需要确定CO2饱和水溶液中的物质,在其基础上分析管道内壁的电化学腐蚀过程。前者采用化学反应来阐述,而后者属于电化学领域。同时,由于管道表面与溶液间存在浓度梯度,离子发生迁移的现象可以通过传质过程来描述。
1.1 均相化学反应
与CO2溶解相关的化学平衡反应已经得到了广泛的研究[16-17]。在腐蚀过程中,CO2在水中发生式(1)—(5)的化学反应:


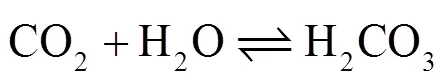
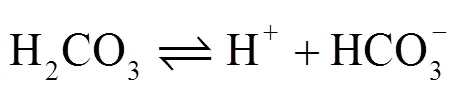
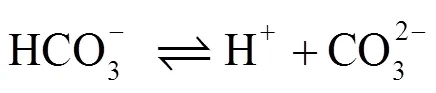
其中,反应(3)是速度控制步骤,CO2的水合反应对腐蚀过程有重要影响[18]。当溶液中离子浓度超过盐的溶解度时,将沉淀出可能形成保护膜的物质,如式(6)—(7)所示,其中最常见的腐蚀产物是FeCO3。
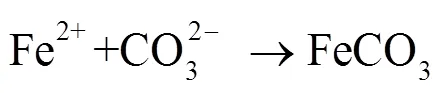
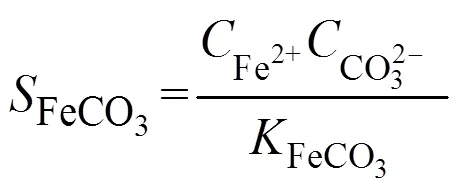
FeCO3腐蚀产物膜的生长及其保护性主要取决于(但不仅限于)沉淀速率,为了获得可观的沉淀水平,必须超过对应条件下FeCO3的过饱和度。在室温下,沉淀过程非常缓慢,即使在非常高的过饱和度下,通常也只能获得无保护性的产物膜。相反,在高温条件下,沉淀过程较快,在低过饱和度下也可以形成具有很强保护作用的产物膜[18]。关于腐蚀产物膜的作用,在下文中进行了详细地说明。
1.2 阴极反应
众所周知,CO2是通过增加阴极析氢的反应速率来提高金属的腐蚀速率[2]。铁在完全解离强酸中的腐蚀速率受传质过程影响,即生成H2的速率不能超过H+从本体溶液中转移到铁表面的速率。但是在弱酸存在时,特别是在碳酸存在的条件下,阴极反应的确切机理还存在争议。目前有三种可能的反应机理被提出,分别是:1)直接还原机制;2)水还原机制;3)缓冲作用。
Dewaard和Milliams[19]是最早试图阐明CO2腐蚀机理的研究人员之一,他们通过定量分析提出了一种CO2腐蚀机制,其中主要的阴极反应是未解离碳酸发生直接还原,如式(8)所示。这种直接还原机制也是过去几十年CO2腐蚀研究的基础[19]。
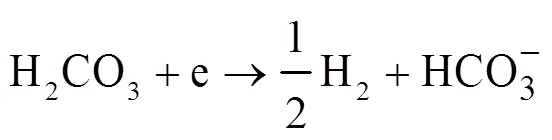
Nesic[20]提出在pH≥5且CO2分压非常低的情况下,由水直接还原产生氢气的过程,在较低的电势下变得很重要,即水还原机制(式(9)):

近些年来,有学者提出在弱酸条件下CO2腐蚀速率较高,是由于扩散边界层内H2CO3均匀解离,为还原H+提供了平行反应,如式(10)—(11)所示[21]。
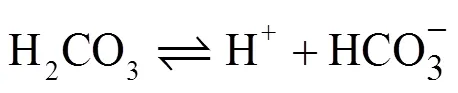


1.3 阳极反应
Bockris等人[25]提出了最公认的铁在酸性介质中的溶解机理,这也被认为是低碳钢在CO2腐蚀中的主要阳极反应,即BDD机理(式(12)—(13)):


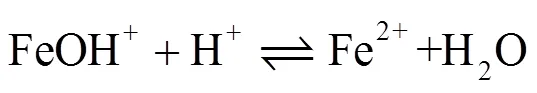
但是,最近有研究发现,在CO2环境中,铁的溶解机理与BDD机理有所不同[20,26]。有学者提出CO2参与了铁的阳极溶解反应,并在反应过程中与铁形成了一种配合物[20]。因此,CO2对铁阳极溶解的作用机理还需进一步研究确认,这也是今后CO2腐蚀的研究重点之一。
1.4 传质过程
传质过程通过以下三种机制发生:因流体的(湍流)运动而产生的对流;因物种的浓度梯度产生的分子扩散;离子的电迁移。虽然相比于强酸,低碳钢的CO2腐蚀对流速变化不敏感(CO2腐蚀的极限电流受水化学反应的控制,而水化学反应主要受温度和CO2分压的影响,与流速无关[27]),但是也有研究表明,完全忽略传质限制将导致腐蚀速率计算结果偏大[28]。
以上对CO2的腐蚀机理的回顾,是理解CO2腐蚀过程、制定防护措施的基础。深入了解CO2的腐蚀机理,探寻腐蚀过程的反应机制,也是进行CO2腐蚀与防护研究的首要任务。
2 CO2腐蚀的影响因素
影响CO2腐蚀的因素多种多样,温度、CO2分压、pH、流速及腐蚀产物膜等都会影响管道的腐蚀。许多情况下,很难将一种影响因素的效果与另一种影响因素的效果完全分开,没有一种理想的方式可以呈现总体情况。在下面的讨论中,将在上述腐蚀机理的背景下考虑各个因素对CO2腐蚀的影响,对于每个参数,都会考虑最常见的条件范围,并且在合理的情况下,引入关键的次要参数。此外,还分析了各因素对防护措施的影响。
2.1 温度
温度加速了腐蚀的所有过程。在没有产生保护性沉淀时,腐蚀速率随温度的增加而增加[29]。当溶液内Fe2+和CO32−的浓度积超过碳酸亚铁的溶解度时(通常在较高的pH下),腐蚀速率的情况会发生变化:温度升高会迅速加速沉淀,并形成致密保护层,从而减缓腐蚀速率的增长速度[30]。但也有学者提出腐蚀速率高峰通常在60~80 ℃之间,具体取决于水的化学性质和流动条件[31]。目前,关于温度对CO2腐蚀速率的影响的理解基本统一:在一定温度以下,提高温度会加快反应进程,从而提高腐蚀速率;但超过一定温度时,由于腐蚀产物的快速沉淀,在金属表面形成了致密的腐蚀产物膜,会使腐蚀速率快速降低。但需要特别指出的是,温度的升高将使CO2溶解度降低,从而导致溶液中CO2分压的降低。此外,温度升高同样会降低CO2的腐蚀速率,而这往往会被研究人员忽视。
同时,已有研究表明,大多数缓蚀剂的性能随温度的升高而增强。有学者在1 mol/L HCl中观察到缓蚀效率随温度的升高而升高,并且缓蚀剂在60 ℃的1 mol/L H2SO4中也保持了非常好的缓蚀性能[32]。
2.2 CO2分压


图1 CO2分压对裸钢腐蚀速率的影响[31]
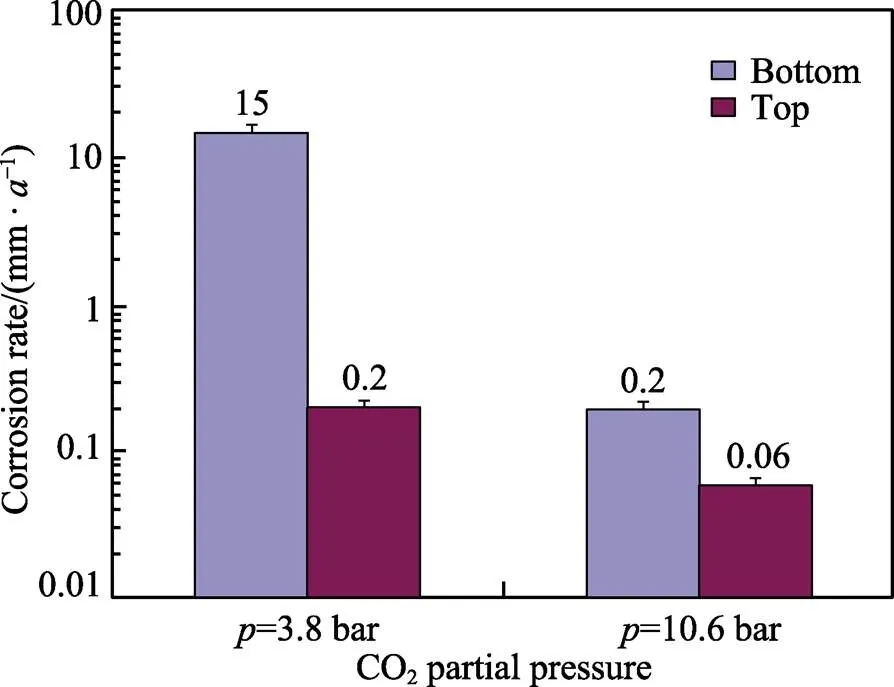
图2 对管道顶部和底部的腐蚀速率的影响[34]

图3 不同阴极反应机理的预期腐蚀电流[24]
2.3 pH
较低的pH值会导致较高的腐蚀速率,反之亦然。pH的另一个重要影响与改变形成碳酸亚铁层的条件有关:较高的pH值会导致碳酸亚铁的过饱和度增加。如图4所示,在pH值为6时,碳酸亚铁的过饱和度很小(SS=7),此时腐蚀速率的变化很小,这表明在pH较低时,形成了相对多孔的无保护层。较高的pH值会导致较高的过饱和度(SS=150),从而有更快的沉淀速度,并形成更多的保护性碳酸亚铁,反映为腐蚀速率随时间的快速下降[36]。

图4 FeCO3过饱和度SS对腐蚀速率的影响[36]
现有的研究结果表明,较高的pH会导致腐蚀速率降低,从而使“pH稳定化”技术成为控制CO2腐蚀的一种方法,但是该技术会导致结垢过多。控制pH来提供中性环境,并刺激形成腐蚀保护膜,会增加局部腐蚀的风险。在管道中也很难做到调节pH值,因此管道的防护措施中往往不考虑调节pH的方法。
2.4 流速

当形成保护膜时(通常在具有较高pH值的环境下),流速对腐蚀的影响还不清楚。一方面,来自现场的经验表明,保护膜在高流速下可能会破裂[38],而壁面剪应力(WSS)通常被认为是主要的破坏原因[39];另一方面,研究发现,在湍流条件下的WSS不会影响腐蚀产物层[40]。
同时,湍流下的高流速还会影响到缓蚀剂的效果。在许多情况下,湍流会使缓蚀剂性能略有改善[41]。同时一些现场和实验室的证据表明,缓蚀剂无法在某些“临界”流速以上提供保护,此时可以通过增加缓蚀剂浓度来抑制腐蚀[42-43]。但是,有一些在高流速条件下进行的研究表明,缓蚀剂的性能不受高WSS的影响[44]。
迄今为止,关于管道内流动效果对腐蚀产物膜影响的研究还很少,影响机理也不明确。而研究流速的影响对油气管道的剩余寿命预测和防护工作具有重要意义,这是今后的一个重点方向。
2.5 腐蚀产物膜
从上述讨论中可以发现,保护膜往往会改变其他因素对CO2腐蚀行为的影响趋势,所以在CO2腐蚀机理的研究过程中,关于腐蚀产物膜对腐蚀过程的影响机制一直是热点研究问题。
如上所述,CO2腐蚀中最常见的腐蚀产物是FeCO3。当FeCO3沉淀在钢表面时,它可以通过以下方式减缓腐蚀过程:1)阻碍物质扩散;2)阻止铁与腐蚀介质接触。FeCO3膜的结构如图5所示。

图5 含有FeCO3腐蚀产物膜的钢试样横截面的SEM图像[30]
有许多因素会影响膜的形成,最重要的是均相化学反应。为了形成产物膜,溶液内Fe2+和CO32−的浓度必须超过对应条件下的饱和度。室温下的沉淀过程非常缓慢,即使在非常高的过饱和度下,也通常会获得无保护性的膜。相反,在高温条件下,即使在低过饱和度下,也可以形成保护膜。实际上,过饱和度无法持久在高温下长期保持稳定,因为加速沉淀过程将使溶液迅速返回热力学平衡状态[27]。
3 防护方法
在石油天然气行业中,管道的腐蚀破坏随处可见,腐蚀事故频频发生。除了低碳钢本身耐蚀性较差的原因外,很大程度上还因为人们对腐蚀的危害性估计不足,对腐蚀防护科学的认识不深。常见的管道腐蚀防护技术主要包括:电化学保护技术、表面保护技术和添加缓蚀剂。
3.1 电化学保护
电化学保护(也称阴极保护,CP)是利用外部电流使管道的电位发生改变,从而防止管道腐蚀的一种方法。管道行业推荐CP电位标准为−850 mV(CSE)[45],但在实际工程中,管线钢的实际电势经常偏离标准值,并且已经有学者发现,杂散电流会影响CP系统的性能[46]。
尽管管道在外加电位时处于宏观阴极极化状态,但是杂散电流引起的电位波动会在表面缺陷处造成阳极临时溶解,从而引发点蚀[47-48]。Liu等人[49]研究了X80钢在酸性环境中不同电位条件下的电化学和应力腐蚀开裂行为,发现不稳定的阴极极化加速了钢的腐蚀。Dai等人[50]利用方波极化技术(SWP)对电位波动引发点蚀的机理进行了深入研究,发现当低电位恒定时,凹坑密度随高电位的增加而线性增加,如图6所示。当高电位固定时,凹坑密度随低电位的增加而线性减小,如图7所示,同时发生均匀腐蚀。
杂散电流的干扰分为交流干扰和直流干扰。在存在交流干扰的情况下,无法保持施加在钢上的CP电位,无论施加的交流电势是正向移动还是负向移动,钢都会遭受腐蚀的加剧[51]。D. Kuang等人[51]研究发现,在交流电流密度为10 A/m2的情况下,所施加的标准CP电位无法使钢发生阴极极化,并且无法保护其免受交流干扰的腐蚀。当施加−0.925 V(CSE)的CP电位时,增强的阴极极化可以保护钢在小于50 A/m2的交流电流下不受腐蚀。随着交流电流密度的增加,CP的保护性越来越差[51]。
而直流电通常会比交流电对管道钢造成更严重的腐蚀。已有研究表明,在60 Hz的交流电(AC)干扰下,钢的腐蚀约为当量的直流电(DC)引起腐蚀的1%[52]。与交流干扰类似,在直流干扰下,CP电位也未保持在施加值,而是分别在阳极和阴极区域向正和负方向移动。管道同时受到阳极和阴极直流干扰,受保护的钢也不能完全避免腐蚀。如图8所示,国际上推荐的标准CP电位在0.1 A/m2的直流电条件下便失去了保护性。当阴极保护电位为−1 V(CSE)时,可保护钢在直流电流密度高达1 A/m2时免受腐蚀[45]。显然,在存在直流干扰的情况下,用于防腐的CP效果显著降低。

图6 固定下限电势(−0.93 V(SCE))下各种上限电势的腐蚀坑SEM图[50]

图7 固定上限电势(−0.65 V(SCE))下各种下限电势的腐蚀坑SEM图[50]
从上述讨论中可以发现,在管道受到杂散电流干扰时,国际推荐阴极保护电位−850 mV(CSE)的保护效果大大降低,因此应当综合考虑管道土壤环境,采用更低电位的阴极保护措施,但是目前还没有统一的标准来规定存在杂散电流时的阴极保护电位。
在偏远地区,电源限制了CP的应用。近年来,利用太阳能作为CP电源的新型CP系统引起了人们的广泛关注[54]。在光致CP系统中,由光敏材料制成的光电极充当阳极,并在光照下产生光致电子空穴对。有学者通过溶胶-凝胶法和微乳液法制备了双层CeO2/SrTiO3纳米复合光电极[55],该电极可以分别通过法拉第反应和离子的非法拉第吸附还原内CeO2层,并在光照下充电,其原理如图9所示。在没有照明的情况下,光电极可以通过将CeO2层中存储的电荷(光电子)释放到钢中,来保持其抗腐蚀性能。国际上,光致CP系统是一个新兴的绿色能源系统,尤其是对新型光敏材料的开发,是今后研究的重点。

图8 钢在不同直流电流密度下于土壤溶液中测试48 h后的腐蚀形貌[53]
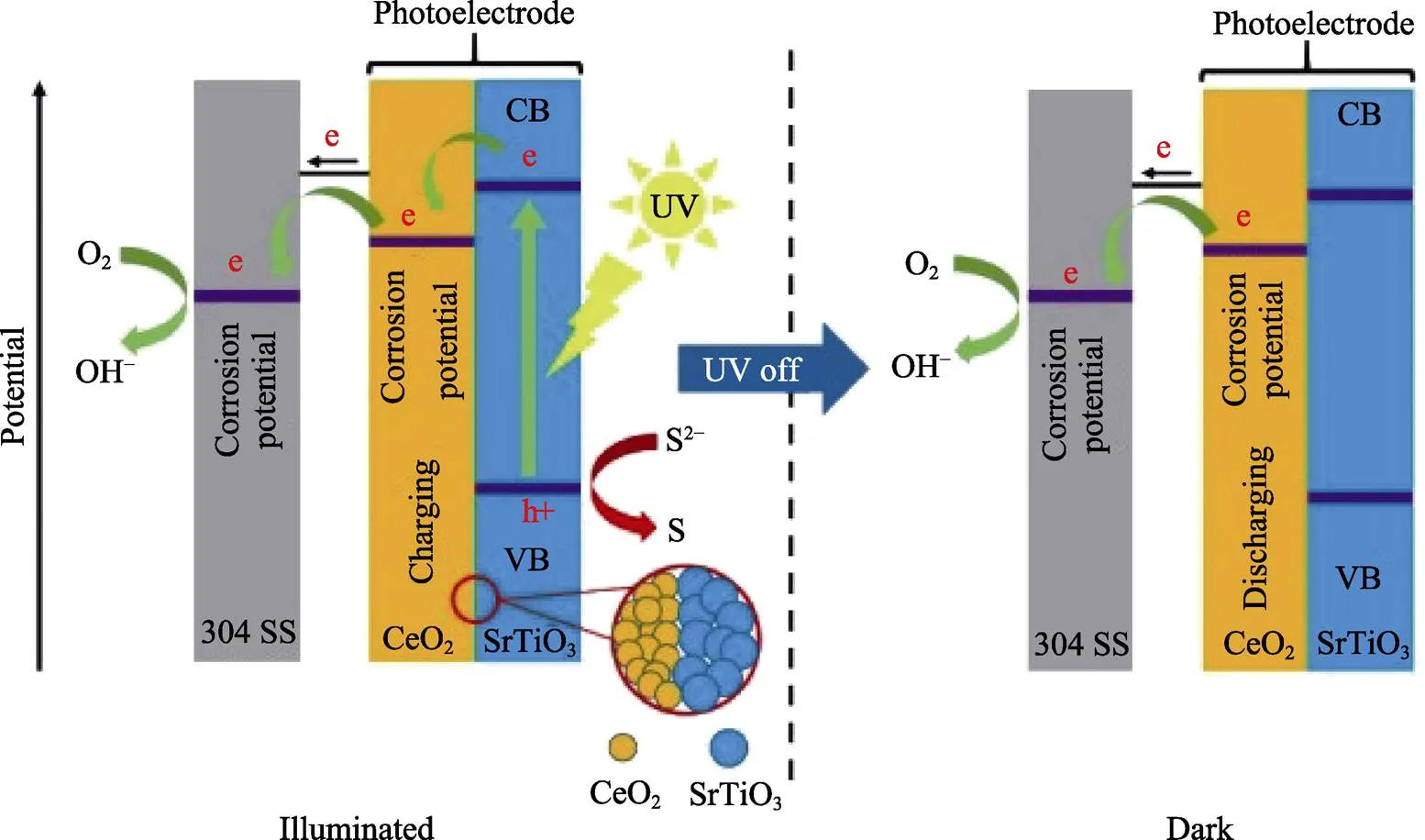
图9 双层CeO2/SrTiO3纳米复合光电极的原理示意图[55]
3.2 表面保护
表面保护是指利用涂层避免管道和腐蚀介质直接接触,从而使管道得到保护的技术。迄今为止,已经开发了各种表面技术来提高工程材料在使用中的性能稳定性和耐用性[56-59]。
尽管管道涂层已经发展了60年,但是常规涂层还是具有很多缺点,例如在使用过程中,发生由结构或降解引起的损坏,使它们无法保护管道。如上所述,杂散电流不仅会引起钢管的腐蚀,还会影响涂层性能。目前已经发现杂散电流会对多种涂层性能造成影响。土壤中存在的直流电流会增加水渗入涂层的能力,降低涂层的防护能力[60],一旦涂层失效,流经涂层缺陷的直流电流会导致阳极区的钢加速腐蚀,并增强阴极区中去极化剂的还原[61]。Qian等人[60]研究发现,当将涂有FBE涂层的地下管道与直流电源并置时,直流干扰的存在会增加涂层中的水渗透和离子扩散,并造成FBE涂层降解,随着直流电压的增加,影响变得更加明显。图10为涂层降解的模型。

图10 用于说明存在直流干扰时FBE涂层降解的概念模型[60]
目前,智能涂层是涂层防护的热门研究方向。智能涂层是指具有“腐蚀感应”和“自我修复”特性的涂层系统。智能涂层不仅提供了屏障,还提供了缓蚀剂的自释放性(缓蚀剂已预先加载到涂料中)。但是,如果涂层直接与缓蚀剂混合,则缓蚀剂分子很容易溶解在水溶液中,从而在涂层中产生微孔[62]。有学者提出将缓蚀剂包封在对主体涂层呈惰性的微容器或纳米容器中[63],即预先添加到纳米容器中的缓蚀剂可以“感知”腐蚀环境的产生,并且自动释放响应触发机制来抑制管道腐蚀。例如,Andreeva等[64]制备了内含缓蚀剂的多层聚电解质纳米容器,这些缓蚀剂会随着溶液pH的变化而释放,从而迅速降低管道的阳极活性。Feng和Cheng[65]基于BTA抑制剂在制备的SiO2纳米颗粒基聚电解质纳米容器中的封装及其自释放性,以及可抑制氯化物溶液中管线钢的腐蚀,从而开发出智能涂层。所开发的一种智能涂层的机理如图11所示。
但是,虽然目前有多种基于在微容器或纳米容器中封装腐蚀缓蚀剂,并基于适当的触发机制使缓蚀剂自我释放的智能涂料已经被开发,但它们都尚未在工业规模上开发,特别是难以用于管道腐蚀。迄今为止,大多数相关研究都是在实验室中进行,而开发一种技术上可行且具有较低经济成本的智能涂层技术对保证管道的完整性具有重要意义,未来纳米容器的研发将会是一个热门的研究领域。
3.3 缓蚀剂防护
缓蚀剂是一种可以减缓腐蚀的化学物质或几种化学物质的混合物。一般认为缓蚀剂的缓蚀机理分为两种:1)缓蚀剂吸附在管道内壁,阻止腐蚀介质与管壁接触;2)缓蚀剂与腐蚀介质发生反应,阻止腐蚀的发生。目前,随着环保意识的提高,缓蚀剂的效果和成本已经不是评价缓蚀剂的唯一指标,缓蚀剂对环境的影响也是一个重要的评价因素。在缓蚀剂的最新进展中,多种缓蚀剂和表面活性剂的协同作用和有机绿色缓蚀剂的研究已经被重点关注[66-69]。
在20世纪80年代就有研究表明,可以将缓蚀剂与其他化合物组合使用,以改善其性能或减少用量[70]。在饱和CO2的盐水溶液中,咪唑啉(IM)和L-半胱氨酸(CYS)之间的协同作用可以保护低碳钢免受CO2引起的腐蚀。此外,Tang等[66]证明4-甲基吡啶季铵盐(PQ)、喹啉季铵盐(QQ)和硫脲(TU)之间存在协同作用,三种缓蚀剂PQ+QQ+TU(1.5∶1.5∶1)组合表现最佳。Qian等[67]发现,咪唑啉和十二烷基苯磺酸钠对X52碳钢在CO2饱和氯化物溶液中的缓蚀作用存在协同效应。
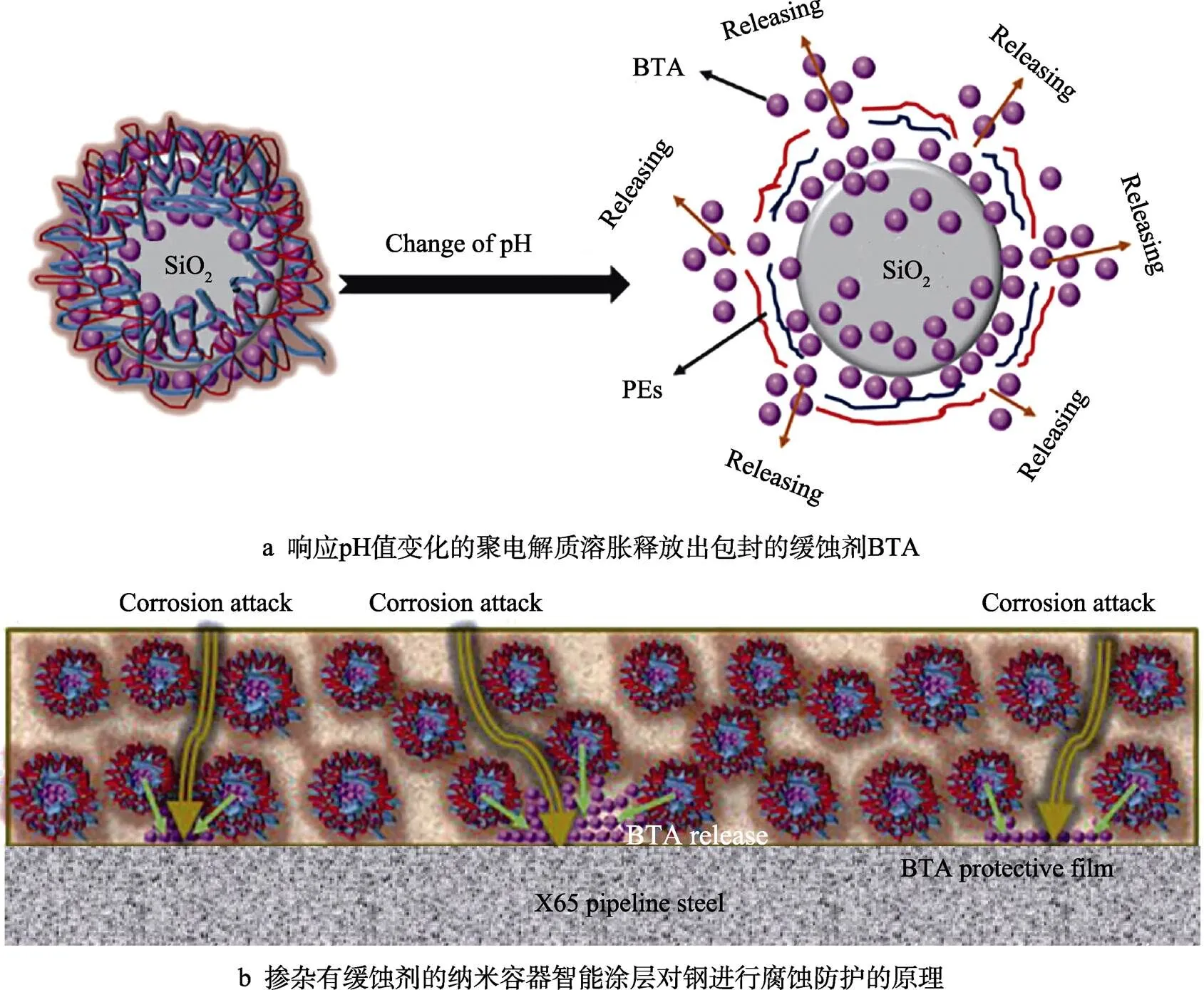
图11 智能涂层示意图[65]

缓蚀剂对环境的影响远大于其他两种防护方法,环境友好型缓蚀剂已经成为腐蚀防护领域的热门领域,而不同绿色缓蚀剂结合使用的效果还有待进一步研究。
4 结论与展望
CO2腐蚀是石油天然气管道中长期存在的问题,对CO2腐蚀机理的研究已经持续了近50年,对现有的研究进行回顾后发现,目前关于CO2腐蚀已经形成了一套完整的腐蚀理论体系,然而具体的反应过程仍然还不是很明确,尤其是腐蚀过程中的电化学反应还没有一个统一的理论。
在管道防护方面,目前已经开发出了许多防护手段,并取得了良好的防护效果。但是目前各种防护手段都还存在一定的局限性(成本、环境等问题),导致不能大规模使用。基于上述研究现状,针对保护管道的完整性,未来管道的CO2腐蚀与防护研究应关注以下三个方向:
1)在现有研究的基础上,深入研究CO2腐蚀过程中的电化学行为,针对不同机制进行大量实验研究,确定CO2的腐蚀机理。
2)完善现有防护手段,建立新的阴极防护电位和涂层材料选用标准,深入研究不同缓蚀剂(尤其是绿色缓蚀剂)的协同作用,开发新的组合方式。
3)借助新能源、新材料,研发新的防护手段,如智能涂层和太阳能阴极保护系统等。
[1] 董绍华, 王东营, 董国亮, 等. 管道内腐蚀直接评估技术与实践应用[J]. 石油科学通报, 2016, 1(3): 459-470. DONG S H, WANG D Y, DONG G L, et al. Direct assessment technology and practical application of pipeline corrosion[J]. Petroleum science bulletin, 2016, 1(3): 459-470.
[2] LI W, BROWN B, YOUNG D, et al. Investigation of pseudo- passivation of mild steel in CO2corrosion[J]. Corrosion, 2013, 70(3): 294-302.
[3] 张清, 李全安, 文九巴, 等. CO2/H2S对油气管材的腐蚀规律及研究进展[J]. 腐蚀与防护, 2003(7): 277-281.ZHANG Q, LI Q A, WEN J B, et al. The corrosion law and research progress of CO2/H2S on oil and gas pipes[J]. Corrosion & protection, 2003(7): 277-281.
[4] NESIC S, NORDSVEEN M, NYBORG R, et al. A diffusion- based model for uniform corrosion[C]// DIMAT2000 Pt.2. Norway:[s. n.], 2000: 1661-1674.
[5] 孙建波, 柳伟, 常炜, 等. 低铬X65管线钢CO2腐蚀产物膜的特征及形成机制[J]. 金属学报, 2009, 45(1): 84-90. SUN J B, LIU W, CHANG W, et al. Characteristics and formation mechanism of CO2corrosion product film on low chromium X65 pipeline steel[J]. Acta metallurgica sinica, 2009, 45(1): 84-90.
[6] 杨建炜, 张雷, 丁睿明, 等. X60管线钢在湿气和溶液介质中的H2S/CO2腐蚀行为[J]. 金属学报, 2008, 44(11): 1366-1371. YANG J W, ZHANG L, DING R M, et al. H2S/CO2corrosion behavior of X60 pipeline steel in wet gas and solution medium[J]. Acta metallurgica sinica, 2008, 44(11): 1366-1371.
[7] 张亮, 李晓刚, 杜翠薇, 等. X70管线钢在含CO2库尔勒土壤模拟溶液中的腐蚀行为[J]. 金属学报, 2008, 44(12): 1439-1444. ZHANG L, LI X G, DU C W, et al. H2S/CO2corrosion behavior of X70 pipeline steel in wet gas and solution medium[J]. Acta metallurgica sinica, 2008, 44(12): 1439-1444.
[8] KAHYARIAN A, NESIC S. A new narrative for CO2corrosion of mild steel[J]. Journal of the Electrochemical Society, 2019, 166: C3048-C3063.
[9] 田永强, 付安庆, 胡建国, 等. 低Cr钢在CO2/H2S环境中的腐蚀行为研究[J]. 表面技术, 2019, 48(5): 49-57. TIAN Y Q, FU A Q, HU J G, et al. Research on corrosion behavior of low Cr steel in CO2/H2S environment[J]. Surface technology, 2019, 48(5): 49-57.
[10] 王月, 王丹, 谢飞, 等. CO2对油田地下水环境中Q235钢和X70钢腐蚀行为的影响[J]. 金属热处理, 2020, 45(6): 226-231. WANG Y, WANG D, XIE F, et al. The effect of CO2on the corrosion behavior of Q235 steel and X70 steel in oilfield groundwater environment[J]. Heat treatment of metals, 2020, 45(6): 226-231.
[11] YANG Y, CHENG Y F. One-step facile preparation of ZnO nanorods as high-performance photoanodes for photoelectrochemical cathodic protection[J]. Electrochmica acta, 2018, 276: 311-318.
[12] YU M D, CUI Z Y, GE F, et al. Facile fabrication of hydrophobic polysiloxane coatings for protection of AZ31 magnesium alloy[J]. Journal of materials science, 2019, 54: 9759- 9774.
[13] 艾志久, 范钰玮, 赵乾坤. H2S对油气管材的腐蚀及防护研究综述[J]. 表面技术, 2015, 44(9): 108-115. AI Z J, FAN Y W, ZHAO Q Q. Summary of research on H2S corrosion and protection of oil and gas pipes[J]. Surface technology, 2015, 44(9): 108-115.
[14] YANG Y, CHENG Y F. Factors affecting the performance and applicability of SrTiO3photoelectrodes for photoinduced cathodic protection[J]. Journal of the electrochmical society, 2017, 164: C1067-C1075.
[15] MURUVE N G G, CHENG Y F, FENG Y C, et al. Peptide-based biocoatings for corrosion protection of stainless steel biomaterial in a chloride solution[J]. Materials science & engineering C: Materials for biological applications, 2016, 68: 695-700.
[16] PALMER D A, ELDIK R V. The chemistry of metal carbonate and carbon dioxide complexes[J]. Chemical reviews, 1983, 83: 651-731.
[17] STUMM W, MORGAN J J. Aquatic chemistry: Chemical equilibria and rates in naturalwaters[J]. Cram101 textbook outlines to accompany, 1995, 179: A277.
[18] NESIC S. Key issues related to modelling of internal corrosion of oil and gas pipelines—A review[J]. Corrosion science, 2007, 49: 4308-4338.
[19] DEWAARD C, MILLIAMS D E. Carbonic-acid corrosion of steel[J]. Corrosion, 1975, 31: 177-181.
[20] NESIC S, THEVENOT N, CROLET J L, et al. Electrochemical properties of iron dissolution in the presence of CO2—Basics revisited[C]// Corrosion. Houston: NACE international, 1996: 23-32.
[21] REMITA E, TRIBOLLET B, SUTTER E, et al. Hydrogen evolution in aqueous solutions containing dissolved CO2: Quantitative contribution of the buffering effect[J]. Corrosion science, 2008, 50: 1433-1440.
[22] GRAY L G S, ANDERSON B G, DANYSH M J, et al. Mechanisms of carbon steel corrosion in brines containing dissolved carbon dioxide at Ph4[C]// Corrosion. Houston: NACE international, 1989.
[23] KAHYARIAN A, BROWN B, NESIC S. Electrochemistry of CO2corrosion of mild steel: Effect of CO2on cathodic currents[J]. Corrosion, 2018, 74(8): 851-859.
[24] TRAN T, BROWN B, NESIC S, et al. Investigation of the electrochemical mechanisms for acetic acid corrosion of mild steel[J]. Corrosion, 2014, 70: 223-229.
[25] BOCKRIS J O M, DRAZIC D. The kinetics of deposition and dissolution of iron: Effect of alloying impurities[J]. Electrochmica acta, 1962, 7: 293-313.
[26] KAHYARIAN A, BROWN B, NESIC S. Electrochemistry of CO2corrosion of mild steel: Effect of CO2on iron dissolution reaction[J]. Corrosion science, 2017, 129: 146-151.
[27] NESIC S, POSTLETHWAITE J, OLSEN S. An electrochemical model for prediction of corrosion of mild steel in aqueous carbon dioxide solutions[J]. Corrosion science, 1996, 52: 280-294.
[28] NYBORG R, ANDERSSON P, NORDSVEEN M. Implementation of CO2corrosion models in a three-phase fluid flow model[C]// NACE international annual conference & exposition. Orlando: [s. n.], 2000: 1-10.
[29] SONG F M. A comprehensive model for predicting CO2corrosion rate in oil and gas production and transportation systems[J]. Electrochmica acta, 2010, 55: 689-700.
[30] NESIC S, LEE K L J. A mechanistic model for carbon dioxide corrosion of mild steel in the presence of protective iron carbonate films—Part 3: Film growth model[J]. Corrosion, 2003, 59: 616-628.
[31] NESIC S. Carbon dioxide corrosion of mild steel[M]. New Jersey: John Wiley & Sons, Inc, 2011: 229-245.
[32] POPOVA A, CHRISTOV M, VASILEV A. Mono- and dicationic benzothiazolic quaternary ammonium bromides as mild steel corrosion inhibitors. Part III: Influence of the temperature on the inhibition process[J]. Corrosion science, 2015, 94: 70-78.
[33] NESIC S, NORDSVEEN M, NYBORG R, et al. A mechanistic model for carbon dioxide corrosion of mild steel in the presence of protective iron carbonate films—Part 2: A numerical experiment[J]. Corrosion, 2003, 59: 489-497.
[34] SUN Y, NESIC S. A parametric study and modeling on localized CO2corrosion in horizontal wet gas flow[C]// Corrosion. Houston: NACE international, 2004: 25-32.
[35] MUSTAFA A H, ARI-WAHJOEDI B, ISMAIL M C. Inhibition of CO2corrosion of X52 steel by imidazoline-based inhibitor in high pressure CO2-water environment[J]. Journal of materials engineering and performance, 2013, 22: 1748- 1755.
[36] SUN W, CHOKSHI K, NESIC S. Iron carbonate scale growth and the effect of inhibition in CO2corrosion of mild steel[C]// Corrosion. Houston: NACE international, 2005: 23-31.
[37] LI Q, HU H T, CHENG Y F. Corrosion of pipelines in CO2- saturated oil-water emulsion flow studied by electrochemical measurements and computational fluid dynamics modeling[J]. Journal of petroleum science and engineering, 2016, 147: 408-415.
[38] GAO K W, YU F, PANG X L, et al. Mechanical properties of CO2corrosion product scales and their relationship to corrosion rates[J]. Corrosion science, 2008, 50: 2796-2803.
[39] ZENG L, ZHANG G A, GUO X P, et al. Inhibition effect of thioureidoimidazoline inhibitor for the flow accelerated corrosion of an elbow[J]. Corrosion science, 2015, 90: 202-215.
[40] YANG Y, BROWN B, NEŠIC S, et al. Mechanical strength and removal of a protective iron carbonate layer formed on mild steel in CO2corrosion[C]// Corrosion. Houston: NACE international, 2010: 19-26.
[41] GULBRANDSEN E, KVAREKVAL J L. Effect of oil-in- water emulsions on the performance of CO2corrosion inhibitors[C]// Corrosion. Houston: NACE international, 2004: 17-24.
[42] POTS B F M, HENDRIKSEN E L J A, PIT H. Field study of corrosion inhibition at very high flow velocity[C]// Corrosion. Houston: NACE international, 2003: 14-25.
[43] HAUSLER R H, CONSULTA C, SCHMITT G. Hydrodynamic and flow effects on corrosion inhibition[C]// Corrosion. Houston: NACE international, 2004: 39-48.
[44] GULBRANDSEN E, GRANA A. Testing of carbon dioxide corrosion inhibitor performance at high flow velocities in jet impingement geometry. effects of mass transfer and flow forces[J]. Corrosion, 2007, 63: 1009-1020.
[45] CHMILAR J F. NACE international standard practice SP0169: Control of external corrosion on underground or submerged metallic piping systems[C]// Corrosion. Houston: NACE international, 2013.
[46] MARTIN B. A history of stray current corrosion[J]. Corrosion & materials, 2006, 31: 12-14.
[47] LIU Z Y, LI X G, CHENG Y F. Electrochemical state conversion model for occurrence of pitting corrosion on a cathodically polarized carbon steel in a near-neutral pH solution[J]. Electrochimica acta, 2011, 56: 4167-4175.
[48] LIU Z Y, LI X G, CHENG Y F. Understand the occurrence of pitting corrosion of pipeline carbon steel under cathodic polarization[J]. Electrochimica acta, 2012, 60: 259-263.
[49] LIU Z Y, CUI Z Y, LI X G, et al. Mechanistic aspect of stress corrosion cracking of X80 pipeline steel under non- stable cathodic polarization[J]. Electrochemistry communications, 2014, 48: 127-129.
[50] DAI M J, LIU J, HUANG F, et al. Derivation of the mechanistic relationship of pit initiation on pipelines resultingfrom cathodic protection potential fluctuations[J]. Corrosion science, 2020, 163: 108226.
[51] KUANG D, CHENG Y F. Effects of alternating current interference on cathodic protection potential and its effectiveness for corrosion protection of pipelines[J]. Corrosion engineering science and technology, 2017, 52: 22-28.
[52] MCINTOSH D H. Grounding where corrosion protection is required[J]. IEEE transactions on industry application, 1982, 18: 600-607.
[53] QIAN S, CHENG Y F. Accelerated corrosion of pipeline steel and reduced cathodic protection effectiveness under direct current interference[J]. Construction and building materials, 2017, 148: 675-685.
[54] SUN M, CHEN Z. Enhanced photoelectrochemical cathodic protection performance of the In2O3/TiO2composite[J]. Journal of the Electrochemical Society, 2014, 162: C96- C104.
[55] YANG Y, CHENG Y F. Bi-layered CeO2/SrTiO3nanocomposite photoelectrode for energy storage and photocathodic protection[J]. Eectrochimical acta, 2017, 253: 134-141.
[56] LI Y, CHENG Y F. Development of nanostructured photocatalytic coatings for anti-bioadhesion and self-cleaning of residual bacterial cells[J]. Chemical engineering journal, 2018, 338: 513-525.
[57] CAO X K, HUANG F, HUANG C, et al. Preparation of graphene nanoplate added zinc-rich epoxy coatings for enhanced sacrificial anode-based corrosion protection[J]. Corrosion science, 2019, 159: 108120.
[58] 黄钰, 程西云, 彭美华, 等. Zn-Al伪合金涂层的耐蚀性能研究[J]. 表面技术, 2014, 43(1): 35-39. HUANG Y, CHENG X Y, PENG M H, et al. Research on corrosion resistance of Zn-Al pseudo alloy coating[J]. Surface technology, 2014, 43(1): 35-39.
[59] 陈郁栋, 曾志翔, 彭叔森, 等. 苯胺三聚体固化环氧树脂制备防腐蚀涂层及其性能研究[J]. 表面技术, 2014, 43(3): 158-162. CHEN Y D, ZENG Z X, PENG S S, et al. Study on anti-corrosion coating prepared by aniline trimer cured epoxy resin and its performance[J]. Surface technology, 2014, 43(3): 158-162.
[60] QIAN S, CHENG Y F. Degradation of fusion bonded epoxy pipeline coatings in the presence of direct current interference[J]. Progress in organic coatings, 2018, 120: 79-87.
[61] BERTOLINI L, CARSANA M, PEDEFERRI P. Corrosion behaviour of steel in concrete in the presence of stray current[J]. Corrosion science, 2007, 49: 1056-1068.
[62] QIANG Y, ZHANG S, XU S, et al. Experimental and theoretical studies on the corrosion inhibition of copper by two indazole derivatives in 3.0% NaCl solution[J]. Journal of colloid and interface science, 2016, 472: 52-59.
[63] SINGH H K, YEOLE K V, MHASKE S T. Synthesis and characterization of layer-by-layer assembled magnesium zinc molybdate nanocontainer for anticorrosive application[J]. Chemical engineering journal, 2016, 295: 414-426.
[64] ANDREEVA D V, FIX D, MÖHWALD H, et al. Self-healinganticorrosion coatings based on pH-sensitive polyelectrolyte/ inhibitor sandwichlike nanostructures[J]. Advanced matericals, 2008, 20: 2789-2794.
[65] FENG Y, CHENG Y F. An intelligent coating doped with inhibitor-encapsulated nanocontainers for corrosion protection of pipeline steel[J]. Chemical engineering journal, 2017, 315: 537-551.
[66] TANG J L, HU Y X, WANG H, et al. Complicated synergistic effects between three corrosion inhibitors for Q235 steel in a CO2-saturated 3.5 wt% NaCl solution[J]. International journal of electrochemical science, 2019, 14: 2246- 2264.
[67] QIAN S, CHENG Y F. Synergism of imidazoline and sodium dodecylbenzenesulphonate inhibitors on corrosion inhibition of X52 carbon steel in CO2-saturated updates chloride solutions[J]. Journal of molecular liquids, 2019, 294: 111674.
[68] UMOREN S A, BANERA M J, ALONSO-GARCIA T, et al. Inhibition of mild steel corrosion in HCl solution using chitosan[J]. Cellulose, 2013, 20: 2529-2545.
[69] RAJESWARI V, KESAVAN D, GOPIRAMAN M, et al. Physicochemical studies of glucose, gellan gum, and hydroxypropyl cellulose-Inhibition of cast iron corrosion[J]. Carbohydrate polymers, 2013, 95: 288-294.
[70] GROWCOCK F B. Kinetics of steel corrosion in hydrochloric acid inhibited with trans-cinnamaldehyde[J]. Journal of the Electrochemical Society, 1988, 135: 817.
[71] ARUKALAM I O. Durability and synergistic effects of KI on the acid corrosion inhibition of mild steel by hydroxypropyl methylcellulose[J]. Carbohydrate polymers, 2014, 112: 291-299.
[72] LUO X H, CI C G, LI J, et al. 4-aminoazobenzene modified natural glucomannan as a green eco-friendly inhibitor for the mild steel in 0.5 M HCl solution[J]. Corrosion science, 2019, 151: 132-142.
[73] LUO X, PAN X, YUAN S, et al. Corrosion inhibition of mild steel in simulated seawater solution by a green eco- friendly mixture of glucomannan (GL) and bisquaternary ammonium salt (BQAS)[J]. Corrosion science, 2017, 125: 139-151.
[74] MORAD M S. Inhibition of iron corrosion in acid solutions by cefatrexyl: Behaviour near and at the corrosion potential[J]. Corrosion science, 2008, 50: 436-448.
Research Progress on CO2Corrosion and Protection of Oil and Gas Pipelines
1,1,1,1,1,2
(1.School of Petroleum and Natural Gas Engineering, Liaoning Petrochemical University, Fushun 113001, China; 2.Liaohe Oil Field of CNPC, Panjin 124010, China)
Corrosion control is an important issue in the process of oil and gas pipeline transportation. CO2is the most common corrosion medium in oil and gas pipelines. It is of great scientific significance and economic value to study the corrosion mechanism and protective measures of CO2. The corrosion mechanism of CO2is reviewed, including chemical reaction, electrochemical reaction and mass transfer process. The existing corrosion theories are discussed in depth, and it is found that the cathodic reaction has an important effect on CO2corrosion, while the effect of CO2on the anodic process is not clear. On the basis of the corrosion mechanism, in view of the actual working conditions of the pipeline, combined with the electrochemical experimental results, the influence of various factors on the corrosion behavior of CO2is expounded. Combined with the influencing factors of CO2corrosion, the defects of common pipeline protection measures are discussed: the cathodic protection system is greatly affected by potential, so a new cathodic protection potential should be established to ensure the cathodic protection effect under the action of stray current. Coating protection is easy to degrade and lose protection under the interference of stray current. Most corrosion inhibitors are harmful to environment. Finally, the development direction of CO2corrosion and protection in the future is prospected: in order to further understand the corrosion mechanism of CO2, systematic experimental tests on the electrochemical corrosion behavior of CO2are needed. It is also one of the future research directions to study the synergistic effect of different corrosion inhibitors, the use of environment-friendly green corrosion inhibitors, the use of new materials to develop intelligent coatings and new cathodic protection systems.
oil and gas pipelines; internal corrosion; mechanism of CO2corrosion; influence factors; corrosion protection method
2020-08-15;
2021-03-04
LI Jia-hang (1997—), Male, Master, Research focus: prediction of residual life of pipeline.
谢飞(1983—),男,博士,副教授,主要研究方向为油气管道腐蚀与防护。邮箱:xiefei0413@163.com
Corresponding author:XIE Fei (1983—), Male, Ph. D., Associate professor, Research focus: corrosion and protection of oil and gas pipeline. E-mail: xiefei0413@163.com
李佳航, 王丹, 谢飞, 等.油气管道的CO2腐蚀及防护研究进展[J]. 表面技术, 2021, 50(4): 172-183.
TG172
A
1001-3660(2021)04-0172-12
10.16490/j.cnki.issn.1001-3660.2021.04.016
2020-08-15;
2021-03-04
辽宁省“兴辽英才计划”资助项目(XLYC1807260);辽宁省自然科学联合基金资助项目(2020-HYLH-14)
Fund:Liaoning Province “Plan of Rejuvenating Liao Talents” Project (XLYC1807260), Liaoning Natural Science Joint Foundation (2020-HYLH-14)
李佳航(1997—),男,硕士研究生,主要研究方向为管道剩余寿命预测。
LI Jia-hang, WANG Dan, XIE Fei, et al. Research progress on CO2corrosion and protection of oil and gas pipelines[J]. Surface technology, 2021, 50(4): 172-183.
