基于原位单向肠灌流模型研究没食子酸的肠吸收特性
2021-05-07程珍珍周本宏李旷宇
程珍珍,周本宏,姜 珊,李旷宇,金 丹
(1.武汉大学人民医院药学部,湖北 武汉 430060;2.武汉大学药学院,湖北 武汉 430072)
没食子酸(Gallic acid)是石榴皮中可水解鞣质的水解产物,是石榴皮中没食子苷的重要生物活性成分之一。已有大量研究表明,没食子酸具有多种生物活性,如抗氧化、抗菌、抗癌、抗炎、心脏保护和神经保护等作用[1-5]。原位单向肠灌流是研究药物在肠道不同区域的通透性和肠道吸收机制最常用的方法[6-7]。本研究采用原位单向肠灌流模型,研究没食子酸在大鼠各肠段的吸收特性。同时考察不同肠段、药物浓度、时间、pH值、P-gp、MRP2对药物吸收的影响。为提高鞣质类成分口服制剂的生物利用度提供理论依据。
1 材料
1.1 药品与试剂没食子酸标准品(成都曼斯特,16022801,纯度99%);葛根素标准品(阿拉丁,P111269,纯度≥98%);盐酸维拉帕米(阿拉丁,K1629079);吲哚美辛(阿拉丁,C1723020);甲醇、乙腈为色谱纯;水为纯净水;其他试剂均为分析纯。
1.2 仪器BT1-200恒流泵(上海琪特分析仪器有限公司);HX1002T电子天平(武汉世纪超杰实验仪器有限公司);分析天平(德国Sartorius);LC-20AT高效液相色谱仪(日本岛津);LGC-1025M柱温箱(荆州市津海化工科技有限公司);色谱柱(英国Fortis);实验室pH计(瑞士Mettler Toledo)。
1.3 实验动物SPF级SD大鼠,体质量(200±20)g,合格证号SCXK(鄂)2015-0018,由武汉大学人民医院动物实验中心提供,实验前在实验环境中适应 1 周。
2 方法
2.1 溶液配制
2.1.1Krebs-Ringer’s溶液的配制 称取NaCl 7.8 g、NaHCO31.37 g、KCl 0.35 g、CaCl20.37 g、MgCl20.02 g、NaH2PO40.32 g、葡萄糖1.40 g,加水定容至1 000 mL,即得(pH 7.4)。
2.1.2对照品溶液的配制 取2.00 mg没食子酸标准品,精密称定,用甲醇溶解后,于25 mL棕色容量瓶中定容,并作为母液贮存于4 ℃冰箱。
2.1.3内标溶液的配制 本实验选用葛根素为内标物质,取葛根素标准品配制浓度为100 mg·L-1的溶液于10 mL容量瓶中,贮存于4 ℃环境中备用。
2.1.4供试品溶液的配制 精密称定没食子酸适量,用空白肠循环液溶解并稀释成含没食子酸质量浓度分别为 20、40、80 mg·L-1的溶液,即得。
2.2 没食子酸的定量测定
2.2.1色谱条件 色谱柱为C18 柱(250 mm×4.6 mm,5 μm);流动相,有机相乙腈(A),水相三氟乙酸(B),洗脱条件如下:0-8min,B 98%-78% 梯度洗脱,8-15min,B为78% 等度洗脱;流速1.00 mL·min-1;检测波长254 nm;柱温30 ℃;进样量20 μL。
2.2.2标准曲线的绘制 分别精密吸取对照品母液0.625 mL、1.250 mL、2.500 mL、3.750 mL、5.625 mL、10.000 mL,加溶剂定容于10.00 mL棕色容量瓶中。每个浓度对照品按照“2.2.1项”色谱条件下实验条件连续进样3次,得出峰面积值,以对照品浓度x轴,对照品和内标峰面积比值y轴绘制标准曲线。得出曲线公式:y=0.307 4 x+0.648 1,R2=0.999 5,没食子酸在5.00-80.00 mg·L-1呈良好的线性关系。
2.2.3精密度考察 日内精密度考察:取“2.1.2项”条件下配制的对照品母液,稀释高、中、低3个不同浓度,按照“2.2.1项”色谱条件每隔2 h进样1次,相同方法进样5次,求出峰面积的RSD值。日间精密度:按照日内精密度的测定方法,连续测定5 d,计算每日峰面积平均值的RSD值。结果显示高、中、低3个质量浓度各指标成分峰面积RSD值均小于3%,表明该方法精密度良好。
2.2.4稳定性考察 按照“2.1.2项”方法平行配制样品3份,取5.00 mL,加肠灌流液定容至10.00 mL于棕色容量瓶中,进行预处理后从0 min开始进样,后第30 min、第60 min、第90 min、第120 min、第150 min分别进样,将每个时间点的峰面积与初始时间峰面积做对比。结果表明,没食子酸在肠灌流液中的稳定性符合要求,满足测定要求。
2.2.5专属性考察 分别取大鼠空白肠灌流液、空白肠灌流液加没食子酸标准品及内标、没食子酸肠灌流液,预处理后按照“2.2.1项”色谱下条件进样分析,得到灌流液中没食子酸色谱图。结果显示没食子酸峰形良好,与内标物分离完全。内源性物质对药物测定的影响忽略不计,该方法具有较好的专属性。
2.2.6回收率考察 取采集后的高、中、低3个不同浓度的肠灌流液,加入已知浓度的对照品溶液,按照“2.2.1项”色谱下条件下进样分析,得到峰面积,按照公式:回收率/%=(加入标准样品量-样品含量)/加入标准样品量×100%进行计算,得到不同浓度样品的加样回收率。结果表明该方法回收率良好。
2.3 大鼠在体单向肠灌流实验[8]取已禁食12 h(不禁水)健康SD大鼠,大鼠腹腔注射水合氯醛300 mg·kg-1麻醉后,固定,沿腹中线剪开小口,将大鼠肠道暴露,小肠两端插管并结扎。用预热至37 ℃的生理盐水排净肠道内容物,换成空白K-R液,平衡15 min,再更换为含药肠灌流液将管道饱和15 min,直至出液口溶液与进液口溶液中药物的质量浓度相等,消除实验过程中肠道对药物的吸附作用。降低灌流体积流量0.20 mL·min-1,每15 min更换1次灌流液和收集瓶,实验持续90 min,实验结束后将大鼠处死,剪下灌流肠段,在37 ℃生理盐水浸润下剪开肠段,测量其长度(l)和横截面半径(r)。
2.4 肠吸收参数计算在体单向肠灌流模型用重量法对灌流液的流入和流出的体积进行校正,消除其体积变化的影响[9]。吸收率常数(Ka)和有效表观渗透率系数(Peff)的计算公式如下:
Ka=(1-CoutQout/CinQin)Q/πr2l
Peff=[Q×ln (CoutQout/CinQin)]/2πrl
其中,Qin和Qout分别为肠段灌入的灌流液和收集液的体积(mL,假定灌流液和收集液的质量浓度为1.0 kg·L-1),Q为灌流体积流量(0.20 mL·min-1),Cin 和Cout分别为灌流液和收集液的药液质量浓度(mg·L-1),l和r分别为被测段的长度(cm)和半径(cm)。

3 结果
3.1 不同肠段对药物吸收的影响取没食子酸质量浓度为40 mg·L-1的供试液,按“2.3”项操作,考察药物在大鼠十二指肠、空肠、回肠、结肠4个肠段的吸收情况。计算Ka和Peff值,结果见Tab 1。结果表明,没食子酸在不同肠段均有吸收,其在不同肠段的Ka大小顺序是空肠>十二指肠>回肠≈结肠。除空肠与结肠(Ka、Peff值比较)之间无差异外,其他各组之间差异有显著性(P<0.05)。肠道上端没食子酸的吸收优于肠道下端的吸收。
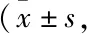
Tab 1 Absorption of gallic acid at various segments in intestine of rats n=5)
3.2 不同药物质量浓度对肠吸收的影响以空肠为考察肠段,取质量浓度为20、40、80 mg·L-1的供试液,按“2.3”项下的方法操作,分别进行实验,考察药物质量浓度对吸收的影响。计算Ka、Peff 值,结果见Tab 2。不同质量浓度下没食子酸大鼠空肠吸收参数差异没有显著性(P>0.05),提示没食子酸在小肠的吸收没有浓度依赖性,吸收机制为被动扩散。
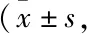
Tab 2 Effect of drug concentration on Ka and Peff of gallic acid n=5)
3.3 不同pH值对肠吸收的影响分别用稀HCl和稀NaOH溶液调节K-R缓冲液pH值为5.4和6.8,配制不同pH值的灌流液(没食子酸40 mg·L-1),考察 pH 值对药物吸收的影响。结果如Tab 3所示,当介质pH 值升高时,没食子酸在空肠的Ka、Peff 值明显降低(P<0.05)。

Tab 3 Effect of pH value on Ka and Peff of
3.4 P-gp对肠吸收的影响按“2.3”项下的方法操作,以空肠为考察肠段,考察 P-gp 抑制剂对药物吸收的影响。计算Ka和Peff,结果如Tab 4所示,加入维拉帕米(P-gp抑制剂)后,没食子酸吸收增加(P<0.05),表明没食子酸可能是P-gp底物。没食子酸的吸收受到P-gp外排作用的影响。
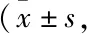
Tab 4 Effect of P-gp on Ka and Peff of gallic acid n=5)
3.5 MRP2对肠吸收的影响按“2.3”项下的方法操作,以空肠为考察肠段,考察MRP2抑制剂对药物吸收的影响。计算Ka和Peff,结果如Tab 5所示,加入吲哚美辛(MRP2抑制剂)后,没食子酸吸收增加(P<0.05),表明没食子酸可能是MRP2底物。
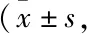
Tab 5 Effect of MRP2 on Ka and Peff of gallic acid n=5)
4 讨论
肠道吸收对口服药物的生物利用度起着至关重要的作用。在肠道中,有许多参与药物药代动力学过程的运输蛋白。因此,研究其转运机制对提高其有效性和安全性具有重要意义[10]。
近年来,国内外对没食子酸的药理活性研究很多,然而对其肠吸收的机制研究相对较少。我们之前的研究阐述了没食子酸在Caco-2细胞单分子膜上的转运和吸收特性[11]。然而,目前为止,利用原位单向肠灌流法研究没食子酸在肠道中的吸收还没有被报道,没食子酸的吸收机制尚未完全阐明。因此,本研究采用原位单向肠灌流模型,进一步探究不同浓度没食子酸在小肠不同肠段的肠道吸收机制以及影响肠道吸收的因素。
在单向肠灌流中可以看出,随着没食子酸浓度的增加,肠道中的Peff值无明显差异,说明没食子酸在肠道的吸收方式主要是被动扩散。对于被动转运,不存在饱和,药物可以沿浓度梯度在没有ATP的情况下跨膜转运,包括载体转运、细胞外转运和细胞旁转运。根据文献,当Peff值<3×10-6cm·s-1时,说明药物吸收不良,当Peff值>2×10-5cm·s-1时,药物吸收良好[12]。在我们的研究中,没食子酸在4个肠段中的Peff值均>2×10-5cm·s-1。因此,没食子酸在肠内吸收良好。没食子酸在小肠上端的吸收好于小肠下端的吸收。可能原因是不同肠段存在生理差异,包括膜成分、粘膜厚度、酶活性、转运数量和能力等[13]。在酸性条件下,没食子酸的吸收较好。可能是由于没食子酸呈酸性,所以在酸性条件下它可能能够被更好地吸收。
P-糖蛋白(P-gp)和多药耐药相关蛋白-2(MRP2)主要分布于细胞质膜上,是影响药物在肠道内转运的主要外排转运蛋白[14]。我们的研究表明,维拉帕米(P-糖蛋白抑制剂)和吲哚美辛(MRP2抑制剂)显著增加空肠没食子酸的有效表观渗透率系数值,说明肠道对没食子酸的吸收受到外排转运体(P-gp、MRP2)的影响。
综上,没食子酸的吸收机制可能是被动扩散,没食子酸在小肠内吸收良好。细胞旁转运通路和外排转运体也参与了没食子酸的转运。P-gp和MRP2可能参与没食子酸的肠道吸收。此外,没食子酸在全肠段都能吸收,肠道上端没食子酸的吸收优于肠道下端的吸收。本实验利用大鼠在体单向肠灌流模型,阐明了没食子酸在肠道中的吸收特性。对于进一步研究鞣质类成分的作用机制、提高生物利用度、指导临床合理用药具有重要的意义。
