纤维素骨架支撑的高吸水性树脂的制备及性能研究
2021-05-06李新平陈立红
李新平 张 力 常 慧 张 召,2,* 陈立红
(1.陕西科技大学轻工科学与工程学院,轻化工程国家级实验教学示范中心,陕西省造纸技术及特种纸品开发重点实验室,陕西西安,710021;2.华南理工大学制浆造纸工程国家重点实验室,广东广州,510640;3.陕西科技大学机电工程学院,陕西西安,710021;4.陕西科技大学前沿科学与技术转移研究院,陕西西安,710021)
高吸水性树脂(SAR)是一种具有强亲水性基团和三维网络结构的功能高分子材料[1]。它不仅具有优良的吸水性能,而且具有良好的保水性能。与普通吸水材料相比,可以吸收大量水或生理盐水,且短时间内吸水量可达自身质量的数百倍,即使在高温高压下也具有良好的保水性能。因此,广泛应用于医药卫生、食品工业、水处理、农林、肥料和药物缓释、化学工业等领域[2-3]。然而,目前使用的高吸水树脂大多以石油为原料,成本高、潜在毒性大,其生物降解性差,存在潜在的环境危害。因此,基于天然高分子材料的高吸水树脂的研究逐渐成为近年来的研究热点之一[4]。
纤维素作为一种天然高分子材料,具有来源广、成本低、无毒、可生物降解、使用安全性高等优点[5]。而且纤维素分子具有刚性平整结构,含有大量亲水基团,能与大部分小分子化合物发生反应,得到取代度较高的衍生物,且纤维素纤维内部有较多的毛细管,比表面积大,适合做吸水材料的原料[6]。在高吸水树脂中添加纤维素作为骨架接枝亲水性烯烃单体,纤维素的加入既能减少石油原料的用量,达到降低成本的目的,又能够使高吸水树脂具备可降解性能。所以许多学者致力于开发性能优良的纤维素基高吸水性树脂。Liu等人[7]制备了一种由麦秸纤维素组成的半互穿聚合物网络的高吸水性材料。其在蒸馏水中的吸水倍率最佳为266.82 g/g,在质量分数0.9%NaCl溶液中的吸水倍率最高为34.32 g/g。Cheng等人[8]以羟丙基纤维素、丙烯酸、2-丙烯酰胺-2-甲基丙磺酸和红土为原料合成了一种吸水、保水性能优异的高吸水树脂,发现在高吸水树脂中加入纤维素可以提高其溶胀率和吸水能力。因此,将纤维素引入高吸水树脂中,可以克服合成高吸水性树脂的缺点,满足高吸水性材料的使用要求,使最终产品具有优良的性能[9-11]。
近年来,竹纤维作为木材纤维的替代品,在生产天然纤维增强生物复合材料方面引起了人们的关注。竹子是地球上生长最快的植物之一,且竹子的机械性能与一般木材相当,但成熟期只需6~8 个月[12-14]。竹子的天然纤维素含量在40%~50%之间,与木材接近,且竹结构疏松,易于降解。所以以竹子为原料制备纤维素产品对环境的负面影响较小,同时可以减少对木材的消耗。因此,对其有效利用的研究就显得尤为重要[15]。
大多数以纤维素为骨架的高吸水性树脂都是用溶液聚合法生产的。在均相聚合中,溶液聚合因其聚合热控制好、成本低、方便等优点而成为首选[16]。纤维素系列大分子、单体、引发剂、交联剂等在水中有良好的溶解性,均可在水中自由溶解。一旦引发剂由温度或辐射引起,即开始聚合过程。该反应的产物经过干燥和粉碎,用于各种领域[17-18]。利用溶液聚合的方法合成高吸水树脂的机理主要归因于自由基诱导聚合[19]。自由基聚合是通过引发剂引发单体聚合的过程,这种聚合由于具有较高的聚合速率,并且发生在水介质中,安全、无害,因此得到广泛应用。以竹纤维为原料制备高吸水材料,能改善材料的吸水性及可生物降解性,达到绿色发展的目的[20-23]。同时可提升天然纤维素的经济附加值,拓展吸水材料的应用领域,具有一定的经济价值和社会效益[24-26]。
鉴于此,本研究采用价格低廉的漂白竹浆作为纤维素的来源,首先对竹浆纤维(bamboo pulp fibers,BPF)进行预处理,创新性地采用纤维素酶与低温碱尿素体系联合处理的方法对竹浆纤维进行改性,得到有利于接枝反应的改性竹浆纤维(modified bamboo pulp fibers,MBPF);然后通过水溶液聚合法,将丙烯酸接枝于改性竹浆纤维上,制得纤维素骨架支撑的高吸水性树脂(MBPF-g-PAA);采用傅里叶变换红外光谱、扫描电子显微镜和热重分析仪对MBPF-g-PAA 进行表征;并且探讨了竹浆纤维及引发剂用量对树脂吸水性能的影响,分析了溶液的pH值、树脂颗粒大小、溶胀介质(离子浓度、阳离子、离子强度)对树脂吸水性能的影响。
1 实 验
1.1 原料、试剂与仪器
漂白竹浆(水分含量7.7%,半纤维素含量14.81%,木质素含量0.64%),取自四川某造纸厂。复合纤维素酶(液体酶,提取自Trichoderma reeseiATCC 26921),型号Cellulase 1.5 L,密度为1.2 g/mL,最适温度为40~50℃,最适pH 值为4~6,其滤纸酶活为104 FPU/mL,购自美国Sigma 公司。丙烯酸(AA)、过硫酸钾(KPS)、N,N’-亚甲基双丙烯酰胺(NMBA)、 柠 檬 酸(C6H8O7·H2O)、 氢 氧 化 钠(NaOH)、乙醇,均为分析纯,购自西安凯洛仪器有限公司。实验室用水为蒸馏水。
DHG-9053A 电热恒温鼓风干燥箱,杭州惠尔仪器厂;HASUC 恒温水浴振荡器,上海合成仪器有限公司;DF-101S 集热式恒温加热磁力搅拌器,上海予申仪器有限公司;顶置搅拌器,郑州长城科工贸易有限公司;SHZ-D(Ⅲ)循环水式多用真空泵,河南予华仪器有限公司;Vertex70 傅里叶变换红外光谱仪(FT-IR),德国Bruker 公司;S4800 场发射扫描电子显微镜(SEM),日本日立公司;D8 Advance X 射线衍射仪(XRD),德国Bruker 公司;同步热分析仪(TG-DSC),德国耐驰仪器制造有限公司;X 光电子能谱仪(XPS),英国岛津/Kratos 公司;纤维形态分析仪,法国Techpap公司。
1.2 实验过程
1.2.1 竹浆纤维预处理
将漂白竹浆用去离子水反复冲洗干净,撕碎,置于50℃电热恒温鼓风干燥箱中干燥。取一定量干燥后的竹浆纤维(BPF)经粉碎机粉碎后筛分,选取80~100 目的竹浆纤维粉末密封备用。准确称取3 g 粉末于锥形瓶中,与pH值4.8的柠檬酸钠缓冲液混合,调节浆料浓度为3%,加入10 FPU/g 复合纤维素酶溶液(酶用量相对于绝干浆质量),然后将锥形瓶置于50℃恒温水浴振荡器中反应3 h。反应结束后,立即将锥形瓶浸入沸水浴中灭活10 min,并在25℃下以2500 r/min转速离心15 min得到复合纤维素酶预处理后的竹浆纤维。接着将纤维素酶预处理后的竹浆纤维溶于预冷(-12.5℃)的NaOH/尿素/H2O(质量比7∶12∶81)水溶液中,并在室温下搅拌2 h 后加5%的硫酸中和至pH 值为7,反应结束后用蒸馏水洗涤以去除残留的酸,然后在25℃下以2500 r/min 转速离心15 min,最后置于50℃电热恒温鼓风干燥箱中干燥12 h,得到改性竹浆纤维(MBPF),将MBPF 用自封袋密封好备用。
1.2.2 纤维素骨架支撑的高吸水性树脂(MBPF-g-PAA)的制备
称取适量MBPF 放入装有机械搅拌器、回流冷凝管和氮气管路的250 mL 三口烧瓶中,加入适量蒸馏水调节至适当的浓度,连续搅拌使其分散,用氮气净化30 min,除去系统中溶解的氧气,形成均匀的溶液。将溶液加热至60℃,加入适量引发剂KPS,保持15 min 引发纤维素生成自由基。15 min 后,依次加入中和度为70%的丙烯酸溶液以及0.06%的交联剂N,N’-亚甲基双丙烯酰胺,当体系出现凝胶后继续反应6 h 后取出产物(其反应过程如图1 所示)。将所得产品倒入无水乙醇中沉淀,并在无水乙醇中浸泡12 h除去未反应的单体,然后用剪刀剪碎,并在50℃下真空干燥24 h;或用各种脱水剂(包括甲醇、乙醇和丙酮)干燥。干燥的凝胶颗粒经过粉碎和筛分,最后得到10~120 目的纤维素骨架支撑的高吸水性树脂(MBPF-g-PAA)。该树脂在60℃下丙酮抽提24 h,除去副反应中产生的均聚物。MBPF-g-PAA 的制备机理如图2 所示[27]。在不添加竹浆纤维的情况下,采用相同的方法制备了高吸水性树脂(PAA)。
1.3 性能测试
1.3.1 吸水倍率
在室温下将0.1 g 样品浸入500 mL 的蒸馏水中,室温下静置8 h,以达到溶胀平衡。然后凝胶在重力作用下通过200 目筛网过滤30 min,使溶胀的样品与未被吸收的水分离,直到没有游离水。吸水倍率Qeq计算如式(1)所示。

式中,M1和M2分别为干燥样品和溶胀样品的质量,g。Qeq为平衡吸水倍率,g/g,定义为以每克样品中的水克数计算。采用同样的方法测定高吸水性树脂在不同盐溶液(NaCl、KCl、NH4Cl、MgCl2、CaCl2和FeCl3)中的吸水倍率。所有样品重复测定3次,取平均值。

图1 纤维素骨架支撑的高吸水性树脂(MBPF-g-PAA)的制备过程示意图Fig.1 Preparation of cellulose-supported superabsorbent resin(MBPF-g-PAA)

图2 纤维素骨架支撑的高吸水性树脂(MBPF-g-PAA)的制备机理示意图Fig.2 Preparation mechanism of cellulose-supported superabsorbent resin(MBPF-g-PAA)
1.3.2 保水倍率
称取一定量树脂样品浸泡在蒸馏水中,室温下达到溶胀平衡。将溶胀的样品放在筛网中静置30 min,以去除多余的水,称量质量,然后将其放在温度分别为25、40、60℃的电热恒温鼓风干燥箱中干燥。每隔30 min 称量1次质量,持续6 h,按式(2)计算不同温度下的保水倍率(R)。

式中,R为保水倍率,%;M4和M5分别为溶胀样品和干燥样品质量,g;M3表示未溶胀样品的质量,g。
1.3.3 不同pH值下的吸水倍率
通过稀释NaOH水溶液(pH 值13.0)和HCl水溶液(pH 值1.0),配制不同pH 值的酸性及碱性溶液,以达到所需的pH值。吸水倍率的测试同1.3.1。
1.3.4 溶胀重复性的测定
溶胀重复性实验过程:准确称取0.1 g 干燥样品,置于500 mL 蒸馏水中,在室温下放置4 h以达到溶胀平衡。然后将完全膨胀的样品置于60℃的烘箱中,直到样品完全干燥。然后加入等量的蒸馏水使其再次膨胀。如此重复5次,并测定每次的溶胀率,计算方法同1.3.1。
1.4 样品结构表征
1.4.1 红外光谱(FT-IR)分析
将KBr 颗粒在60℃下干燥4 h。将待测样品研磨至粉末,真空干燥48 h 用于FT-IR 分析。采用KBr 压片法,扫描范围4000~500 cm-1。
1.4.2 扫描电子显微镜(SEM)分析
取适量待测样品采用真空冷冻干燥的方式脱除水分,将干燥的样品固定在贴有导电胶的样品台上,经喷金60 s后,进行SEM分析。
1.4.3 X射线衍射(XRD)分析
将干燥后粉末样品置于微量样品载物台上,用X射线衍射仪进行扫描分析。实验测试条件为:Cu 靶Ka射线,X射线衍射仪发生器电压40 kV,电流40 mA,扫描速度4°/min,扫描范围2θ在5°~60°之间,扫描时间566.4 s,扫描增量0.02°。
1.4.4 热重(TGA)分析
样品干燥后,取2~3 mg 置于坩埚中,用热重分析仪进行测试,实验所需仪器参数为:温度范围25~600℃,升温速率10℃/min,氮气流量40 mL/min。
1.4.5 X射线光电子能谱(XPS)分析
取少量干燥后的样品固定在样品台上,用XPS测定样品表面化学元素的化学状态。实验所需仪器参数:光源A1Kα激发光能量(1486.61 eV),电压10 kV,电流10 mA。
2 结果与讨论
2.1 FT-IR分析
图3(a)所示为竹浆纤维、改性竹浆纤维和高吸水性树脂的FT-IR 图。从图3(a)可以看出,在BPF 和MBPF 光谱中,3343.8 和2911cm-1的吸收峰分别是由羟基(OH)和C—H的伸缩振动引起的。1036 cm-1处的吸收峰与—CH—O—CH 拉伸振动有关,这些均为纤维素结构的特征吸收峰。在MBPF-g-PAA 光谱中,从3455.9 cm-1变化到3437.8 cm-1,这是由于—OH 拉伸振动引起的。在2911 cm-1处的峰是由亚甲基引起的,在1690 cm-1处的吸收峰与羧酸有关。在1322~1044 cm-1处的特征峰为酯基吸收峰,在2690 cm-1处出现1个特征峰,这是羰酸的—OH伸缩振动,说明丙烯酸成功接枝在改性竹浆纤维上。此外,对比PAA和MBPF-g-PAA 光谱发现,在1038 cm-1和880 cm-1处观察到新的吸收峰,分别—CH—O—CH 结构的拉伸振动和=C—O—C—结构的伸缩振动,提供了聚合过程中MBPF 接枝PAA 官能团的证据[28]。综上所述,FTIR 图验证了树脂中存在丙烯酸中的羧基以及烷基碳。因此,MBPF-g-PAA 包含共聚物和纤维素的交联结构,该树脂确实为丙烯酸和纤维素的共聚产品。
2.2 XRD分析

图3 竹浆纤维、改性竹浆纤维和高吸水性树脂的FT-IR图、XRD图、TG图和DTG图Fig.3 FT-IR,XRD,TG and DTG of bamboo pulp fiber,modified bamboo pulp fibers and superabsorbent resin
图3 (b)所示为竹浆纤维、改性竹浆纤维和高吸水性树脂的X 射线衍射图。从图3(b)可以看出,BPF 在2θ为16.5°、22.1°和34.5°处表现出典型的衍射,分别对应101 晶面、002 晶面和040 晶面的衍射吸收峰,可以得出纤维素具有多晶结构的结论。对比MBPF 可以看出,经复合纤维素酶和低温碱尿素共同处理后的MBPF 在2θ为21.9°处出现1个衍射峰,该峰为纤维素I 的特征峰,且有部分衍射峰消失。可能是因为预处理过程中纤维素的结晶区遭到了破坏,氢键部分断裂,使纤维素的晶格发生了一定程度的溶胀和拆散,导致结晶度降低[29]。从MBPF-g-PAA 的图谱中可以看出,尖锐的特征衍射峰消失,出现了强度小而范围宽的衍射峰,且树脂比纤维素表现出更大的非晶态结构。可能的原因是MBPF 的晶体结构转换为非晶态结构,这是因为纤维素和聚合单体之间的接枝反应使得纤维素单体的环状结构遭到破坏,改变了纤维素的聚合状态,晶体结构被破坏。
2.3 热稳定性分析
图3(c)和图3(d)所示为竹浆纤维、改性竹浆纤维和高吸水性树脂的TG和DTG曲线。从图3(c)和图3(d)可以看出,BPF 和MBPF 的热降解曲线有3 个过程:第一阶段是从室温到280℃,质量损失9.36%,这是由于水分蒸发;第二阶段发生在286~365℃之间,这是因为纤维素开始分解,纤维素的热解始于糖苷键的随机分裂,质量损失68.48%,最大质量损失速率出现在356℃附近;第三阶段是由于纤维素的碳化,质量损失8.73%,最后的残留质量为15.72%。PAA 和MBPF-g-PAA 的质量损失过程表现出相似的趋势,热分解主要分为4个过程,第一阶段发生在216℃之前,是由于高吸水树脂和未反应原料中的水分蒸发;第二阶段在228~422℃之间,树脂中的小分子和低聚物开始分解[30-32];第三阶段在422~490℃之间,这归因于聚合物中支链的分解,为接枝聚合物的损失峰,质量损失率约为19.49%,最大分解温度在430℃左右;第四阶段的分解温度为490~600℃,这是由于聚合物主链的分解和三维网络的破坏。因此,接枝反应后纤维素的结构发生了变化,这一质量损失过程也证明了高吸水性树脂的成功制备及其具有良好的热稳定性。
2.4 形态分析
MBPF-g-PAA 经粉碎筛选后呈白色粉末状,吸水溶胀饱和后是透明的水凝胶,图4 所示为MBPF-g-PAA 溶胀前后的形貌。高吸水性树脂的吸水机理可以通过Flory-Huggins[33]溶胀公式(3)解释。

式中,Qeq为平衡吸水倍率,S为溶液的离子强度,i/Vu为聚合物的电荷密度,(0.5-x1)/V1为树脂对溶剂的亲和力,Ve/V0为树脂的交联密度。
高吸水性树脂的吸水倍率和保水倍率取决于树脂的孔隙率。因此,树脂的微观结构形态是最重要的性能之一。图5为竹浆纤维、改性竹浆纤维和高吸水性树脂的SEM 图。由图5(a)和图5(b)可以看出,经过预处理后竹浆纤维形状和尺寸都产生了改变,纤维变短,有部分细小再生纤维素分散其中且结构疏松,溶剂更易进入纤维素分子内进行作用[34]。由图5(c)~图5(f)可以看出,PAA 有少量孔结构。加入竹浆纤维后,MBPF-g-PAA 的表面形态发生了显著变化,表面呈现出相对均匀疏松的三维网络孔隙结构,具有多孔的表面形貌,有利于水迅速渗入高吸水性树脂颗粒。这种多孔结构可以通过在膨胀介质中提供更多的接触表面积来增加树脂的溶胀速率,使得产品表现出优良的吸水性能。这一观察表明,纤维素的引入有利于改善树脂的网络结构。
2.5 反应物的质量比对吸水倍率的影响

图4 MBPF-g-PAA溶胀前后的形貌对比图Fig.4 Comparison before and after swelling of MBPF-g-PAA
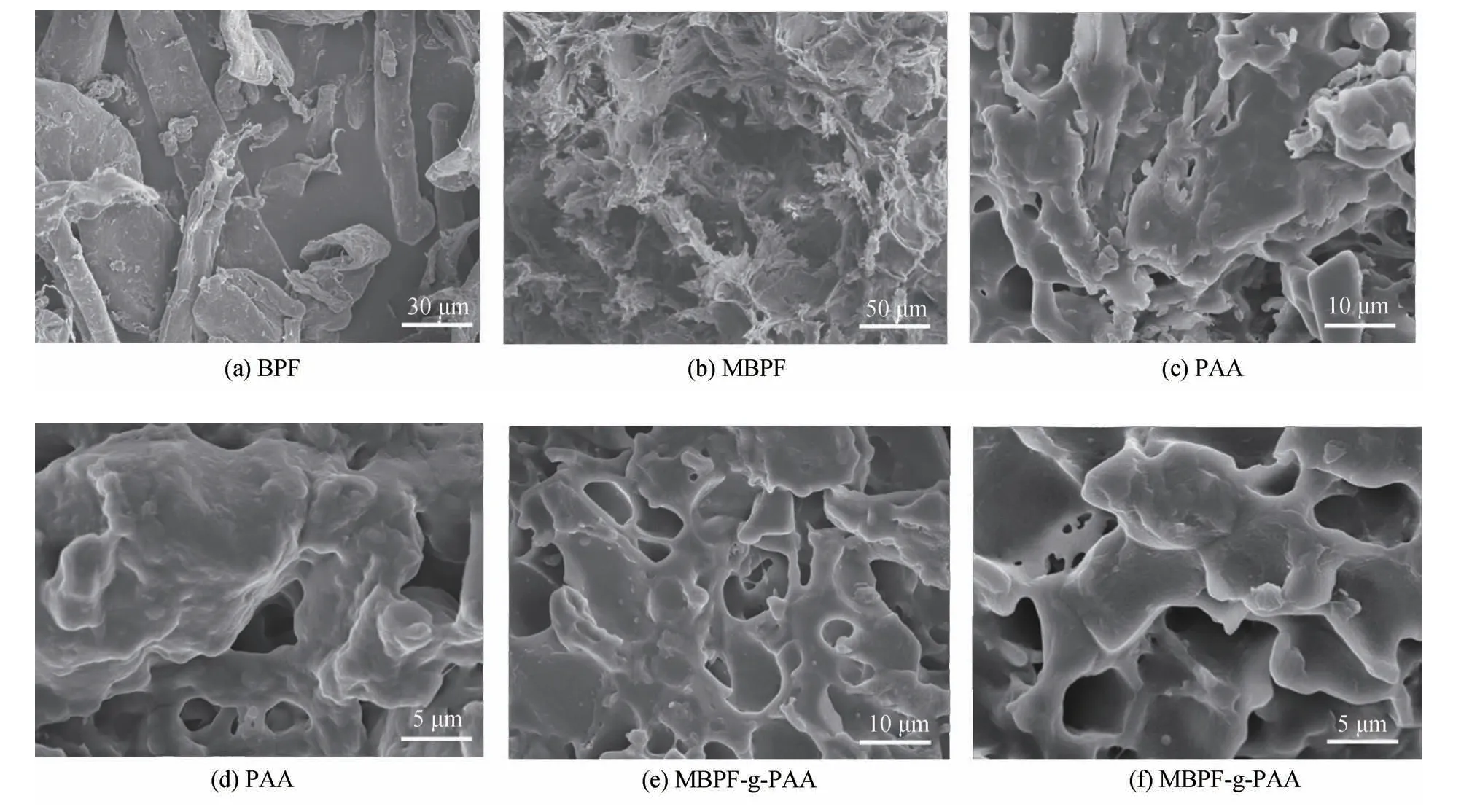
图5 竹浆纤维、改性竹浆纤维和高吸水性树脂的SEM图Fig.5 SEM images of bamboo pulp fiber,modified bamboo pulp fiber,modified bamboo pulp fibers and superabsorbent resin
图6 (a)所示为改性竹浆纤维与丙烯酸的质量比对MBPF-g-PAA 吸水倍率的影响。从图6(a)可以看出,当m(MBPF)∶m(AA)在1∶15、1∶10、1∶8 之间时,随着MBPF 比例的增加,MBPF-g-PAA 吸水倍率显著提高。这是因为网络介质亲和力增加,聚合物链的增长形成致密的三维网状结构,使溶胀能力增加。但m(MBPF)∶m(AA)为1∶5 时,MBPF-g-PAA 的吸水倍率出现降低。可能的原因是随着MBPF 比例的增加,反应体系的黏度增加,从而降低了AA 与接枝链主动碰撞的概率,不利于聚合物网络结构的形成[35-37]。另一方面,MBPF 的用量对接枝聚合很重要,纤维用量过少对接枝聚合有不利的影响。
图6(b)所示为引发剂用量对MBPF-g-PAA 吸水倍率的影响。从图6(b)可以看出,当KPS用量从0.2%增加到0.5%时,吸水倍率增加。然后随着引发剂用量的增加,吸水倍率显著下降。在KPS 用量为0.5%时获得最大的吸水倍率。这是由于在引发剂的作用下增强了纤维素网络骨架,导致更高的接枝聚合程度,吸水倍率增大。而KPS用量高于最佳值则会导致低溶胀比,这种溶胀损失可能是由于分子碰撞导致“终止阶跃反应”的增加,交联密度增大。Chen等人[38]将这种可能的现象称为“自交联”。还可能是由于纤维素葡萄糖单元,多糖主链中存在更多的可利用位点与丙烯酸反应,但是过量的KPS产生更多的自由基,加速链终止反应。

图6 改性竹浆纤维与丙烯酸质量比和引发剂用量对MBPF-g-PAA吸水倍率的影响Fig.6 Effect of ratio of bamboo pulp fiber to acrylic monomer and initiator amount on water absorption performance of MBPF-g-PAA
2.6 吸水倍率、溶胀重复性和保水倍率分析
图7(a)为MBPF-g-PAA 在蒸馏水中的动态溶胀行为。从图7(a)可以看出,在蒸馏水中MBPF-g-PAA在160 min内达到溶胀平衡,此时吸水倍率为980.87 g/g。在溶胀过程中,水需要不断克服树脂内部的渗透压,渗透压差越大,水渗透到树脂内部的速度越快。在溶胀过程开始时,由于树脂的低弹性,渗透压较低,在树脂网络中亲水性基团和阴离子基团的排斥增强了渗透压差。因此,树脂具有较高的吸水倍率。随着时间的延长,更多的水进入树脂网络内部,渗透压差逐渐减弱。因此,水需要克服较大的渗透压,吸水倍率变得越来越小,即溶胀能力逐渐达到平衡。
高吸水性树脂的溶胀重复性是其应用的关键,因此研究了MBPF-g-PAA 的溶胀重复性,结果如图7(b)所示。从图7(b)可以看出,MBPF-g-PAA 在重复使用后仍具有良好的溶胀能力。吸水倍率随着循环溶胀次数的增加而降低,但下降趋势减缓。这可能是由于重复吸水后聚合物链的结构发生变化,导致吸水倍率降低。经过5 次循环溶胀后,MBPF-g-PAA 仍保持62%以上的吸水能力。表明MBPF-g-PAA 为一种可重复吸水的材料。
图7(c)显示了MBPF-g-PAA 在温度25、40、60℃下的保水倍率。图7(c)表明,在室温下MBPF-g-PAA具有较高的保水倍率。在40℃和60℃下的保水倍率相比于室温来说略有下降,解吸过程中水扩散速率较高,树脂失水速率较快,解吸6 min 时,保水倍率分别为85%和78%。保水倍率的差异可以通过范德华力和氢键的影响来确定。随着温度的升高,保水倍率降低的原因可能是氢键断裂,氢键主要吸收树脂中的水分子。通过在不同转速下的离心实验,测试了MBPF-g-PAA在不同离心力下的保水倍率,图7(d)显示了MBPF-g-PAA 保水倍率与转速之间的关系。从图7(d)可知,随着转速的增加,保水倍率降低;当转速升至4800 r/min 时,保水倍率仅为78%左右。原因可能是不断增加的离心力打破了水分子与聚合物网络上亲水基团之间的连接。
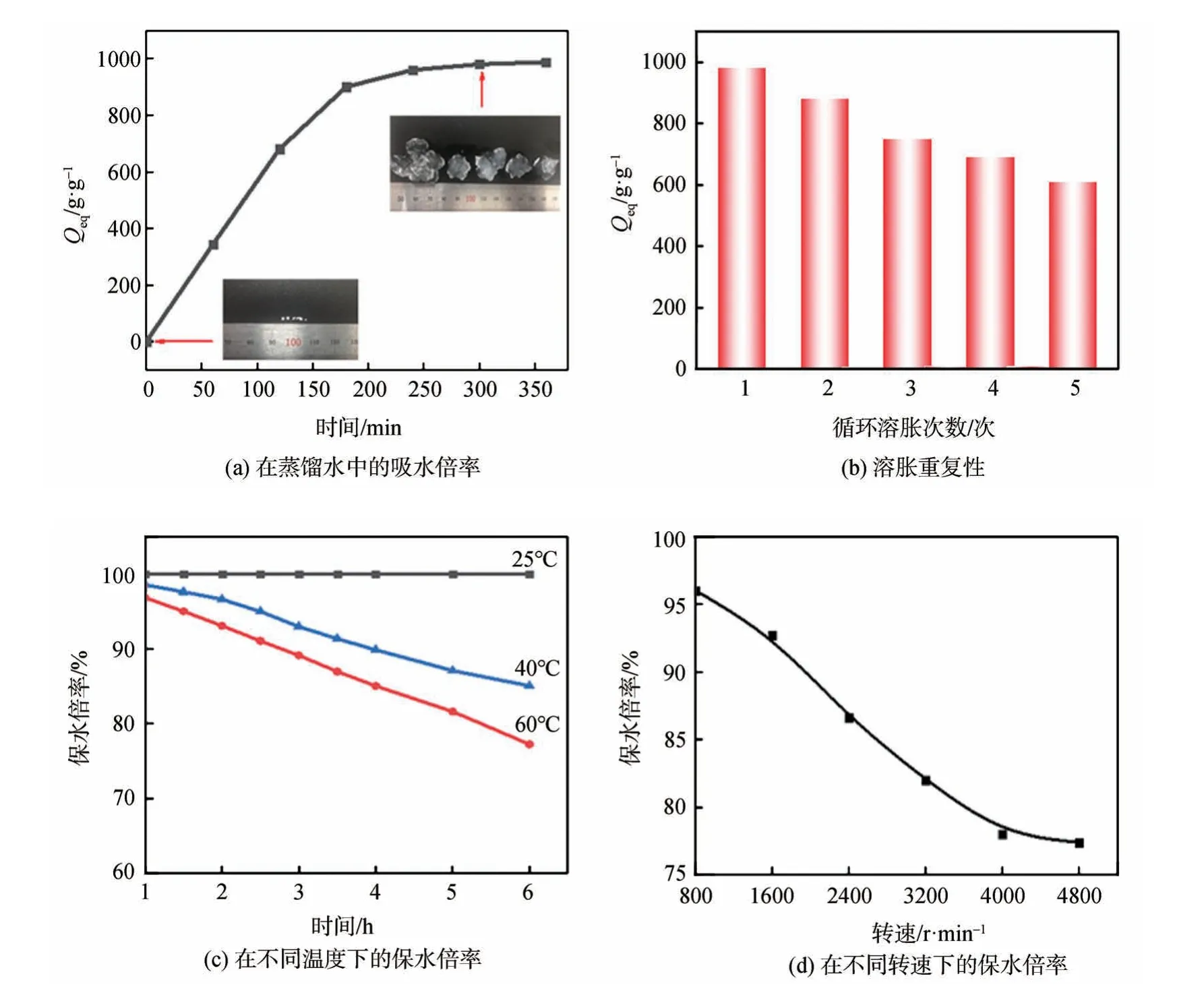
图7 MBPF-g-PAA的吸水倍率、溶胀重复性和保水倍率Fig.7 Water absorption,cycle performanceand and retention rate of MBPF-g-PAA
2.7 pH值对吸水倍率的影响
图8 为MBPF-g-PAA 在不同pH 值(1.0~13.0)溶液中的吸水倍率。从图8 可以看出,在pH 值为1.0~6.0 范围内,MBPF-g-PAA 的吸水倍率随pH 值的增加而显著增加;在pH 值为6.0 时,MBPF-g-PAA 的吸水倍率最大,有明显的溶胀行为;在pH 值为6.0~13.0范围内吸水倍率降低。在pH值<5.0时,羧酸阴离子大部分被质子化。一方面,羧酸盐之间的氢键相互作用增强,产生附加的物理交联;另一方面,羧酸盐之间的静电斥力受到限制,网络结构收缩,吸水倍率降低。在5.0 <pH 值<9.0 时,部分羧酸盐被电离,氢键相互作用被打破,使MBPF-g-PAA 吸水能力增强。当pH 值>9.0 时,吸水倍率降低的原因是介质中过量Na+的“电荷屏蔽效应”,有效防止了阴离子-阴离子静电排斥。
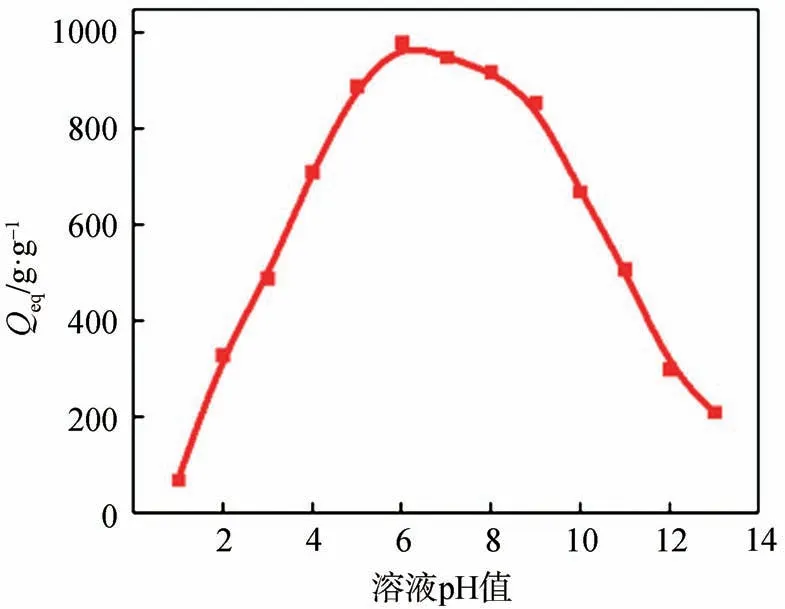
图8 溶液pH值对MBPF-g-PAA吸水倍率的影响Fig.8 Effect of solution pH on water absorption rate of MBPF-g-PAA
2.8 粒度对吸水倍率和保水倍率的影响
图9 为不同粒度的MBPF-g-PAA 的吸水倍率和保水倍率。从图9可以看出,在相同条件下,粒度在10~80目之间的MBPF-g-PAA 的吸水倍率随着粒径的增加而增大。这可能是因为粒度较大的MBPF-g-PAA比粒度较小的在水中吸收速率慢,颗粒尺寸大的吸水量可能是不饱和的。且随着颗粒尺寸的不断减小,孔隙体积变小。因此,粒度从80~120 目,MBPF-g-PAA的吸水倍率降低。随着粒度的减小,保水倍率也降低。这种现象主要是由于颗粒较小的MBPF-g-PAA 与水的接触面积增大所致。
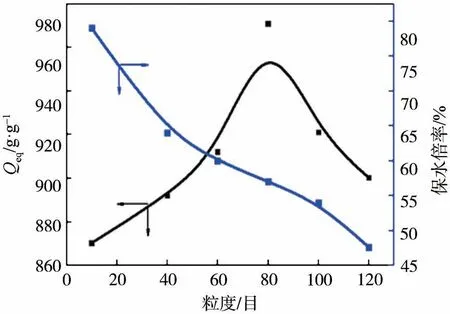
图9 不同粒度的MBPF-g-PAA的吸水倍率和保水倍率Fig.9 Water absorption rate and water retention rate of MBPF-g-PAA with different particle sizes

图10 盐溶液对MBPF-g-PAA吸水倍率的影响Fig.10 Effect of salt solution on water absorption of MBPF-g-PAA
2.9 盐溶液质量分数对吸水倍率的影响
高吸水性树脂在盐溶液中的溶胀能力有许多重要的实际应用,特别是在农业和园艺方面。图10(a)显示了MBPF-g-PAA 在不同质量分数的NaCl、KCl、NH4Cl、MgCl2、CaCl2和FeCl3溶液中的吸水倍率。从图10(a)可以看出,随着盐溶液质量分数的增加,溶胀能力明显降低。这一结果可能是由于聚合物网络与外部溶液的渗透压差减小所致。在相同的盐溶液质量分数下,MBPF-g-PAA 的吸水倍率随着阳离子电荷(一价>二价>三价)的增加而降低。随着金属阳离子活性的增加(从Na+到Ca2+和Fe3+),吸水倍率降低。这是由于介质的阳离子电荷和离子强度的增加。另一方面,交联程度的增加导致溶胀能力的降低。此外,阳离子半径越小,吸水能力越强(Na+>k+和Mg2+>Ca2+)。不同氯盐溶液中的吸水倍率为Na+>K+>NH4+>Mg2+>Ca2+>Fe3+。这与图10(b)中质量分数0.3%盐溶液无量纲盐敏感性因子的结果相对应,高吸水性树脂对各种阳离子的敏感性为:Na+<K+<N H4+<Mg2+<Ca2+<Fe3+,一般为:一价阳离子<二价阳离子<三价阳离子。这主要与离子强度有关,根据Flory 方程,当盐溶液的离子强度增加时,吸水率降低,对盐溶液的敏感性增加。根据式(4)计算无量纲盐敏感性因子,比较水凝胶对水性流体的敏感性[39]。

式中,f为盐敏感性因子,无量纲;Qs和Qd分别是盐溶液和蒸馏水中的溶胀比。
2.10 XPS分析
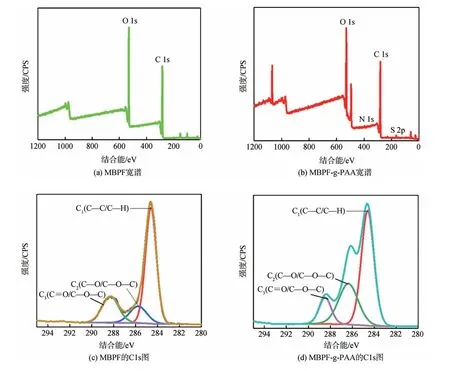
图11 改性竹浆纤维和MBPF-g-PAA的XPS图Fig.11 XPS diagram of bamboo pulp fiber and MBPF-g-PAA
利用XPS分析了改性竹浆纤维和高吸水性树脂的主要化学元素组成。图11 为MBPF 和MBPF-g-PAA 的XPS图。表1列出了碳的键能赋值。如图11(a)和图11(b)显示,MBPF 和MBPF-g-PAA 分别在529.0 eV 和284.60 eV 处出现峰值,分别对应O1s和C1s,而XPS未检测到纤维素分子的氢原子、氮原子、硫原子。与MBPF 相比,MBPF-g-PAA 的N1s 峰转化为更高的结合能,表明纤维素和丙烯酸接枝反应形成的化学键合结构破坏了纤维素分子链之间的氢键相互作用,导致结合能的增加。图11(c)和图11(d)中,样品在284.60、285.77和288.29 eV 处结合能的拟合峰分别对应C—C/C—H、C—O 和C=O。由于较高的能带对应更高的氧化状态,MBPF-g-PAA 在401.8 eV 处的峰可归因与氮原子中的一对孤电子被捐赠给N原子和丙烯酸单体之间的共享键,导致氮原子的电子云密度降低,结合能增加。在聚合反应过程,可以明显观察到S2p 作为树脂的特殊元素,这是由于纤维素发生接枝聚合生成新结构所致。

表1 XPS中结合能(BE)的分配Table 1 Allocation of binding energy(BE)in XPS
3 结 论
本研究以竹浆纤维为原料,并对竹浆纤维素进行预处理,通过纤维素与丙烯酸在水溶液中接枝共聚反应,合成了一种新型的纤维素骨架支撑的高吸水性树脂(MBPF-g-PAA),所制备的新型复合材料具有良好的吸水和保水性能,在现代卫生和农业领域具有潜在的应用前景。并采用分析手段对其进行表征。
3.1 通过复合纤维素酶+低温碱尿素预处理体系,得到易于接枝反应的改性竹浆纤维(MBPF)。进一步制备得到的MBPF-g-PAA 具有优良的吸水性能,在优化反应条件下其吸水倍率高达980.87 g/g。
3.2 MBPF-g-PAA 从纤维素致密的生物结构中形成了孔结构,这些孔结构为后续水分子的进入打开了通道。且树脂中存在丙烯酸中的羧基以及烷基碳,是丙烯酸单体和纤维素的共聚产品。
3.3 利用竹浆纤维为原料制备高吸水性树脂,不仅能够达到降低成本的目的,而且使制备的MBPF-g-PAA 具有良好的热稳定性、pH 值敏感性和循环利用性。此外,盐溶液中金属阳离子的种类影响树脂的溶胀行为。受金属阳离子“电荷屏蔽效应”的影响,不同阳离子盐溶液对树脂溶胀的影响依次为:Na+>K+>>Mg2+>Ca2+>Fe3+。
