金合欢素对心肌梗死大鼠诱导的室性心律失常影响*
2021-05-06王倩文李剑怡王龙
王倩文 李剑怡 王龙
随着医疗技术的提高,大多数国家急性心肌梗死(MI)的死亡率呈下降趋势,但是MI后长期幸存者的比例显著增加,加重了社会医疗负担[1]。与健康人群相比,急性MI幸存者是发生心血管疾病的高风险人群,包括室性心律失常[2]。金合欢素是一种类黄酮化合物,作为传统中药有多种用途。近年来,不断有研究证明金合欢素可以对心血管疾病产生多种有益的生物学效应[3-5]。已证明,心肌缺血前给予金合欢素可以减少室性心律失常评分[6]。然而,MI后期时使用金合欢素是否会对室性心律失常产生影响鲜有相关研究。因此,笔者在建立MI大鼠模型4周后,利用单次尾静脉给药的方式研究金合欢素对MI诱发室性心律失常诱发率和持续时间的影响。
1 材料与方法
1.1 实验动物分组及处理 30只健康SPF级雄性大鼠购自湖南斯莱克景达实验动物有限公司,体重为180~200 g,许可证号:SCXK(湘)2016-0002。动物在20~22 ℃,相对湿度55%~65%,12 h昼夜节律灯照,随意进食进水的无菌环境中适应性饲养1周。随后将30只大鼠随机分为3组:假手术组、MI组、金合欢素组,每组10只。MI组和金合欢素组均采用冠状动脉左前降支结扎术制备MI模型,造模前禁食12 h,禁水4 h。腹腔注射3%戊巴比妥钠(50 ~60 mg/kg)麻醉,颈部及胸前剃毛备皮,将大鼠仰卧位固定于手术台上,利用水循环保温系统(RWD-001)维持手术台温度为(22±2)℃,备皮区0.5%碘伏消毒,后爪伤害性刺激无反应证实麻醉深度适当。在大鼠甲状软骨水平将颈部皮肤纵向剪开一长约1 cm 切口,钝性分离组织,暴露气管后插入自制气管导管。确认成功插入后,接通小动物呼吸机(特力TKR 400H)行控制性机械辅助通气,呼吸机设置参数:呼吸频率70次/分,吸呼比1∶1.5,潮气量3.0 ml/kg。观察气道压力以及胸廓动度,保证呼吸回路通畅。大鼠四肢用针刺电极连接电生理记录仪(MP150,BIOPAC),用Power Lab数据采集系统(AD Instruments)进行Ⅱ导联心电图监测。于大鼠胸骨左侧平行切开2 cm 的切口,钝性分离胸大肌等组织,显露助骨。将第三和第四根肋骨断开,用开胸器撑开肋骨以显露心脏,撕裂心包,在左心耳下方约2 mm 处以6/0缝线结扎冠状动脉前降支。结扎点以下心肌由红变白、心尖搏动减弱、心电图示ST 段抬高证明MI模型制作成功。清理胸腔后逐层缝合关胸。待大鼠恢复规律自主呼吸后拔管撤离呼吸机,保暖直至清醒。假手术组大鼠开胸后仅在冠状动脉下穿线但不结扎,其余步骤同MI造模。本实验符合动物伦理规范,并获得了武汉大学动物实验管理部门的伦理批准。
1.2 心脏超声检查 MI造模4周后第1天,用超声仪器(GE E95)评估大鼠心脏功能。腹腔注射少量3%戊巴比妥钠(10~20 mg/kg)麻醉,保留大鼠自主呼吸。胸部备皮完成后,将大鼠仰卧位固定于操作台上进行超声心动图检测。测量左室射血分数(LVEF)、左室短轴缩短率(LVFS)、左室收缩未期内径(LVIDS)及左室舒张未期内径(LVIDD)。检查完成后大鼠充分保暖直至清醒。
1.3 体表心电图记录和电生理实验 MI造模4周后第2天至第5天,假手术组、MI组和金合欢素组大鼠进行电生理实验并同时记录体表心电图。腹腔注射3%戊巴比妥钠(50 ~60 mg/kg)麻醉,颈部和胸前区备皮消毒,仰卧位固定于操作台,行气管插管术并连接呼吸机正压通气,大鼠四肢用针刺电极连接Power Lab数据采集系统记录Ⅱ导联心电图,利用LabChart8.0 自 动 分 析 心 率(HR)、RR 间 期、PR 间期、QRS波时限和QT 间期。用调整后的Bazett算法计算QTc间期,QTc =QT/ (RR/f),f=150 ms[7-8]。金合欢素组大鼠尾静脉注射金合欢素(大连美仑生物技术有限公司)10 mg/kg[6]。假手术组和MI组均以相同的给药方式,给予等量生理盐水。给药30 min后于第3、4肋水平开胸,用开胸器固定,充分暴露左室游离壁同时注意避免损伤肺脏。将刺激电极置于梗死周边区,分别用6 V、8 V、10 V 的Burst刺激(50 Hz,100个脉冲,持续2 s)刺激大鼠心脏,诱发室性心律失常,包括室性早搏、室性心动过速或心室颤动,每次进行20次重复Brust刺激记录室性心律失常的持续时间,计算诱发率(Burst刺激诱发出室性心律失常的次数除以总次数)。每只大鼠每种强度下刺激6次,每次间隔3 min以恢复自发搏动并消除心电记忆,每只大鼠心脏一共进行了18次Burst刺激。
1.4 组织病理学观察 电生理实验后剪取大鼠心脏,用PBS缓冲液反复冲洗心脏,除去左右心房、右室以及大血管等多余组织,取左室心肌组织,用4%的多聚甲醛溶液固定,酒精脱水、石蜡包埋、制作切片并进行Masson染色,观察心肌形态学变化。Masson染色蓝色表示胶原纤维,红色表示心肌细胞。
1.5 统计学方法 采用SPSS 22.0统计软件进行分析,数据以±s 表示,2组比较采用t 检验,多组比较采用单因素的方差分析,以P<0.05为差异有显著性。
2 结果
造模过程中,假手术组、MI组和金合欢素组大鼠分别死亡2只、2只和1只。MI造模1周内,假手术组、MI组和金合欢素组大鼠分别死亡1 只、2只和3只。
2.1 三组大鼠心脏超声指标比较 与假手术组相比,MI组和金合欢素组大鼠LVEF 及LVFS明显下降,LVIDS以及LVIDD 明显增加。见表1。

表1 三组大鼠心脏超声指标比较
2.2 三组大鼠体表心电图指标比较 各项体表心电图指标中,与假手术组比较,金合欢素组的HR明显增加,PR 间期显著降低,MI组和金合欢素组的QTc间期降低。与MI组比较,金合欢素组的HR 增快,QTc间期缩短,但无统计学差异。见表2。
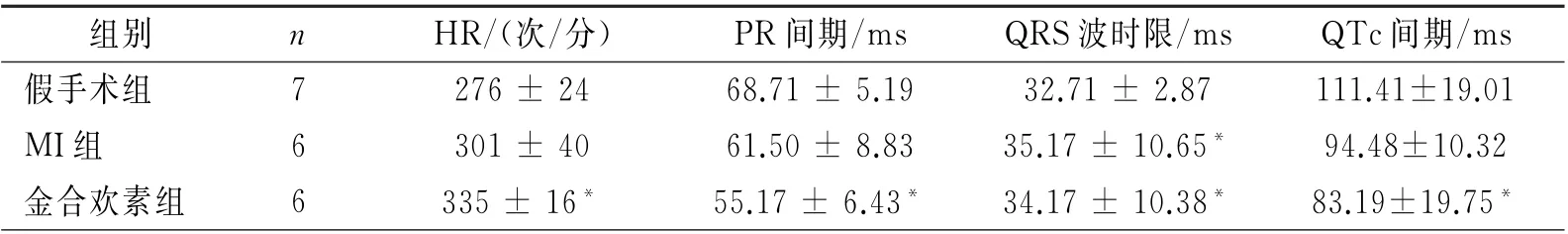
表2 三组心电图指标比较
2.3 三组大鼠室性心律失常诱发率和持续时间比较 用6 V、8 V 以及10 V 的Burst刺激大鼠心脏诱发室性心律失常时发现,假手术组大鼠未能诱导,但MI组和金合欢素组均诱发出了室性心律失常。与MI组比较,金合欢素组在8 V 和10 V 的Burst刺激下,室性心律失常诱发率显著降低,6 V 的Burst刺激时诱发率有下降趋势,但无统计学差异(表3)。与MI组比较,金合欢素组大鼠室性心律失常的持续时间显著缩短(表4,图1)。
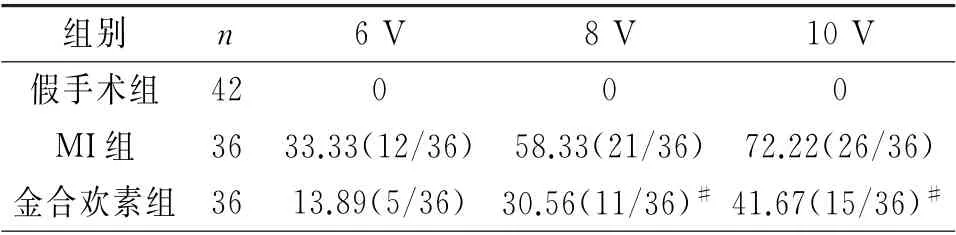
表3 三组室性心律失常诱发率比较/%
2.4 三组大鼠心脏形态结构学变化 Masson染色结果显示,假手术组大鼠左室心肌细胞走行规整,大小形态均匀,细胞膜完整,无炎性细胞浸润,未见明显病理改变。MI组和金合欢素组大鼠左室心肌细胞排列紊乱,形态不规则,细胞膜不完整,心肌组织细胞浆着色变深,有炎性细胞浸润,存在大量蓝色胶原纤维,心肌细胞间广泛纤维化。见图2。

表4 三组诱发室性心律失常持续时间比较/s
3 讨论
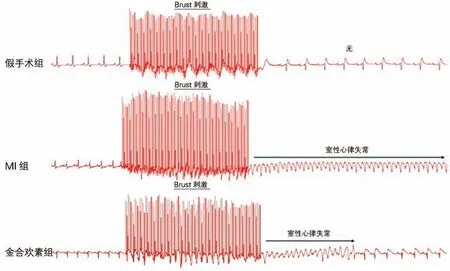
图1 三组室性心律失常诱发情况
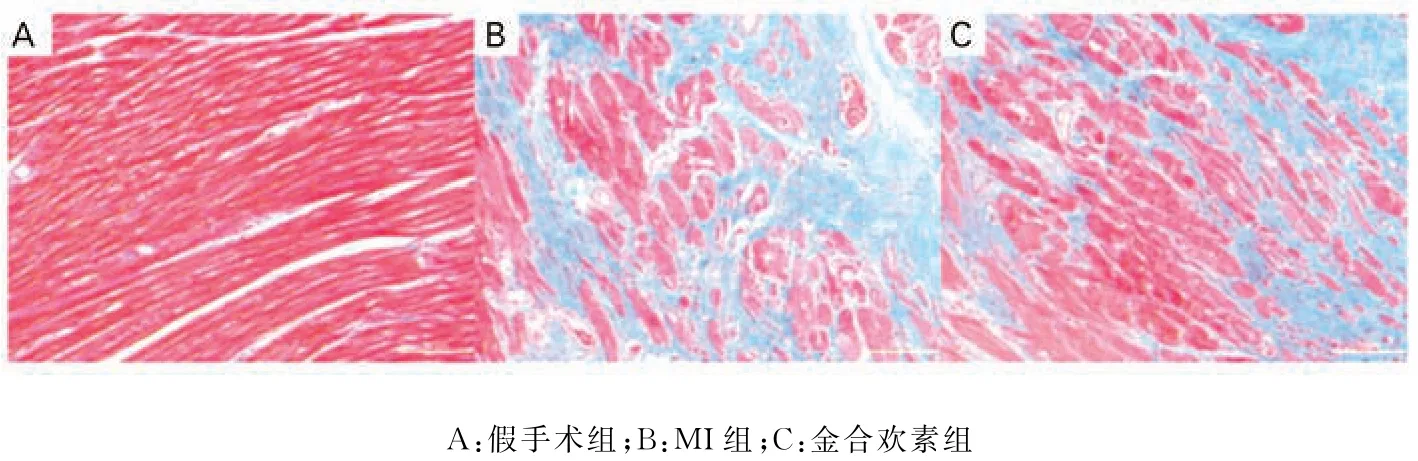
图2 三组左室心肌组织Masson染色比较
金合欢素是一种广泛存在于自然界的天然类黄酮化合物。既往研究表明摄入类黄酮化合物会对MI和心律失常等心血管疾病产生有利影响。Chang等[3]和Liu等[6]实验表明,在急性MI治疗窗口期给予金合欢素,可以改善左室心功能和心梗面积。此外,有文献报道金合欢素可以抑制心律失常[4]。在本研究中,笔者发现金合欢素显著降低了不同强度Burst刺激下MI大鼠诱发的室性心律失常诱发率以及持续时间,尤其是以8V 刺激时。这提示金合欢素可以抑制室性心律失常。QTc间期与室性心律失常密切相关。在心肌梗死和左室功能障碍患者中,QTc间期更容易延长[9]。有研究报道,QTc间期每延长10 ms,病人发生恶性心律失常事件的风险上升15%[10]。与MI组相比,金合欢素组大鼠的HR 增快,QTc间期缩短,表明金合欢素可能通过缩短QTc间期,影响心室复极过程,从而降低室性心律失常诱发率。但是与假手术组比,MI组及金合欢素组的QTc间期均缩短,这可能和样本量较少有关。现有临床研究报道胺碘酮和索他洛尔等抗心律失常药存在增加QTc间期的副作用[11]。因此,金合欢素有望作为即时抑制MI患者诱发的室性心律失常的选择之一。
虽然本实验表明金合欢素可能是一种即时抑制MI诱发室性心律失常的候选药物,但仍具有局限性。首先,离子通道与室性心律失常密切相关[12],金合欢素是否作用于离子通道抑制室性心律失常,有待进一步研究。其次,鉴于本研究已证明金合欢素可即时抑制室性心律失常,长期使用金合欢素对MI诱发室性心律的影响如何有待探讨。最后,所有的结果都是在啮齿类动物模型上得到的,尚需在大型动物(如犬)上进行进一步的实验研究,获得临床前数据,为将来的临床试验提供参考。
