行介入三尖瓣置换术治疗起搏器引起的重度三尖瓣关闭不全1例
2021-05-04王伟安朝李宁乔帆蔡成良李白翎韩林徐志云陆方林
王伟 安朝 李宁 乔帆 蔡成良 李白翎 韩林 徐志云 陆方林
经静脉右心系统导线植入是目前永久起搏器植入术的基石。但跨三尖瓣的导线植入可引起导线相关性三尖瓣关闭不全(lead induced tricuspid regurgitation, LITR),其通常为起搏器植入术的迟发性并发症,发生率据不同研究报道为10%~39%[1-2]。LITR的发病机制可分为机械性和电生理性。机械性因素中最重要的因素是导线碰撞三尖瓣瓣叶,三尖瓣后瓣及隔瓣最易受影响[2];而电生理因素则主要与房室收缩不同步有关[3]。因此对于除颤仪/起搏器植入患者,一旦新发现右心杂音或者出现右心衰竭的症状应该怀疑合并LITR。中重度LITR病程较长,容量负荷、瓣叶牵拉、瓣叶对合不良等因素均可加重三尖瓣关闭不全(tricuspid regurgitation,TR)。当LITR进展至右心功能不良时,拔除导线风险较大,即使拔除并重置导线对心力衰竭的好转也无帮助,通常需要外科手术治疗[1]。海军军医大学附属长海医院心血管外科研发的介入三尖瓣置换装置LuX-Valve(宁波健世生物科技有限公司, 中国)治疗高危重度TR患者取得了较好的临床效果。LuX-Valve介入三尖瓣置换系统由输送器与LuX-Valve瓣膜两部分组成,其中LuX-Valve瓣膜是一种非径向力支撑原位三尖瓣置换瓣膜,由牛心包生物瓣叶、镍钛合金瓣架与非径向力锚定系统组成[4]。本研究通过回顾1例LuX-Valve治疗LITR患者资料,并结合国内外文献对介入三尖瓣置换技术治疗LITR的机制进行探讨。
1 临床资料
患者 女,75 岁。“反复胸闷、气急6年”于2018年9月20日入住海军军医大学附属长海医院。患者入院前1年行起搏器植入术。入院查体示:患者一般状况差,三尖瓣听诊区可闻及收缩期杂音,腹部膨隆,肝肋缘下2指,双下肢中度水肿。实验室检查示胆红素增高(25.3 μmol/L)。超声心动图示:三尖瓣重度反流,瞬时量49 ml/min,反流束流颈宽度12.7 mm,有效反流口面积81.5 mm2。右心导管检查示:肺动脉高压,肺动脉收缩压48 mmHg(1 mmHg=0.133 kPa)。患者拟行介入三尖瓣置换术。术前评估显示患者存在严重肝疾病(终末期肝病模型评分10.6 分),估算的肾小球滤过率67 ml/(min · 1.73m2),欧洲心血管手术风险评分7.21%,6 min步行试验距离345 m,堪萨斯城生活质量评分45分,纽约心脏病协会心功能分级Ⅲ级。
患者入院后完善相关检查,超声心动图及右心室CT血管造影检查明确TR严重程度及三尖瓣瓣环大小、室间隔角度等指标,以确定LuX-Valve的规格;同时排除手术禁忌后,于数字减影血管造影(digital subtraction angiography,DSA)手术室全身麻醉气管插管下行LuX-Valve置换术。具体操作如下:患者稍左侧倾斜,右后肩垫高,术中取右前胸外侧第5肋间小切口,显露右心房后在经食管超声心动图引导下定位穿刺点,双层荷包缝合后穿刺,首先置入6 F猪尾导管,测量肺动脉及右心室、右心房压力。根据术前右心室CT分析结果,确定X线投照体位,保持室间隔平面展开,行右心室造影,根据右心室造影初步定位三尖瓣瓣环,确定后置入LuX-Valve输送器,于DSA引导下到达释放位置后逐步释放瓣膜,根据经食管超声心动图提示调整输送器位置,固定三尖瓣装置后撤除输送器,行右心室造影及经食管超声心动图检查确认TR完全纠正(图1)。右心房荷包线打结,彻底止血后逐层关胸。术后患者安返监护室,呼吸机辅助时间6 h。于监护室停留4 d后将患者转入普通病房。术后20 d患者顺利出院。术后复查超声心动图提示LuX-Valve瓣膜功能正常,三尖瓣轻度瓣周漏。术后1个月随访,超声心动图提示三尖瓣人工瓣膜功能良好,无明显反流及瓣周漏;纽约心脏病协会心功能分级Ⅱ级,6 min步行试验距离384 m,堪萨斯城生活质量评分53 分。术后6个月随访,超声心动图提示三尖瓣人工瓣膜功能良好,无瓣周漏;纽约心脏病协会心功能分级Ⅱ级,6 min步行试验距离369 m,堪萨斯城生活质量评分62分,患者生活质量较术前明显改善。
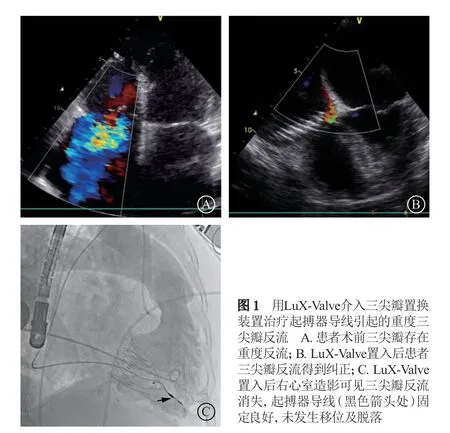
2 讨论
LITR进展至右心功能不良时,拔除导线风险较大,通常需要外科手术治疗。然而高龄、二次手术、长期右心功能不全导致的肝肾功能不全、凝血功能障碍、营养状态差等各种因素使这部分患者再次开胸手术风险极大,同时因手术时机选择、手术技术、手术适应证把控等因素的综合影响,使得传统三尖瓣手术死亡率、并发症发生率居高不下。本研究报告了1例高危重度LITR患者接受 LuX-Valve介入三尖瓣置换术并取得良好的临床效果。相关文献检索发现的三尖瓣成形以及三尖瓣置换装置也逐步进入临床,展现出较好的应用前景。
以“Transcatheter tricuspid valve replacement(TTVR)and pacemaker”“TTVR and pacemaker”“Transcatheter tricuspid valve intervention and pacemaker”为关键词通过PubMed数据库对2010年1月至2020年10月发表的介入三尖瓣介入技术治疗LITR相关文献进行检索。文献检索纳入了1种三尖瓣成形装置以及2种原位三尖瓣置换装置。 MitraClip为经股静脉三尖瓣瓣叶缘对缘缝合技术,其原理为提高三尖瓣瓣叶边缘之间的对合程度进而缓解收缩期TR,目前在介入三尖瓣中该装置应用最为广泛。Regazzoli等[5]于2017年首次报道将MitraClip装置(雅培血管,圣克拉拉, 加利福尼亚)用于修复1例因双腔起搏器植入后引发的LITR患者,首先经右侧股静脉置入MitraClip装置后,先将一个夹持键抵达三尖瓣前隔瓣交界区,随后将第二个夹持键置于后隔瓣从而有效避免起搏导线进入交界区从而减少TR。这种手术方式被称之为“三孔技术”,应用最为广泛。随后,用MitraClip装置这种缘对缘的手术方式可通过钳夹三尖瓣前隔瓣使三尖瓣二瓣化,也被证明可以改善LITR患者TR程度及心功能[6]。Lurz等[7]于2019年报道了102例TR患者行缘对缘手术治疗的结果,其中33例(32.4%)患者合并右心电极植入,其结果证实患者右心是否合并电极并不影响手术结果以及术后TR改善程度。Taramasso等[8]通过分析TriValve临床注册中纳入的470例重度症状性TR患者的临床数据,87%的导线植入组患者接受了MitraClip治疗,手术成功率为78.6%,院内死亡率3.7%,术后30 d时73.7%患者残余TR≤2+。以上结果证明右心导线植入对LITR患者行MitraClip并无明显影响,然而最大的不足在于MitraClip术后仍然存在残余TR,其远期效果值得进一步随访研究。
此外,近年来有2类原位三尖瓣置换介入装置也被报道用于治疗LITR。2015年Paradis等[9]通过利用Edwards Sapien XT(爱德华生命科学,尔湾市,加利福尼亚)介入系统及瓣中瓣置换技术治疗LITR,起搏导线被固定在两个瓣膜中间并且功能良好。术后超声心动图提示只有导线边缘轻度瓣周漏。Eleid等[10]也于2016年报道了3例三尖瓣生物瓣置换术后再次行经导管三尖瓣置换术(transcatheter tricuspid valve replacement,TTVR),使用的瓣膜为Melody及Sapien XT并获得成功,起搏导线功能良好。Anderson等[11]分析了VIVID数据库中329例患者临床资料,有58例患者既往有经静脉起搏器植入病史,且31例为起搏导线跨越三尖瓣,其中3例患者再次经股静脉TTVR前将起搏电极拔除(1例患者转为心外膜起搏,而另外2例在TTVR术后再次将起搏电极重新跨越三尖瓣),28例患者起搏电极均被固定至两个瓣膜之间,该研究提示术前合并跨三尖瓣起搏导线的TTVR术安全性较高。
LuX-Valve三尖瓣是用牛心包组织及镍支架制成的非径向支撑力自膨式生物瓣,创新性地利用右心室特殊锚定元件、2个三尖瓣前瓣夹持键以及心房盘片将支架固定在病变三尖瓣瓣环上,其自适应的“裙摆”可减少瓣周漏[4]。2020年,Lu等 [12]报道了12例救治性LuX-Valve治疗结果,手术成功率为100%,平均瓣膜释放时间为9 min,术后患者TR水平显著下降,术后30 d死亡率为0,9.1%患者合并轻度TR,证实LuX-Valve 瓣膜置入治疗重度高危TR患者安全可靠。
目前对于LITR介入治疗,瓣膜成形装置MitraClip应用最为广泛,但是患者术后随访仍能观察到残余TR,其远期效果尚不明确,在有些介入修复装置临床试验阶段,甚至将起搏导线引起的TR列为禁忌。三尖瓣原位置换介入瓣膜起步较晚,作为第一款公开报道的三尖瓣原位介入置换装置——Navigate,其治疗LITR的报道有限[13-14],未见其应用于起搏导线引起的TR患者中。从目前报道的文献来看,将起搏导线推至介入瓣与原始瓣膜,或两个人工瓣膜之间并不会影响TTVR的效果,术后导线导致的轻微瓣周漏似乎也是可以接受的。综上所述,从本例临床置入结果显示LuX-Valve置入是一种可靠的LITR治疗方式。
