人工湿地砷污染去除研究进展
2021-05-02杨刚马云龙白银萍周磊刘坤
杨刚,马云龙,白银萍,3,周磊,刘坤
(1. 西南科技大学生命科学与工程学院,四川 绵阳 621010;2. 银川市生态环境监测站,宁夏 银川 750001;3. 西南科技大学环境与资源学院,四川 绵阳 621010;4. 西南科技大学核废物与环境安全国防重点学科实验室,四川 绵阳 621010;5. 重庆市生态环境科学研究院固体废物与土壤研究所,重庆 401147)
砷元素以其氧化物三氧化二砷即砒霜被人们熟知,被认为是主要的环境致死、致癌物之一。其污染途径主要是通过土壤及水体进行。环境保护部和国土资源部2014年发布的全国土壤污染状况调查公报显示,我国砷无机污染物点位超标率为2.7%。在2000—2010年间,我国贵州省独山县、湖南省辰溪县、广西壮族自治区河池市以及河南省大沙河等地发生大规模砷污染和砷中毒事件。给人民群众的人身安全及生命财产带来了很大威胁,如湖南辰溪县砷污染导致上千人砷中毒。造成这些污染及中毒事件的主要原因是含砷矿物直接转化并转移到水体所致。有研究显示:砷污染造成的影响关系到全球四亿人的饮水安全[1]。现有的砷污染去除方式主要有吸附、离子交换、电凝聚、化学沉淀、植物修复、纳米植物修复和膜修复等[2]。这些处理方法不可避免的都要在水体中进行。因此,湿地生态系统砷污染去除作为一种有效途径进入了人们的视野。湿地占全球陆地面积的6%,被认为是主要的砷库,在砷的存储、迁移与转化中发挥着重要的作用。湿地作为砷库被认为是理想的砷富集去除场所,大量的研究通过人工湿地进行砷的去除[3-4]。人工湿地作为砷库的主要原因是腐殖质、植物、微生物相互作用。大量研究表明,人工湿地具有较好的砷污染去除效果[4]。此外,人工湿地作为新兴的水处理系统,具有环境友好,污染物去除率高,成本及能耗低等优点,并具有较好的生态效应。因此,本文梳理了砷污染的治理历史和技术发展,从人工湿地的兴起及其在砷污染处理中发挥的主要作用等几个方面,综述了人工湿地砷污染去除研究进展,并对后续发展方向进行了展望,以期为砷污染治理提供科学依据。
1 砷污染治理历史及技术发展
1.1 砷污染的危害
砷污染源主要有自然及人为两种。砷污染的自然源主要来自于岩石及土壤的淋溶、砷污染也可通过火山作用释放到大气,然后沉降到土壤表面。砷的人为源主要包括采矿、有色金属冶炼和化石燃料的燃烧。农业土壤中人为砷沉积的其他因素包括使用含砷除草剂、杀虫剂和木材防腐剂、施用磷肥和用砷污染的地下水灌溉[5]。世界卫生组织建议饮用水的砷浓度控制在10 μg/L以下。未被污染河流底泥及水体中可溶性砷的含量约为5~40 mg/kg和0.1~0.8 μg/L[6],然而被污染的土壤及水体中砷浓度高达1 000 mg/kg和5 000 μg/L[6-8]。砷的污染可引发心血管疾病及诸多癌症。全球约有一亿人处在砷污染的风险之下,砷污染逐渐成为严重的环境和公共健康问题。砷污染仅次于致病微生物,是全球第二大水健康危害因素[9]。砷污染分为无机砷污染和有机砷污染两种。无机砷污染对代谢不利,能够改变人类细胞及遗传物质的完整性,砷酸盐还可以通过与蛋白巯基进行反应或者取代磷酸基的位点来造成毒性,造成皮肤、血管及神经系统紊乱,诱发各种癌症。尤其是通过大米等含砷污染食物的摄入,诱发皮肤癌、肺癌及膀胱癌等[2]。有机砷污染相对于无机砷污染来说,毒性较低,主要是通过畜牧业的饲料、药物添加剂的形式通过畜禽排泄物进入土壤中。其危害除了高剂量有机砷残留使畜禽食欲不振、体重下降、严重可导致死亡外。通过畜禽粪便进入土壤的有机砷污染还可造成植物营养吸收受阻。此外,有机砷进入土壤后还可通过一系列化学反应,转化成毒性较大的无机砷。鉴于砷污染通过水体及土壤对动植物、人体及环境造成较大影响,需要对其污染历史及治理技术进行梳理,以利于后续砷污染的管控。
1.2 砷的利用及砷污染历史
砷是一种天然物质,医学应用已经超过2 400多年。18世纪到20世纪以来,托马斯·富勒研发的碳酸氢钾三氧化二砷溶液更是用于治疗包括哮喘、湿疹及银屑病等多种疾病。这种多用途的药剂直到放射疗法及细胞毒性化疗的出现才被逐渐取代。砷的利用最具代表性的是我国学者自二十世纪七十年代开始利用三氧化二砷制剂治疗白血病,获得很好的疗效[10]。但在过去一百多年来,砷的使用急剧下降,主要原因是担心长期服用砷导致中毒以及它的潜在致癌性[11]。从十九世纪开始一直到二十世纪,医务人员、环境保护主义者等群体日益关注砷对人类健康和环境的潜在影响[6]。早在1661年,英国人John Evelyn就认识到煤的燃烧导致了当地居民的砷中毒。1812年,英国医生John Paris注意到铜冶炼厂附近的工人和农场动物频发癌症,他推测癌症频发与金属砷有关[6]。随后,世界各地由于砷污染导致的死亡事件时有发生,最为严重的是1955年日本砷中毒事件,导致839名儿童丧生[6]。近年来,砷逐渐被用于畜禽产业,将砷制剂加入饲料用于促进畜禽生长。然而,其过量使用增加了环境负担。因此,科学家们逐渐意识到其危害性,促使国家不断出台相应政策文件,加强污染防治及生态系统的保护。
1.3 砷污染治理技术发展
由于日益频繁的砷污染及中毒事件,学者们逐渐关注并不断拓展砷污染去除技术。砷污染在水体中的去除技术主要包括吸附、离子交换、沉淀/共沉淀、各种分离技术(过滤、膜、甚至磁性方法)、生物方法和自然修复。砷污染在土壤等固体中的去除技术主要有钝化、玻璃化、物理分离、淋洗、挥发回收及电化学等方法[6]。吸附技术主要是通过固体吸附剂来吸附污染物,具有成本低,效率高的优点。但是吸附剂达到饱和需要进行频繁更换,并且只适用于低浓度含砷污水处理。离子交换技术可完全去除并回收金属离子,但是必须定期恢复离子交换活力,确保完全清楚有害离子并且成本昂贵。植物修复是利用植物进行砷污染去除,具有生态环保的优点,但耗时太久,并受到环境条件的影响。化学沉淀法可有效去除特定离子且方便高效,但会形成较多污泥,而且成本太高。膜处理技术同样具有成本高的特点。电化学技术处理高效但是只适用于少量污染物处理[2]。通过以上介绍,我们发现有些处理方式只适合在水体中进行,而有些只适合在土壤中进行。湿地生态系统是水土一体的复合系统,可实现多种处理方法的联合实施,具有较好的推广价值。
2 人工湿地的兴起及砷在湿地中的赋存状态
2.1 人工湿地的兴起及技术发展
2.1.1 人工湿地的兴起 湿地由地球上的水陆相互作用形成,与森林、海洋一起,并列为全球三大生态系统。它是重要的生存环境和自然界最富生物多样性的生态景观之一[12]。现有最权威的湿地定义来自于《湿地公约》,即“草本沼泽、碱沼、泥炭地或水域,不论它们是天然的或人工的,永久的或暂时的,水体是静止的或流动的,水质是淡水、半淡水或咸水,也包括退潮时水深不超过6 m的海水水域”。湿地系统一般可以分为两大类:天然湿地和人工湿地。人工湿地的设计建造是通过对湿地生态系统中的物理、化学和生物作用的优化组合来实现对废水的有效处理[13]。人工湿地水处理研究最早开始于西欧,西德在二十世纪五十年代初期就开始建立了人工湿地用于处理污水并取得了较好的效果。同一时期,英国也开展了利用芦苇进行污水净化的研究。随后,各个国家对人工湿地用于污水处理展开了大量工作。美国是在1977年“清洁水法”颁布后,逐渐对天然湿地污水净化展开了大量研究。人工湿地在我国的发展始于1987年,自从天津市环境保护研究所在1987年建成了我国第一座芦苇床人工湿地工程以来,人工湿地在我国迅速发展。随后的十年间我国超过200个人工湿地在运行,面积从100 m2到10万m2不等[14]。中国现有人工湿地数量及面积逐渐扩大,其应用领域涉及到农村和城市生活污水处理、养殖、印染及工业废水处理、重金属及危险废物处理等各个方面[14-15]。
2.1.2 人工湿地类型及技术发展 人工湿地类型主要有表面流湿地和潜流湿地两种类型。表面流湿地水流缓慢,水位较浅,与自然湿地较为接近。优点是设计简单、投资少,缺点是负荷小,卫生条件较差。早期在北美及澳洲较为常用,现在由于其缺点突出,较少使用。潜流湿地分为水平流和垂直流两种,其中垂直流人工湿地又可分为上下流两种。潜流湿地的优点是作用位点多、微生物丰富、负荷大、污水处理效率较高等,缺点是造价及维护费用高。在实际应用中,水平流湿地占主导地位[13,16]。人工湿地兴起于欧洲并广泛应用,最初因人工湿地可广泛处理有机及无机物被德国学者seidel发现,后续被用于处理工业污水、生活污水、最终被扩大到矿山废水处理、农场废水处理及农业污染等[13,17-18]。随着人们对人工湿地的深入认识,其应用前景将会得到更好的开发。此外,我国的乡村振兴战略的实施,将会给人工湿地技术带来更大的机遇与挑战。
2.2 砷在湿地生态系统中的赋存状态
砷是一种类金属元素,主要以硫化物形式存在,其化学性质与磷相似。砷可以化合出无色、无嗅、结晶型的氧化物As2O3和As2O5,As2O3和As2O5会以超高的溶解度溶于水[19]。砷在自然环境中主要以0,-3,+3和+5价存在,其毒性取决于砷的化合价和存在形态[20]。厌氧条件下砷主要以三价存在,三价砷比五价砷具有更高的溶解性、流动性和植物毒性。好氧土壤条件下砷主要以五价存在。一般来说,砷化物、硫化砷和富砷硫化物矿物都是伴生的。一旦这些矿物在地表或近地表条件下暴露在氧气中,它们就会风化成亚砷酸盐和砷酸盐矿物[6]。在湿地生态系统中,砷在水体、植物和底泥中广泛存在。砷在水中主要以砷酸根离子和亚砷酸根离子存在[5]。湿地生态系统底泥中的砷酸盐容易与铁、铝、锰、钙形成沉淀或共沉淀[21],而这一过程主要受pH的调控。有研究表明,铁、铝的氧化物及氢氧化物在低pH值条件下对五价砷更具吸附性,而在高pH条件下对三价砷更具吸附性[22]。除此之外,砷在湿地生态系统中的赋存状态还受到氧化还原电位、水化学特征及生物活性等因素的影响。即便是水体中较为温和的还原条件,也可使五价砷向三价转变。富含磷的水体也可使五价砷从湿地生态系统底泥中被解析并增加其在土壤溶液中的浓度,主要原因是由于五价砷与磷酸盐的化学性质比较相似,可相互替代[5]。生物作用对湿地生态系统砷赋存状态的影响主要体现在其甲基化作用,有研究表明,浮游植物可将五价砷甲基化形成甲基化砷,甲基化砷具有低毒性和高稳定性的特点[23]。可见,砷在湿地生态系统中的赋存状态随着其环境变化而转变,环境可通过改变砷的价态和赋存形式来影响其毒性大小。
3 砷污染去除技术及其在人工湿地生态系统中的应用
重金属污染土壤修复技术研究始于20世纪70年代后期,其修复原理是降低污染金属的总浓度及有效浓度,经过多年来全球范围的研究及应用,已经形成物理修复、化学修复、生物修复及其联合修复等技术体系[24]。这些技术在土壤及水体修复中得到了广泛应用。对于人工湿地生态系统来说,主要以生物修复中的植物和微生物修复为主,植物和微生物修复砷污染已被广泛应用[25-27]。湿地中富含的腐殖酸对强化湿地植物及微生物修复也起到重要的作用。
3.1 砷污染的水生植物修复
新西兰学者Brooks等[28]在1974年首先报道了植物超富集现象,在1983年美国学者提出了植物修复概念,使植物修复得到快速发展。由于人工湿地在二十世纪八十年代末期才开始兴起。当时重金属污染修复技术逐渐从物理-化学稳定修复技术向植物修复技术过度。进入二十一世纪,植物修复技术得到快速发展,成为绿色环保修复技术之一[29]。在诸多砷污染去除技术中,植物修复因其环境友好、成本低廉的特性,广受研究者关注。
3.1.1 水生植物类型与砷污染去除效果 水生植物的砷污染修复是随着人工湿地的发展逐渐兴起。水生植物一般分为沉水植物、浮叶植物、挺水植物、湿生植物和漂浮植物几种。常见的砷富集沉水植物有黑藻、金鱼藻、狐尾藻、菹草和苦草等。有学者将这五种沉水植物放入砷浓度为5 mg/L的溶液中培养一周,发现它们在植物中的砷浓度可达1 100~1 800 mg/kg,其中苦草富集能力最高[30]。砷污染去除效果较明显的湿生植物有灯心草、蜈蚣草、酸模等。灯心草和蜈蚣草对砷污染具有较好的去除效果,前人研究发现,种植蜈蚣草和灯心草,砷的去除率分别可达91%和95%[31]。湿生植物珠芽廖,也常被用于砷污染的修复,其对砷的转运系数可高达3.7[32]。挺水植物香蒲和菖蒲对砷污染水体也具有较强的修复效果,它们对水体中砷去除总量可达1 036 μg和843 μg[33]。漂浮植物如浮游植物已进化出不同策略来改善砷的毒性。一是通过磷的替代,二是通过转化为低毒性且容易被排出的甲基化砷[23]。可见,水生植物类型直接影响砷污染去除效果。我们对上述提到的水生植物砷污染去除实验及效果进行了对比汇总(表1)。
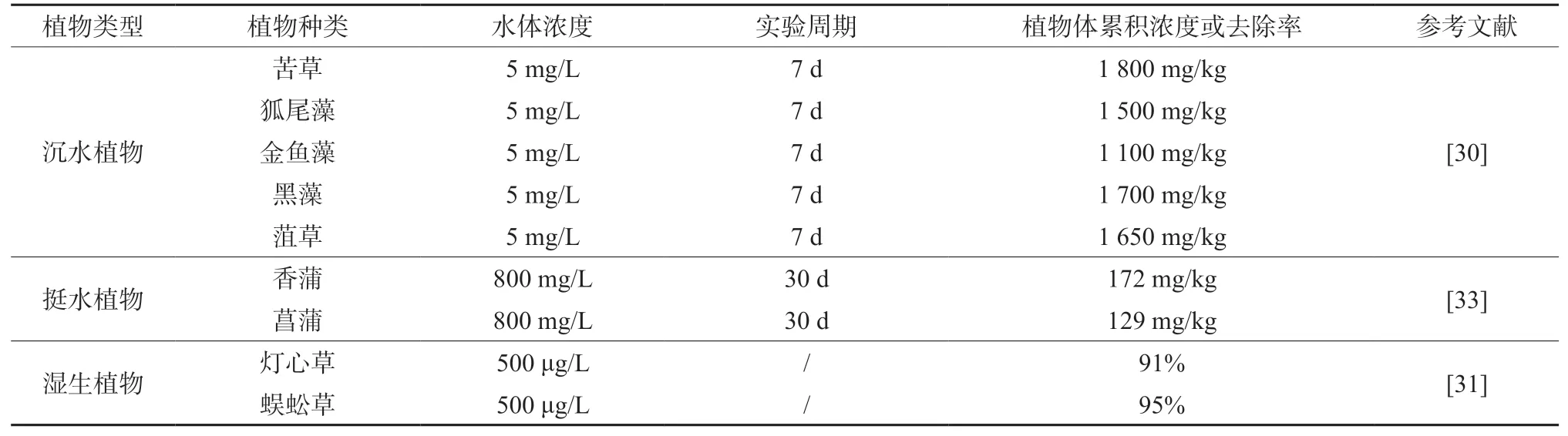
表1 水体砷污染去除的常用植物及其处理效果Table 1 Main plants for arsenic removal in water and their treatment efficiency
3.1.2 水生植物砷污染修复的其他影响因素 水生植物对砷的修复除受到不同植物种类影响之外,还受水体pH、氧化还原电位、磷酸盐等因素调控[34]。其影响的主要机理是因为pH和氧化还原电位可通过改变砷的溶解性来调控其毒性。磷元素影响水生植物砷去除的方式主要是通过与砷元素竞争相同的吸附位点。因此,高浓度的磷明显可抑制砷富集植物对砷污染的吸收[34]。可见,未来水体砷污染植物修复应主要从砷超富集水生植物筛选、砷富集植物的处置与利用、污染水体自身环境调控、重金属污染与修复效果评价等几个方面重点考虑。
3.2 砷污染的微生物修复技术
微生物修复研究具有重要意义,近年来,国际上相继报道了耐重金属及细胞内可累积重金属的微生物[35]。现有发现的可促进砷累积及钝化的微生物有青霉菌、肠杆菌(Enterobactersp. FM-1)、假单胞菌和砷氧化菌等(表2)。除了某些特定微生物自身可累积重金属以外,有些微生物如大肠杆菌(Escherichiacoli) 可直接吸附共沉淀处理砷污染水体,有研究表明,过表达大肠杆菌中的ArsR蛋白可有效去除水体中的三价砷[36]。根际微生物还可通过根际强化作用加强重金属富集植物的修复效果[37]。有研究发现,对植物进行接种砷忍耐性微生物可促进砷的转移效率[35],增强砷在富集植物中的富集量[38]。从植物根际筛选出的假单胞菌可显著提升蜈蚣草和凤尾蕨对砷的富集作用,最高可提升146%和233%[39]。接种肠杆菌能通过提高植株抗氧化酶活性来减轻镉砷富集对水蓼和酸模叶蓼的胁迫,从而提高水蓼和酸模叶蓼对镉-砷复合污染土壤的修复效率[26]。根际促生菌Cupriavidus basilensis菌株也可增加蜈蚣草对砷的植物提取效率,其提升效果可达1.71倍[40],矿区提取的砷耐受菌株还能够促进砷的转移速率[35]。除此之外,在二价铁和氧参与下,微生物可大幅度降低三价砷含量,其机理是微生物可将二价铁催化氧化为三价,将三价砷催化氧化为五价。氧化产生的铁氧化物可将五价砷从水体中去除[41]。通过以上分析发现,微生物主要通过以下几种途径影响砷污染水体。一是通过自身的富集作用或微生物自身吸附来实现砷的累积与钝化;二是通过根际强化作用加强植物的富集效果;三是通过微生物将三价砷催化氧化后通过铁氧化物实现去除。
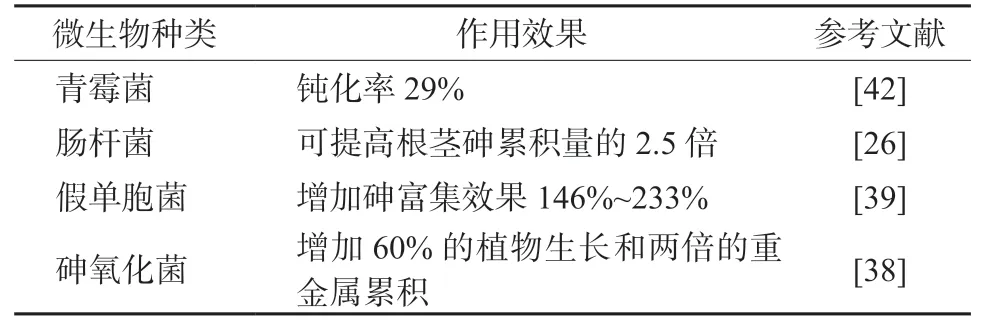
表2 砷污染去除微生物及处理效果Table 2 Main microorganisms for arsenic removal and their treatment efficiency
3.3 砷污染的腐殖酸修复技术
腐殖酸广泛存在于土壤有机质、泥炭、褐煤、湖泊和海洋沉积物中,腐殖酸中具有大量的极性基团,拥有酸性、亲水、阳离子交换、络(螯)合吸附、高分子胶体等特殊化学性质。可在水中形成聚集物,对金属离子具有较强的吸附性能[43]。因此,腐殖酸的存在可促进含砷矿物的生物氧化与砷的固定[44]。腐殖酸对砷污染的处理与修复主要通过以下几个方面来实现:
1)腐殖酸通过高吸附性能与砷形成难以被植物吸收的络合物。腐殖酸具有疏松的“海绵体”结构和较大的比表面积和表面能,因此可对重金属形成较强的物理吸附。其吸附效果取决于砷的初始浓度、pH值、反应时间和载体温度等[45],研究表明五价砷更易与腐殖酸结合,其结合率受到pH值的影响,在pH值为7时结合率最高,砷与腐殖酸的结合率还受到腐殖酸类型的影响,实验表明,陆生腐殖酸的砷结合率是水生腐殖酸的1.5~3.0倍[46]。
2)腐殖酸可通过自身的多种官能团与砷进一步作用。腐殖酸中主要包含的官能团主要有酚羟基、醇羟基、羟基醌、醌、羧基等[47]。其中羧基和酚羟基作用最强,它们可与金属形成金属-腐殖酸配合物[48]。腐殖酸中的还原性官能团(酚基、醌基)提供电子可将高价态的砷还原成低价态,从而改变其迁移特征。
3)腐殖酸和天然有机物(NOM)及湿地中金属氧化物的氧化还原作用。腐殖酸的添加可以促进砷黄铁矿的生物氧化和砷的固定。如有研究发现,在嗜热硫氧化硫化杆菌生物氧化砷黄铁矿的过程中,添加有机酸可大幅提高砷黄铁矿的微生物溶解,同时在微生物细胞和黄铁矿表面会形成絮状多孔结构并吸附砷[44]。砷在湿地中的流动性和生物有效性受到NOM的强烈控制[49],当pH值大于7时,NOM的添加可显著增强砷的迁移[50]。NOM还可促使金属氧化物的还原溶解,从而导致五价伴生砷酸盐的释放并氧化还原转化为生物毒性更大的三价亚砷酸盐。由于湿地生态系统水位波动及生物活性的变化使土壤氧化还原状况不断改变。在氧化环境下,有机质促使砷从金属氧化物中释放出来,增加砷的移动性。在强还原环境中,有机物会引发固砷硫化物的形成,导致砷的迁移率降低。其主要原理是三价砷与有机硫形成共价键而固定砷[51]。因此,湿地植物修复过程中,应结合湿地生态系统的结构和功能,辅以泥炭腐殖酸和功能微生物来提升超富集植物对砷的吸收去除率。
4 展望
综上所述,湿地生态系统作为砷库被认为是砷污染富集及处理的重要场所。人工湿地的快速发展使其成为砷污染去除较为经济、高效的技术。由于人工湿地的兴起至今仅四十余年,其在砷污染去除方面的研究还有待进一步深入。另外,湿地生态系统作为一种复杂介质,其植物微生物的相互作用与协同演化均直接影响砷的代谢过程。因此,在了解砷在湿地生态系统中扩散迁移的基础上,加强认识湿地生态系统中砷在土壤-植物系统中的转化和累积过程,可逐步降低湿地生态系统的砷污染。未来的研究应主要集中在以下几个方面:
1)砷在湿地生态系统中的扩散迁移及演变规律研究;由于不同类型砷矿开采历史、地质结构、气候条件及污染程度差异较大,直接影响了砷污染的迁移与转化过程。人工湿地砷污染去除是基于生态系统的绿色可持续发展理念,实现污染物的有效去除。因此,应该是基于先进的监测技术,对污染物迁移规律清晰认识的基础上,全面实现污染物去除。
2)构建湿地生态系统沉水-浮水-挺水植物立体结构,实现梯级联合去除砷污染的优化组合探索。现有研究表明,蜈蚣草、粉叶蕨、大叶井口边草、珠芽廖、香蒲、菖蒲、苦草、黑藻等均可作为砷的超富集植物,用于污染土壤及湿地的砷去除[25,27,52-53]。而这些植物在生态系统中具有不同的生态位,可根据其特征构建沉水-挺水-缓冲带植物复合生态系统,实现砷的高效去除。
3)植物-微生物及腐殖酸强化修复对砷污染的协同阻滞及界面作用研究。根际促生菌可增加超富集植物对砷的提取效率并促进砷的转移速率。因此,可以利用根际促生菌强化超富集植物对重金属污染土壤的修复效率,在植物修复过程中添加根际促生菌可改善污染土壤养分状况,有助于改善重金属污染土壤的植物修复效果。此外,腐殖酸分子结构中所含的活性基团能与金属离子交换、络合或螯合反应。也具有强化修复砷污染的效果。
