Ag@Cu2O 核壳纳米晶体结构光催化性能的研究
2021-04-26卜军燕
卜军燕 刘 欣 覃 超 李 艳
(西南大学物理科学与技术学院,重庆400715)
随着当今社会的快速发展,环境污染和能源消耗已成为人类面临的主要难题,特别是有机染料造成的水污染,已经限制了工业的可持续发展,危及人类的健康和生命[1]。众所周知,光催化是解决当前环境问题的一种有效方法,与其它常规方法相比,在有机染料引起的环境问题中尤其有用[2-3]。让我们值得庆幸的是,人们发现了一种高效的光催化剂可以解决当前紧迫的环境问题,半导体光催化剂具有优异的催化活性,在光辐射下可以产生光电子和自由基[4-8]。近年来,Cu2O-CdS 、Cu2O-ZnO、Cu2O-ZnS、BiVO4/Ag/Cu2O、Cu2O/TiO2[9-13]等一系列光催化剂已被报道用于环境修复。然而,这些光催化剂的光反应速率低和光利用率低,限制了它们的商业潜力和实际应用[12-14]。为了提高光生电子和空穴的分离效率及光催化活性,人们做了很多努力。其中通过合成Cu2O 纳米粒子(NPs)或纳米线(NWs)来增加材料的比表面积这种方法尤为突出,但是人们发现带隙较窄的纯Cu2O 由于光生电子-空穴对的快速复合,稳定性较差,量子效率较低,为了解决这一难题,通过大量研究发现金属-Cu2O 核-壳纳米结构的催化性能比较好,因此金属-Cu2O 核-壳纳米结构的制备受到了越来越多的关注,银具有高导电性、低成本、可调谐的局部表面等离子体共振(LSPR)频率以及与Cu2O 的晶格失配小于4%等优点,因此被认为是一种提高Cu2O 光催化性能的高效敏化剂[2]。
通过多种方法制备的Ag@Cu2O 纳米复合材料,与纯相的Cu2O 材料相比[15],Ag/Cu2O 复合材料在降解废水中有机污染物方面表现出良好的光催化性能,已得到广泛的研究。本文通过简单的一步法制备的催化剂Ag@Cu2O,对可持续能源、公共卫生和水安全具有重要意义。实验结果表明,Ag@Cu2O 纳米复合材料的催化性能与纯Cu2O 相比有了很大的提高,这种独特的复合材料是一种很有前途的光催化剂[1]。
1 Cu2O 和Ag@Cu2O 的制备及性能研究
1.1 实验药品
一缩二乙二醇 (C4H10O3(DEG),≥98%);乙酰丙酮铜(C10H14CuO4,≥98.5%,化学纯);硝酸银(AgNO3,AR);聚乙烯吡咯烷酮((C6H9NO)nPVP,K30);罗丹明B(C28H31ClN2O3(RhB));所有的药品均从国药集团化学试剂有限公司购买,使用前未经进一步提纯。
1.2 Cu2O/Ag@Cu2O 的制备
Cu2O 的制备我们以乙酰丙酮铜(0.5mmol)作为铜源,聚乙吡咯烷酮(PVP,0.5g)作为氧化剂,加入多元醇DEG(10ml)中,在室温条件下持续搅拌(500rpm) 30min,然后加热,将溶液加热至180℃,在此温度下持续反应40min,获得Cu2O 纳米材料。
Ag@Cu2O 的制备我们也利用简单的一步法合成。将乙酰丙酮铜(0.5mmol)、AgNO3(1ml0.1M)和聚乙烯吡咯烷酮(PVP,0.5g)以及一缩二乙二醇(10ml)加入至三颈瓶中,在室温条件下持续搅拌(500rpm) 30min(溶液的颜色变成了灰蓝色),然后打开加热开关,将溶液加热至180℃,在此温度下持续反应30min,获得Ag@Cu2O 核-壳纳米材料。实验结束,将其自然冷却至室温,以数值速率8000r/min 离心10min,用去离子水和乙醇洗涤3-5次,得到黑色沉淀,分散在乙醇中进一步表征。
1.3 光催化测试
在本实验中我们对RhB 染料在可见光照射下进行了催化活性实验。实验中我们将30mg 的催化剂分解在40ml 的RhB(20mg/L)水溶液中。在光照前,将混合溶液在黑暗条件下磁力搅拌30min,以确保建立吸附-解吸平衡。然后静置5min,然后用一个500w 的氙灯,在磁性搅拌(500rpm,离氙灯的距离为10cm)下照射色散。在给定的时间间隔内,将分散液取样并离心分离催化剂。采用紫外/可见/近红外分光光度计(日立U-4100)测定溶液中RhB 的浓度。
2 实验结果与讨论
图1(f)为样品的XRD 谱图,我们用x 射线衍射(XRD)对样品进行了成分分析和相纯度测定。Cu2O 的XRD 图谱在 2θ值以及核壳结构Ag@Cu2O 核壳结构的XRD 图谱中2 θ值在29.56、42.31和61.37 处的衍射峰与Cu2O (111)、(200)和(220) (PDF#75-1531)平面相一致。核壳结构Ag@Cu2O 核壳结构的XRD 图谱中2θ值在37.93、44.14 和64.68 处的衍射峰与Ag(111)、(200)和(220)(PDF#01-1164)平面相一致,XRD 谱图中未发现Cu 和CuO 等其他相,说明溶剂热法在乙二醇溶液中可以很容易地合成出纯Cu2O 晶体。这些结果表明,样品由Cu2O 和Ag 组成,这与其他文献研究结果一致[1,14-15]。

图1 Ag/Cu2O 样品的SEM 图像(a),Ag/Cu2O 样品的“Ag”(c)、“O”(d)和“Cu”(e)的典型元素映射图像,Cu2O 和Ag/Cu2O 样品的XRD 图像,Ag/Cu2O 样品的TEM (g)和HRTEM (h)图像,Ag@Cu2O 样品的粒径大小数据图(i)

图2 Ag/Cu2O 的XPS 光谱:(a)全谱;(b)Ag3d 和(c)Cu2p;(d)O1s

图3 光照、Cu2O 纳米粒子和Ag@Cu2O 纳米粒子作为光催化剂时RhB 溶液的光催化降解行为(a);Ag/Cu2O 复合材料光催化循环性能的研究(b)

图4 Ag@Cu2O NWs 的光催化性能及机理研究。(a)光照、Cu2O 纳米粒子和Ag@Cu2O 纳米粒子作为光催化剂时,RhB 降解样品的动力学研究;(b)Ag@Cu2O 纳米粒子在可见光照射下的电荷分离过程和光催化机理示意图。这里Ef 是费米能级,CB 是导带,VB 是价带[2]
为了更进一步了解样品的微观结构,我们采集了SEM 和TEM 图像。如图1(a)是Ag@Cu2O 产物的扫描电镜图像,从图中我们可以明显的看到许多单分散均匀、形貌尺寸均一的Ag@Cu2O 微球。从低倍透射电子显微镜(TEM)图像中(1(i)),我们可以清晰地看到产物的结构,具有规则的核壳结构。这些核壳的平均直径大约为88nm,其中Ag 核的尺寸大约为62nm,Cu2O壳厚度约为22nm。图1(h)所示,核壳Ag@Cu2O 复合纳米球晶格分别为的0.49nm 和0.295nm 分别与Ag 的(111) 面和Cu2O 的(211)面对应,Ag 和Cu2O 的界面清晰可见。同时,如图1(b-e)元素映射结果证实,元素Cu 和O 在空心结构外壳分布均匀,而Ag 信号仅在中心区域检测到,这进一步证实了产物的核壳结构,Ag 纳米球被Cu2O 外壳包裹。
通过XPS 分析了Ag@Cu2O 的表面元素组成和化学状态,结果如图2 所示。全谱显示了铜光电子峰(Cu 2p)、银光电子峰(Ag 3d)、氧光电子峰(O 1s)和碳光电子峰(C 1s)。C 峰值的出现可能来自测试仪器。没有其他峰出现,表明形成的Ag@Cu2O 复合材料为纯相,图2(b)为Ag 3d 区域的XPS 谱,位于373.6 eV 和367.7 eV 的两个峰来自于Ag 3d5/2和Ag 3d3/2。三d 偶极体的分裂为6.0 eV,表明银以Ag0态存在的金属性质[1]。图2(c)所示的XPS 光谱显示,Cu 2p1/2和Cu 2p3/2自旋轨道光电子的结合能分别为954.2 eV 和934.2 eV,这与Cu2O 的报道值非常一致。图2(d)显示了O 1s 峰的结合能为530.18eV,531.18eV 处的O 1s 峰可能与吸附氧的晶格氧有关,结果更进一步一致证实了Ag 和Cu2O 的形成。
图3 比较了制备样品在可见光下对RhB 降解的光催化活性。从图3(a)可以看出,在只有光照的情况下,可见光对RhB 的直接光解作用几乎被忽略。纯Cu2O 在60 min 内对RhB 的降解率为43.6%,而Ag@Cu2O 在60 min 内降解了97.6%的RhB。显然,Ag@Cu2O 在这些样品中表现出最高的光催化活性,这比文献中看到的提高了很多[2,14]。这主要是由于Ag@Cu2O 核壳结构具有高比表面积、快速而长距离的电子转移特性和优越的电子导电性,因此比纯Cu2O 表现出更好的光催化性能。
为了进一步确定材料的稳定性,我们对材料进行了循环测试(图3(b)),循环使用Ag@Cu2O 核壳纳米材料对污染物进行光催化降解。实验设定为五次循环,每次光照90min。在第1 次光催化循环过程中,其对RhB 污染物的降解率为97.68%,表现出优异的光催化性能。为了确定其再现性,进行多个降解循环,通过过滤有机染料水溶液,评估剩余有机染料的浓度,确定其降解率。随着循环次数的增加,虽然该催化剂对染料的降解率逐渐降低,但是经过五次循环,Ag@Cu2O 光催化试剂仍能降解罗丹明B(92.7%)。这就证明,Ag@Cu2O 核壳纳米材料在催化氧化反应过程中表现出优异的稳定性,因此我们可以回收利用,节约资源,对环境起到很好的保护作用。
如图4(b)是整个催化反应过程,主要有以下三个过程:首先,当入射光的能量(hv)大于或等于光子匹配的带隙值的能量(禁带宽度Eg)时,产生光生载流子。其次,半导体俘获能量使价带(VB) (Ecb-)上的电子被激发跃迁到导带(CB),并在价带上留下一个空穴hvb+。最后,在光催化剂表面引入亲水基团,提高了染料的快速吸附和染料之间的氧化还原反应。整个光催化过程的反应机理如下[2]:
产物+hv→e-+h+
h++H2O→·OH+H+
O2+e-→·O2-
·O2-+H+→HO2·
2HO2·→O2+H2O2
H2O2+·O2→·OH+OH-+O2
h++OH-→·OH
为了保证染料在催化剂上的吸附-解吸达到平衡,将光催化剂与染料混合,在黑暗条件下搅拌半小时,在黑暗反应完成后,引入光源,并定时取样离心样品。将取出样品的上清液转移到石英试管中进行UV-Vis 测量,在催化过程中不增加额外的能量。根据反应前后溶液的吸光度值(是燃料浓度的一个指标,用来测量染料的分解程度),我们用下面的表达式来计算染料的分解速率:
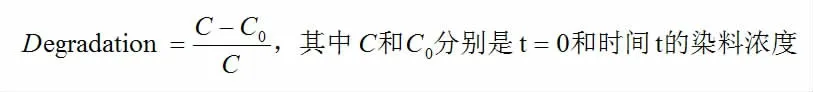
在这篇文章中我们主要选择RhB 作为降解燃料来进行分析研究。监测了RhB 在552nm 处的特征吸收峰,跟踪了催化剂的催化降解过程。RhB 的光降解可描述为伪一阶:ln(C/C0)=-Kt,其中C0和C 分别是初始时间t0和时间t 以后的RhB 浓度,并且确定其速率常数(K,min-1)由ln(C/C0)与照明时间的关系图确定。图4(a)显示了我们工作中使用的RhB 为催化剂的ln(C/C0)与反应时间t 的线性关系,其值接近1,R 值越接近1,模型与实验数据之间的一致性越好,实验数据表明,实验严格遵并模拟了染料降解的动力学方法。
3 结论
综上所述,我们通过简单的一步法合成了Ag@Cu2O 核壳复合纳米材料。从实验中我们发现合成的核壳Ag@Cu2O 复合纳米材料在RhB 的光降解中表现出比工业Cu2O 更好的光催化性能。我们对RhB 的光降解实验结果也表明,产物中Ag 含量过高或过低都不利于Ag/Cu2O 复合材料的光催化活性。经过连续五个周期后,核壳Ag@Cu2O 复合纳米材料的光催化活性基本保持不变,说明它们在RhB 的光降解过程中具有光稳定性。最重要的是,Ag@Cu2O 这种核壳复合纳米材料结构,能够在短时间内通过自然沉降轻易地从溶液中回收和再利用。这些结果表明,核壳Ag@Cu2O 复合纳米材料在可见光光催化环境修复方面具有潜在的应用前景。
