HEOS 系统治疗子宫内膜息肉的效果及预后研究
2021-04-24桂云高婷
桂 云 高 婷
中国科学技术大学附属第一医院 安徽省立医院妇产科,安徽合肥 230001
子宫内膜息肉是临床常见的妇科宫腔疾病[1]。主要表现为经期延长,经量增多及不孕等,部分患者会发生贫血,对患者生活质量造成严重影响[2-3]。既往临床多通过传统宫腔镜电切系统治疗子宫内膜息肉,但其中的电热作用易造成患者出现子宫内膜损伤,从而引发宫腔粘连,预后较差[4-5]。近年来,随着宫腔镜技术的不断发展,双重宫腔镜手术系统(HEOS 系统)逐渐被提出[6]。HEOS 系统是一种冷刀技术,通过非能量器械进行手术,无传统电切术可能产生的电热风险,且该技术通过生理盐水膨宫,安全性更高,但临床对于HEOS 系统治疗子宫内膜息肉的相关报道较少[7-8]。为进一步证实HEOS 系统在子宫内膜息肉患者中的应用效果,为临床治疗提供依据,本研究报道如下:
1 资料与方法
1.1 一般资料
回顾性选取2018 年1 月—2020 年6 月中国科学技术大学附属第一医院(以下简称“我院”)接受HEOS 系统治疗的子宫内膜息肉患者35 例为观察组,另选取同期于我院接受传统宫腔镜电切系统治疗的患者35 例为对照组。观察组年龄22~44 岁,平均(33.24±2.43)岁;流产次数(0.74±0.15)次;病灶大小(15.35±3.24)mm;对照组年龄21~45 岁,平均(33.53±2.38)岁;流产次数(0.78±0.13)次;病灶大小(15.53±3.16)mm。纳入标准:符合子宫内膜息肉诊断标准[9]。排除标准:①合并有与妊娠相关的宫腔疾病;②资料不全。两组一般资料比较,差异无统计学意义(P >0.05),具有可比性。
1.2 方法
观察组采用HEOS 系统治疗,具体步骤为:①术前患者进行经阴道彩超及凝血功能、血常规、生化等相关检查,若有严重贫血患者,入院后需进行输血,血红蛋白(Hb)>80 g/L 后才可进行手术,所有患者均经评估无手术麻醉禁忌证。②静脉麻醉后,取膀胱截石位,使用HEOS 系统套装(法国摄普乐-高美格公司)及相关工作站、膨宫机、光源系统及成像系统,膨宫介质为0.9%生理盐水,将膨宫压力设置为100~150 mmHg(1 mmHg=0.133 kPa)。③首先通过诊断性宫腔镜对患者宫腔及宫颈情况进行相关检查,以进一步对HEOS 系统治疗的安全性和可行性进行评估,接着扩宫至10 号,并将HEOS 宫腔镜在直视下置入,进行相应手术。④通过夹持力较大的微型钳和微型剪将宫内膜息肉直接钳夹摘除。
对照组采用传统宫腔镜电切系统治疗。手术步骤为:消毒后扩张宫口,膨宫介质为甘露醇溶液或生理盐水,将膨宫压力设置为100~150 mmHg,通过宫腔电切镜对病灶进行观察,并根据患者具体情况进行手术。
1.3 观察指标
比较两组手术时间,术前及术后1 d(术后)生化指标,术后2 个月子宫内膜恢复情况及并发症发生情况。
生化指标检测:分别于手术前后1 d 取患者空腹静脉血5 mL,通过美国贝克曼库尔特公司生产的BECKMAN COULTER CX9 生化仪及COULTER J TIR 血液分析仪对生化指标水平进行检验记录。
1.4 统计学方法
采用SPSS 19.0 统计学软件进行数据分析,计量资料用均数±标准差()表示,两组间比较采用t 检验;计数资料用例数或百分率表示,组间比较采用χ2检验。以P <0.05 为差异有统计学意义。
2 结果
2.1 两组手术情况比较
观察组手术时间为(19.62±0.95)min,短于对照组的(25.09±1.07)min,差异有高度统计学意义(t=22.616,P <0.01)。
2.2 两组术前后生化指标比较
手术前后两组生化指标比较,差异无统计学意义(P >0.05)。见表1。
2.3 两组手术后2 个月子宫内膜恢复情况比较
两组月经恢复时间、阴道流液或流血时间比较,差异无统计学意义(P >0.05);观察组子宫内膜厚度大于对照组,差异有统计学意义(P <0.05)。见表2。
表1 两组手术前后生化指标比较()
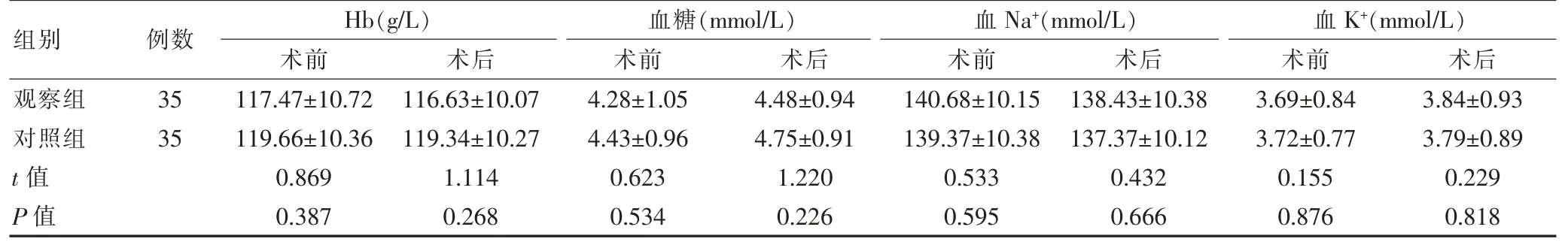
表1 两组手术前后生化指标比较()
注:Hb:血红蛋白
表2 两组术后2 个月子宫内膜恢复情况比较()
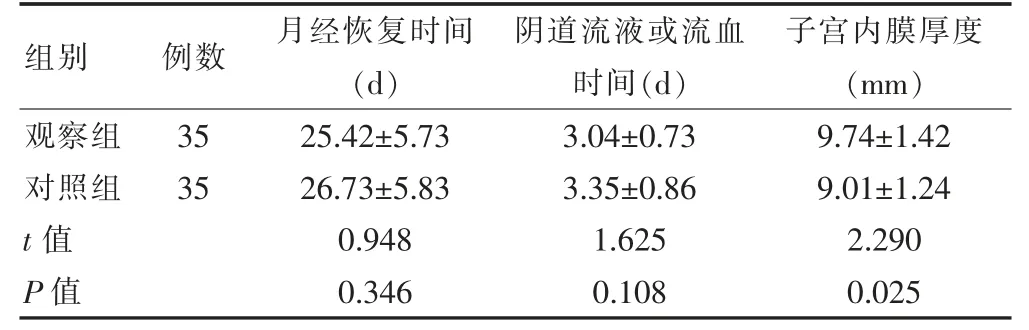
表2 两组术后2 个月子宫内膜恢复情况比较()
2.4 两组并发症发生情况
随访2 个月,所有患者均未出现宫颈粘连等并发症。
3 讨论
宫腔疾病主要包含子宫内膜息肉、胚胎残留、宫腔粘连、黏膜下肌瘤等[10]。子宫内膜息肉是临床最为常见的宫腔疾病,发病率高达2%~2.5%,多发于育龄期女性,对患者生育及生活造成严重影响[11-13]。目前临床对于宫腔疾病主要通过宫腔镜手术治疗,临床疗效较好[14-15]。但实践证实,该治疗方法可能存在低钠血症、手术时间长、术中出血多、干扰源多、内膜电损伤等不良现象,严重者会出现子宫穿孔,妊娠后子宫破裂、宫颈粘连等并发症[16-20]。因此,亟需更为安全可靠的治疗方法,在治疗的同时可对患者子宫内膜起到保护作用,基于该目的,宫腔镜冷刀技术逐渐应用于临床[21]。
HEOS 系统是一种新型宫腔镜冷刀技术,包含电切镜基本套装及HEOS 系统套装,配备3 mm 非能量硬性器械,主要包含分离钳、抓钳、硬式双关节和单关节剪刀等[22-23]。较之于传统电切手术,具有操作灵活,器械作用率高,手术时间短,安全性高等特点[24]。且HEOS 宫腔镜是视野更清晰更大、镜体更粗的一体镜,配合易于操作功能强大的冷器械,使得宫腔镜手术的风险及难度更低[25-26]。研究显示[27],将HEOS 系统应用于宫腔疾病的治疗中安全性高,可减少并发症发生,疗效显著。本研究结果显示,观察组手术时间短于对照组(P <0.01)。提示HEOS 系统可减少子宫内膜息肉患者手术时间,与类似研究结果一致[28]。
本研究对患者手术前后生化指标进行比较,结果显示,手术前后,两组生化指标比较,差异无统计学意义(P >0.05)。提示两种手术方式对患者生化代谢影响较小,但还需加大样本更进一步探讨研究。本研究结果显示,两组月经恢复时间、阴道流液或流血时间比较,差异无统计学意义(P >0.05);观察组子宫内膜厚度大于对照组(P <0.05)。随访2 个月,所有患者均未出现宫颈粘连等并发症。提示HEOS 系统治疗子宫内膜息肉安全性高,患者内膜及手术创面的恢复均较快。分析其原因可能为,HEOS 系统是一种冷刀技术,属于冷器械,不会出现电热辐射,因此在治疗过程中子宫内膜出现热损伤的可能性较小,故而对患者子宫内膜的保护效果更为明显,患者恢复更快[29-30]。
综上所述,HEOS 系统治疗子宫内膜息肉临床效果显著,安全性高,可减少手术时间,促进患者恢复,值得临床推广应用。
