异甘草酸镁预防恶性肿瘤化疗药致肝损伤的有效性和安全性的系统评价
2021-04-23吴玉娇杨艳玲
吴玉娇,张 晶,杨艳玲
(恩施土家族苗族自治州中心医院临床药学科,湖北 恩施 445000)
*主管药师。研究方向:临床药学。E-mail:835012896@qq.com
我国恶性肿瘤患者不断增多,手术、辅助放疗及化疗仍是目前恶性肿瘤的主要治疗手段。抗肿瘤化疗药本身、其代谢产物及患者自身特殊体质往往使得抗肿瘤药对机体产生一系列的毒性反应。肝脏是药物聚集、转化或代谢为其他产物的重要器官,也是一些药物的主要靶器官,因此,在化疗过程中易发生药物性肝损伤[1-2]。药物性肝损伤可致化疗方案的更换、化疗药的减量或延迟化疗,从而延缓患者治疗,导致病情进展[3]。联合应用护肝药是否可以预防化疗导致的药物性肝损伤尚无定论。本研究收集异甘草酸镁预防恶性肿瘤患者使用化疗药发生肝损伤的临床研究文献,通过荟萃分析(Meta分析)方法进行系统定量分析,为异甘草酸镁能否预防化疗药所致肝损伤提供理论参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型:国内外有关使用异甘草酸镁预防恶性肿瘤患者使用化疗药发生肝损伤的临床对照研究,文种为中英文。
1.1.2 研究对象:具有明确的细胞或组织病理学诊断依据,确诊为恶性肿瘤的患者;明确使用全身抗肿瘤化疗药;年龄≥18岁;预估生存期>3个月;化疗前肝功能正常,无肝转移、病毒性肝炎及其他肝脏疾病。
1.1.3 干预措施:研究组患者使用异甘草酸镁注射液,对照组使用其他护肝药(硫普罗宁、甘草酸二铵、谷胱甘肽、肌酐、多烯磷脂酰胆碱、门冬氨酸钾镁及复方二氯醋酸二异丙胺);给药方式为静脉滴注。两组患者均进行常规化疗。
1.1.4 结局指标:(1)主要结局指标为肝功能异常发生率,依据为世界卫生组织化疗药急性及亚急性毒性反应分度标准。(2)血清丙氨酸转氨酶(ALT)、碱性磷酸酶(ALP)和总胆红素(TBIL)是用于诊断和指导药物性肝损伤分型的主要指标,因此,本研究采用肝功能生物化学指标ALT、ALP和TBIL为次要指标。(3)根据不良反应发生情况评价用药安全性。
1.1.5 排除标准:综述性文献;重复性文献;原始文献中研究设计不严谨、样本信息不清以及疗效判定标准不规范等;研究组患者干预措施为异甘草酸镁,但对照组患者未使用其他护肝药的文献;联合应用护肝药的研究。
1.2 文献检索策略
检索的主要文献数据库包括中国知网、万方数据库、维普网、PubMed和the Coehrane library等,检索从建库至2020年12月针对异甘草酸镁预防肿瘤患者使用化疗药发生肝损伤的临床研究。中文检索词包括“异甘草酸镁”“肿瘤”和“药物性肝损伤”;英文检索词包括“Magnesium isoglycyrrhizinate”“Drug-induced liver injury”“DILI”“Cancer”和“Tumour”。
1.3 资料提取与方法学质量评价
由2名研究人员根据上述纳入与排除标准对检索出的文献进行独立阅读全文,以确定是否纳入研究,并交叉核对,对有异议的文献通过讨论或由第3名研究者决定是否最终纳入。对最终纳入的研究采用Excel软件提取并录入资料,包括作者姓名及发表年份、研究对象、总病例数、研究组与对照组病例数、具体的干预措施及明确的评价指标。采用Cochrane偏倚风险表,从是否采用随机方法、是否分配隐藏及是否运用盲法、是否有完整的结局数据、是否选择性报告研究结果以及是否存在其他偏倚来源等方面评价所纳入文献的质量,每条标准根据文献具体描述情况以“低风险”“高风险”和“未知风险”进行评价。
1.4 统计学方法
遵循Meta分析步骤,完善文献检索、资料提取。若研究设有多组对照,研究组为异甘草酸镁,对照组有空白对照和其他护肝药,Meta分析时则剔除空白对照组即未使用护肝药组;若对照组有异甘草酸镁联合应用其他护肝药,Meta分析时亦剔除该组,仅纳入单独使用其他护肝药的对照组;若对照组为谷胱甘肽和多烯磷脂酰胆碱,研究组为异甘草酸镁,研究结局指标为二分类变量,Meta分析时先合并对照组的相关数据。运用RevMan 5.3软件进行统计学分析,其中连续性数据分析结果通过均差(MD)和95%置信区间(CI)报告,二分类数据的分析结果通过相对危险度(RR)和95%CI报告,P<0.05表示差异具有统计学意义。纳入的研究间如无明显异质性(P≥0.1,I2≤50%),运用固定效应模型进行统计分析;反之,则运用随机效应模型进行统计分析,并对可能造成异质性的来源进行分析。采用漏斗图评价是否存在发表偏倚。
2 结果
2.1 文献检索结果及纳入文献的基本特征
进行相关文献检索,初检出449篇文献,排除361篇与选题不符的文献,排除46篇重复文献,初步纳入42篇文献;然后排除29篇不符合纳入标准的文献(包括联合应用护肝药3篇、干预措施不符合14篇、综述与评论5篇、硕士学位毕业论文3篇和疗效判断标准不明确4篇);最终纳入13篇文献[3-15],均为中文文献。纳入文献的基本特征见表1。其中,5篇文献[5-6,11-12,14]设有多组对照,研究组为异甘草酸镁,对照组有空白对照和其他护肝药;2篇文献[5-6]的对照组有异甘草酸镁联合应用其他护肝药;文献[4]的对照组为谷胱甘肽和多烯磷脂酰胆碱,研究组为异甘草酸镁,该研究结局指标为二分类变量肝功能异常发生率和不良反应发生率。
2.2 纳入文献的方法学质量评价
纳入13篇文献[3-15]中,10篇[3-5,7-9,11-13,15]为随机对照试验(其中1篇[4]采用随机数字法进行分组,1篇[5]采用计算机随机分组),3篇[6,10,14]未提及是否随机分组;所有研究均未提及是否采用盲法及分配隐藏,评价为“未知风险”;纳入研究未有数据缺失,结局指标报告完整;是否有其他偏倚评价为“未知风险”,见图1—2。
2.3 Meta分析结果
2.3.1 肝功能异常发生率:9篇文献[3-7,11-12,14-15]报告了肝功能异常发生率,涉及的研究间无异质性(P=0.90,I2=0%),因此Meta分析运用固定效应模型。统计结果显示,研究组患者化疗过程中肝功能异常发生率明显低于对照组,差异有统计学意义(RR=0.44,95%CI=0.33~0.59,P<0.000 01),见图3。2.3.2 ALT:8篇文献[3,6,8-10,13-15]报告了ALT水平对比结果,涉及的研究间具有较大统计学异质性(P<0.000 01,I2=90%),因此Meta分析运用随机效应模型。统计结果显示,研究组患者的ALT水平明显低于对照组,差异有统计学意义(MD=-10.81,95%CI=-14.20~-7.43,P<0.000 01),见图4。敏感性分析发现,文献[3]、文献[15]的研究对异质性的影响大,剔除上述2项研究后,剩余研究间无异质性(P=0.44,I2=0%),运用固定效应模型再次进行Meta分析,结果显示,研究组患者的ALT水平明显低于对照组,差异有统计学意义(MD=-12.33,95%CI=-13.51~-11.16,P<0.000 01)。

表1 纳入文献的基本特征Tab 1 Basic characteristics of included literature
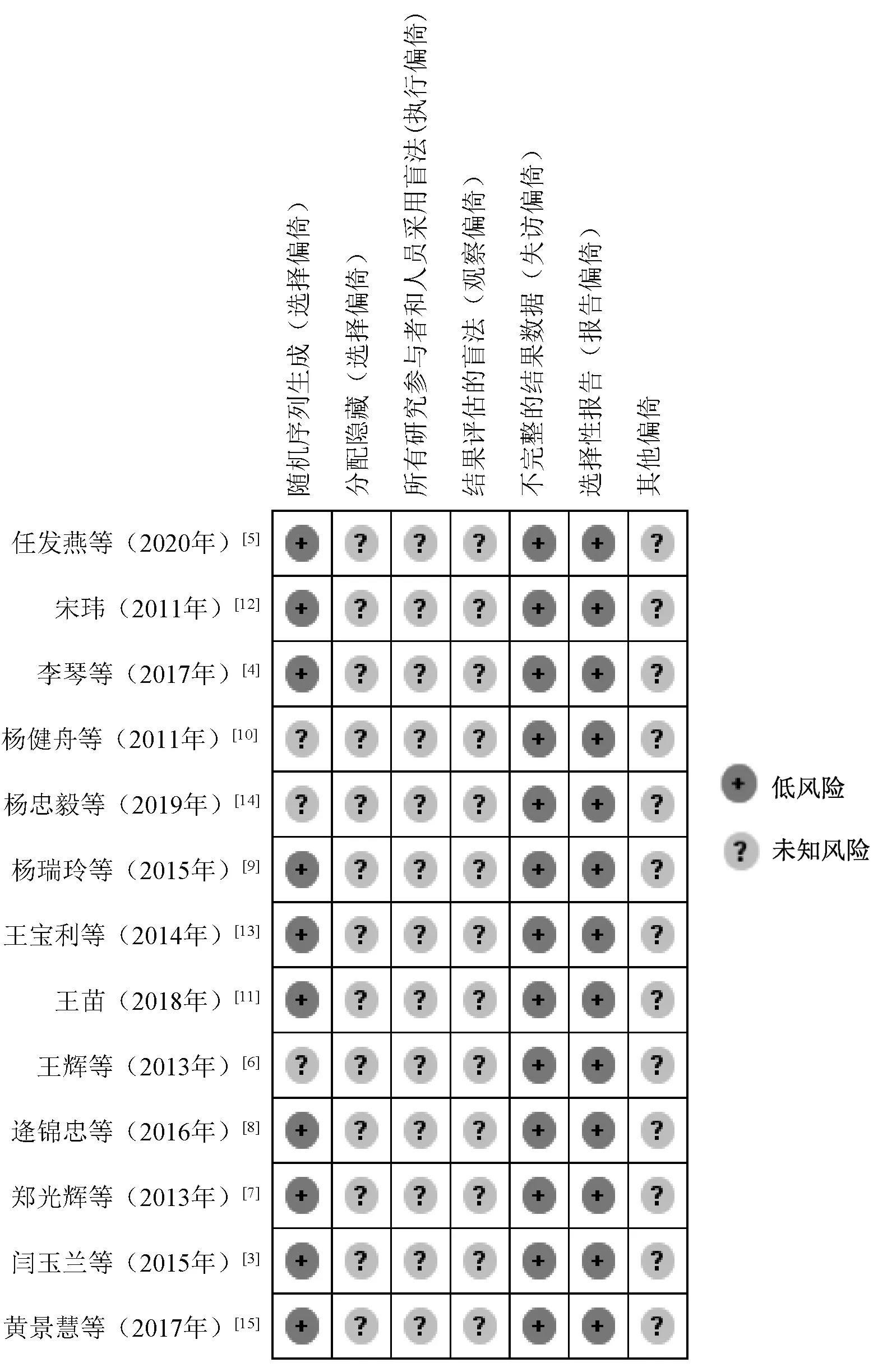
图2 纳入研究的风险偏倚图Fig 2 Summary of risk bias of included literature
2.3.3 ALP:5篇文献[3,6,13-15]报告了ALP水平对比结果,涉及的研究间具有较大异质性(P=0.04,I2=61%),因此Meta分析运用随机效应模型。统计结果显示,研究组患者的ALP水平明显低于对照组,差异有统计学意义(MD=-15.56,95%CI=-20.78~-10.34,P<0.000 01),见图5。敏感性分析发现,文献[14]的研究对异质性的影响大,剔除该研究后,剩余研究间无异质性(P=0.47,I2=0%),运用固定效应模型再次进行Meta分析,结果显示,研究组患者的ALP水平明显低于对照组,差异有统计学意义(MD=-12.15,95%CI=-15.34~-8.95,P<0.000 01)。
2.3.4 TBIL:7篇文献[3,6,8,10,13-15]报告了TBIL水平比较结果,涉及的研究间具有较大异质性(P=0.003,I2=70%),因此Meta分析运用随机效应模型。统计结果显示,研究组患者的TBIL水平明显低于对照组,差异有统计学意义(MD=-4.00,95%CI=-5.24~-2.77,P<0.000 01),见图6。敏感性分析发现,文献[15]的研究对异质性的影响大,剔除该研究后,剩余研究间异质性较小(P=0.34,I2=11%),运用固定效应模型再次进行Meta分析,结果显示,研究组患者的TBIL水平明显低于对照组,差异有统计学意义(MD=-3.41,95%CI=-3.95~-2.87,P<0.000 01)。
2.3.5 不良反应发生率:6篇文献[4,9-13]报告了不良反应发生情况,其中,研究组患者均未发生严重不良反应;文献[12]的对照组1例患者发生过敏性休克的严重不良反应,经处理后好转。涉及的研究间异质性较小(P=0.23,I2=27%),因此Meta分析运用固定效应模型。统计结果显示,两组患者不良反应发生率的差异不具有统计学意义(RR=0.72,95%CI=0.37~1.38,P=0.32),见图7。
2.3.6 发表偏倚:针对肝功能异常发生率绘制漏斗图,结果显示,漏斗图分布不呈左右对称性,纳入的研究较少,提示所纳入研究可能存在一定的发表偏倚,见图8。
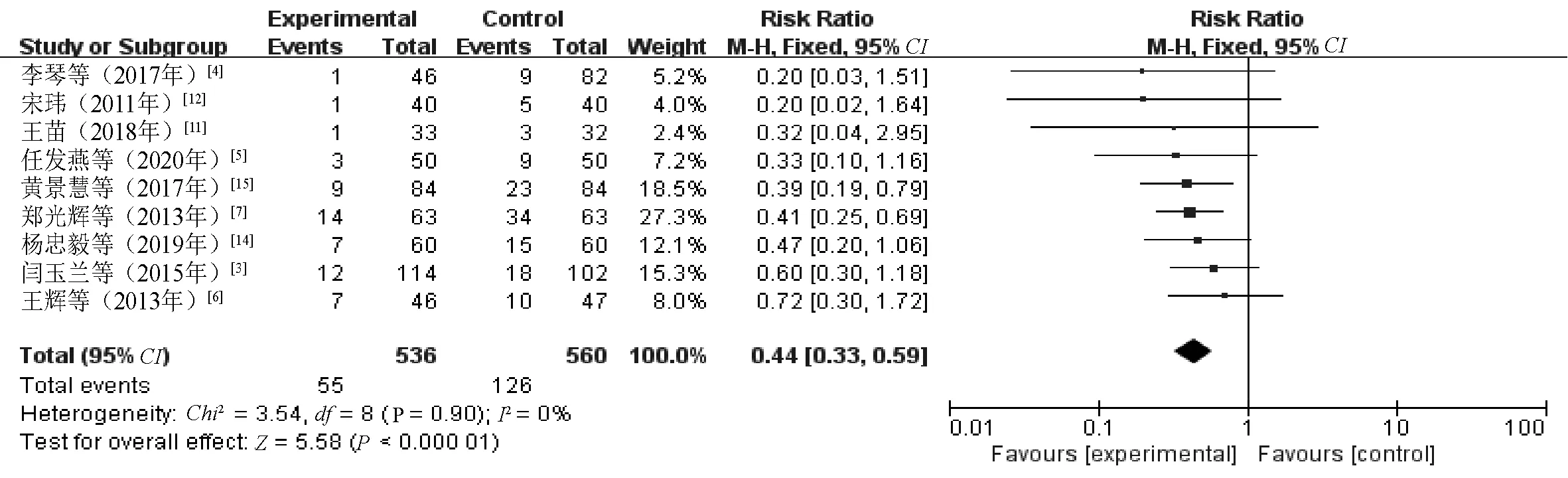
图3 两组患者肝功能异常发生率比较的Meta分析森林图Fig 3 Meta-analysis of comparison of incidence of abnormal liver function between two groups
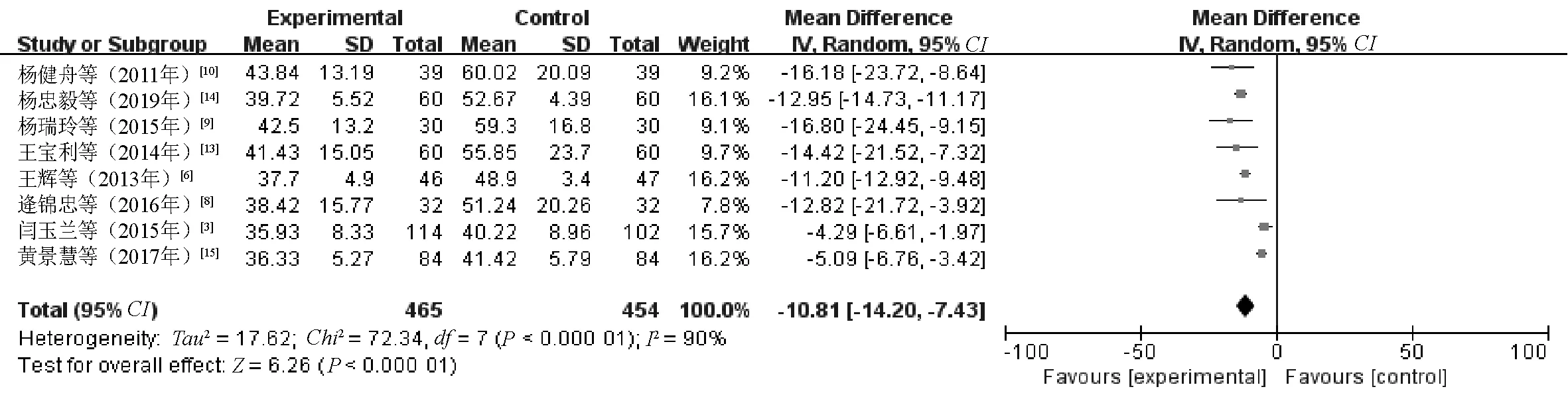
图4 两组患者ALT水平比较的Meta分析森林图Fig 4 Meta-analysis of comparison of level of ALT between two groups
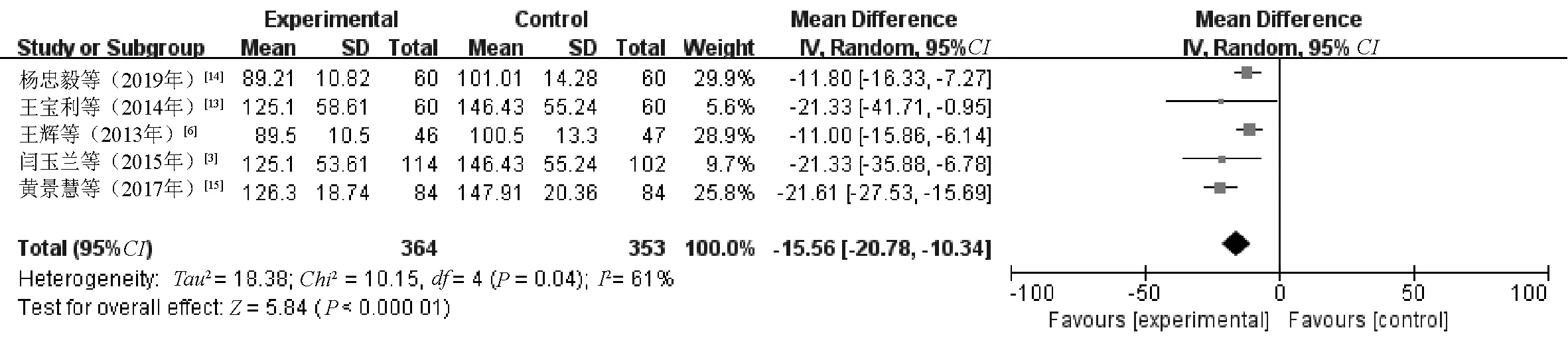
图5 两组患者ALP水平比较的Meta分析森林图Fig 5 Meta-analysis of comparison of level of ALP between two groups
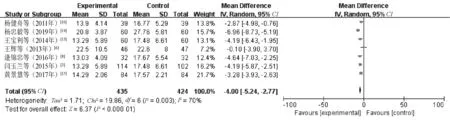
图6 两组患者TBIL水平比较的Meta分析森林图Fig 6 Meta-analysis of comparison of level of TBI between two groups
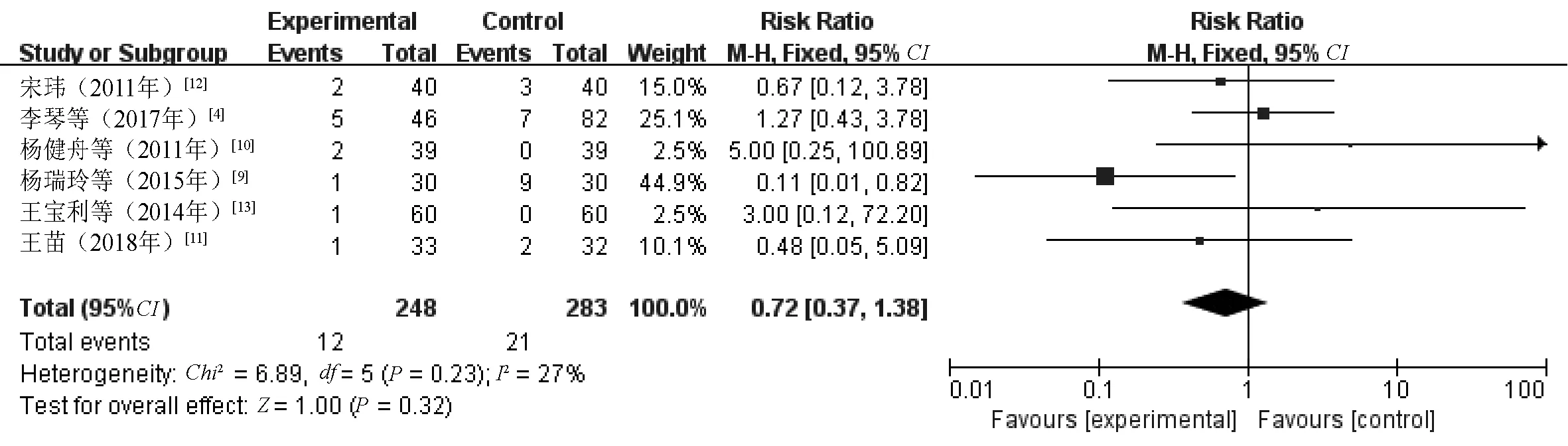
图7 两组患者不良反应发生率比较的Meta分析森林图Fig 7 Meta-analysis of comparison of incidence of adverse drug reactions between two groups
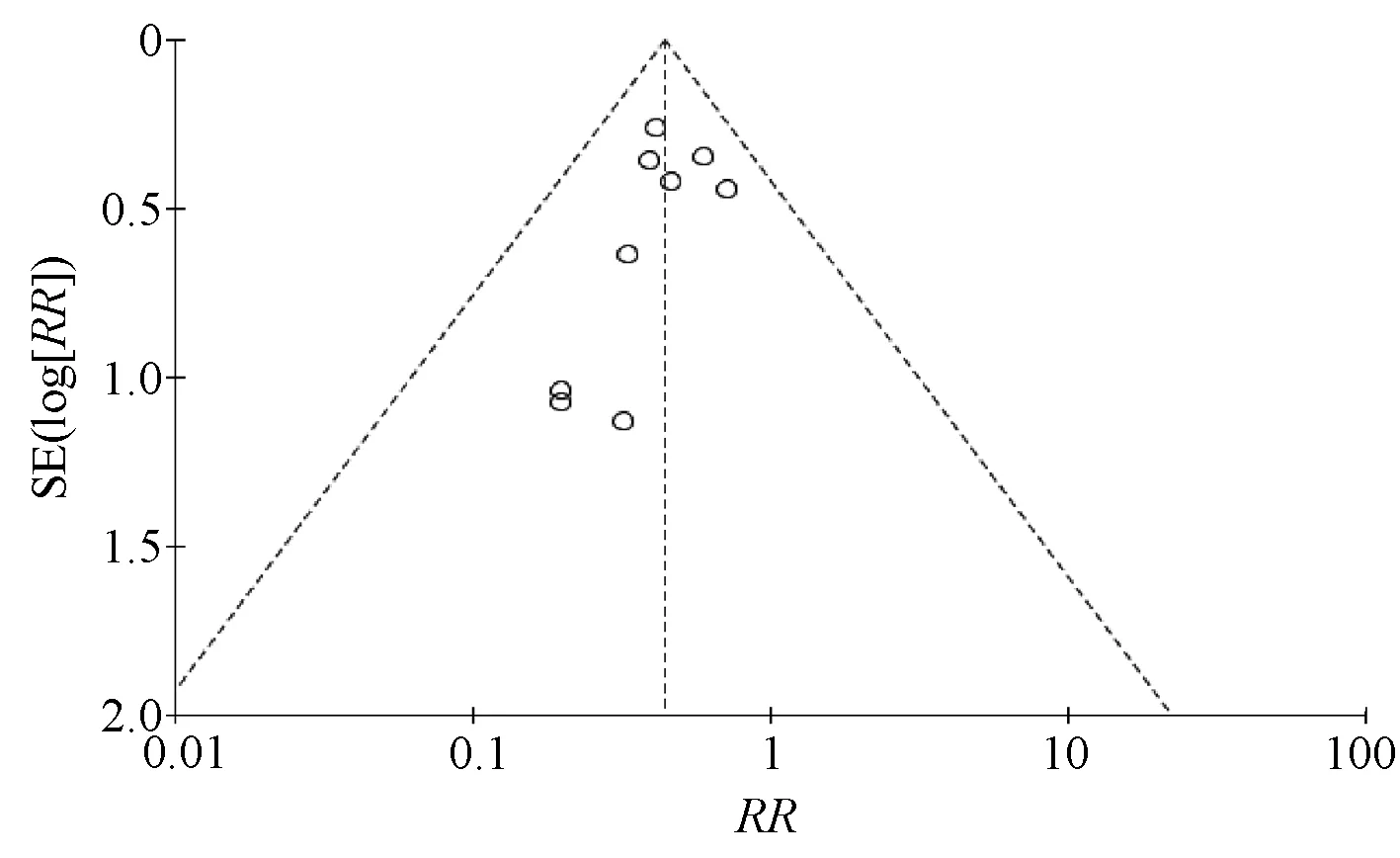
图8 肝功能异常发生率的漏斗图Fig 8 Funnel plot of incidence of abnormal liver function
3 讨论
药物性肝损伤是指人体在使用药物的过程中,由药物或活性代谢物引起的直接毒性作用,或由人体对药物及其代谢物的特异质反应所致肝功能损害或异常[16]。部分患者可发生不可逆肝损伤、暴发性肝衰竭,甚至危及生命。有文献报道,抗肿瘤药及其代谢产物可因免疫介导直接损伤肝细胞,也可因为患者代谢异常,如遗传多态性所致药物代谢酶的活性降低,使得药物原形和中间代谢产物增加,直接损伤肝细胞,从而导致肝细胞变性,甚至坏死[3]。
本研究结果表明,与其他护肝药比较,预防性使用异甘草酸镁可明显降低化疗过程中肝功能异常发生率,明显降低生化指标ALT、ALP及TBIL水平,可能与异甘草酸镁的药理机制相关。异甘草酸镁为第4代甘草酸制剂,具有类似肾上腺皮质激素的非特异性抗炎作用,具有保护肝细胞膜、改善肝功能的多重作用[17]。药理实验结果证明,异甘草酸镁可针对炎症通路,抑制3条炎症通路相关炎症反应信号的活性,下调炎症通路上游相关促炎因子的表达,减少核因子κB过度表达诱发的炎症反应,阻断炎症通路下游;同时,其能够促进肝细胞的增殖,抑制肝星形细胞的形成而抑制肝纤维化的发生,从而发挥免疫调节功能,减轻肝脏的病理损害,改善受损的肝细胞功能[17-18]。
本研究亦存在一定局限性。Meta分析结果显示,ALT、ALP和TBIL指标涉及的研究间统计学异质性较大,故进行相应的敏感性分析。阅读文献发现,纳入的研究对象不完全一致,患者所患肿瘤类型不完全一致,所用化疗药不尽相同,另外,干预措施中研究组异甘草酸镁的剂量和对照组其他护肝药种类、剂量、疗程不一致,均可能导致各研究间的统计学异质性。对报告了肝功能异常发生率的9项研究绘制漏斗图,结果显示,漏斗图不呈左右对称,说明可能有阴性结果尚未发表;纳入的文献是否采用盲法研究尚未交待清楚,可能使得结果存在一定偏倚。期待纳入更多高质量、大样本、多中心研究,对异甘草酸镁预防化疗药所致肝损伤提供更多证据。
本研究中所纳入的研究对象均为我国肿瘤患者,在一定程度上避免了基因多态性对结果的影响;纳入的肿瘤患者范围广,涉及病种多,使用的化疗药种类繁多。本研究结果显示,抗肿瘤化疗过程中使用异甘草酸镁,能够预防化疗药所致肝损伤,明显降低肝功能异常发生率,具有临床使用价值。但临床预防性使用异甘草酸镁的指征、给药时间和疗程等,尚需进一步探讨。
