黏液炎性纤维母细胞性肉瘤合并脊柱旁转移病例的分析
2021-04-23罗雁安宁康雅琼何欣宋丽娟李晓琴
罗雁 安宁 康雅琼 何欣 宋丽娟 李晓琴
甘肃省肿瘤医院,甘肃 兰州730050
黏液炎性纤维母细胞性肉瘤(myxoinflammatory fibroblastic sarcoma,MIFS)是一类极为罕见的好发于肢端的低度恶性的软组织肿瘤[1],目前国内外关于黏液炎性纤维母细胞肉瘤的报道非常少,且极易于结节性筋膜炎、腱鞘囊肿、炎性肌纤维母细胞瘤等软组织肿瘤相混淆,故认识并掌握其组织学特征尤为重要。本文回顾性分析1 例黏液炎性纤维母细胞性肉瘤并脊柱旁转移,并结合相关文献,探讨其临床病理学特征、免疫表型、诊断及鉴别诊断,以增强对该肿瘤的认识。
1 材料与方法
1.1 临床资料 患者男性,55 岁,因左拇趾肿物1 年余,逐渐增大,于2018 年3 月在外院行左拇指截肢术,术后病理提示:间叶源性恶性肿瘤,多考虑上皮样肉瘤。2019 年5 月无明显诱因出现左下肢反射性疼痛,进行性加重,遂来我院入院治疗,病理切片会诊提示黏液炎性纤维母细胞性肉瘤。腰椎MRI 提示:脊柱旁恶性占位性病变,累及左侧髂腰肌、腰大肌、腰5 锥体及椎弓,腰背部软组织肿胀、模糊、水肿。
1.2 方法 送检组织均经10%中性福尔马林固定,常规脱水,石蜡包埋,4μm 厚切片,行HE 染色,光镜观察。免疫组化采用Envision 法,所用抗体包括Vimentin、CD34、D2-40、CD68、CK-Pan、EMA、SMA、Desmin、S-100、P53、EGFR、Ki-67 均购自迈新生物技术开发有限公司,操作步骤按试剂说明书进行,免疫组化根据不同抗体阳性部位和强度进行判读。
2 结果
2.1 眼观 脊柱旁肿物:8cm×6cm×4cm 灰褐色不整形组织,质地中等,切面灰白,局部呈半透明黏液样,可见出血。
2.2 镜检 肿瘤组织弥漫分布,低倍镜下显示,病变主要由黏液样变区、炎症性区域及玻璃样变区域组成,黏液样变区中可见组织细胞样或上皮细胞样的畸形大细胞(图1)分布其中,局部有黏液湖的形成,其内细胞和血管较稀疏,肿瘤细胞多围绕血管分布(图2),炎症性区域内可见多量的淋巴细胞及浆细胞浸润。本例中玻璃样变区域较少,局灶可见间质呈玻璃样变性。肿瘤细胞多分布在大片出血及炎细胞的背景中(图3),局灶有凝固性坏死。
2.3 免疫表型 肿瘤细胞弥漫表达Vimentin(图4)、EGFR(图5),部分表达CD68、EMA(图6),D2-40、CKPan 及P53(局灶弱+),SMA、Desmin、CD34 及S-100 均(-),Ki-67 增殖指数约20%。
2.4 病理诊断 左拇趾黏液炎性纤维母细胞性肉瘤并脊柱旁转移。
2.5 随访 患者脊柱旁肿物切除后行化疗,术后随访6 个月,无复发。
3 讨论
MIFS 是一类好发于四肢远端的纤维母细胞性肉瘤[2]。MIFS 由Meis-Kindblom、Montgomery 及Michal三人于1998 年提出[3],因极易发生于肢端,故曾命名为“肢端黏液炎性纤维母细胞肉瘤”,但随后报道显示也可以发生于肘部、上臂、肩部、大腿等肢体的近端[4]。2002 年软组织和骨肿瘤病理学和遗传学分类中将其命名为黏液炎性纤维母细胞性肉瘤[5]。
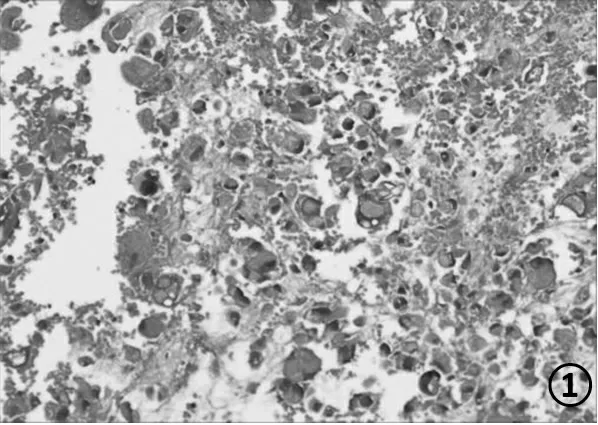
图1 黏液样变及大片出血中可见畸形大细胞
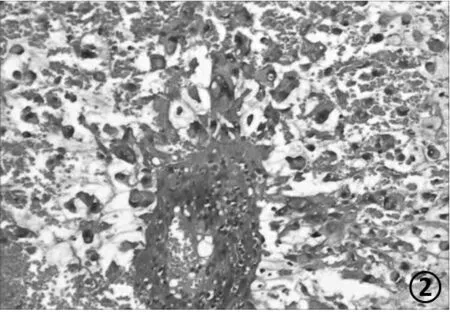
图2 异型大细胞围绕血管分布
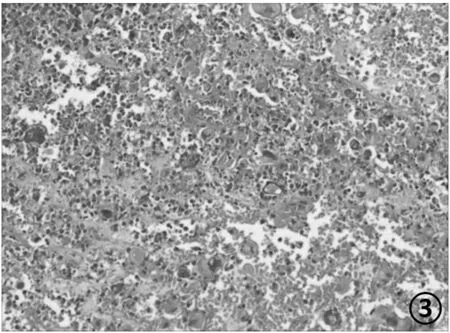
图3 瘤细胞分布在大片出血及炎细胞的背景中
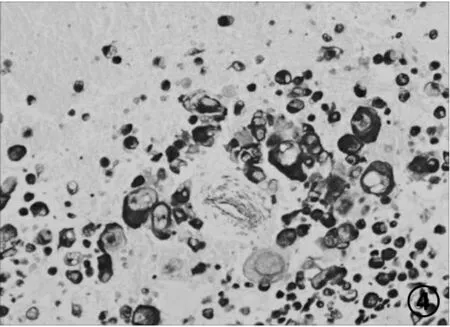
图4 肿瘤细胞Vimentin 弥漫胞质(+),EnVision 法
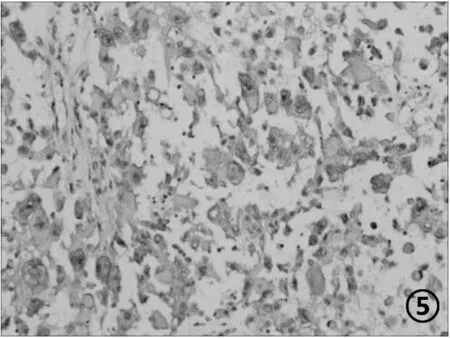
图5 肿瘤细胞EGFR 胞质(+),EnVision 法
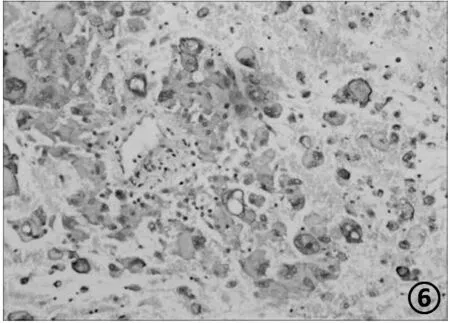
图6 肿瘤细胞EMA 胞质弱(+),EnVision 法
3.1 临床特征 MIFS 好发于成年人,高峰年龄30~50岁[6],好发于肢体的远端,多见于手指和足。崔淼等[7]于2016 年报道过1 例发生于小肠的MIFS,极为罕见。临床上常表现为缓慢性生长的无痛性肿块,部分患者曾有外伤史,临床上常被误诊为腱鞘囊肿、结节性筋膜炎。
3.2 病理特征 肿瘤常位于皮下,被脂肪小叶间的纤维结缔组织分隔。病变主要由黏液样区域、炎症性区域及玻璃样变区域所组成。各区域混杂存在并且之间常有移行。瘤细胞形态多样,形态上有类似于R-S 细胞、节细胞的大细胞,含大核仁,胞质嗜酸性。还有类似于组织细胞样或上皮细胞样的畸形细胞,主要分布于炎症性区域和玻璃样变区域。黏液样区域内可见多泡状假脂母细胞,稀疏的漂浮于黏液湖中,可围绕血管分布。炎症性区域内可见大量淋巴细胞和浆细胞浸润。局部间质呈玻璃样变,局灶可伴出血及含铁血黄素的沉积。少数病例可出现凝固性或纤维素样坏死,但不常见。本例患者为MIFS 术后脊柱转移,可见大片出血及凝固性坏死,提示MIFS 转移后的级别增高,生物学活性及侵袭性增强。
3.3 免疫表型 MIFS 瘤细胞弥漫性表达Vimentin,畸形的大细胞可表达CD68、CD34、D2-40、SMA,部分弱阳性表达CK-pan、EMA。炎细胞主要为T 淋巴细胞。有报道[8]部分MIFS 呈表皮生长因子受体EGFR 的弥漫阳性表达,可辅助诊断和靶向治疗提供一定的依据,本例中EGFR 弥漫性胞质弱阳性,与报道较一致。有报道认为Ki-67 在初发病例中指数一般较低<1%,而在复发病灶中指数可升高到10%~50%[9],本例中原发病灶中Ki-67 指数约5%,脊柱转移后Ki-67 指数明显提高到20%,提示转移后肿瘤细胞的增殖活性增高,更具侵袭性。
3.4 细胞遗传学 目前,对于MIFS 细胞遗传学的研究相对较少。2001 年Lambert 等[10]首先报道了t(1;10)(p22;q24),对t(1;10)断裂点分析发现,1 号染色体断裂点(1p22)涉及TGFBR3 基因,10 号染色体断裂点(10q24)涉及MGEA5 基因,导致NPM3 基因转录上调。TGFBR3 和MGEA5 基因重排可通过FISH 检测,对MIFS 的诊断有很大帮助。
3.5 鉴别诊断 MIFS 极易与一些软组织良性病变或其他恶性肿瘤相混淆,故需与下列疾病鉴别:(1)结节性筋膜炎:是一种自限性疾病,多发生于青壮年,好发于上肢,主要位于前臂屈侧,极少发生于肢端。结节性筋膜炎中存在MYH9-USP6 融合基因,可通过FISH 检测进行鉴别。(2)弥漫型腱鞘巨细胞瘤:也称色素性绒毛结节性滑膜炎,多发生于青年人,主要发生于膝部、髋部等大关节。肿瘤内无黏液样和玻璃样变的区域,也不见假脂母细胞及畸形的大细胞。(3)炎性肌纤维母细胞性肿瘤(IMT):是一种好发于儿童和青少年的肌纤维母细胞性肿瘤。IMT 常伴有ALK 基因的重排,分子检测可与MIFS 相鉴别。(4)肢端浅表性纤维黏液瘤:好发于手足,常累及甲板,病变位于真皮内。免疫组化除Vimentin 外,绝大多数表达CD34,CD99,不表达SMA、desmin 等肌纤维母细胞的标志物。(5)黏液纤维肉瘤:很少发生于手足,生长快,恶性程度高。无MIFS所具有的炎症性区域及硬化性区域,也无R-S 样细胞或畸形的大细胞。(6)结外霍奇金淋巴瘤:原发于软组织的霍奇金淋巴瘤非常罕见,无纤维肌纤维母细胞,也无黏液区,常在炎性背景中见到R-S 样细胞,R-S 样细胞表达CD30 及CD15。
3.6 治疗及预后 MIFS 属于一种中间性肿瘤,呈低度恶性经过。目前临床对原发性肿瘤采取局部广泛切除,并确保切缘阴性,但具有较高的局部复发率(22%~67%)[11]。多次复发并累及肢体时,考虑截肢。很少发生远处转移,目前已发现有转移到淋巴结、肺、颅底等部位[12-13]。Michal[14]等报道过一组高级别MIFS,18 例患者中,9 例发生转移,7 例发生死亡,提示MIFS 并非都是一种中间型偶有转移的软组织肿瘤,其中有一小部分可能呈高级别形态,此型极易复发并且发生转移。本例在原发病灶切除1 年后发生脊柱旁转移,并伴片状凝固性坏死,可能为高级别MIFS。术后辅以放、化疗的效果目前不肯定,尚在探索中。
