医疗器械生产企业厂房与设施合规管理要点
2021-04-22许慧屈昆鹏
许慧 屈昆鹏
漫修医疗器械企业合规研究中心,中国·江苏 苏州 215000
1 引言
对于医疗器械生产企业而言,合规管理的头条任务就是建立和健全与所生产医疗器械相适应的质量管理体系并保证其能够有效运行,而厂房与设施恰是做好质量管理合规的基础。论文从相关合规要点及问题的综合梳理、研判出发,旨在探索如何做好医疗器械生产企业厂房与设施合规管理工作。
2 医疗器械生产企业厂房与设施合规管理基本要求
根据《医疗器械监督管理条例》《医疗器械生产质量管理规范》(以下简称《生产质量管理规范》)和《医疗器械生产监督管理办法》(以下简称《生产监督管理办法》)等法规的要求,医疗器械生产企业厂房与设施必须符合表1的要求[1]。
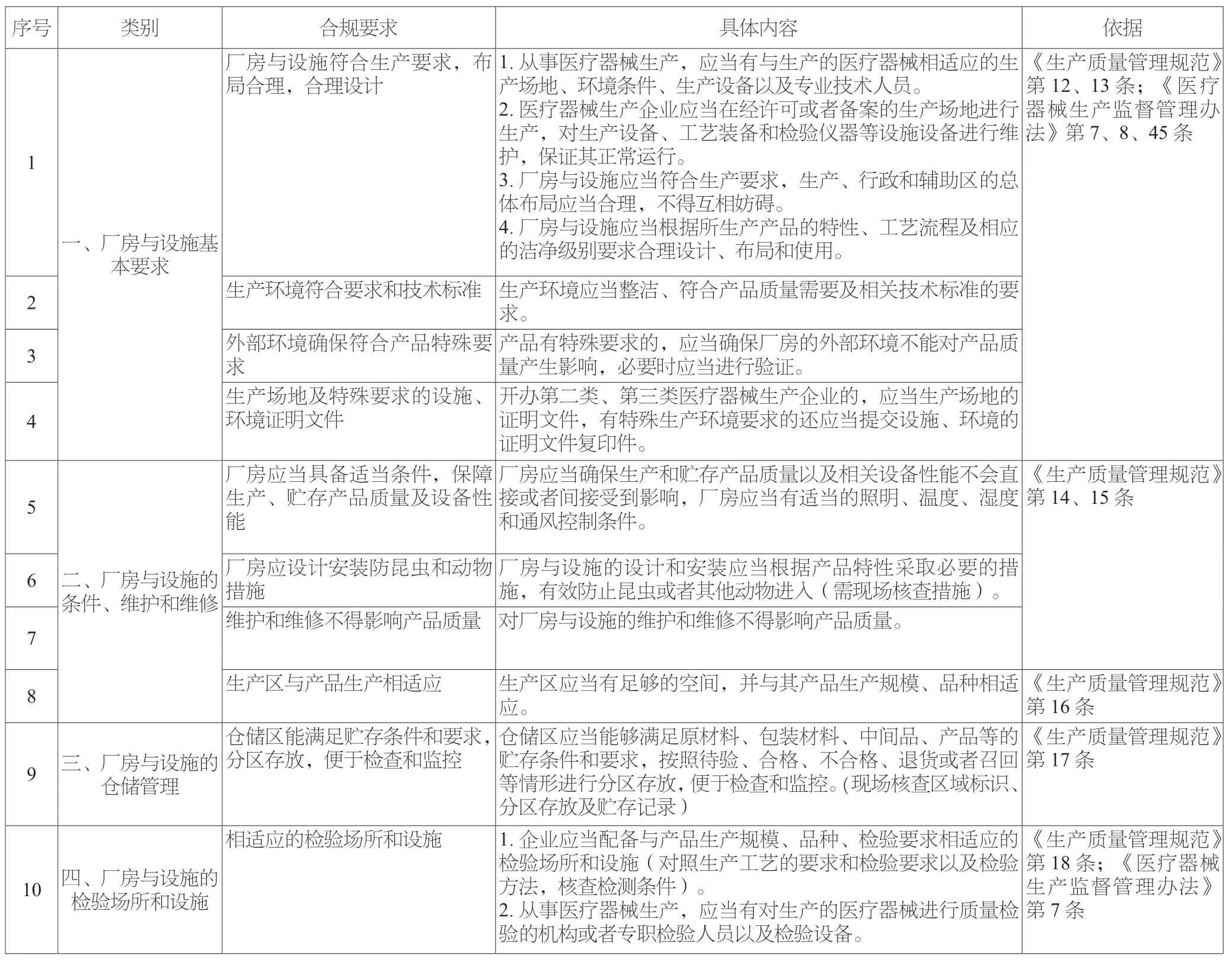
表1 医疗器械生产企业厂房与设施的要求
3 医疗器械生产企业厂房和设施常见合规风险
根据国家药监局公布的2019—2020年期间相关飞行检查的情况汇总、检查情况通报等,医疗器械生产企业厂房和设施的相关合规风险主要有以下六类情况[2]。
3.1 厂房与设施环境管理无法持续满足规范要求
常见问题主要是随着时间和条件变化,有的企业厂房与设施产生损坏、老化或者调整,不再符合质量管理规范的基本要求。例如,厂房与设施老化,墙面地面开裂、屋顶漏水,未能及时维修;厂区环境脏乱,路面不平整、杂草丛生,存在明显的扬尘、积水和蚊蝇不整洁现象等。
3.2 厂房条件无法保障生产、贮存的产品质量及设备性能
厂房缺乏功能设施或设施损坏、未正常运行管理,无法保障符合生产条件。常见为缺少生产或贮存环境所需要的温度、湿度、通风、避光、绝缘、防静电、防爆、消毒、清洗、烘干、防倒灌、防尘、缓冲设施以及测量设备等设施,或者相应设施损坏、管理不善导致无法开启、有效运转,厂房和设施出现必要功能缺失,无法满足管理规范要求。同样突出的问题是相关设施缺乏操作规范或者日常使用(常见为未按规定使用)、管理异常,导致实际环境条件不符合管理控制要求。例如,测温、测量湿度设施虽有,但现场核查或核实记录发现不符合环境要求;核查发现相关设施未开启或者运行记录不正常;生产用计算机无防水、防静电设施,外接口无物理病毒防护措施;原材料仓库没有挡鼠板、防蚊虫设施等。
3.3 仓储区不能满足贮存条件和要求,日常管理混乱
仓储区域是出现问题的重灾区,常见的突出问题有:仓储区无有效地控制管理制度措施;仓储区域面积或功能划分不符合要求;仓储容量不足,大量物品外放而无控制管理措施;物料的存放和领用不符合管理要求、未存放在要求的区域;未根据需要划分区域并进行明显标识,现场存放的物料、产品与标识的数量、品种不一致;仓储区堆放杂物或来源不明的物品,原料与产品混放、不合格品未能单独存放并标识;临时区域设置不合理或不符合要求;原料存放区域不具备贮存条件,缺乏必要的监控设施等。
3.4 厂房功能区域划分、布局和设计不能满足规范要求
例如,没有符合产品工艺流程要求的必要功能区域划分;没有相应的功能区域管理规范;功能区域设置(如缓冲区)及运行不符合要求;厂房整体区域日常管理未有效监管,存在管理或污染风险;功能区域设定与标识不一致(如研发室、高端定制室房间实际为加工区、打磨间);区域布置缺乏标识(生产区域地面标识不规范);物料区域间流通路线不符合洁净区管理要求;生产工艺流程在实验室完成;物料未在规定区域生产;生产场地变更未做验证等。
3.5 洁净区管理不符合管理规范要求
对于设置洁净区域的企业,对于洁净区域的管理是核查的一项重点,发现的问题也比较多。例如,洁净区维护规程不符合要求或未按规定执行,停用后未按要求进行必要的测试或验证;洁净车间有粉尘、污染物,不符合洁净要求;洁净区的检测数据、监测数据和维护记录异常,日常检测周期、项目不符合要求(如空气洁净度、悬浮粒子、微生物限度等监测);洁净区设计不合理,影响洁净要求实现;洁净区最大承载人数验证未进行,人员上限管理公示、提示等措施不规范;洁净区维护不到位或者不规范(如使用易挥发物保养设备、未采取有效措施防护和隔离);洁净区的水池、地漏等装置不具备空气阻断功能、回风口、进风口设置不合理,直排口直通普通环境,无防倒灌设施;洁净区隔离线、缓冲区的设定不符合要求;无菌及微生物实验室压力差设定、监测不符合要求;洁净车间工艺管道表面不光洁、不耐腐蚀,表面存在锈迹和灰尘,设施日常维护不到位,管道、墙体、电线和消防栓等未密封等。
3.6 空气净化系统、工艺用水系统和洁净压缩空气系统管理不规范
虽相关空气净化及用水系统与洁净区管理密切相关,但因相关问题突出,所以单独进行梳理:无相关系统的质量标准及检验规程、操作规程或管理规定;企业制度和规程与《空气净化系统清洁、维护保养检查记录》不一致;记录显示未按照操作规程操作;相关系统的验证、确认程序不全或不规范;设施的运行、维护记录不规范,未按照日常检测周期和检测项目进行管理,无法提供日常检测记录;空气净化系统停用后再次开启的验证记录和验证报告不规范;空调机组设施布置难以清洗、维护和维修;空调新风口设于空调设备间室内,未对进风窗建立相关清洁卫生操作规程;验证报告中的检测数据不在压缩空气系统验证方案中温湿度判定标准要求范围内等。
4 医疗器械生产企业厂房与设施合规管理要点
4.1 重视厂房与设施合规管理,严格执行相关规范,保障企业生产质量管理体系中相关内容得到有效执行
医疗器械行业需要企业生产经营持续性满足相关规范和质量管理体系的要求,对于因为损坏或者老化的厂房、设施应定期检查和维护,以保障能够满足规范要求,尤其是对于厂区环境卫生、厂房、道路和设施的维护、厂房的维护等要更加重视,这些在检查中可以非常直观观察到的问题经常会被列为缺陷项。
4.2 加强厂房日常管理,确保条件能保障生产、贮存产品的质量及设备性能
从飞行检查通报梳理结果来看,如果因生产工艺或产品本身特点的要求,需要厂房具备温度、湿度、通风等特定条件的,就必须做到配置相关设施以满足厂房的功能要求,而且要做好日常管理以确保相关设施可以正常运转,且运转能保障厂房的状态持续处于达标状态。这也需要从管理、操作规范的制定和实施、日常监管的有效运行等方面进行不断完善,同时相关设施的运行和维护记录,及时关注异常情况并进行有效处置。通报案例中出现的检查人员在日常运行记录中发现记录的温湿度环境不符合控制要求却未被企业发现和重视的问题就可反映出相关厂房与设施的运行条件是失控的。要注意厂房与设施的设计和安装应当根据产品特性采取防止昆虫或者其他动物进入的措施。
4.3 生产、仓储和检验的功能区域划分、布局和设计应满足规范要求并标识规范、有效管理
具备符合产品工艺流程要求的必要功能区域划分,具备有效的管理规程和措施,且标识清楚设置和运行均符合要求,便于检查和监控;功能面积应符合生产工艺、检验及贮存功能要求,不应出现标识与现场不一致或功能区混用的情况。在设计和运行物料区域间流通路线时必须关注洁净区管理要求;生产场地的启动、变更未严格按照规程进行验证和管理,并保留相关的记录;仓储区域必须注意物料、产品存放区域的明确划分,存储记录完整、清楚,可以如实反映产品、物料的贮存情况;所有物品来源清楚,绝对不允许混合堆放或者标识不清、标示错误(包括品种、数量和类型)的情况,尤其关注不合格品不能产生可能被认为无法识别或可能同合格品混同的情况;临时区域的管理必须有完整的规范和管理措施,很多临时仓储或操作区域都因标识不清、功能欠缺或管理不规范而被认定为存在缺陷,所以要予以特别的关注。
4.4 洁净区域管理问题高发,需要予以特别关注
洁净区设计合理足以实现相应洁净要求。对于洁净区的功能设施的管理必须做到功能设施齐全且正常运转,严格按照规程操作和维护;系统设施的日常运行、维护保养和相关日常检测的记录完整、规范。
根据规范和操作规程所要求的监测和定期检验项目应依规按照周期和项目进行,保留完整的操作和结果记录,关注数据是否满足区域功能管理要求;出现的异常和问题及时解决并保留相关记录。
做好日常管理工作,洁净区域的环境、无物料管理。做到干净、整洁,日常区域内设备管理维护注意不产生影响洁净区因素,不允许出现积水、污染物和粉尘等问题。另外,要注意洁净区最大承载人数验证和日常人员管理的措施应当规范。
有效做好洁净区域和外界的隔断。很多企业都存在洁净区的水池、地漏等装置不具备空气阻断功能、风口设置缺陷、压力差设定和检测不符合要求或设备不能工作等问题;洁净区隔离线、缓冲区的设定不符合要求也较为常见。同时,洁净车间相关工艺管墙体、电线和消防栓等都要按照要求进行处理并定期关注是否出现损坏或者脱落,保证设施日常维护到位。
4.5 高度重视空气净化、工艺用水和洁净压缩空气三大系统管理工作
要严格执行相关系统的操作规程,做到各系统及相关设备的操作和检验规程、管理制度齐全并依规操作,相关系统的验证、确认程序应完整和规范。
系统设施的日常运行、维护保养和相关日常检测的记录完整、规范,尤其特别要注意相关记录所显示的工作内容符合法规、管理制度和规程要求;也要对记录的信息内容是否可以反映系统的正常、有效运转予以特别的关注。此外,按照日常的检测周期和项目进行有效管理。注意在相关系统停用后重启时根据要求进行验证并做好验证报告。
多家企业因空调、新风机组的风口布置不当、设施位置难以清洗、操作和维修而被认定存在缺陷,因此在相关设施的布局和设置上要关注,不能因仅关注设备运行及记录规范完整,而忽略存在的一些功能或效果上实质性缺陷。
5 结语
医疗器械企业在厂房与设施合规方面应确保管理体系及规程系统和完整,且相关系统日常的运行、管理和维护严格按照规范进行、持续性符合法规要求。在厂房与设施的环境保持、厂房与设施功能的规划与实现、仓储区和洁净区的管理以及空气净化、工艺用水和压缩空气等设施系统的验证、确认和日常维护方面都应当实现有效管控,才能保证厂房与设施符合法规和质量管理体系的监管要求。
