光学分子影像技术在药物疗效评估和乳腺癌外科手术导航中的应用进展
2021-04-15林琳玲何悦洋杜智铖张国君
陈 敏,林琳玲,何悦洋,杜智铖,张国君
(厦门大学医学中心,厦门大学附属翔安医院,厦门市内分泌肿瘤精准诊治重点实验室,福建 厦门 361111)
乳腺癌是全球最常见的恶性肿瘤之一,发病率居女性恶性肿瘤的第一位,死亡率居第二位[1].我国是世界乳腺癌发病率最高的国家,2015年的统计数据显示,年新发病例数和年死亡人数分别约占全世界的12.2%和9.6%,发病人数增长快且趋于年轻化[2].
乳腺癌的治疗采用手术为主的综合治疗策略,手术方式也逐渐从最大可耐受性手术向最小有效性手术演变.对于早期乳腺癌,保乳术和/或保腋窝是标准的手术方式[3].保乳术成功的关键在于术中完整切除病灶,保腋窝的前提是前哨淋巴结无转移,而现阶段对于术中肿瘤边界的判定以及前哨淋巴结的识别主要凭借术者的经验、眼看、手摸等,不能从微观层面判断是否存在肿瘤残留,术后切缘阳性需要再次手术的患者高达20%~55%[4-5],增加了患者的心理负担及二次手术感染、术后外观不满意等风险.因此,精准地评估切缘状态对于保乳术患者的预后至关重要.术中病理、超声、微计算机断层扫描(micro-CT)、正电子发射断层扫描(PET)等技术也相继尝试应用于术中肿瘤边界评估,可在一定程度上降低手术切缘阳性率[6],但目前仍没有一种理想的手段用于术中精准评估切缘.光学分子影像可实时动态地监测分子变化,具有高灵敏度、高时空分辨率等优点,近年来已广泛应用于生物医学领域[7].新的光学分子影像技术可以填补术前影像学检查和术中手术切除之间的诊断空白,引导外科医生在术中精准切除肿瘤,进而提高手术效果、改善患者预后[8].
对于中晚期乳腺癌患者,全身系统治疗对患者生存十分重要,尽早、准确地评价疗效是改善预后的关键.目前临床上普遍使用的是RECIST1.1的评价标准,借助X线、CT、磁共振成像(MRI)等传统影像技术,通过测量病灶最大直径的变化来判断疗效[9];但这些传统影像技术仅能提供解剖结构信息,难以客观反映药物治疗的真实反应,存在评估滞后的问题.在肿瘤大小发生变化前,利用光学分子影像技术可在体内监测上述变化,为尽早、准确地判定药物疗效提供了可能[10].
本团队近年来研发了靶向细胞周期的一系列光学报告系统,不仅为肿瘤的早期诊断奠定了基础,而且提供了药物疗效评估的手段;更重要的是,还将近红外荧光分子示踪技术应用于乳腺癌的外科手术导航.本文将讨论光学分子影像技术在医学领域的研究及临床应用现状,并结合本团队在该领域的最新研究成果,对其在乳腺癌诊断、药物疗效评估、外科手术导航中的应用进展进行综述.
1 光学分子影像技术和光学分子探针
1.1 生物发光成像
生物发光成像是指在体内表达荧光素酶融合报告基因,利用其产生的荧光素酶与荧光底物的生化反应把化学能转化为光能,从而产生荧光信号[11].生物发光成像灵敏度高,即使只有几千个肿瘤细胞,也能够通过生物发光成像在体内精确探测[12],并且信背比高,有着良好的应用前景[13].
1.2 荧光成像
1.2.1 荧光成像光区及发光材料
根据光的波长不同,可分为可见光和不可见光,可见光波长在400~700 nm之间,近红外光(near-infrared,NIR)波长在700~3 000 nm之间,其中近红外一区(NIR-Ⅰ)波长为700~900 nm,近红外二区(NIR-Ⅱ)波长为1 000~1 700 nm.组织对可见光的吸收和散射较强,并且存在较强的自发荧光,信背比不高,成像效果差[14-15];相比之下,组织在NIR波段自发荧光弱,并且对NIR的散射和吸收较弱,成像的空间分辨率和组织穿透深度更佳[16-17],信背比更高[18-19],更适用于体外和体内的成像,是目前荧光成像的研究热点(表1).目前已开发的NIR荧光探针包括小分子有机染料、碳纳米管、量子点和镧系稀土纳米材料等,其中碳纳米管和量子点由于毒性作用而临床转化受限.
1) NIR-Ⅰ荧光成像
临床上最常用的NIR-Ⅰ染料是ICG[48],其激发和发射波长分别为780和805 nm.ICG进入人体后被肝细胞摄取,经胆道入肠,随粪便排出体外,常被用于人体腔道的成像,包括胆道[49]、淋巴[50]、输尿管[51]和眼底血管[52]等,在肿瘤显像、淋巴结定位及外科手术导航中也有广泛应用[53-54].此外,ICG还可与靶向载体结合构成光学分子探针,如ICG结合贝伐单抗(Bevacizumab-ICG)靶向VEGF,可在内窥镜系统中诊断结直肠癌[37].菁染料IRDye800CW(激发和发射波长分别为774和789 nm)[55]易于化学修饰,可与抗体、多肽等靶向载体结合,如:HER2抗体荧光分子探针,可对人乳腺肿瘤异种移植小鼠进行光学成像[27];西妥昔单抗荧光分子探针,用于评估头颈癌患者颈部淋巴结转移情况及手术导航[28-29].

表1 NIR荧光成像技术在肿瘤诊疗领域的临床转化研究及临床应用Tab.1 Clinical translational research and clinical application of NIR fluorescence imaging technology in tumor diagnosis and treatment
除ICG和IRDye800CW外, 其他菁染料如IR775、IR780、IR783、IR797、IR806、IR808、IR820、IR825和Cypate等均可用于癌症光学成像;NIR-Ⅰ染料还有黄嘌呤、卟啉、方脑、酞菁、硼二吡咯甲烷、两性离子染料和聚集诱导发光(aggregation-induced emission,AIE)材料,可用于癌症的诊断[56].
NIR-Ⅰ无机染料在肿瘤成像、肿瘤药物输送和光热治疗方面具有潜在的应用前景.如:可生物降解的多孔硅纳米荧光探针,可用于人乳腺癌移植瘤的荧光成像[36];谷胱甘肽包裹金纳米荧光探针,在小鼠体内可快速从血液通过肾脏排泄[57].最新报道的K3ZrF7:Yb/Er稀土荧光探针对乳腺癌成像效果良好,可在活体内生物降解为无毒的小分子排出[35].上述NIR-Ⅰ纳米荧光探针均具有临床转化的可能.
2) NIR-Ⅱ荧光成像
相比于NIR-Ⅰ,NIR-Ⅱ具有“组织透明窗口”的独特性,背景信号和自发荧光更弱,对光的散射和吸收也更弱,成像的空间分辨率和组织穿透深度进一步提高,因而备受关注[16-17].
有机NIR-Ⅱ染料由于其组织相容性好,有潜在的临床转化和应用前景.研究发现ICG和IRDye800CW的发射波长可延伸到NIR-Ⅱ[58].此外,新研制的有机染料CH1055代谢快,毒性小,在小鼠脑血管、淋巴系统和肿瘤成像方面均明显优于ICG,在NIR-Ⅱ成像分辨率、信背比及成像深度等方面都有很大的提升[38].进一步将CH1055官能团上的羧酸改变为磺酸合成的有机染料CH-4T,水溶性好,量子产率高,可在成像时大幅降低染料剂量[59].
此外,具有NIR-Ⅱ发光的新型无机荧光染料也不断被报道.其中,稀土纳米材料因其易偶联、高信背比、低光漂白、低细胞光损害的特性,在手术导航、造影成像和肿瘤光敏治疗等领域被广泛研究[60].Wang等[41]使用肿瘤靶向肽修饰的NaGdF4:5%Nd@NaGdF4稀土荧光探针,显示出了良好的光稳定性和组织穿透深度(8 mm),可用于卵巢转移癌灶的示踪及手术导航.小分子量的NIR-Ⅱ镧系稀土配合物Nd-DOTA代谢快,其NIR-Ⅱ荧光成像可对直径≤1 mm的卵巢癌转移癌灶进行示踪并引导术中精准切除[42].
相比于NIR-Ⅱa(1 000~1 300 nm),波长范围为1 500~1 700 nm的NIR-Ⅱb荧光成像具有更高的信背比与更大的穿透深度,使NIR-Ⅱb荧光材料成为研究热点.如利用激光气化法合成半导体单壁碳纳米管,对小鼠乳腺癌组织及其后肢血管进行成像时,相较于其NIR-Ⅰ和NIR-Ⅱa成像,NIR-Ⅱb成像效果更佳[46];由硫化铅/硫化镉核壳结构合成的量子点可产生1 600 nm的发射光,活体示踪肿瘤的分辨率高,还可实现肿瘤血管的3D成像[47];偶联上CD8抗体的硫化铅量子点,其NIR-Ⅱb成像可活体示踪肿瘤部位的细胞毒性T细胞,用于评估肿瘤免疫治疗的效果[44];稀土纳米颗粒NaLnF4:Gd/Yb/Er掺杂Ce3+后,其NIR-Ⅱb荧光可活体示踪小肿瘤和转移瘤,还可对脑血管和肿瘤血管进行无创成像[43];另外,在稀土纳米颗粒(NaYbF4:Er,Ce@NaYF4)中掺杂Zn可使NIR-Ⅱb荧光更强,将其与PD-L1抗体偶联后可对肿瘤免疫治疗过程中PD-L1的变化进行动态监测[44].上述纳米材料表现出良好的NIR-Ⅱb发光性能,如能提高其生物安全性,将有广阔的临床应用前景.
1.2.2 光学分子探针
1) 非靶向光学分子探针
与正常组织相比,实体瘤组织中血管丰富,血管壁间隙较宽,结构完整性差,淋巴回流缺失,对大分子类物质和纳米颗粒的通透性高,导致大分子和纳米颗粒滞留在肿瘤组织中,这种现象被称作实体瘤组织的高通透长滞留(enhanced permeability and retention,EPR)效应[61].EPR效应的强弱与实体瘤的血管状态有关[62-63].荧光染料可直接通过EPR效应累积在肿瘤部位,也可包裹在非靶向性药物载体中(如白蛋白[64]、红细胞膜[65]和脂质体及病毒蛋白笼[66]),增强EPR效应,延长血液循环时间.
2) 靶向光学分子探针
相比于被动聚集,利用肿瘤特异性分子修饰荧光材料的靶向性更强,可明显提高肿瘤部位与瘤周正常组织的信背比,实现高特异性肿瘤成像.靶向肿瘤的抗体类、多肽类和核酸适配体受到广泛关注,这些探针在临床癌症诊断和治疗中具有潜在的应用价值.
抗体与受体之间具有高度的特异性和亲和力,将荧光材料与抗体结合可实现靶向成像,用于肿瘤诊疗和手术导航[67].如:靶向癌胚抗原(carcinoembryonic antigen,CEA)的AlexaFluor 488-conjugated anti-CEA单抗荧光探针,能够可视化大肠癌和胰腺癌裸鼠模型中的原发和转移癌灶[68];靶向MUC1的聚乙二醇(PEG)化脂质体-ICG-hCTM01单抗荧光探针,可用于小鼠乳腺肿瘤成像[23].
相比于其他偶联物,多肽对靶点亲和力高,特异性强且毒性小,具有良好的临床应用前景[69].其中,天冬酰胺-甘氨酸-精氨酸肽(NGR)和精氨酸-甘氨酸-天冬酰胺肽(RGD)被广泛用于制备肿瘤靶向探针.如:NGR修饰的PEG化量子点可用于神经胶质瘤和肿瘤脉管系统的荧光成像[70];化学交联RGD的NIR-Ⅱ纳米探针(APP-Ag2S-RGD)可用于切除直径约0.2 mm的微小肿瘤转移灶[45].

图1 一系列用于活体可视化细胞周期不同时相的基于生物发光报告基因的光学分子影像技术Fig.1 A series of optical molecular imaging techniques based on bioluminescent reporter genes to visualize different phases of the cell cycle
核酸适配体通常由20~60个核苷酸组成.适配体对靶标的识别方式和抗体对抗原的识别类似,解离常数(Kd)能达到皮摩尔至纳摩尔级,被称为“化学抗体”,分子量小且免疫原性低[71].如靶向MUC1的核酸适配体-镧系元素铽荧光传感器[40],可以简便、敏感地对乳腺癌MCF-7细胞进行检测,表现出极高的灵敏度(检测限低至70个细胞),且传感器的合成过程简单,光学性能稳定,生物相容性良好.
2 可视化光学分子影像平台用于癌症药物的疗效评估
2.1 可视化监测细胞周期
肿瘤是一种细胞周期相关性疾病,因细胞周期的异常激活引起细胞的失控性增殖[72].细胞周期的正常运转依赖于细胞周期蛋白(Cyclins)的时相性表达及细胞周期蛋白依赖性激酶(Cyclin dependent kinases,CDKs)的活化[73].2008年日本理化研究所的Miyawaki团队首先用红色和绿色荧光蛋白分别标记细胞周期特异性蛋白Cdt1和Geminin,研发出FUCCI细胞周期传感器,通过红绿两色荧光的改变显示G1期与S/G2/M期[74].2016年,Lin团队在FUCCI系统的基础上又添加了2个报告因子,使该传感器可以把G1期到M期4个不同时相分别通过青、绿、橙、紫4种颜色呈现出来,并能够监测不同时相转变的过程[75].
本团队2004年应用p27融合蛋白技术和生物发光成像手段,研制出CDK2的生物发光报告系统,实现在活体水平监测CDK2的活性和细胞周期的改变,并用于细胞周期特异性抗癌药物的筛选[76];此后,又研发了一系列靶向Cyclins/CDKs的生物荧光报告质粒,在细胞和小动物水平上实现了细胞周期不同时相的可视化,如CYCA-Luc[77]可视化S期,CyclinB-Luc[78]可视化G2/M期;在此基础上,应用这些报告系统在细胞和小动物水平对常用的细胞周期特异抗肿瘤药物,如黄吡哆醇(flavopiridol)、紫杉醇(paclitaxel)、多西紫杉醇(docetaxel)、羟基喜树碱(HCPT)和5-氟尿嘧啶(5-Fu)进行疗效评价[76-77,79-80](图1).这些生物发光报告系统与高内涵成像系统结合,可对活细胞的细胞周期实现高效精确的测量,用于高通量抗癌药物筛选[79,81-82].
2.2 可视化监测细胞凋亡
大多数化疗药物是通过诱导细胞凋亡导致肿瘤细胞的死亡[83],因此可视化监测细胞凋亡可用来评估抗肿瘤药物疗效.在细胞凋亡过程中,半胱氨酸蛋白酶(caspase)家族是关键的生物标志物[83].基于天冬氨酸-谷氨酸-缬氨酸-天冬氨酸(DEVD)多肽序列可以被caspase-3/7识别和切割,Ozawa团队[84-85]开发出一种基因编码的环状萤火虫荧光素酶pcFluc-DEVD,当细胞凋亡时,caspase-3识别并切割DEVD,使其恢复荧光素酶活性,在细胞或活体动物中均可检测到这种生物发光.在转染了pcFluc-DEVD生物发光报告质粒的人头颈部鳞状细胞癌细胞和小鼠乳腺癌4T1细胞中,可视化不同浓度阿霉素诱导转染细胞发生凋亡的过程,发现细胞凋亡与阿霉素杀伤效果呈时间与剂量依赖性[86].
膜联蛋白V(Annexin V)可特异性结合凋亡细胞的磷脂酰丝氨酸(PS),对凋亡细胞亲和力高,且免疫原性和毒性低,广泛应用于体内细胞凋亡的检测[87].Shah等[30]使用NIR700-Annexin V探针对曲妥珠单抗治疗的HER2阳性乳腺癌模型鼠进行成像,可实时动态监测曲妥珠单抗治疗引发的乳腺癌细胞凋亡和肿瘤消退.Leng等[31]利用NIR荧光探针Annexin Vivo 750来检测人源性骨髓间充质干细胞治疗中的乳腺癌细胞凋亡,在乳腺癌移植瘤中实时动态监测骨髓间充质干细胞的抑瘤效果.
3 光学分子影像技术在乳腺癌外科手术导航中的应用
早在2011年,van Dam等[88]合成了可见光染料FITC标记叶酸的分子探针,首次将光学靶向分子探针应用到外科手术中,开展术中探测卵巢癌及其腹膜转移灶的临床试验,使肿瘤术中诊疗精准度提升至分子水平.从此开启了荧光分子影像技术在肿瘤外科手术导航中的应用[56].
3.1 示踪乳腺癌前哨淋巴结
传统腋窝淋巴结清扫术(axillary lymph node dissection,ALND)会大范围切除腋窝淋巴结,易导致上肢淋巴水肿、功能障碍和感觉丧失等并发症,降低了患者的术后生活质量.前哨淋巴结活检术(sentinel lymph node biopsy,SLNB)作为腋窝分期的重要手段,通过NSABP-B32[89]、ACOSOG Z0011[90]和IBCSG 23-01[91]等大量临床试验证实,目前已经成为临床腋窝淋巴结阴性早期乳腺癌的标准手术方式,取代了常规的ALND,避免ALND所致并发症,改善了乳腺癌患者的生活质量.鉴于此,临床上通过SLNB来判断SLN是否受肿瘤影响,若SLN阴性,则可避免不必要的淋巴结切除,显著提高了患者的术后生存质量[92],对乳腺癌手术方式的改革具有重要意义.目前临床上用于SLNB的染料主要有美蓝染料、放射性胶体、ICG和纳米碳.其中,ICG信背比更高[93-94],价格便宜且毒性低[95],更具优势.
本团队利用ICG指导乳腺癌术中SLNB(图2),检出率可达99%[20-22].此外,发现ICG示踪上臂回流至腋窝的淋巴管和淋巴结的准确率(87.2%)显著高于美蓝组(52.5%),提示ICG也可用于腋窝淋巴系统逆向造影[96].Valente等[97]也将ICG成功用于乳腺癌患者的SLN识别,可达到与99mTc类似的效果,证实了其有效性.Schaafsma等[98]通过ICG和99mTc 整合制备ICG-99mTc-纳米胶体,可精确识别乳腺癌患者的SLN,且淋巴管清晰可见.
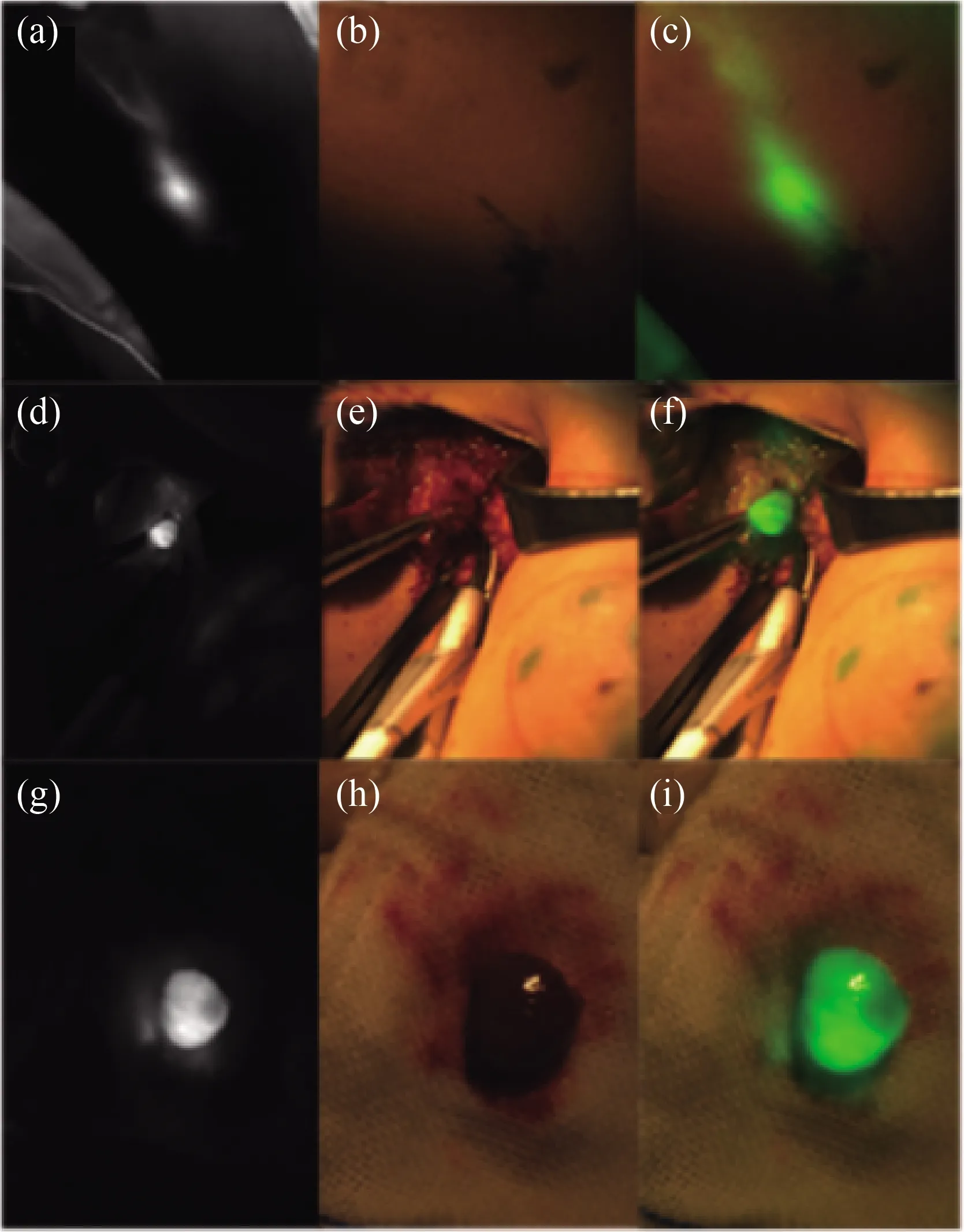
(a)~(c)术前ICG示踪腋窝SLN;(d)~(f)术中ICG 示踪腋窝SLN;(g)~(i)术后离体SLN荧光成像.图2 ICG引导的人体乳腺癌腋窝SLN术中示踪及切除[21]Fig.2 ICG-guided intraoperative detection and resection of the SLN in humans[21]
光学靶向分子探针也逐渐应用于乳腺癌淋巴结识别.如:乳腺珠蛋白A抗体荧光分子探针(MamAb-680)可示踪乳腺癌荷瘤小鼠淋巴结中的癌转移[99];CD206抗体-Dylight755荧光分子探针靶向示踪肿瘤相关性巨噬细胞,可在乳腺癌小鼠模型中检测到SLN的肿瘤转移[32];而有机染料XB1034结合西妥昔单抗制备的NIR-Ⅱ荧光分子探针,可在小鼠中示踪淋巴结的肿瘤转移,并在术中引导淋巴结的切除[39].
3.2 保乳术中肿瘤边缘界定
乳腺癌保乳术是指切除原发肿瘤和邻近的乳腺组织,术后辅以放疗.经过NSABP-B06[100]、Milan trial[101]和EORTC[102]等多项大型前瞻性临床试验证实,保乳术辅以放疗在局部复发率和总体生存率方面,与改良根治术的疗效相比并无统计学差异.这些研究结果验证了保乳术的安全性,使其被逐渐推广,现已成为早期乳腺癌患者的首选术式.保乳术缩小手术范围减少了创伤,但增加了病灶残留和二次手术的风险;而光学分子影像技术可以“点亮”肿瘤组织,引导外科医生精准切除肿瘤并保护正常组织.
在一项将ICG用于保乳手术导航的临床研究中,NIR成像显著提高了阳性边缘检出率,但50%(6/12) 的患者在肿瘤切除后瘤床存在异常荧光信号,提示肿瘤残留;而术后病理检测证实切缘阴性,究其原因可能是探针缺乏靶标,滞留于周围正常组织而产生假阳性[103].因此,使用肿瘤特异性靶向探针开展手术导航至关重要.
荷兰van Dam团队在2017年将靶向VEGF的荧光探针Bevacizumab-IRDye800CW用于乳腺癌保乳术切缘界定的Ⅰ期临床试验[24]:对20例原发性浸润性乳腺癌患者的保乳术切缘残留肿瘤组织进行靶向性“点亮”和精准示踪,其结果与病理诊断相符且无一例发生不良反应(图3).2018年,张国君团队与van Dam教授合作开展了此探针的Ⅱ期临床试验,对使用剂量进行摸索,从微观和宏观的水平对探针进行全面评估,结果显示相比于传统方式,此探针的应用将肿瘤边界的术中检出率提高到88%,为后期Bevacizumab-IRDye800CW推向临床奠定了基础[26].此外,van Dam团队[25]在Bevacizumab-IRDye800CW引导的保乳术中建立了fSTREAM的分析方法,综合处理荧光、颜色和组织学信息,设定区分肿瘤组织与正常组织的阈值,使术中对肿瘤边界的判定更加客观.
Whitley等[33]利用组织蛋白酶底物肽将Cy5荧光团与猝灭剂QSY21连接,构建了酶响应性LUM015光学智能分子探针,并于2016年开展了首个光学智能探针用于乳腺癌手术切缘评估的Ⅰ期临床试验.2018年Smith等[34]证明用LUM015智能探针开展手术导航的平均信背比可达到4.7,切缘判定与术后病理检测结果一致.
多个目前处于动物实验阶段的用于手术切缘评估的分子探针也表现出一定的临床转化潜力.如:连接环肽cRGD的生物响应性NIR-AZAs探针,有较高的信背比和较短的体内清除时间[104];利用anti-EGFR-IRDye800CW的荧光寿命成像,可以在人类乳腺癌的临床前模型中,提供比基于强度的连续波荧光成像更显著的肿瘤对比度[105];抗B7-H3抗体[106]、透明质酸[107]连接ICG构成的探针也能靶向肿瘤组织,用于保乳术导航.
4 总结与展望

(a)~(c)对切除的肿块进行体外光学成像,可在阳性边缘中检测到贝伐单抗-IRDye800CW示踪剂,其中(a)为白光,(b)为荧光,(c)为假彩色覆盖;(d)~(f)面包切片;(g)~(i)石蜡切片;(j)~(l)4 μm石蜡切片,其中(j)为苏木精-伊红染色,(k)为荧光平板 扫描,(l)为(j)和(k)图像重叠(*皮肤缝合,**卫星肿瘤病灶;红/白/黑色虚线:肿瘤轮廓;白/黑色箭头:阳性肿瘤边缘).图3 光学分子影像用于肿瘤边缘界定(修改自文献[24])Fig.3 Optical molecnlar imaging of tumor margin identification (modified from Ref.[24])
现有的光学造影剂和光学分子影像系统凭借其高分辨率、实时可视化等优势,广泛应用于临床和临床前研究.目前已批准应用于临床的荧光分子染料仅有ICG,IRD800CW已经被批准进行临床试验,未来更多的近红外荧光分子探针有望用于临床,如可在活体实现生物降解的稀土发光材料[35].与此同时,光学分子影像技术还有许多可改进的空间:首先,光学影像穿透深度相对较低,采用波长更长的荧光染料(如NIR-Ⅱ荧光染料)更适合于活体组织成像[38].光声成像与光学分子影像类似,是一种无创、无辐射的影像技术;但相比之下,光声成像具有更高的对比度、空间分辨率和更大的穿透深度,并且对组织特征敏感,可以呈现良好的解剖和生理学特征[108].目前,基于内源性对比剂黑色素的光声成像可用于黑色素瘤肝脏微转移的早期诊断,并指导术中肿瘤切除[109].相信不久的将来,光声成像技术在乳腺癌检测、外科导航以及药物疗效评估中也将发挥更大的作用.其次,光学分子影像融合CT、MRI、PET以及光声成像等技术,通过多模态间的优势互补,能大幅度提高实时手术中导航与疗效监测的精准度.再者,由于肿瘤存在异质性,单靶点分子探针对肿瘤组织的整体靶向性不足,所以开发具有多靶点、亲和力强的分子探针也是未来发展的方向.此外,采用能够识别肿瘤组织和正常组织的多光谱同时成像,辅以多参数分析方法和人工智能技术,光学分子影像技术将有望为乳腺癌患者提供个体化、精准化的诊疗方案,提高生存率和生活质量.
致谢:感谢厦门大学医学院2019级生理学博士张永渠、汕头大学医学院2017级肿瘤学博士王尊,以及厦门大学医学院2020级肿瘤学研究生罗忠、明梓何、陈洪宇、党永颖的大力协助.
