免疫亲和层析净化高效液相色谱法测小麦中呕吐毒素不确定度评定*
2021-04-15兰雪萍廖子龙
兰雪萍 廖子龙 杨 娟
(中储粮成都储藏研究院有限公司 610091)
呕吐毒素(DON),即脱氧雪腐镰刀菌烯醇,是由小麦赤霉病菌禾谷镰刀菌复合群(Fusariumgraminearumspecies complex)产生的单端孢霉烯族毒素[1]。饲料中含有一定剂量脱氧雪腐镰刀菌烯醇可引起猪呕吐、拒食、腹泻、出血甚至死亡,顾得名呕吐毒素,属三级致癌物[2~3]。同样,粮食中的呕吐毒素严重危害人类健康,是收储和加工环节重点关注的食品安全指标[4~6]。有研究表明,生霉粒和霉变粒含量与真菌毒素的含量不存在相关性,不能通过感官检验生霉和霉变情况来判断真菌毒素的含量,要控制真菌毒素的含量需用仪器进行定量检测[7]。
免疫亲和层析净化高效液相色谱法具有操作简单、检测灵敏度较高的优点,应用较广,是GB 5009.111-2016《食品安全国家标准 食品中脱氧雪腐镰刀菌烯醇及其乙酰化衍生物的测定》中的第二法[8~10]。不确定度是表征被测量真值与实测值差值的量,能够表达测量结果的可信度,并对引入不确定度的各操作步骤进行评估分析,给出减少不确定度的建议[11~12]。本文以小麦样品的检测为例,建立了评估免疫亲和层析净化高效液相色谱法测小麦中呕吐毒素不确定度的方法,评估了各步骤对总不确定度的影响程度,为提高检测质量提供了依据。
1 材料与方法
1.1 材料与仪器
主要仪器有高效液相色谱仪(Agilent Technologies 1260 Infinity)、紫外检测器(vwd)、DONStar脱氧雪腐镰刀菌烯醇免疫亲和层析柱;主要试剂为聚乙二醇(PEG8000,分析纯)、甲醇(色谱纯)、脱氧雪腐镰刀菌烯醇标准溶液(ROMER LABS®)。
1.2 检测方法
前处理:称取20 g(准确到0.01 g)磨碎的试样于100 mL具塞三角瓶中加入5 g聚乙二醇,加水100 mL,混匀,振荡20 min,离心。免疫亲和柱中原油液体流尽,用注射器将2 mL提取液以1滴/s的速度通过免疫亲和柱。用5 mL PBS缓冲盐溶液和5 mL水先后淋洗免疫亲和柱,抽干。将2 mL甲醇以1滴/s的速度洗脱亲和柱,收集全部洗脱液,滤膜过滤入进样瓶。
标液配制:购买脱氧雪腐镰刀菌烯醇标准溶液(ROMER LABS®),浓度标示值为100.0 μg/mL,U=0.8 μg/mL。稀释100倍作为标准工作溶液,浓度为1000 ng/mL。
色谱条件:色谱柱DIKMA Diamonsil C18 5 μm 250×4.6 mm,流动相为甲醇水溶液(20∶80),流速为0.8 mL/min,检测波长为218 nm,进样量为50 μL,柱温为35℃。
试样中脱氧雪腐镰刀菌烯醇的含量的计算公式为:
其中:X为DON含量,单位为μg/kg;ρ样为试液中呕吐毒素的浓度,单位为ng/mL;V为试样提取液体积,单位mL;m为称样质量,单位为g;f为样液稀释因子,1000为单位换算系数。
2 识别不确定度来源
按照计算公式和操作步骤逐级分析不确定度的来源,绘制因果图(图1),使不确定度分量清晰,逐级评定过程逻辑清楚[12]。
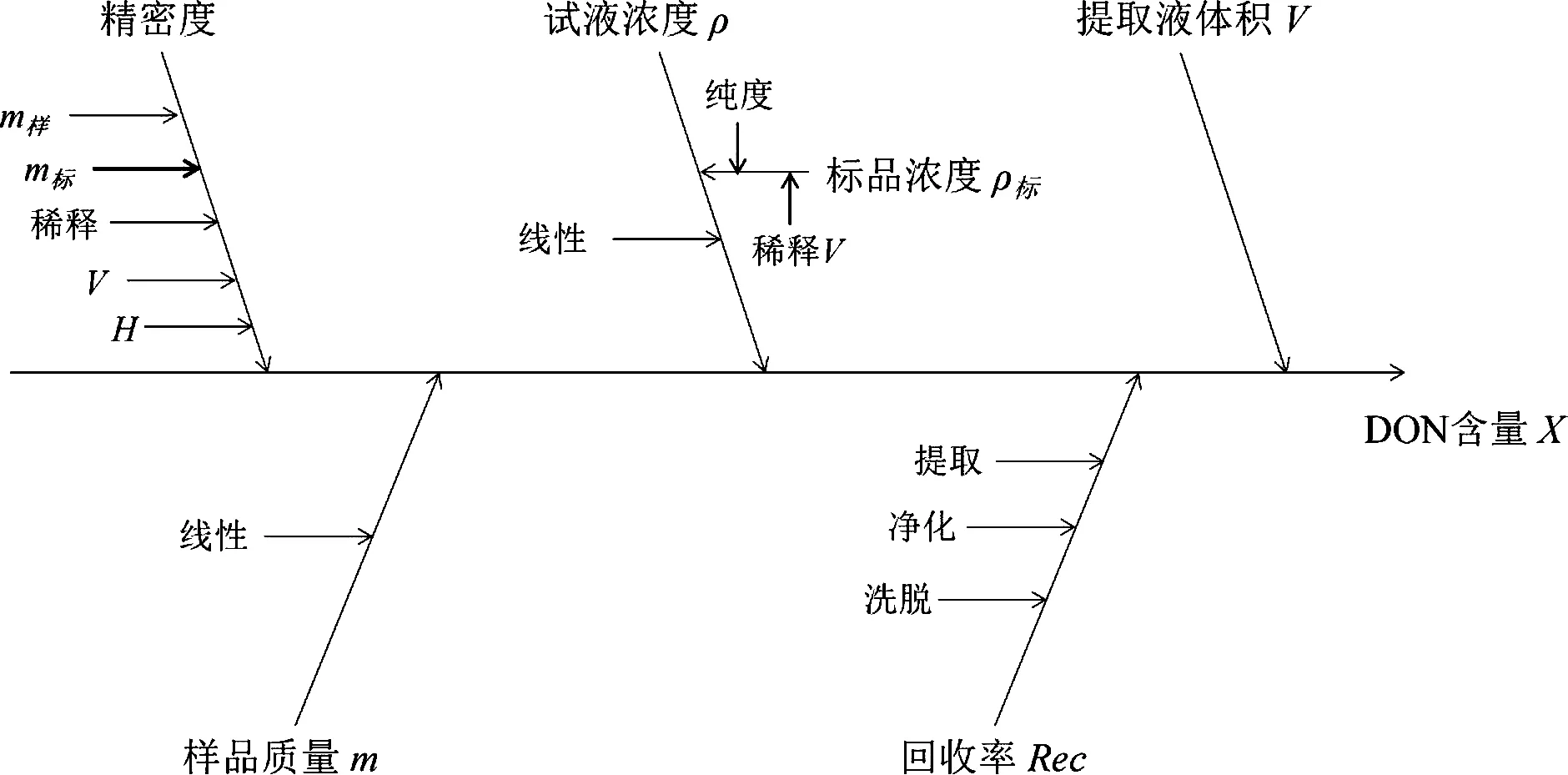
图1 不确定度因果图
真菌毒素是产毒真菌在一定环境下产生的毒性次级代谢产物,产生过程具有较强的随机性和不确定性,且真菌毒素看不见摸不着,具有高度隐蔽性,在谷物及制品中的分布不均一[13]。一般认为,真菌毒素分析检测总误差由三项组成:扦样误差、制样误差和分析误差,由于前二者的讨论涉及更广的领域,本文仅针对分析误差进行讨论。
为使计算输入数据的关系和覆盖面更加明确,增加精密度分支以代表中间精密度研究所覆盖的所有影响因子,在其他分量的分析中不再考虑重复性影响。样品提取、净化和洗脱过程涉及目标物质的多次转移,将回收率单列一项,以考虑转移过程引入的不确定度。提取液经同体积净化和洗脱,样液稀释因子为1,由此产生的不确定度也应归入回收率的不确定度分量考虑。
采用单点标定法计算试液浓度,相较于标准曲线法,操作流程更加简单。单点标定假定线性截距为0,但由于仪器灵敏度等原因,实际上不一定是这样的。单点标定法的使用前提是试液浓度在标准品浓度的线性范围以内,此处使用单点定量的线性验证数据对试液浓度的不确定度分量进行计算。
3 不确定度分量的计算
3.1 精密度研究
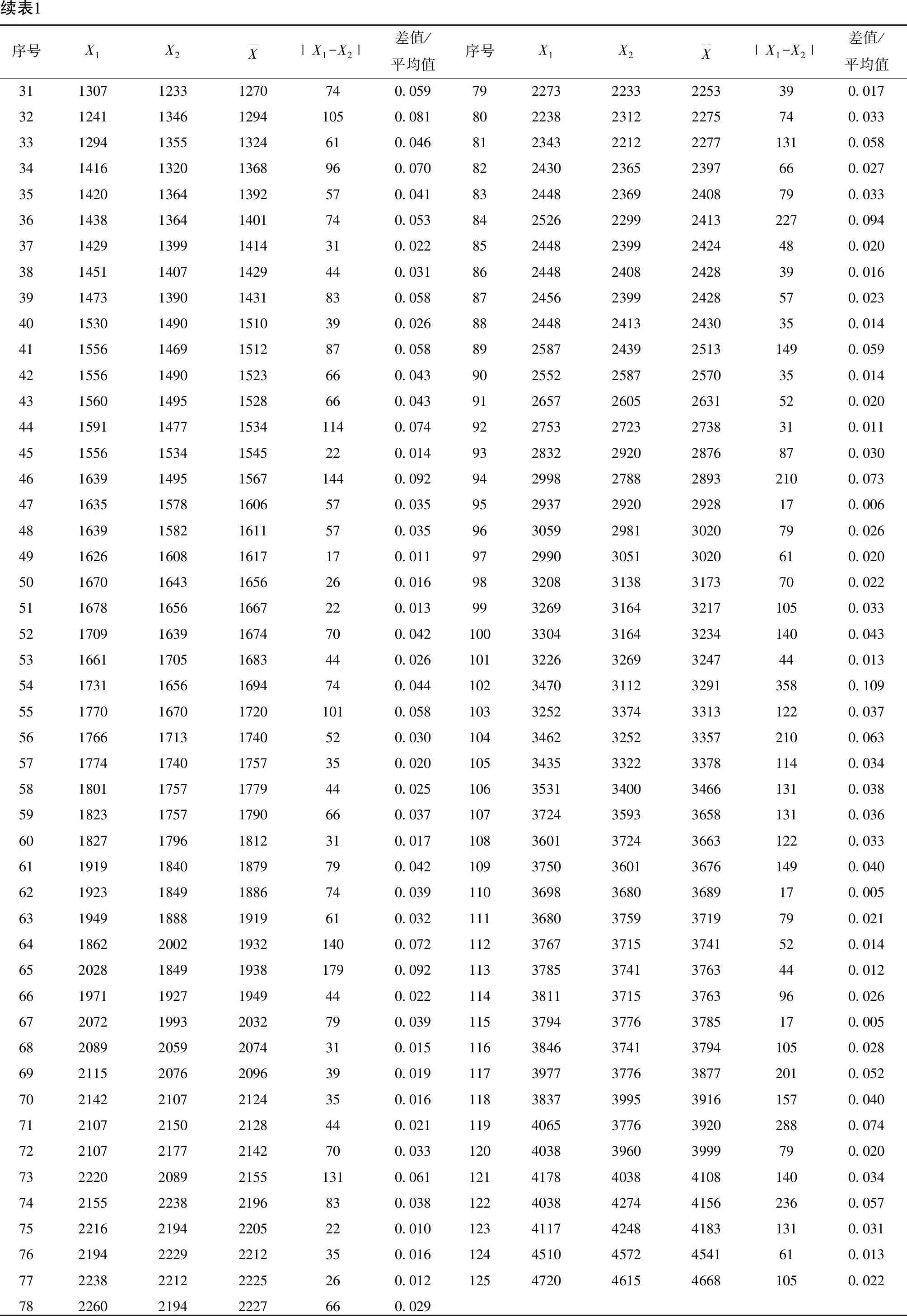
按1.2检测方法对多个不同含量梯度的小麦样品平行测定,以获得该分析程序中的随机变异,结果如表1所示。

表1 精密度研究数据 (单位:μg/kg)
续表1序号X1X2X|X1-X2|差值/平均值序号X1X2X|X1-X2|差值/平均值31130712331270740.059321241134612941050.08133129413551324610.04634141613201368960.07035142013641392570.04136143813641401740.05337142913991414310.02238145114071429440.03139147313901431830.05840153014901510390.02641155614691512870.05842155614901523660.04343156014951528660.043441591147715341140.07445155615341545220.014461639149515671440.09247163515781606570.03548163915821611570.03549162616081617170.01150167016431656260.01651167816561667220.01352170916391674700.04253166117051683440.02654173116561694740.044551770167017201010.05856176617131740520.03057177417401757350.02058180117571779440.02559182317571790660.03760182717961812310.01761191918401879790.04262192318491886740.03963194918881919610.032641862200219321400.072652028184919381790.09266197119271949440.02267207219932032790.03968208920592074310.01569211520762096390.01970214221072124350.01671210721502128440.02172210721772142700.033732220208921551310.06174215522382196830.03875221621942205220.01076219422292212350.01677223822122225260.01278226021942227660.02979227322332253390.01780223823122275740.033812343221222771310.05882243023652397660.02783244823692408790.033842526229924132270.09485244823992424480.02086244824082428390.01687245623992428570.02388244824132430350.014892587243925131490.05990255225872570350.01491265726052631520.02092275327232738310.01193283229202876870.030942998278828932100.07395293729202928170.00696305929813020790.02697299030513020610.02098320831383173700.022993269316432171050.0331003304316432341400.043101322632693247440.0131023470311232913580.1091033252337433131220.0371043462325233572100.0631053435332233781140.0341063531340034661310.0381073724359336581310.0361083601372436631220.0331093750360136761490.040110369836803689170.005111368037593719790.021112376737153741520.014113378537413763440.012114381137153763960.026115379437763785170.0051163846374137941050.0281173977377638772010.0521183837399539161570.0401194065377639202880.074120403839603999790.0201214178403841081400.0341224038427441562360.0571234117424841831310.031124451045724541610.0131254720461546681050.022
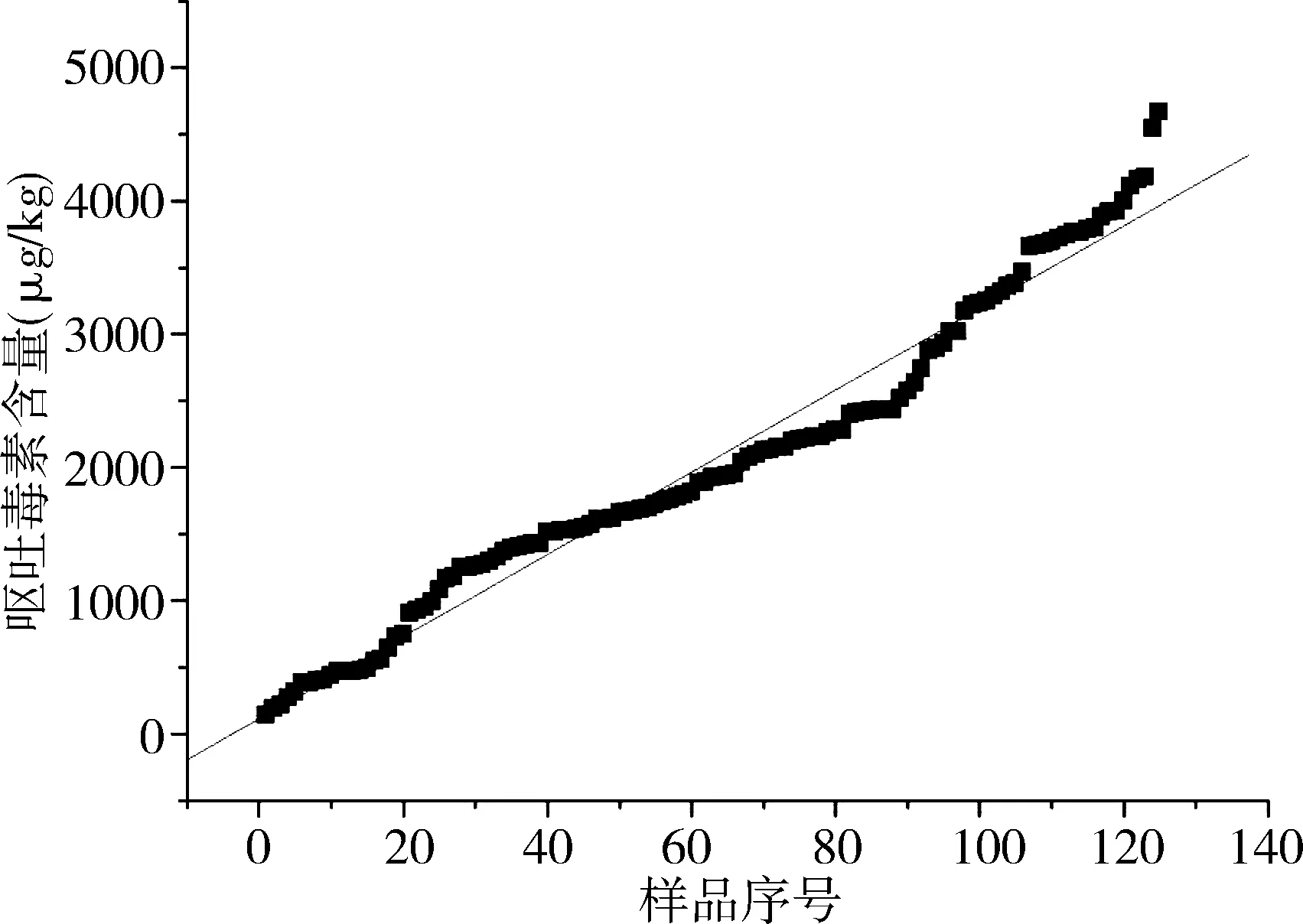
图2 样品DON含量梯度
3.2 试液浓度的不确定分量
本试验中,试液浓度ρ由标准工作溶液单点定量计算得出。单点定量的前提是该点和试液浓度处于线性范围之内,该分量须考虑标准溶液示值浓度和最小二乘法线性拟合两方面影响因素。
标准储备液浓度示值100.0 μg/mL,U=0.8 μg/mL,k=2。对于标称容量为100 mL的单标线的容量瓶,在室温下测溶液体积的标准不确定度为:
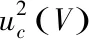
uc(V)=0.0874 mL
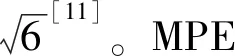
同理,对于标称容量为1 mL的分度移液管,δ为0.01 mL,MPE为0.008 mL,经计算,标准不确定度为0.0032 mL。
则标准工作溶液浓度的不确定度分量计算为:
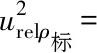
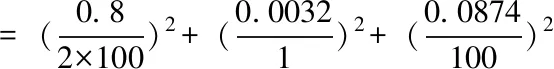
urelρ标=0.0052
单点定量的线性验证数据如表1所示,每个点重复上机检测3次。试样溶液重复上机检测6次,峰面积分别为18.2、18.3、18.3、18.1、18.1、18.1,平均值为18.2。校准曲线的表达式为Ii=Ci×B1+B0+ei,Ii为第i次测量的峰面积;Ci为对应于第i次峰面积的校准标准溶液的浓度;B1为斜率,B0为截距,ei为残差。经计算,线性最小二乘法拟合曲线,相关系数为0.9999,B1为54.79,B0为3.4979。
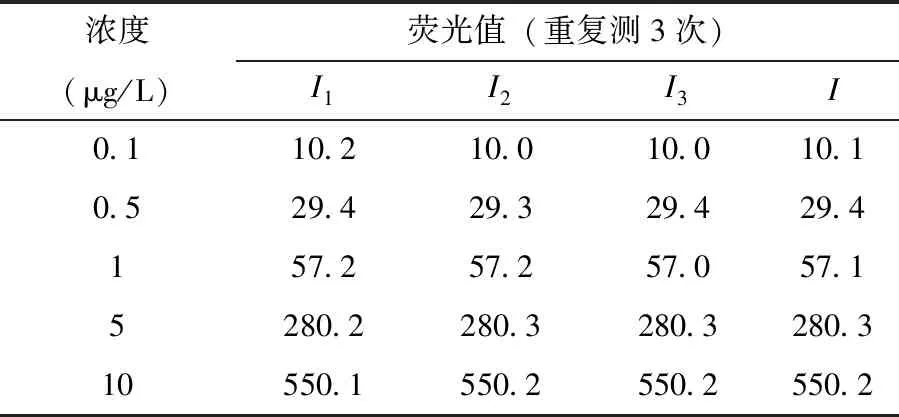
表2 单点定量线性验证数据
与线性最小二乘法拟合曲线程序有关的不确定度公式为:
其中残差标准偏差为:
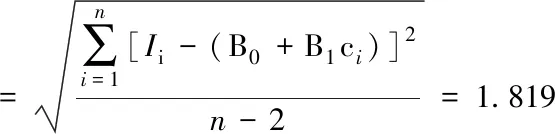
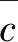
单点定量公式为ρ=ρ标×A样÷A标,经计算试液浓度c为0.32 μg/L,由上述标准工作溶液浓度和拟合线性合成试液浓度的不确定度分量:
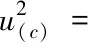
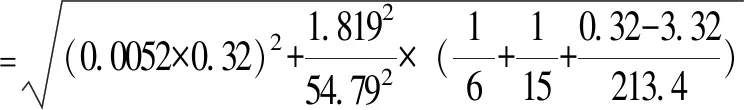
uc1=0.044 μg/L
3.3 称量不确定度分量
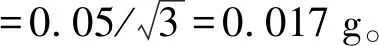
3.4 提取液体积的不确定度分量
回顾前处理过程,提取液体积并未准确定容,计算公式中提取液体积取100 mL。上机检测的溶液未进行定容,浓度计算是按稀释因子f追溯为提取液的浓度。提纯过程包含的稀释转化由回收率分量一并计算不确定度,此处仅考虑提取液体积取100 mL引入的不确定度分量。假定提取过程中溶质与溶剂分布均匀,不考虑物料的吸水性,加入的提取溶剂与提取液体积相等。同3.2中容量瓶的标准不确定度计算过程,uV=0.25 mL。
3.5 回收率不确定度分量

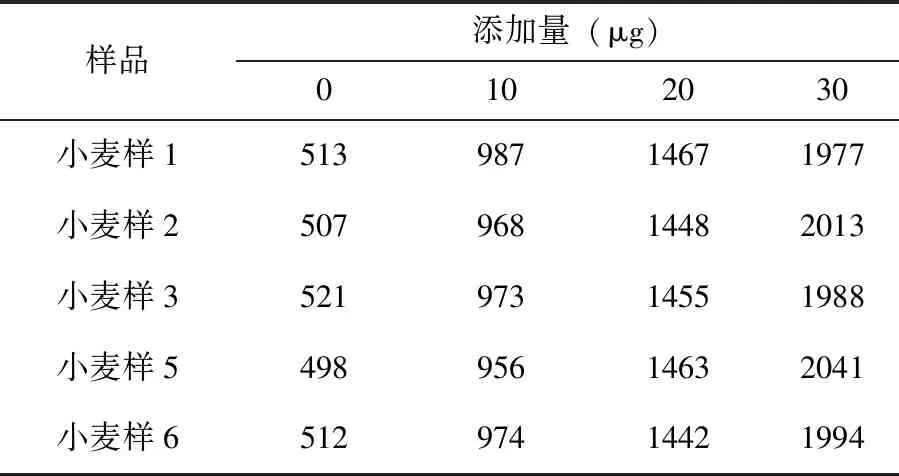
表3 回收率试验
用t检验来确定平均回收率是否与1.0有显著性差异,计算如下:
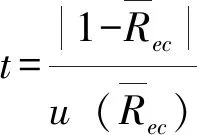
该值与95%置信度,n-1自由度下的双侧临界值比较,t=0.237≤tcrit,14≌2.145,因此,Rec与1无显著性差异,公式中无需包含修正因子。
4 计算合成不确定度
根据DON含量的计算公式以及上述各分量的计算,合成不确定度的计算公式为:
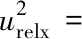
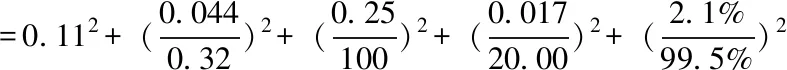
urelx=0.18
Urelx=2×urelx=0.18×2=0.36
因此,该小麦样品称样量为20.00 g,按上述步骤提取、净化和洗脱,配制浓度为1000 ng/mL的DON标准工作溶液单点定量,标品峰面积均值为57.2,样品峰面积均值为18.2。经计算,DON含量为1591 μg/kg,U=0.36×1591=573 μg/kg,k=2。
各分量的相对标准不确定度的贡献如图3所示,对不确定度合成影响较大的三个分量分别为试液浓度、精密度和回收率,相对不确定度分别为0.14、0.11和0.021。
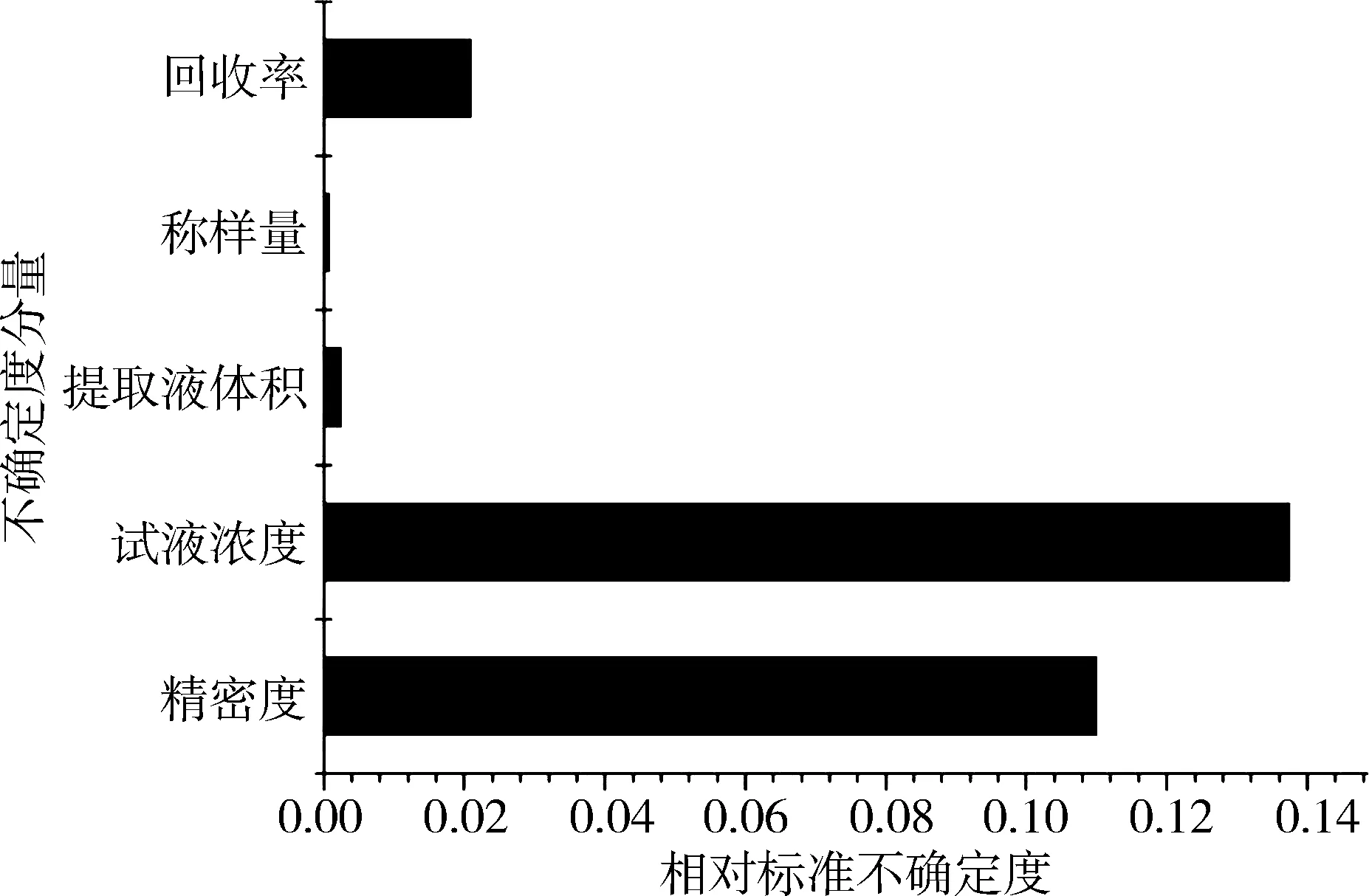
图3 不确定度分量贡献比较
5 结论
本文依据JJF 1059.1-2012《测量不确定度评定与表示》和CNAS-GL006《化学分析中不确定度的评估指南》中的相关规定,通过对免疫亲和层析净化高效液相色谱法检测小麦中呕吐毒素的检验步骤进行分析,得出影响该检测不确定度的主要因素为试液浓度、精密度和回收率,称样量和提取液体积引入的不确定度分量较小。根据试液浓度不确定度分量的计算过程,单点标定时试液浓度越接近标准工作溶液浓度,不确定度越小。
