健脾补肾方治疗肌萎缩侧索硬化的机制研究
2021-04-14王明哲李婷婷潘卫东
朱 玮,王明哲,李婷婷,刘 云,潘卫东
1.海军医科大学附属公利医院神经内科,上海 200135
2.上海中医药大学附属曙光医院脑病科,上海 201203
肌萎缩侧索硬化(amyotrophic lateral sclerosis,ALS)是以脊髓前角细胞、脑干运动神经核及锥体束受累为主的运动神经元病(motor neuron disease,MND),是一种发病后快速进展的致命性神经退行性变性疾病,其中主要为散发性ALS,而家族性ALS 仅占约5%。由于目前尚缺少针对ALS 的确切有效的化学药物或生物药物,因此该病的预后极差,患者在发病后2~5 年可因多系统衰竭而死亡[1]。
无论是散发性ALS 还是家族性ALS,因其表现为渐进性的肌肉痿软无力甚至萎缩,而归为中医学的“痿症”。现代中医医家认为ALS 的病机多以本虚为主或虚实夹杂,其中本虚以脾肾阳虚为主,而夹杂胃、肝和肺等亏虚,因此多施以健脾益气补肾之法治疗ALS,取得了一定的临床疗效[2]。本课题组基于“脾主四肢肌肉”“肾为作强之官”的中医理论,对近300 例ALS 患者进行随访,发现ALS 病程初期多以脾肾阳虚为主证,同时夹杂胃、肝和肺等亏虚;而病程中晚期则除脾肾阳虚之外,还多表现为虚实夹杂兼瘀血痰湿[3-4]。通过明确ALS 的基本病机为脾肾阳虚,并且确立治则为健脾补肾后,制定健脾补肾方(又称温肾四君子汤或加味四君子汤),已治疗超过500 例ALS患者,取得了较好的临床疗效。
尽管通过施以温肾健脾法能够延缓ALS 的病程进展并且改善临床症状,但是尚不清楚其作用机制。研究发现,无论是在散发性ALS 还是超氧化物歧化酶1(superoxide dismutase 1,SOD1)相关家族性ALS 动物模型中,含有离子型谷氨酸受体亚基的α-氨基-3-羟基-5-甲基-4-异噁唑丙酸受体(α-amino-3-hydroxy-5-methyl-4-isox-azolepropionic acid receptor,AMPAR)的亚单位谷氨酸受体2(glutamic acid receptor 2,GluR2)所介导的毒性作用均在ALS 的发病机制中发挥重要作用[1]。
本课题组采用潘卫东和KWAK Shin 等[5]建立的模拟ALS 发生与进展的AR2 小鼠模型,观察中药健脾补肾方对AR2 小鼠模型运动功能的影响,并探讨其作用机制。
1 材料与方法
1.1 健脾补肾方
健脾补肾方(即加味四君子汤)为《太平惠民和剂局方》所载四君子汤加黄芪、肉苁蓉和淫羊藿所组成:人参15 g,茯苓15 g,白术15 g,甘草10 g,黄芪30 g,肉苁蓉30 g,淫羊藿25 g。中药由上海中医药大学附属曙光医院提供。用500 mL蒸馏水煎药1 h,过滤后取上清液;再加入500 mL蒸馏水煎药1 h,过滤后取上清液;合并2 次的上清液,用微火煮成50 mL 浓缩药液;冷却后,加入无水乙醇,磁力搅拌器上搅拌过夜,25 000g离心20 min;取上清液,恒温条件下待乙醇蒸发完全后,用蒸馏水调整药液浓度为1 g/mL;高压灭菌后,置于-20℃冰箱保存备用。采用高效液相色谱法(high performance liquid chromatography,HPLC)对中药的主要成分进行分析和鉴定。
1.2 实验动物
建立条件性ADAR2(adenosine deaminase acting on RNA 2)基因敲除AR2 小鼠模型[5],选择保留部分运动神经元功能的AR2 小鼠[3]。
1.3 随机分组与干预
将48 只保留部分运动神经元功能的AR2 小鼠随机分为4 组:健脾补肾方低剂量组(12 只),健脾补肾方中剂量组(12 只),健脾补肾方高剂量组(12 只),对照组(12 只)。
4 组小鼠均自由进食和饮水。对照组小鼠除正常饮食外,不给予其他干预。补肾健脾方低、中、高剂量组小鼠接受补肾健脾方灌胃1 次/d(按人体用药剂量的1/20 进行配制,低剂量组为15 mg/kg,中剂量组为30 mg/kg,高剂量组为45 mg/kg),连续干预9 个月。
1.4 观察指标[6]
采用单盲法,由不知晓小鼠鼠龄、基因型和分组情况的研究人员对各组小鼠进行观察。
1.4.1 一般情况
每个月观察各组小鼠的体质量、姿势、活动度和生存情况。每3 个月检测各组小鼠的血常规和肝肾功能。
1.4.2 运动和平衡能力
分别于干预前以及干预1、3 和6 个月后对各组小鼠进行疲劳转棒实验(型号为RD1123-RS-M,上海移数信息科技有限公司产品)、爬杆实验(自制实验器材)、平衡木实验(自制实验器材)和跑步机实验(型号为FT-2000,成都泰盟软件有限公司产品)。每次实验一般均在连续的3 个工作日内完成,前2 d 为训练日,第3 天为正式实验日。每次实验之前,提前30 min 将小鼠从饲养室转运至实验场所,以促使小鼠适应环境。
疲劳转棒实验用于检测小鼠的动作协调性和抗疲劳特性。转轴以20 转/min 的恒定速度转动,记录小鼠从开始运动至掉落的时间(重复测试3 次),最长测试时间为300 s,如果小鼠能够在300 s 内不掉落,则无需重复测试。
爬杆实验用于检测小鼠的运动协调能力。将小鼠头朝上放置于高60 cm 爬杆的顶端处,记录小鼠从头朝上转为头朝下所用的时间(杆上掉头时间),以及从测试开始至小鼠四肢全部着地所用的全程时间(爬杆实验的全程时间),以评估小鼠的运动协调能力。
平衡木实验用于检测小鼠的平衡能力、肌力以及运动协调力。平衡木一端放置在黑色方盒内,将小鼠放置在平衡木另一端。记录小鼠通过平衡木进入黑色方盒内的时间(从开始至小鼠四肢全部进入黑盒中所用的时间)。
跑步机实验用于检测小鼠的运动体能和耐力。实验装置为变速皮带跑步机,由一个速度可调节的传送带以及电击装置所组成。传送带被分隔成5条跑道,可以同时对6 只小鼠进行测试;电击装置的电压恒定设为50 V。跑步机实验分为适应阶段和测试阶段。在适应阶段,跑步机的传送带速度为5 m/min,传送带的倾斜角度为0°,将小鼠放入跑道,先进行5 min 的适应运动;随后进入测试阶段,将小鼠放入跑道,跑步机的传送带速度从5 m/min 缓慢提升至20 m/min(每隔15 min 增加3 m/min),同时将传送带的倾斜角度由0°缓慢提升至12°(每隔15 min 增加3°),直至小鼠在传送带上的运动时间达到90 min 或其运动能力达到极限,则结束实验。如果小鼠被连续电击20 s 后仍不能进入正常跑步状态,则认为该小鼠的运动能力已达极限。记录运动时间和运动路程。
1.4.3 脊髓前角神经元数
对条件性ADAR2 基因敲除后AR2 小鼠模型在不同鼠龄时的ADAR2 免疫反应性以及缺失免疫反应性脊髓前角神经元的数量进行检测。同时,在干预1 和3 个月后,检测补肾健脾方各剂量组小鼠的脊髓前角细胞数量。
1.5 统计学方法
应用SPSS 15.0 软件进行统计学分析。多组均数的比较采用单因素方差分析,方差不齐采用非参数检验。P<0.05 为差异有统计学意义。
2 结果
2.1 一般情况
4 组小鼠均存活24 周以上。24 周龄时,4组小鼠的体质量差异无统计学意义(P>0.05),肝肾功能的差异亦无统计学意义(P>0.05)。
2.2 运动和平衡能力
干预前,4 组小鼠的疲劳转棒实验、爬杆实验的杆上掉头时间与爬杆实验的全程时间、平衡木实验以及跑步机实验的运动时间的差异均无统计学意义(P>0.05)。
4 组小鼠从干预第3 个月起,均出现不同程度的运动能力减退。随着干预的进行,补肾健脾方各剂量组小鼠的运动和平衡能力均较对照组小鼠有所改善(图1)。干预3 个月后,补肾健脾方中剂量组的疲劳转棒实验、平衡木实验和跑步机实验结果均显著优于对照组(P<0.05)。干预6 个月后,补肾健脾方各剂量组的疲劳转棒实验、平衡木实验和跑步机实验的结果均显著优于对照组(P<0.05);补肾健脾方中剂量组和高剂量组爬杆实验的全程时间均显著短于对照组(P<0.05)。

图1 各组小鼠干预前以及干预1、3 和6 个月后的疲劳转棒实验(A)、爬杆实验(B)、平衡木实验(C)以及跑步机实验(D)结果的比较。15、30 和45 分别为补肾健脾方低、中和高剂量组。
2.3 脊髓前角神经元数量
干预3 个月后,小鼠的ADAR2 免疫反应性以及缺失免疫反应性脊髓前角神经元的数量开始减少,与ALS 的病程进展一致(图2A)。干预1 个月和3 个月后,小健脾补肾方中剂量组和高剂量组小鼠的脊髓前角神经元数量均多于对照组(图2B)。
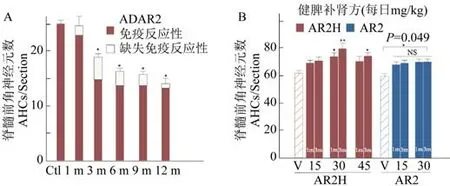
图2 选择性ADAR2 敲除后AR2 小鼠模型在不同鼠龄时的ADAR2 免疫反应性(灰色)以及缺失免疫反应性(白色)脊髓前角神经元的数量(A)(与Ctl 比较,*P <0.05)。在干预1 和3 个月后,补肾健脾方各剂量组小鼠的脊髓前角细胞数量(B)(与V 比较,*P <0.05,**P<0.01)。A:Ctl 为对照组,1m、3m、6m、9m、12m 分别为1 个月、3 个月、6 个月、9 个月和12 个月;B:AR2H 为杂合子小鼠模型,AR2 为纯合子小鼠模型,V 为溶剂对照组,15、30 和45 分别为补肾健脾方低、中和高剂量组,1m 和3m 分别为1 个月和3 个月,NS 为差异无统计学意义。
3 讨论
ALS 是一类病因和发病机制尚未明确的神经退行性变性疾病,呈慢性进展病程。在ALS 早期,基于不同的发病部位和症状而被分成许多亚型,反映出病程进展速度和主要症状的差异。大多数的ALS 患者随着病程的进展,最后均会出现咽肌、舌肌、口轮匝肌以及颈部以下全部肌肉的无力和萎缩,需要接受呼吸机辅助通气,以及通过鼻饲管或胃造瘘进食,必须依靠外部辅助手段而存活。目前在国际上已获得批准的ALS 治疗药物如利鲁唑和依达拉奉等的疗效并不显著。也有学者尝试采用抗癫痫药物吡仑帕奈以及间充质干细胞治疗ALS[7],但是绝大多数患者的病情依然无法得到控制。
ALS 在中医属于“痿症”范畴,中医学认为其发生和进展应分别责之于“先天”“后天”。中医认为“先天因素”就是肾的功能,易患神经退行性变性疾病(如帕金森病和阿尔茨海默病等)均与肾的先天不足有关。“肾为作强之官”就是指肾是统帅,是掌管人类出生、生长、发育、代谢和衰老的指挥中心。中医认为“后天”与脾相关,出生之后的生长发育和新陈代谢均需得到后天营养以及精气神的支持,而其来源就是后天之本的脾(阳明经络)。脾功能正常,后天营养就充足。此外,中医认为“脾主四肢肌肉”。《素问》云:“论言治痿者,独取阳明何也?”《灵枢》云:“太阳为开,阳明为合,少阳为枢……合折则气所止息,而痿疾起矣。故痿疾者,取之阳明”。因此,在治疗ALS 患者的肌肉萎缩时,应关注中医脾的功能。“治痿独取阳明”就是强调脾胃在痿症治疗中的重要地位。因此,基于中医理论,ALS 的发生和发展均与肾和脾相关,治疗应从补益脾肾入手。健脾补肾方是在传统四君子汤基础上增加黄芪、肉苁蓉和淫羊藿3 味温肾补气之药,以脾肾为中心治疗ALS,符合大多数ALS 患者的证型,诸药合用可温肾健脾和胃,强五脏六腑之海,补益气血,营养宗筋,从而达到“治痿独取阳明”之目的。
本研究发现,干预1、3 和6 个月后,健脾补肾方各剂量组小鼠的运动和平衡能力均较对照组小鼠有所改善。与对照组相比,无论是低剂量、中剂量还是高剂量健脾补肾方,均可显著延缓模型小鼠脊髓前角神经元的衰退。其中,健脾补肾方中剂量组的疗效相对优于低剂量组和高剂量组。干预3、6 和9 个月后,健脾补肾方各剂量组小鼠的肝肾功能均未见明显受损。
虽然在一些神经退行性变性疾病如帕金森病的治疗中,中医药无法完全替代西药,但是基于中医理论开展辨证论治,也取得了一定的疗效[8-9]。本研究发现,健脾补肾方能够缓解AR2 小鼠模型的体质量下降,改善小鼠四肢的活动能力、肌肉活动的持久性、肌力以及身体的灵活性,这些作用可能与延缓脊髓前角神经元的丢失和变性以及降低AR2 小鼠模型的ADAR2 免疫反应性有关。今后需要进一步研究长期使用健脾补肾方是否能够延缓ALS 的进展。此外,新的观点认为包括帕金森病和阿尔茨海默病在内的神经退行性变性疾病的发病可能与肠道菌群失调有关[10-11],尤其是肠道内的一些特殊菌群,而中医认为脾主运化水谷精微,因此从脾论治神经退行性变性疾病可能会成为中医治疗的新靶点[12]。
总之,健脾补肾方能够改善ALS 小鼠的运动和平衡能力,可能与延缓脊髓前角神经元的丢失和变性以及降低AR2 小鼠模型的ADAR2 免疫反应性有关,且安全性较高。在当前缺少能够有效治疗ALS 的西药的情况下,采用健脾补肾方治疗ALS 不啻是一种选择。
