藏药岩生忍冬多糖抗氧化的实验研究
2021-04-08张熙苓苏小锋
张熙苓,苏小锋,刘 群
(西南民族大学畜牧兽医学院,四川成都 610041)
岩生忍冬(Lonicera rupicola Hook. f. et Thoms.)属忍冬科忍冬属植物。目前对忍冬科忍冬属药物植物的研究主要集中于金银花的研究,对同属植物岩生忍冬研究较少。相关研究报道,忍冬属药物植物含环烯醚萜[1]、黄酮[2]、绿原酸[3]、挥发油[4]、皂苷[5]等多种具有药理作用的活性物质。为了探讨藏药岩生忍冬多糖的抗氧化作用,采用水煎醇沉法制备岩生忍冬多糖干膏制剂,通过体外DPPH·自由基体系、·OH 自由基体系、Fe3+还原力体系及S180 荷瘤小鼠大脑、肝脏、心脏、血液的SOD、CAT 活性、MDA 含量的研究以阳性药物维生素C 为对照,探究藏药岩生忍冬多糖的抗氧化作用,现将研究结果报告如下。
1 材料
1.1 研究药物
岩生忍冬采自四川省甘孜州色达地区。岩生忍冬多糖,由西南民族大学畜牧兽医学院提供。
1.2 实验动物
6 周龄清洁级昆明小鼠,体质量(20±2)g/只,由成都达硕生物科技有限公司提供。
1.3 主要试剂及仪器
S180 瘤细胞株(国家细胞共享资源库提供);羟自由基测定试剂盒(南京建成公司);DPPH·溶液(Huaxia Reagent 公司);维生素C 溶液(上海易恩化学技术有限公司);SOD(南京建成生物工程研究所有限公司);MDA、CAT 测定试剂盒(北京索莱宝科技有限公司;紫外-可见分光光度计(日本岛津公司);全波长酶标仪(ThermoFisher 公司)等。
2 方法
2.1 体外抗氧化实验
按照生药100%浓度,制备岩生忍冬多糖样品溶液,4℃冰箱保存、备用;参考丁良等[6~7]的研究,以维生素C 为阳性对照药物,DPPH·自由基、羟自由基、Fe3+为研究体系,检测岩生忍冬多糖体外的抗氧化作用。DPPH·自由基清除能力的测定按试剂盒操作测定IC50值;羟自由基清除能力测定按试剂盒操作测定抑制羟自由基能力(U/ml);Fe3+还原能力测定按照铁氰化钾还原法,测定Fe3+还原力。
2.2 体内抗氧化实验
2.2.1 岩生忍冬多糖口服液的制备
将岩生忍冬多糖配制成低、中、高的岩生忍冬多糖口服液(50%、100%、200%)。
2.2.2 S180 瘤细胞悬液的制备
S180 肉瘤制备瘤细胞悬液并确定接种小鼠,整个实验过程中瘤体不被破裂死亡,以确定接种S180瘤细胞浓度。
2.2.3 实验动物分组及处理
参照范旭楠等[8~10]的研究,84 只昆明小鼠随机分成6 组。空白对照组:正常小鼠,每天灌胃生理盐水;S180 荷瘤对照组:每只小鼠右前肢腋下注射瘤细胞悬液0.2 ml/只,每天灌胃生理盐水;维生素C 组:每只小鼠右前肢腋下注射瘤细胞悬液0.2 ml/只,每天灌胃维生素C(100 mg/kg·d)。高剂量多糖组、中剂量多糖组、低剂量多糖组,每只小鼠右前肢腋下注射瘤细胞悬液0.2 ml/只,每天灌胃岩生忍冬多糖分别为200 mg/kg·d、100 mg/kg·d、50 mg/kg·d。连续28 d。
2.2.4 抗氧化指标测定
摘除小鼠眼球,收集小鼠静脉血,柠檬酸钠抗凝,制备小鼠血浆样本;颈椎脱臼法处死小鼠,取脑、肝脏、心脏,制备10%组织匀浆上清液,测定其SOD、MDA、CAT 按试剂盒操作。
2.2.5 数据处理
实验数据以(±s)表示,采用SPSS21.0 软件进行统计学分析。
3 结果与分析
3.1 体外抗氧化实验结果
3.1.1 DPPH·清除能力
不同浓度岩生忍冬多糖和维生素C 对DPPH·自由基清除作用见表1~2。岩生忍冬多糖对DPPH·的清除能力随着浓度的增加而增大。当多糖浓度达到3.0 mg/ml 时,清除率达到最大值60.95%,IC50值为2.123 mg/ml;阳性药物维生素C 浓度为2.0 mg/ml 时,清除率达到最大值100%。实验结果表明:当岩生忍冬多糖质量浓度为2.123 mg/ml,能有效清除DPPH·自由基体系中一半的DPPH·并随着浓度的增加清除率增加,存在一定的量效关系。采用DPPH·自由基IC50清除率的岩生忍冬多糖浓度时,对DPPH·清除作用具有动态特点,说明岩生忍冬多糖对DPPH·清除作用可能存在一定的时效关系。藏药岩生忍冬多糖对DPPH·具有一定的清除作用,其IC50=2.0 mg/ml,清除作用具有一定的量效关系和时效关系。
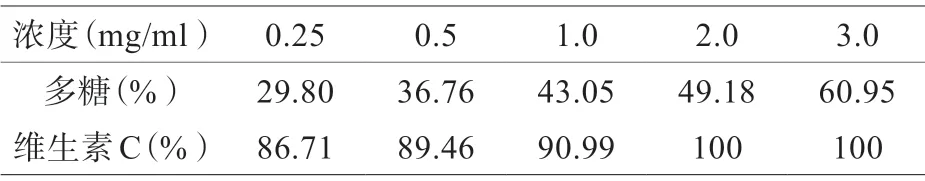
表1 DPPH·自由基清除率(%)

表2 DPPH·自由基清除率(%)
3.1.2 ·OH 清除能力
不同浓度岩生忍冬多糖和维生素C 对·OH 自由基清除作用见表3。岩生忍冬多糖对羟自由基清除力随着岩生忍冬多糖浓度的增加而增大并稳定在一定水平上。当多糖浓度达到1.0 mg/ml 时,清除率达到最大,阳性药物维生素C 对羟自由基清除力高于岩生忍冬多糖的清除力。综上藏药岩生忍冬多糖对羟自由基具有一定的清除作用。

表3 ·OH 自由基清除率
3.1.3 Fe3+还原能力
不同浓度岩生忍冬多糖和维生素C 对Fe3+还原能力作用见表4。岩生忍冬多糖对Fe3+还原能力随着岩生忍冬多糖浓度的增加而增大。当多糖浓度达到1.0 mg/ml 时,还原力达到最大值,阳性药物维生素C 对Fe3+还原能力高于岩生忍冬多糖的还原能力。综上,藏药岩生忍冬多糖对Fe3+具有一定的还原作用。

表4 Fe3+还原能力
3.2 体内抗氧化实验结果
3.2.1 SOD 活性
各组小鼠血浆及脏器组织中SOD 活性见表5。小鼠肝脏SOD 活力极显著低于对照组SOD 活力(P<0.01),三个剂量多糖组SOD 均极显著高于荷瘤小鼠组的SOD 活力(P <0.01),显著高于对照组SOD 活力;三个剂量多糖组SOD 活力表现出正向量效关系。小鼠大脑SOD 活力极显著低于对照组SOD 活力(P <0.01),三个剂量多糖组SOD 均极显著高于荷瘤小鼠组的SOD 活力(P <0.01);小鼠心脏SOD 活力极显著低于对照组SOD 活力(P <0.01),三个剂量多糖组SOD 活力均极显著高于荷瘤小鼠组SOD 活力(P <0.01),三个剂量多糖组SOD 活力表现出正向量效关系。小鼠接种S180 瘤细胞后,血液及脑、心、肝SOD 活力极剧下降;阳性药物维生素C 具有增强荷瘤小鼠和正常小鼠SOD 活力;三个剂量多糖能够增强低下的荷瘤小鼠SOD 活力并表现出对心、肝良好的正向量效关系,且预示三个多糖组对正常小鼠SOD 活力也具有增强作用。研究结果表明:岩生忍冬多糖具有增强机体SOD 活性的作用。
表5 小鼠血清及脏器组织中SOD 活力( ±s,n = 14)
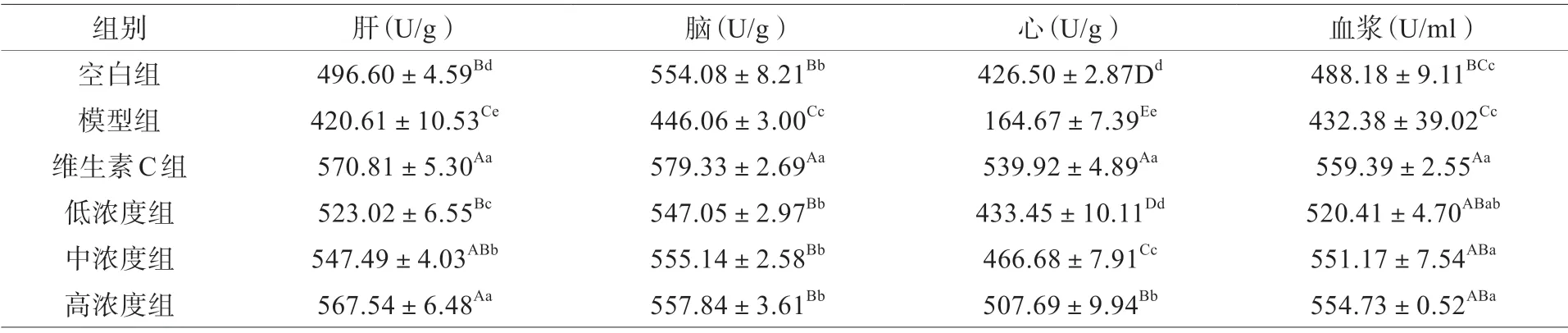
表5 小鼠血清及脏器组织中SOD 活力( ±s,n = 14)
注: 同列数据肩上标有相同小写字母表示差异不显著(P >0.05),标有不同小写字母表示差异显著(0.01 <P <0.05),标有不同大写字母表示极显著差异(P <0.01)。下同。
组别肝(U/g)脑(U/g)心(U/g)血浆(U/ml)空白组496.60±4.59Bd554.08±8.21Bb426.50±2.87Dd488.18±9.11BCc模型组420.61±10.53Ce446.06±3.00Cc164.67±7.39Ee432.38±39.02Cc维生素C组570.81±5.30Aa579.33±2.69Aa539.92±4.89Aa559.39±2.55Aa低浓度组523.02±6.55Bc547.05±2.97Bb433.45±10.11Dd520.41±4.70ABab中浓度组547.49±4.03ABb555.14±2.58Bb466.68±7.91Cc551.17±7.54ABa高浓度组567.54±6.48Aa557.84±3.61Bb507.69±9.94Bb554.73±0.52ABa
3.2.2 CAT 活性
各组小鼠血浆及脏器组织中CAT 活性见表6。小鼠肝脏CAT 活力显著低于对照组CAT 活力(P <0.05),三个剂量多糖组CAT 活力均极显著高于荷瘤小鼠组的CAT 活力(P <0.01),低剂量多糖组CAT 活力显著高于对照组;荷瘤小鼠大脑CAT 活力显著低于对照组(P<0.05),三个剂量多糖组中、高剂量多糖组CAT 活力极显著高于荷瘤小鼠CAT 活力(P <0.01),三个剂量多糖组CAT 活力平均值逐渐增大;荷瘤小鼠心脏CAT 活力极显著低于对照组(P <0.01),三个剂量多糖组CAT 活力低于阳性药物组(P <0.01)。三个剂量多糖组中高剂量多糖组CAT 活力极显著高于荷瘤小鼠组CAT活力(P <0.01)显著高于对照组(P <0.05);荷瘤小鼠血浆CAT活力显著低于对照组SOD活力(P<0.05),三个剂量多糖组CAT 活力低于阳性药物组(P <0.01)且三个剂量多糖组CAT 活力平均值逐渐增大,中、高剂量多糖组极显著高于低剂量多糖组(P <0.05)。小鼠接种S180瘤细胞后28 d,血液及脑、心、肝CAT活力下降;阳性药物维生素C 具有增强荷瘤小鼠和正常小鼠CAT 活力;三个剂量多糖不仅具有增强低下的荷瘤小鼠CAT 活力的作用并表现出一定的正向量效关系,研究结果表明:岩生忍冬多糖具有增强机体CAT 活性的作用。
表6 小鼠血清及脏器组织中CAT 活力( ±s,n = 14)

表6 小鼠血清及脏器组织中CAT 活力( ±s,n = 14)
组别肝(U/g)脑(U/g)心(U/g)血浆(U/ml)空白组49.42±5.56Cc16.88±1.45BCDcd125.84±10.63Bc2.59±0.96BCb模型组21.96±2.58Cd11.22±1.11De38.25±1.83Ce1.27±0.08Cc维生素C组130.20±12.34Aa29.07±1.75Aa202.11±8.48Aa4.96±0.91Aa低浓度组42.46±4.18Ccd12.44±1.97CDde39.40±4.08Cde2.48±0.25BCbc中浓度组98.00±11.11Bb19.43±2.69BCbc56.30±12.16Cde2.74±0.21BCb高浓度组98.91±4.58ABb23.72±1.68ABb165.10±10.63ABb3.17±0.37Bb
3.2.3 MDA 含量
各组小鼠血浆及脏器组织中MDA 含量见表7。荷瘤小鼠肝脏MDA 含量极显著高于对照组的含量(P<0.01)。三个剂量多糖组MDA 含量极显著低于荷瘤小鼠组(P <0.01),三个剂量多糖组MDA 含量平均值随剂量增加逐渐减小,表现出良好的负向量效关系。荷瘤小鼠大脑MDA 含量极显著高于对照组MDA 含量(P<0.01),三个剂量多糖组MDA 含量高于阳性药物组,表现为低剂量差异极显著(P <0.01),中、高剂量差异显著(P <0.05);荷瘤小鼠心脏MDA 含量极显著高于对照组MDA 含量(P <0.01),三个剂量多糖组MDA 含量高于阳性药物组(P <0.01),均极显著低于荷瘤小鼠(P <0.01);荷瘤小鼠血浆MDA 含量极显著高于对照组(P <0.01),三个剂量多糖组和阳性药物MDA含量极显著低于荷瘤小鼠组(P<0.01)。小鼠接种S180 瘤细胞28 d 后,血液及脑、心、肝MDA 含量升高;维生素C 能够降低荷瘤小鼠和正常小鼠MDA 含量;三个剂量多糖组具有降低荷瘤小鼠MDA含量且表现出对心、肝良好的负向量效关系,研究结果表明:岩生忍冬多糖具有降低机体MDA 含量的作用。
表7 小鼠血清及脏器组织中MDA 含量( ±s,n = 14)

表7 小鼠血清及脏器组织中MDA 含量( ±s,n = 14)
组别肝(U/g)脑(U/g)心(U/g)血浆(U/ml)空白组49.42±5.56Cc16.88±1.45BCDcd125.84±10.63Bc2.59±0.96BCb模型组21.96±2.58Cd11.22±1.11De38.25±1.83Ce1.27±0.08Cc维生素C组130.20±12.34Aa29.07±1.75Aa202.11±8.48Aa4.96±0.91Aa低浓度组42.46±4.18Ccd12.44±1.97CDde39.40±4.08Cde2.48±0.25BCbc中浓度组98.00±11.11Bb19.43±2.69BCbc56.30±12.16Cde2.74±0.21BCb高浓度组98.91±4.58ABb23.72±1.68ABb165.10±10.63ABb3.17±0.37Bb
4 讨论与结论
4.1 岩生忍冬多糖体外抗氧化作用
体外抗氧化研究方法目前主要采用DPPH·、·OH 自由基体系和Fe3+还原力测定体系,并以维生素C 作为对照,用于研究中药的抗氧化活性。中草药及其化学成分的抗氧化能力随其浓度增加逐步上升,表现出明显的量效关系,但明显低于维生素C 的抗氧化能力。IC50为清除率达到50%时所需药物的浓度,IC50值的大小表明了抗氧化剂清除自由基的能力高低,IC50值越小,抗氧化剂能力越强[11]。藏药岩生忍冬多糖抗氧化作用的结果表明,藏药岩生忍冬多糖对DPPH·具有一定的清除作用,其IC50=2.0 mg/ml,清除作用具有一定的量效关系和时效关系。研究结果也表明,藏药岩生忍冬多糖对·OH 自由基、Fe3+具有一定的清除和还原作用。
4.2 岩生忍冬多糖体内抗氧化作用
SOD 广泛存在于各组织细胞中,通过歧化O2-·为H2O2与O2,减少O2-·聚集。在氧化应激引发的炎症动物模型、衰老动物模型、癌症动物模型等中,血清和组织SOD 含量下降,说明SOD 的活性受到了影响。CAT 酶活力是生物体抗氧化水平的另一指标,肝脏具备高效降解、解毒作用的原因之一是肝细胞的过氧化物体内存在有大量的CAT,CAT将H2O2分解为H2O 和O2。MDA 是自由基与脂质生物膜发生脂质过氧化反应产生的过氧化物,在一定程度上反应机体的抗氧化能力。植物多糖作为中药有效成分之一,具有抗氧化、降血糖、降血脂、抗肿瘤、调节机体免疫力等活性,尤其是近年来多糖的抗氧化作用受到广泛的重视[12]。张丽梅[13]发现银耳多糖对衰老大鼠的血清、肝脏及脑组织中的SOD、CAT酶的活力有增强作用。药岩生忍冬多糖体内抗氧化研究表明,不同剂量岩生忍冬多糖不仅具有增强低下的荷瘤小鼠肝、脑、心脏、血液SOD、CAT 活力,降低荷瘤小鼠肝、脑、心脏、血液高MDA 含量的作用,对心、肝表现出良好的量效关系。
目前,对岩生忍冬的药理学研究还未见报道。实验表明:S180 荷瘤小鼠肝、脑、心脏、血液SOD、CAT 活力显著低于正常小鼠,MDA 含量高于正常小鼠;不同剂量岩生忍冬多糖不仅具有增强低下的荷瘤小鼠肝、脑、心脏、血液SOD、CAT 活力,降低荷瘤小鼠肝、脑、心脏、血液高MDA 含量的作用,对心、肝表现出良好的量效关系。并且100 ~200 mg/kg·d 岩生忍冬多糖连续给药28 d,对正常小鼠也具有增强SOD、CAT 活力、降低MDA 含量的作用。研究结果表明,藏药岩生忍冬多糖具有增强机体的抗氧化能力并具有量效关系。
