基于多种基因突变状态的骨髓增生异常综合症患者预后预测模型的构建与验证
2021-04-08尚硕红糟秀梅权晓燕
尚硕红,糟秀梅,何 瑛,马 强,权晓燕
骨髓增生异常综合症(MDS)是一类以无效造血和高风险进展至白血病为特点的髓系肿瘤性疾病,预测预后是本病治疗方案选择的关键。研究表明超过90%的MDS患者至少携带一种血液肿瘤相关基因突变[1],诸如RUNX1、SF3B1、GATA等突变基因还与预后和治疗方案选择相关[2],在预后预测模型中纳入突变基因或有利于完善预后分层。本研究基于此,纳入MDS患者总生存(OS)相关因素构建预后预测列线图,报告如下。
1 资料与方法
1.1 一般材料:回顾性纳入2015年5月-2017年5月多家医院的156例MDS患者临床资料,纳入标准:符合MDS诊断标准[3]的首诊患者,年龄≥18岁。排除标准:①其他原因死亡;②伴随其他恶性肿瘤;③未遵医嘱治疗和自动出院患者。所有患者中男89例,女67例,年龄25~81岁,平均年龄(56.90±18.24)岁。分型:难治性贫血(RA)4例,难治性贫血伴有环状铁粒幼细胞(RARS)9例,难治性血细胞减少伴有多系发育异常(RCMD)45例,难治性贫血伴原始细胞过多-1型(RAEB-1)31例,难治性贫血伴原始细胞过多-2型(RAEB-2)40例,MDS不能分类型(MDS-U)6例,5q-综合征1例。依收治时间先后顺序将前2/3(104例)纳入试验组,后1/3(52例)纳入验证组,试验组再根据随访3年期间存活情况分为存活组和死亡组。本实验设计已由医院伦理学委员会审核。
1.2 方法
1.2.1 数据采集和调查内容:对较低危组[4]患者给予成分输血、祛铁、雄激素、环孢素等支持治疗为主,对较高危组[4]主要给予化疗和去甲基化治疗,有条件者施以异基因造血干细胞移植(allo-HSCT)。收集患者入组时临床资料,主要包含国际预后积分系统(IPSS-R分级)、基因检测结果、WHO分型等。所有患者以电话或门诊方式行随访至2020年5月30号,每15 d 1次,了解患者健康和存活情况。
1.2.2 IPSS-R分级:根据骨髓原始细胞占比、染色体核型、血细胞减少系列数评定积分进行分级:≤1.5分为极低危组,2~3分为低危组,3.5~4分为中危组,4.5~6分为高危组,>6分为极高危组。
1.2.3 基因检测:采用靶向检测突变基因,经骨穿取患者骨髓2mL,用乙二胺四乙酸抗凝后,应用血液基因组DNA提取试剂盒(北京海斯特检验中心提供)获取DNA。样本经PCR引物扩增目的基因热点区域[112种MDS或急性髓系白血病(AML)相关基因],目标区域DNA富集后,在Ion Torrent PGM测序平台进行基因测序。测序后用CCDS、人基因组数据库(HG19)、COSMIC、1000 genomes、dbSNP、SIFT等数据库分析数据,明确相关基因突变位点。平均基因覆盖率超过98%,平均测序深度为1500×,95%的目标区域测序深度超过500×,灵敏度5%。最终将突变频率最高的10个基因纳入观察指标。

2 结果
2.1 试验组和验证组、存活组和死亡组资料比较:因资料不全剔除6例后共纳入150例患者,截至最后随访期限共有15例(10.00%)转急性白血病,死亡53例(35.33%),均死于MDS进展,所有患者3年OS率为44.67%;两组年龄、WHO分型、IPSS-R分级等各项资料比较差异均无统计学意义(P>0.05);死亡组年龄(58.04±13.75)岁、存活组年龄(47.41±9.33)岁,2组比较基因突变率见表1。
2.2 MDS患者3年OS相关因素COX回归分析:年龄(OR=1.099,P<0.05)、ASXL1(OR=5.404,P>0.05)、SRSF2(OR=12.221,P>0.05)、DNMT3A(OR=14.116,P>0.05)、TP53(OR=9.602,P>0.05)为MDS患者3年OS的危险因素,IPSS-R分级低危(OR=0.042,P>0.05)和中危(OR=0.131,P>0.05)为保护因素,见表2。
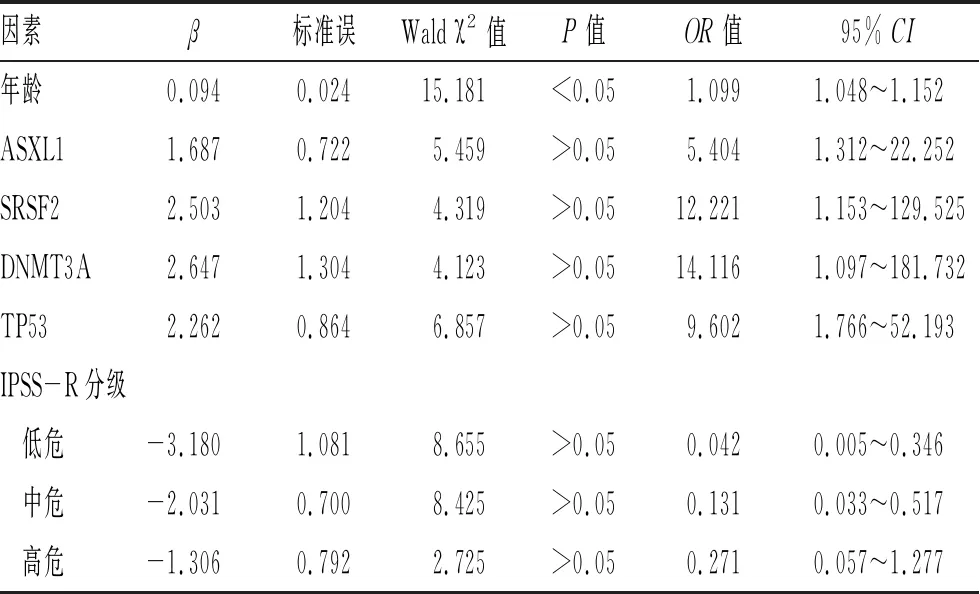
表2 MDS患者3年OS相关因素COX回归分析结果
2.3 列线图模型及校正曲线:将MDS患者3年OS相关因素纳入列线图,预测OS相关因素的C-index为0.921(95%Cl0.881~0.939)。
3 讨论
不同MDS患者预后和治疗效果差异较大,这对预后预测和治疗方案选择都是巨大挑战。近年来越来越多的研究证实MDS的生存期、治疗反应率、转白血病情况、治疗效果与部分基因突变相关[5]。建造一个纳入多种高频突变基因为因素的预测模型将有助于精确个体化治疗。
本研究中死亡组年龄高于存活组,年龄为MDS患者3年OS的独立危险因素。老年MDS患者治疗过程中并发症较多,死亡风险较高。但老年患者较年轻患者多倾向于保守治疗或放弃,这一差异影响了研究群体的年龄结构,造成结果偏倚。IPSS-R分级在衡量病情和预后上发挥着重要作用。本研究观察到死亡组和存活组IPSS-R分级存在统计学差异,IPSS-R分级低危和中危为3年OS的保护因素。相关研究报道IPSS-R极低危组至极高危组的中位OS分别为105.6、63.6、36.0、19.2、9.6个月[6],但临床工作中发现同一IPSS-R分级患者之间治疗敏感性和总生存期也具有明显差异,预后预测需要进一步精确化。
本研究中死亡组ASXL1、SRSF2、DNMT3A、TP53突变例数均高于存活组,四者为MDS患者3年OS的危险因素。MDS进展是一个涉及多基因的过程,TET2、DNMT3A、ASXL1与患者转白密切相关[7],其中ASXL1已被证实是MDS不良预后因素[8]。有研究报道TP53是MDS预后危险因素,伴有TP53突变的复杂核型MDS患者即使行allo-HSCT治疗,大部分也会死于早期复发[9]。Wu等[10]报道伴有SRSF2突变的MDS患者OS显著缩短,其为OS独立影响因素,支持了本研究结果。本研究建立的预测模型C-index为0.921,可见其具有显著应用意义,并发挥了突变基因在个体水平上预测预后的临床价值。但本研究样本较少,不利于检测出更多与预后相关的基因突变,有待进一步扩展。MDS患者ASXL1、SRSF2、DNMT3A、TP53基因突变与OS相关,基于多种突变基因构建的列线图可实现MDS预后预测精确化,为改善个体化治疗和延长总体生存提供新的策略。
