丁香酚在生物质半焦催化下的转化行为
2021-03-31黄勇刘沙沙吴益霜周建斌张书
黄勇,刘沙沙,吴益霜,周建斌,张书
(南京林业大学材料科学与工程学院,南京 210037)
生物质热转化技术是将低品位的生物质通过热化学反应向高品位能源转化的高值化利用方式,主要分为热解、气化和直接液化3种[1-2]。热解因高效率、低成本等优点成为最有前途的热转化技术之一。其中,快速热解在中等热解温度下所得的生物油产量可达70%,具有作为液体烃类原料补充原油的潜力。然而,初级热解生成的生物油因含氧量高、腐蚀性强、热稳定性差等特点,作为燃料油使用时受到一定的限制。催化热解能够改善生物油品质,但催化剂的选择对催化热解影响很大。天然矿石(如白云石、橄榄石等)作为价廉易得的催化剂,却因其催化性能和强度低未获得广泛应用;而人工开发的催化剂(如镍基、贵金属等)具有优越的催化性能,但成本高、易结焦失活[3-4]。因此,采用热解过程中自产的生物质半焦作为生物油提质的催化剂,具有简单易得、廉价等特点,更有利于产业化利用[5]。
生物质半焦的催化性能受孔隙结构、表面活性基团以及所含金属元素等协同影响。Lee等[6]利用生物质半焦催化转化生物油中苯酚时发现,生物质半焦表面活性官能团与酚羟基通过氢键所形成的过渡态在催化过程中起主导作用。Feng等[7]在同一条件下比较了3种生物质半焦对酸洗稻壳气化焦油的催化重整效果,结果表明,催化效果与半焦含有的碱金属和碱土金属的含量完全不成正比,半焦自身结构(孔隙结构)和碳结构对催化作用具有重要影响。Huang等[8]进一步研究发现,灰分含量极低的生物质半焦能够有效促进生物油挥发组分间的相互作用,实质上是半焦表面活性官能团(—OH、—COO等)在催化热解组分反应中作为活性位点起着关键性作用。
笔者以木质素衍生的丁香酚作为生物油模型化合物,重点探究丁香酚在生物质半焦催化作用下的转化途径,并结合产物分布和反应前后生物质半焦结构变化规律,理解生物质半焦表面基团与丁香酚的相互作用机制,为生物质半焦的催化性能优化提供相关的理论基础。
1 材料与方法
1.1 试验材料
典型木质素模型化合物(丁香酚,纯度99%),购于上海阿拉丁生化科技股份有限公司。
生物质半焦制备:选取粒径过40~60目(孔径0.30~0.45 mm)的松木屑原料,经干燥后置于管式炉中热解;热解过程在氮气(99.99%)氛围下进行,气体流量为200 mL/min,热解温度设定400和600 ℃,保温时间2 h;待冷却至室温后取出半焦样品,分别标记为400BC和600BC,经催化反应后的半焦样品对应标记为400BC-H和600BC-H,其元素和工业分析结果如表1所示。
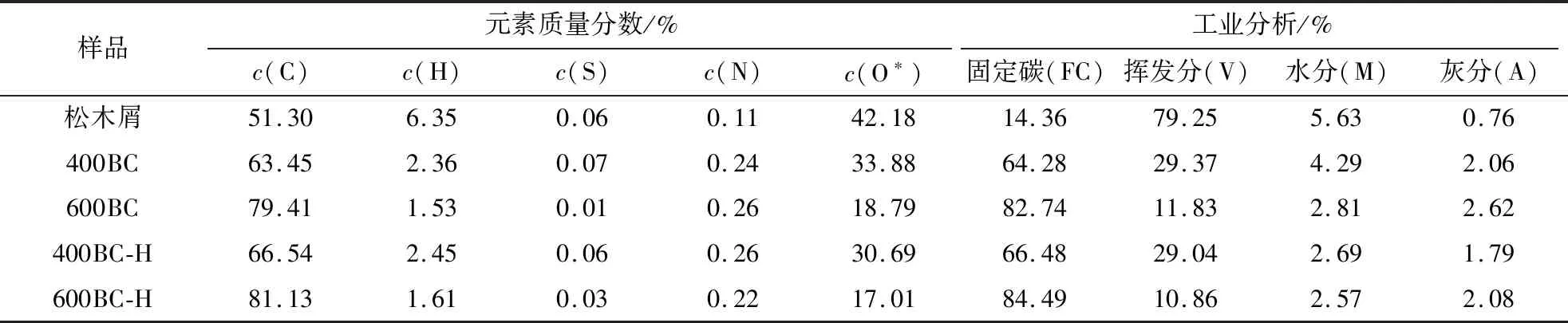
表1 生物质半焦催化反应前后的元素与工业分析Table 1 Ultimate and proximate analysis of bio-char before and after catalytic reaction
1.2 试验设备
催化热解实验装置如图1所示。丁香酚通过液相泵从石英反应器顶端注射,通过T1受热挥发后与热解区的生物质半焦发生相互作用。反应过程在氮气氛围下进行,气体流量为200 mL/min。其中,丁香酚的注射速率为5 mL/h,T1温度设定255 ℃以确保上端液态组分全部以气态的形式存在于反应器中,注射量为2 mL,反应过程需24 min;T2反应温度结合原料特性设定为400 ℃;半焦用量为5 g左右;液体冷凝主要采用二级冷凝,即第1级为冰水浴,第2级采用液氮与工业酒精的混合物冷凝,温度控制在-70 ℃左右。
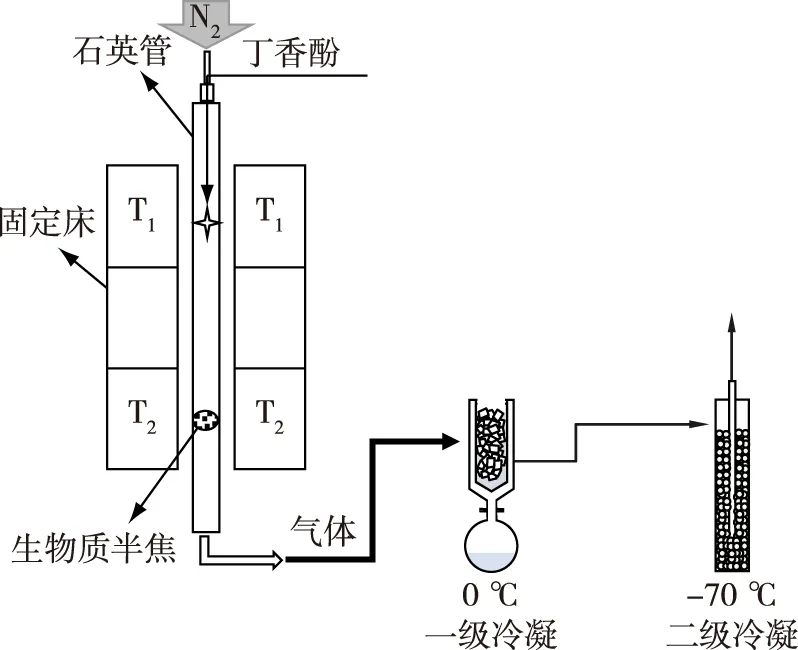
图1 催化热解实验装置Fig.1 The experimental equipment for catalytic pyrolysis
1.3 试验方法
1.3.1 热解产物分析
催化反应后收集的液体利用色谱级丙酮溶液按照体积比1∶3进行稀释,接着采用气相色谱质谱仪(GC-MS)考察产物成分及含量分布。分析进样时分流比为100∶1,使用HP-5MS毛细管柱(长度×内径×膜厚=30 m×0.25 mm×0.25 μm)进行产物分离,升温程序如下:温度40 ℃保持2 min,接着以5 ℃/min的速度升至200 ℃,再以10 ℃/min的速率加热到280 ℃并保持3 min。质谱(MS)以70 eV的电子能在EI模式下运行,质荷比(m/z)的扫描范围为50~300。根据美国国家标准技术研究所NIST11谱库进行检索,通过峰面积百分比获得热解产物成分及相对含量。
1.3.2 半焦结构表征
X-射线光电子能谱分析(XPS):采用AXIS UltraDLD型X-射线光电子能谱仪(日本岛津)分析半焦焦样中表面碳和氧的元素特征。
红外光谱分析(FT-IR):采用KBr压片法,半焦焦样与KBr混合质量比为1∶100,利用VERTEX80V型红外光谱仪(德国Bruker)透射试验,扫描16次,扫描范围400~4 000 cm-1,分析半焦反应前后的表面官能团变化。
拉曼分析(Raman):采用DXR532型拉曼光谱仪(美国Thermo)测定半焦中非晶态碳结构,激发激光波长为780 nm,功率为24 mW。
2 结果与分析
2.1 催化作用下的产物分析
丁香酚作为生物质热解产物中具有典型木质素单元结构的有机化合物,对其催化热解过程的研究甚少。笔者从生物质半焦催化角度出发考察其热分解后的产物含量和产物生成途径。由于生物质半焦的制备温度为400和600 ℃,为了避免较高温度下生物质半焦残留挥发分的析出,统一反应温度为400 ℃,催化热解反应后的产物含量及分布如图2所示。由图2可知,在无半焦催化剂(Blank)作用时,GC-MS检测到的物质大部分仍是丁香酚,其分解产物较少,仅形成4-丙烯基苯酚和丁香酚甲醚。然而,在生物质半焦催化作用下能够显著地促进丁香酚内部结构发生转化,主要是自身化学键中双键位置的改变,即生成顺反异丁香酚(图2中产物3和4),且在400BC和600BC的催化作用下其含量占热解产物的66.7%和60.1%。异丁香酚作为配制香料和制备香兰素的重要原料,应用极为广泛。传统的丁香酚异构化反应通常需要在污染严重的高温浓碱条件下或采用贵金属催化剂。何金义等[9]通过Pd (Ⅱ)催化丁香酚异构化反应时,生成顺反异丁香酚的收率为96.3%。此外,根据产物分布可知,400BC催化效果明显高于600BC,且与丁香酚作用生成的香草醛(产物6)是世界上需求量最大的单体香料之一。

图2 丁香酚催化热解后的产物分布Fig.2 Distribution of products after catalytic pyrolysis for eugenol
探究丁香酚热解转化途径对理解生物质半焦催化行为起到关键性作用。热解过程中丁香酚可能的转化途径如图3所示。Huang等[10]研究发现甲氧基—OCH3醚键中的键解离能最小,这与Ledesma等[11]计算得到的丁香酚中可能的键断裂反应相似,其键解离能如表2所示。由表2可以看出,甲氧基中的化学键1的键解离能最小,结合图3中路径3,化学键断裂后与氢自由基结合脱羟基后形成4-丙烯基苯酚(化合物1);而化学键3经断裂后通过与氢自由基结合也形成化合物1,由于化学键3解离能明显比化学键1高,因此主要是以化学键1断裂的形成过程为主。
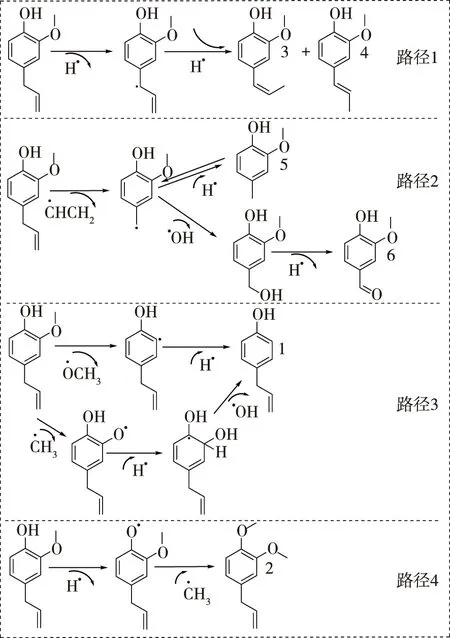
图3 丁香酚的转化路径Fig.3 Distribution of products after catalytic pyrolysis for eugenol

图4 半焦焦样的XPS分峰图Fig.4 The peak spectrum of bio-char by XPS
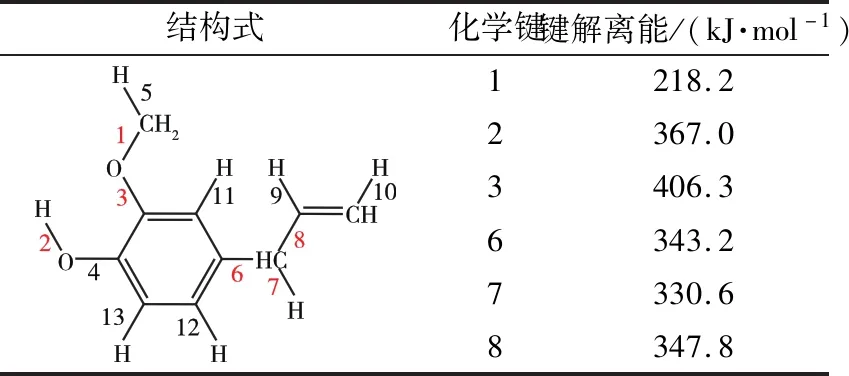
表2 丁香酚的键解离能Table 2 Bond dissociation energy of eugenol

2.2 半焦的结构表征
2.2.1 XPS分析
由于热解温度对生物质半焦的形态、化学结构及自由基浓度等有很大影响[12-13],笔者对半焦结构进行进一步表征。半焦催化剂的表面碳和氧元素组成及其结合方式对其催化性能有重要的作用,400BC和600BC焦样中O1s和C1s光谱分析结果如图4所示。

2.2.2 FT-IR分析


图5 半焦催化反应前后的FT-IR图Fig.5 FT-IR spectrum of bio-char before and after catalytic reaction
通过半焦反应前后对比发现,催化反应后的半焦中—OH 官能团含量明显降低。Meng等[18]指出,碳基材料中具有的主要含氧官能团的反应活性顺序为羟基>羧基,这也更好地解释丁香酚在半焦催化作用下通过—OH中的氢键相互作用其催化效果强于—COO,与上述XPS分析中的结果一致。此外,反应前后400BC中含有的官能团峰值明显减弱,更加说明了400BC有利于丁香酚催化反应的进行。随着反应的进行,半焦的催化活性也明显降低,表1中也能明显观察到反应前后半焦的氧含量呈现逐渐减少的趋势。同时,表1中反应前后半焦炭含量的升高,说明丁香酚在半焦表面发生了一定程度的碳化,从而覆盖了半焦表面活性位,也导致半焦活性的下降。此外,冯冬冬[19]指出半焦自身的碳结构也存在一些活性位点,从而表现出一定的催化活性。
2.2.3 Raman分析
为了测定上述半焦中碳结构的活性来源,对半焦进行了拉曼分析,结果如图6所示。根据拉曼光谱分峰拟合,主要由10个谱峰表达半焦焦样的芳环系统的结构特性,其中G、GR、VL、VR、D峰分析半焦的主要结构特性,其余峰起到分峰拟合过程中协助拟合效果的作用。拉曼曲线中用I(GR+VL+VR)/ID面积比值表示小芳环结构(芳环数≤5)与大芳环结构(芳香环数≥6)的比值,作为评价半焦焦样表面的芳香性[20]。当催化剂制备温度从400 ℃升至600 ℃时,I(GR+VL+VR)/ID比值则从1.64降至1.46,表明半焦内的小芳环结构减少。考虑到600BC的催化活性较弱,说明其本身碳结构中的小芳环对催化性能也起到重要的作用。
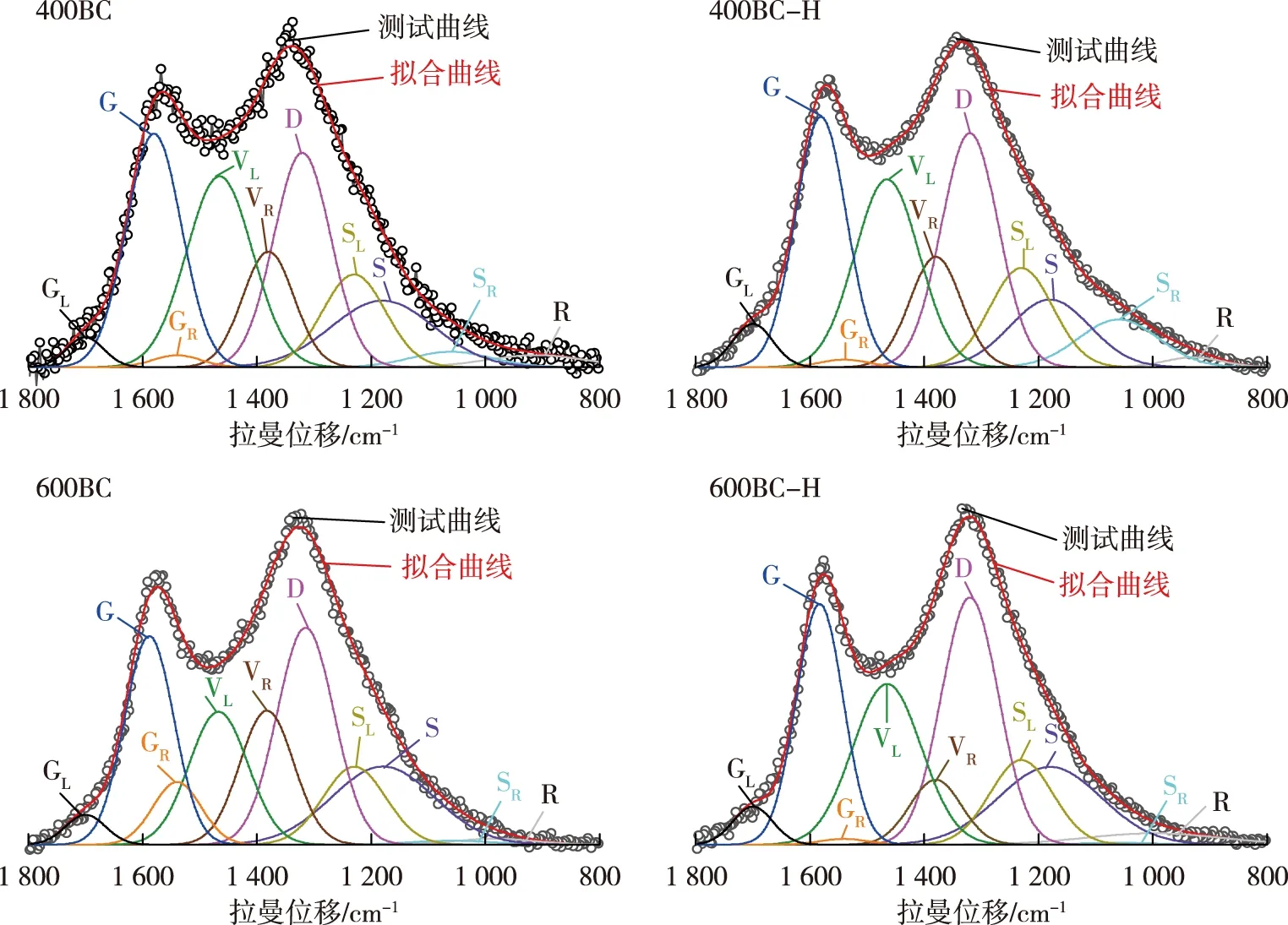
图6 半焦的拉曼曲线峰拟合Fig.6 Raman curve peak fitting of bio-char
碳结构中的小芳环和丁香酚中的苯环可通过π-π堆积效应相互作用,从而改变丁香酚分子的电子云密度分布,促使反应进行。催化反应后400BC和600BC的I(GR+VL+VR)/ID比值都呈现显著下降趋势(400BC为1.35,600BC为1.04),说明半焦与丁香酚催化作用时,半焦炭结构中的活性位点小芳环结构被消耗,促进了向大芳环结构的转化,导致半焦表面的芳香性增强,从而使催化反应后的半焦催化活性降低。
综上所述,丁香酚在生物质半焦催化作用下明显促进了异构化反应过程。一方面,半焦表面的—OH 和—COO等含氧官能团通过氢键与丁香酚中—OH或苯环发生相互作用后,导致电子迁移,从而起到催化热解的作用;另一方面,半焦中的碳结构和丁香酚中的苯环还可以通过π-π堆积效应促进反应的发生。丁香酚在生物质半焦催化作用下的转化行为见图7。

图7 半焦官能团的作用机理Fig.7 The mechanism of action of bio-char functional groups
3 结 论
1)在催化反应过程中,生物质半焦能够明显促进丁香酚的转化,热解产物主要为异构化反应生成的异丁香酚和侧链烯丙基断裂形成的香草醛,且400BC的催化效果明显高于600BC。
2)通过FT-IR和XPS表征分析可知,半焦中的—OH官能团通过氢键的相互作用对丁香酚的分解起重要的促进作用,且400BC催化效果优于600BC;Raman分析表明半焦炭结构中的小芳环具有一定的催化活性,半焦制备温度越高,小芳环含量就越低,从而催化活性就越低。此外,催化反应消耗了半焦炭结构中的小芳环,也使其活性降低。
