草乌甲素片治疗轻中度癌痛多中心、随机对照、非劣效性研究 *
2021-03-29李宝兰吴晓明李萍萍
王 薇 李 杰 刘 航 孙 红 李宝兰 吴晓明 李萍萍
(1 北京大学肿瘤医院暨北京市肿瘤防治研究所中西医结合科,恶性肿瘤发病机制及转化研究教育部重点实验室,北京100142;2 首都医科大学附属医院胸科医院综合科,北京101149;3 北京市朝阳区桓兴肿瘤医院麻醉科,北京100005;4 中国医学科学院肿瘤医院综合科,北京100021)
癌性疼痛 (cancer pain) 是癌症病人最常见的症状之一,约有1/4 新诊断恶性肿瘤的病人、1/3 正在接受治疗的病人以及3/4 晚期肿瘤病人合并疼痛。目前镇痛治疗仍然遵循WHO 三阶梯镇痛原则。在推广癌痛规范化治疗中,我们发现临床中存在过渡使用非甾体消炎镇痛药(NSAIDs)及NSAIDs 药物滥用的问题,NSAIDs 药物镇痛疗效具有“天花板效应”,并且具有明显的不良反应,临床应用存在很多限制。以弱阿片类为代表的第二阶梯药物由于其类似阿片类药物的不良反应,病人对其耐受性、依从性较差,在临床使用中一直难以推广。这些都是推行癌痛规范化治疗面临的困境,因此迫切需要提供疗效确切、不良反应少的镇痛药物,丰富三阶梯药物的选择,以满足病人舒适镇痛的需求。中医中药在我国有着悠久的历史,深受广大病人的认可,现实中癌痛病人使用中医中药控制疼痛是普遍现象,中药具有不良反应少的优势,但是临床实际应用不规范,缺少循证医学依据[1]。尽管中医药治疗轻中度癌痛相关报道已经较多,但大多数设计不够严谨,难以提供高级别的循证医学证据。草乌甲素用于治疗关节炎相关慢性疼痛,对于轻中度疼痛的镇痛作用确切,不良反应较少。本研究是首次进行的草乌甲素(bulleyaconitine A)单药治疗轻中度癌痛的随机、对照、非劣效性临床研究,目的是证实草乌甲素与第一阶梯、第二阶梯镇痛药物比较,疗效相等、不良反应更少,为癌痛病人提供更多舒适镇痛的药物选择,惠及更多癌痛病人。
方 法
1. 一般资料
本研究经北京大学肿瘤医院医学伦理委员会批准,从2016 年3 月至2019 年10 月在北京市三家研究中心筛选符合纳入标准的入组病例:轻度癌痛共36 例,去除出组病例(3 例)、脱落病例(1 例)后,实际完成研究病例共32 例(对照组16 例,试验组16 例);中度癌痛共68 例,去除出组病例(3 例)、脱落病例(2 例)后,实际完成研究病例共63 例(对照组29 例,试验组34 例)。脱落率轻度组2.78%,中度组2.94%。所有病人均签署知情同意书,各参与中心入组情况见表1。
纳入标准:①病理诊断明确的恶性肿瘤病人(原发性肝癌可以临床诊断),预计生存期≥3 个月;②年龄≥18 岁,性别不限;③疼痛数字评分法(numeric rating scales, NRS)评分1~6 分、未使用阿片类药物;④入组前1 周内至观察期结束,未进行新方案化疗或新方案靶向治疗以及疼痛部位的放疗。既往周期性化疗无明显不良反应干扰本研究结果;⑤血小板、天冬氨酸转氨酶、丙氨酸氨基转移酶、肌酐在正常值范围内,心电图正常或大致正常;⑥病人神志清楚,阅读、理解能力正常,同意入组,并签署知情同意书。
排除标准:①有活动性消化道出血的病人;②正在使用华法林或肝素抗凝治疗的病人;③已知对乌头碱、非甾体消炎镇痛药过敏的病人;④妊娠及哺乳期妇女;⑤与手术、操作、治疗相关的急性疼痛。
剔除标准:①研究过程中出现不可耐受的不良反应,终止用药,判定为提前出组;②研究过程中出现严重脏器功能损害,终止用药,判定为提前出组;③病人拒绝继续用药或失访,判定为脱落;④经研究者判断病人病情不适于继续参加本研究,终止用药,判定为提前出组。
基线调查结果显示(见表2),在轻度癌痛病人以及中度癌痛病人两组中,对照组和试验组在病人年龄、性别、体重指数(body mass index, BMI)等方面的分布均匀,两组间无统计学差异;两组在疼痛性质、ID-PAIN 量表评估中也基本一致,轻度癌痛病人中对照组“牵拉痛”比例高于试验组(P < 0.05),中度癌痛病人中试验组 “胀痛”的比例高于对照组(P < 0.05)。
2.治疗方法
(1)随机方法:使用随机数字表进行区组随机,区组长度为4,为轻度和中度癌痛病人分别设计随机分组表,由总中心登记入组。轻度癌痛病人、中度癌痛病人均是1:1 分入对照组和试验组。
(2)镇痛治疗方案:轻度癌痛病人,对照组口服布洛芬缓释胶囊(芬必得,中美天津史克制药有限公司生产)每粒0.3 g、每日2 次、每次1 粒治疗;试验组口服草乌甲素片(赛福美,云南昊邦制药有限公司生产)每片0.4 mg、每日2 次、每次1 片治疗,两次之间的间隔至少6 h。
中度癌痛病人,对照组口服曲马多缓释片(奇曼丁,萌蒂(中国)制药有限公司生产)每片0.1 g、每12 h 1次、每次1片治疗;试验组口服草乌甲素片(赛福美,云南昊邦制药有限公司生产)每片0.4 mg、每日3 次、每次1 片治疗,两次之间的间隔至少6 h。
观察期间若病人出现NRS ≥4 分的爆发痛时可以考虑给予短效药物解救治疗。若病人每日需要处理的爆发痛的次数超过3 次,由研究者评估是否由于镇痛治疗无效所致。若考虑镇痛治疗效果不足以控制疼痛,则该病人判定为无效出组,进行重新评估、调整镇痛治疗方案。
(3)不良反应处理:不预期处理镇痛药物的不良反应(包括便秘),若病人出现不良反应,详细记录,再给予对症治疗。
(4)观察时间:连续服药7 天,每日观察。
3. 疗效评定
(1)一般资料:记录病人性别、年龄、诊断、分期、疼痛性质等一般资料。
(2)疼痛指标:在观察期每日疼痛采用NRS评估并记录平均疼痛评分,将处理的爆发痛次数记录。中度癌痛病人在基线和观察结束后使用简明疼痛量表(brief pain inventory, BPI)全面评估疼痛情况。以BPI 中病人的最重疼痛、最轻疼痛、平均疼痛评分(NRS)为指标,对比对照组与试验组是否疗效相当。
(3)不良反应:记录病人治疗期间出现的不良反应并判断是否与本研究用药有关。对比对照组与试验组是否存在差异。
(4)生活质量指标:中度癌痛病人在基线和观察结束后使用EORTC 生命质量测定量表 QLQ-C30 (qual-ity of life questionnaire-core 30, QOL-C30) (V3.0)进行生活质量评估。 QOL-C30 包括5 个功能领域(躯体、角色、认知、情绪和社会功能)、3 个症状领域(疲劳、疼痛、恶心呕吐)、1 个总体健康状况/生命质量领域和6 个单一条目,转化为标准化得分进行比较。对于功能领域和总体健康状况领域,得分越高表示功能或健康水平越好;对于症状领域得分,得分越高表示症状或问题越多(生命质量越差)。
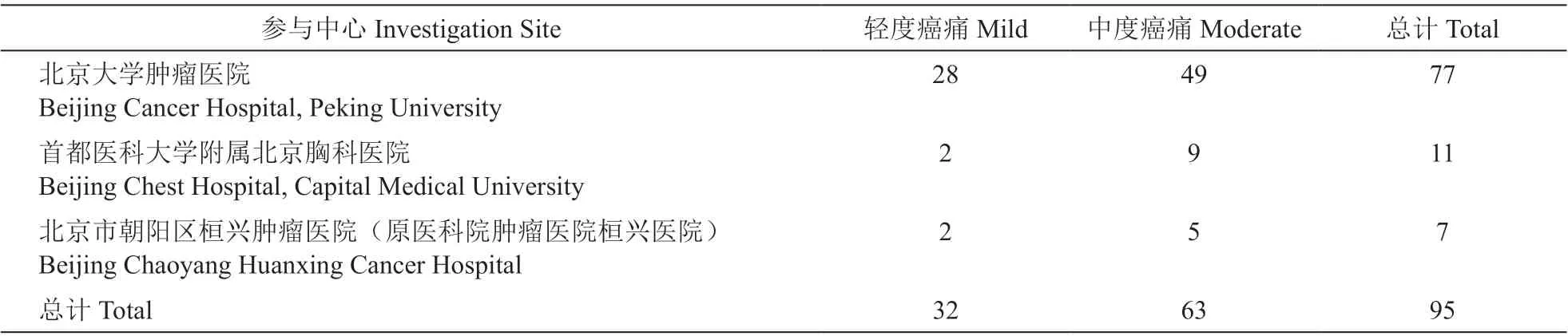
表1 参与中心入组情况Table1 Participation in the investigation site
表2 两组的基线一般情况比较(±SD)Table 2 General conditions were compared between the control group and the experimental group (±SD)
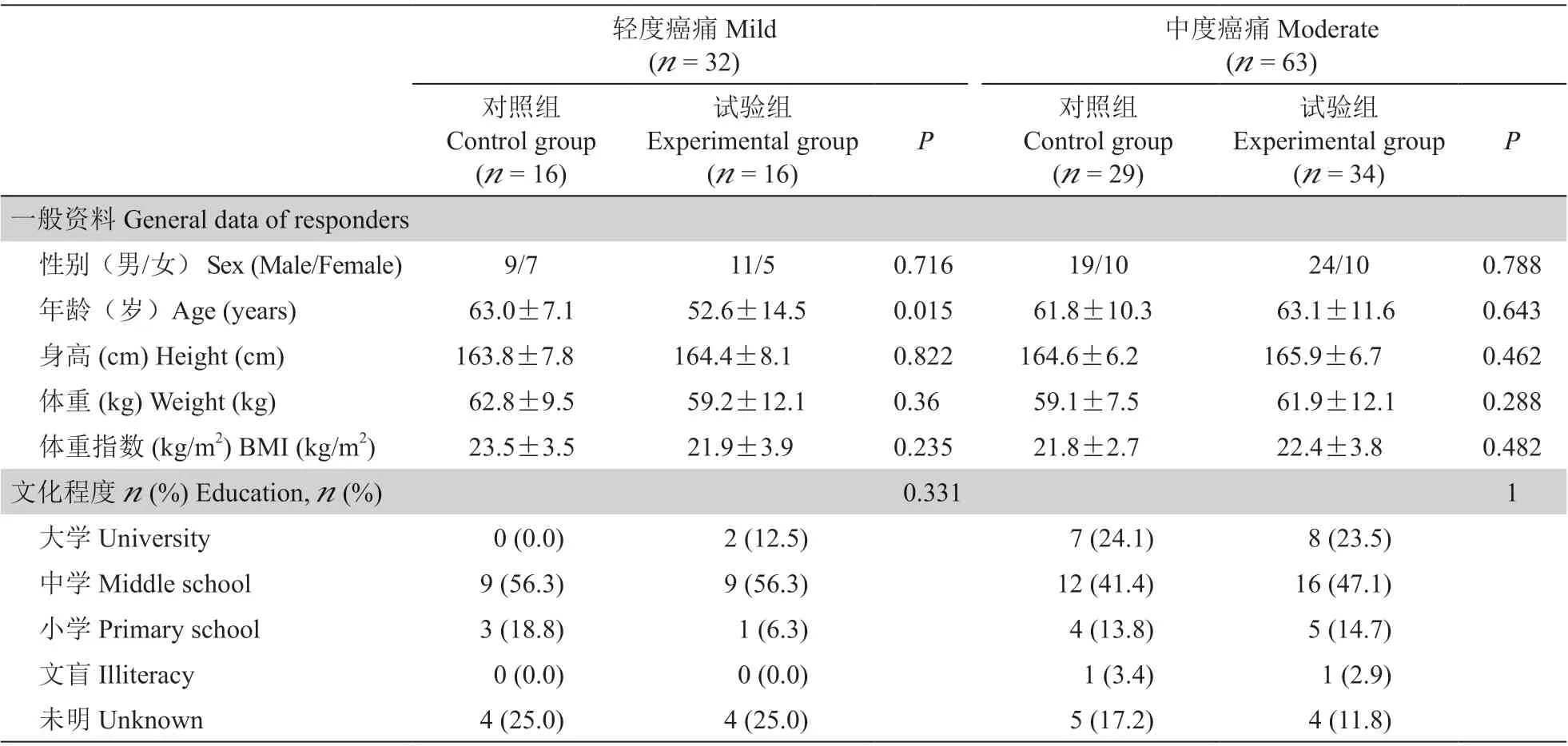
表2 两组的基线一般情况比较(±SD)Table 2 General conditions were compared between the control group and the experimental group (±SD)
轻度癌痛Mild(n = 32)中度癌痛Moderate(n = 63)对照组Control group(n = 16)试验组Experimental group(n = 16)P对照组Control group(n = 29)试验组Experimental group(n = 34)P一般资料General data of responders 性别(男/女) Sex (Male/Female) 9/7 11/5 0.716 19/10 24/10 0.788年龄(岁)Age (years) 63.0±7.1 52.6±14.5 0.015 61.8±10.3 63.1±11.6 0.643身高(cm) Height (cm) 163.8±7.8 164.4±8.1 0.822 164.6±6.2 165.9±6.7 0.462体重(kg) Weight (kg) 62.8±9.5 59.2±12.1 0.36 59.1±7.5 61.9±12.1 0.288体重指数(kg/m2) BMI (kg/m2) 23.5±3.5 21.9±3.9 0.235 21.8±2.7 22.4±3.8 0.482文化程度n (%) Education, n (%) 0.331 1大学University 0 (0.0) 2 (12.5) 7 (24.1) 8 (23.5)中学Middle school 9 (56.3) 9 (56.3) 12 (41.4) 16 (47.1)小学Primary school 3 (18.8) 1 (6.3) 4 (13.8) 5 (14.7)文盲Illiteracy 0 (0.0) 0 (0.0) 1 (3.4) 1 (2.9)未明Unknown 4 (25.0) 4 (25.0) 5 (17.2) 4 (11.8)
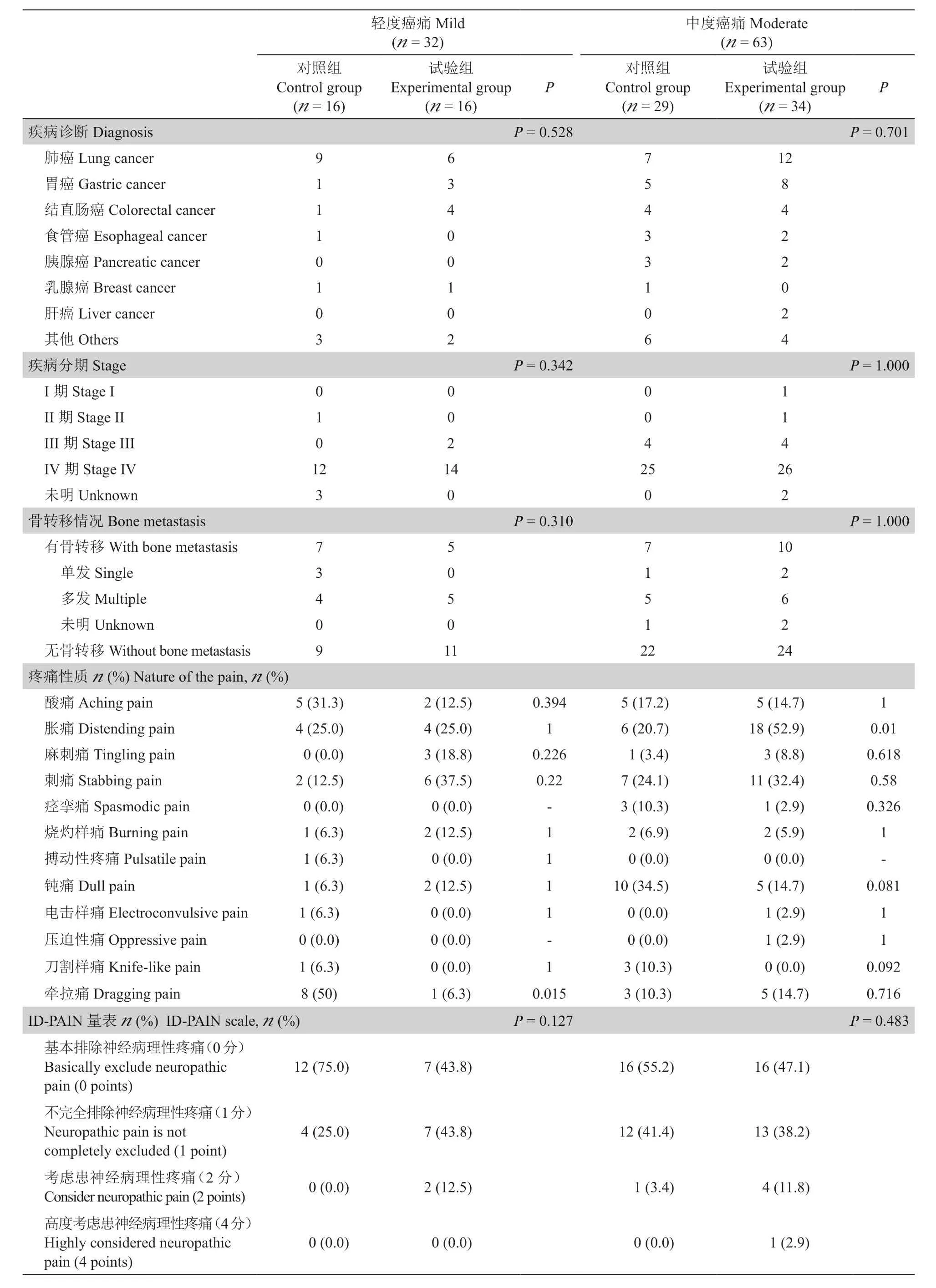
轻度癌痛Mild(n = 32)中度癌痛Moderate(n = 63)对照组Control group(n = 16)试验组Experimental group(n = 16)P对照组Control group(n = 29)试验组Experimental group(n = 34)P疾病诊断Diagnosis P = 0.528 P = 0.701肺癌Lung cancer 9 6 7 12胃癌Gastric cancer 1 3 5 8结直肠癌Colorectal cancer 1 4 4 4食管癌Esophageal cancer 1 0 3 2胰腺癌Pancreatic cancer 0 0 3 2乳腺癌Breast cancer 1 1 1 0肝癌Liver cancer 0 0 0 2其他Others 3 2 6 4疾病分期Stage P = 0.342 P = 1.000 I 期Stage I 0 0 0 1 II 期Stage II 1 0 0 1 III 期Stage III 0 2 4 4 IV 期Stage IV 12 14 25 26未明Unknown 3 0 0 2骨转移情况Bone metastasis P = 0.310 P = 1.000有骨转移With bone metastasis 7 5 7 10单发Single 3 0 1 2多发Multiple 4 5 5 6未明Unknown 0 0 1 2无骨转移Without bone metastasis 9 11 22 24疼痛性质n (%) Nature of the pain, n (%)酸痛Aching pain 5 (31.3) 2 (12.5) 0.394 5 (17.2) 5 (14.7) 1胀痛Distending pain 4 (25.0) 4 (25.0) 1 6 (20.7) 18 (52.9) 0.01麻刺痛Tingling pain 0 (0.0) 3 (18.8) 0.226 1 (3.4) 3 (8.8) 0.618刺痛Stabbing pain 2 (12.5) 6 (37.5) 0.22 7 (24.1) 11 (32.4) 0.58痉挛痛Spasmodic pain 0 (0.0) 0 (0.0) - 3 (10.3) 1 (2.9) 0.326烧灼样痛Burning pain 1 (6.3) 2 (12.5) 1 2 (6.9) 2 (5.9) 1搏动性疼痛Pulsatile pain 1 (6.3) 0 (0.0) 1 0 (0.0) 0 (0.0) -钝痛Dull pain 1 (6.3) 2 (12.5) 1 10 (34.5) 5 (14.7) 0.081电击样痛Electroconvulsive pain 1 (6.3) 0 (0.0) 1 0 (0.0) 1 (2.9) 1压迫性痛Oppressive pain 0 (0.0) 0 (0.0) - 0 (0.0) 1 (2.9) 1刀割样痛Knife-like pain 1 (6.3) 0 (0.0) 1 3 (10.3) 0 (0.0) 0.092牵拉痛Dragging pain 8 (50) 1 (6.3) 0.015 3 (10.3) 5 (14.7) 0.716 ID-PAIN 量表n (%) ID-PAIN scale, n (%) P = 0.127 P = 0.483基本排除神经病理性疼痛(0 分)Basically exclude neuropathic pain (0 points)12 (75.0) 7 (43.8) 16 (55.2) 16 (47.1)不完全排除神经病理性疼痛(1分)Neuropathic pain is not completely excluded (1 point)4 (25.0) 7 (43.8) 12 (41.4) 13 (38.2)考虑患神经病理性疼痛(2 分)Consider neuropathic pain (2 points) 0 (0.0) 2 (12.5) 1 (3.4) 4 (11.8)高度考虑患神经病理性疼痛(4分)Highly considered neuropathic pain (4 points)0 (0.0) 0 (0.0) 0 (0.0) 1 (2.9)
4. 统计学分析
使用SPSS 16.0 进行统计学分析,以均数±标准差(±SD)表示。计量资料t 检验,计数资料使用卡方检验。以P < 0.05 为差异具有统计学意义。
结 果
1.疼痛指标
(1)观察期间每日平均疼痛评分变化:观察期间每日于固定时间记录平均疼痛评分(见表3),轻度癌痛病人对照组与试验组的评分两组之间无差异。中度癌痛病人每日平均疼痛评分对照组与试验组在第4 天有差异,对照组低于试验组,两者之间的差异有统计学意义(P = 0.032),其余时间两组之间无差异。
(2)中度癌痛病人治疗前后BPI 量表评估结果的对比:通过BPI 量表对中度癌痛病人进行疼痛评估(见表4),在基线调查时和研究结束后,病人BPI 量表对照组和试验组之间无差异。
2. 不良反应
轻度癌痛病人中未记录到与治疗相关的不良反应。中度癌痛病人对照组共记录不良反应35 人次,其中14 人次与服药有关(便秘13 例次、排尿困难1 例次);试验组共记录不良反应18 人次,其中2人次与服药有关(口唇发麻2 例次)。试验组不良反应发生人次数明显低于对照组,差异有统计学意义(P < 0.001)。
3. 生活质量指标
中度癌痛病人的生活质量评估结果见表5。基线评估时,对照组和试验组功能领域得分没有差异。治疗结束时再次评估并,试验组情绪功能得分83.1±20.5,显著优于对照组的70.5±19.8 (P < 0.05)。从症状领域来看,在基线评估时两组无差异。治疗结束时再次评估,试验组的疼痛症状、腹泻症状得分(分别为8.3±19.9,19.8±32.6)显著低于对照组得分(分别为25±32.1,39.7±34)(P < 0.05),即症状更轻。但是总体健康状况方面,在治疗后对照组反而优于试验组(P < 0.05),这可能与在基线评估时对照组得分明显高于试验组有关。
讨 论
癌痛的药物治疗可选择的药物种类一直比较有限,在WHO 三阶梯原则指导下,通常以NSAIDs、阿片类药物(包括弱阿片类药物和强阿片类药物)两大类为主,以抗抑郁药物、抗惊厥药物等为辅助。NSAIDs 药物不良反应与滥用问题一直存在。而阿片类药物临床使用面临更多问题,许多病人使用时有顾虑,或由于其不良反应比较大而拒绝用药[2],这些是我国癌痛控制水平难以提高的原因之一。在资源丰富的中医药中寻找疗效确切、不良反应更少的药物,提高病人用药的依从性,可以解决部分临床用药的困境,进一步改善癌痛控制水平[3]。
表3 每日平均NRS 评分(±SD)Table 3 Daily average NRS score (±SD)
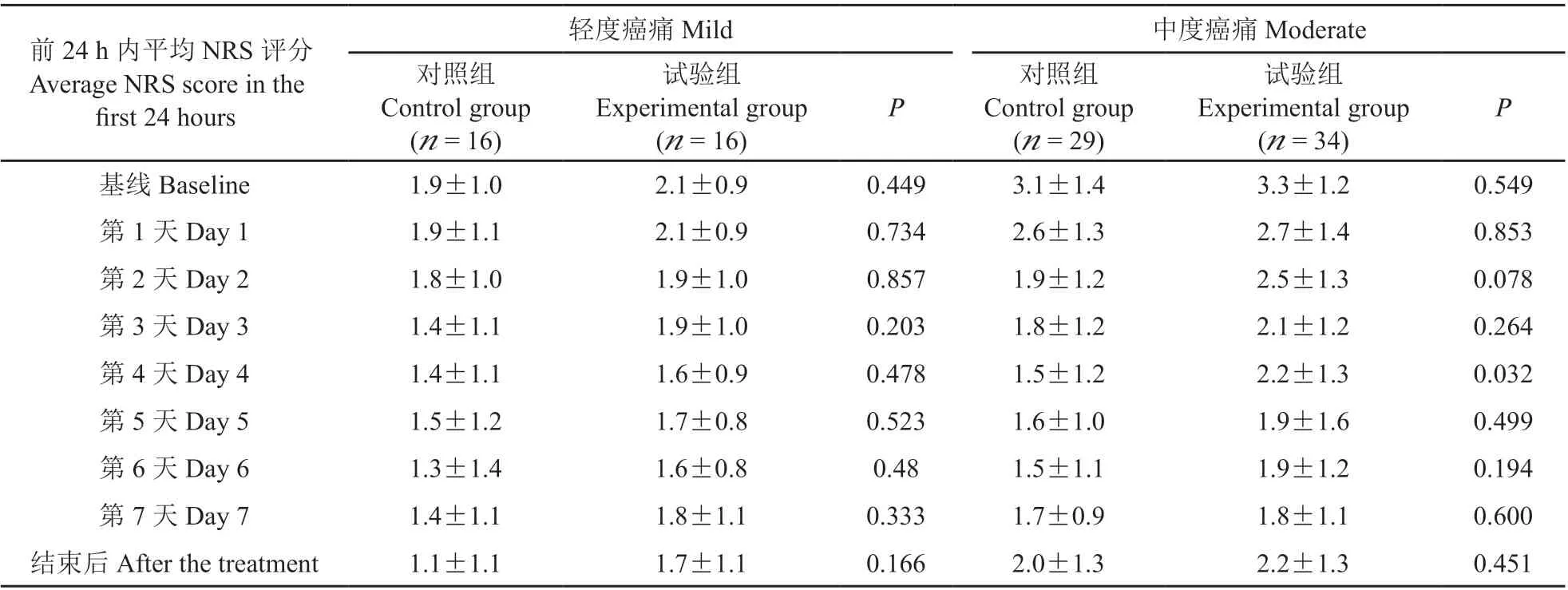
表3 每日平均NRS 评分(±SD)Table 3 Daily average NRS score (±SD)
前24 h 内平均NRS 评分Average NRS score in the first 24 hours轻度癌痛Mild 中度癌痛Moderate对照组Control group(n = 16)试验组Experimental group(n = 16)P对照组Control group(n = 29)试验组Experimental group(n = 34)P基线Baseline 1.9±1.0 2.1±0.9 0.449 3.1±1.4 3.3±1.2 0.549第1 天Day 1 1.9±1.1 2.1±0.9 0.734 2.6±1.3 2.7±1.4 0.853第2 天Day 2 1.8±1.0 1.9±1.0 0.857 1.9±1.2 2.5±1.3 0.078第3 天Day 3 1.4±1.1 1.9±1.0 0.203 1.8±1.2 2.1±1.2 0.264第4 天Day 4 1.4±1.1 1.6±0.9 0.478 1.5±1.2 2.2±1.3 0.032第5 天Day 5 1.5±1.2 1.7±0.8 0.523 1.6±1.0 1.9±1.6 0.499第6 天Day 6 1.3±1.4 1.6±0.8 0.48 1.5±1.1 1.9±1.2 0.194第7 天Day 7 1.4±1.1 1.8±1.1 0.333 1.7±0.9 1.8±1.1 0.600结束后After the treatment 1.1±1.1 1.7±1.1 0.166 2.0±1.3 2.2±1.3 0.451
表4 中度癌痛病人治疗前后的BPI 量表比较(±SD)Table 4 Comparison of BPI scale of patients with moderate cancer pain before and after treatment (±SD)
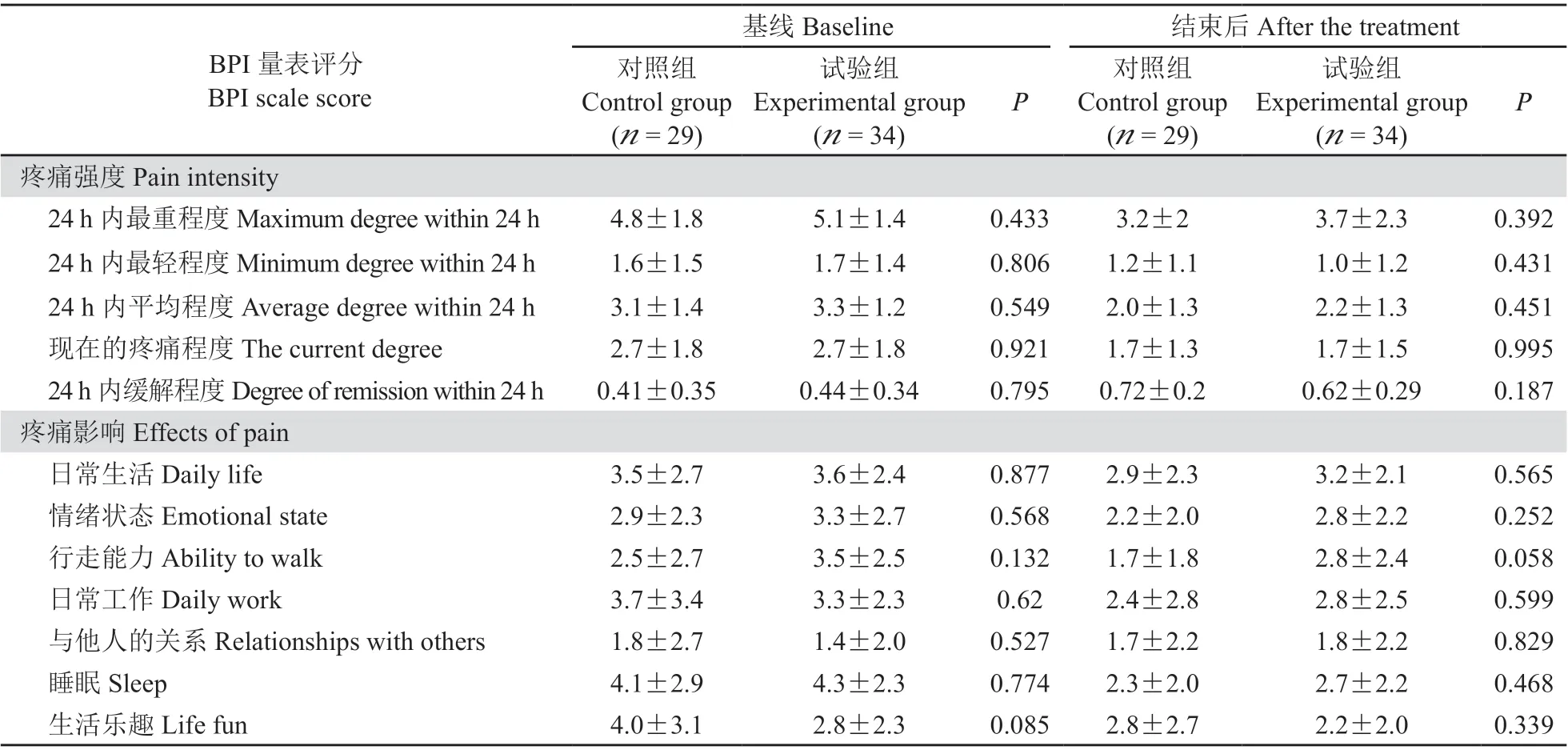
表4 中度癌痛病人治疗前后的BPI 量表比较(±SD)Table 4 Comparison of BPI scale of patients with moderate cancer pain before and after treatment (±SD)
基线Baseline 结束后After the treatment对照组Control group(n = 29)BPI 量表评分 BPI scale score试验组Experimental group (n = 34)P对照组Control group(n = 29)试验组Experimental group (n = 34)P疼痛强度Pain intensity 24 h 内最重程度Maximum degree within 24 h 4.8±1.8 5.1±1.4 0.433 3.2±2 3.7±2.3 0.392 24 h 内最轻程度Minimum degree within 24 h 1.6±1.5 1.7±1.4 0.806 1.2±1.1 1.0±1.2 0.431 24 h 内平均程度Average degree within 24 h 3.1±1.4 3.3±1.2 0.549 2.0±1.3 2.2±1.3 0.451现在的疼痛程度The current degree 2.7±1.8 2.7±1.8 0.921 1.7±1.3 1.7±1.5 0.995 24 h 内缓解程度Degree of remission within 24 h 0.41±0.35 0.44±0.34 0.795 0.72±0.2 0.62±0.29 0.187疼痛影响Effects of pain 日常生活Daily life 3.5±2.7 3.6±2.4 0.877 2.9±2.3 3.2±2.1 0.565情绪状态Emotional state 2.9±2.3 3.3±2.7 0.568 2.2±2.0 2.8±2.2 0.252行走能力Ability to walk 2.5±2.7 3.5±2.5 0.132 1.7±1.8 2.8±2.4 0.058日常工作Daily work 3.7±3.4 3.3±2.3 0.62 2.4±2.8 2.8±2.5 0.599与他人的关系Relationships with others 1.8±2.7 1.4±2.0 0.527 1.7±2.2 1.8±2.2 0.829睡眠Sleep 4.1±2.9 4.3±2.3 0.774 2.3±2.0 2.7±2.2 0.468生活乐趣Life fun 4.0±3.1 2.8±2.3 0.085 2.8±2.7 2.2±2.0 0.339
表5 中度癌痛病人治疗前后的生活质量量表比较(±SD)Table 5 Comparison of life quality scales of patients with moderate cancer before and after treatment pain (±SD)
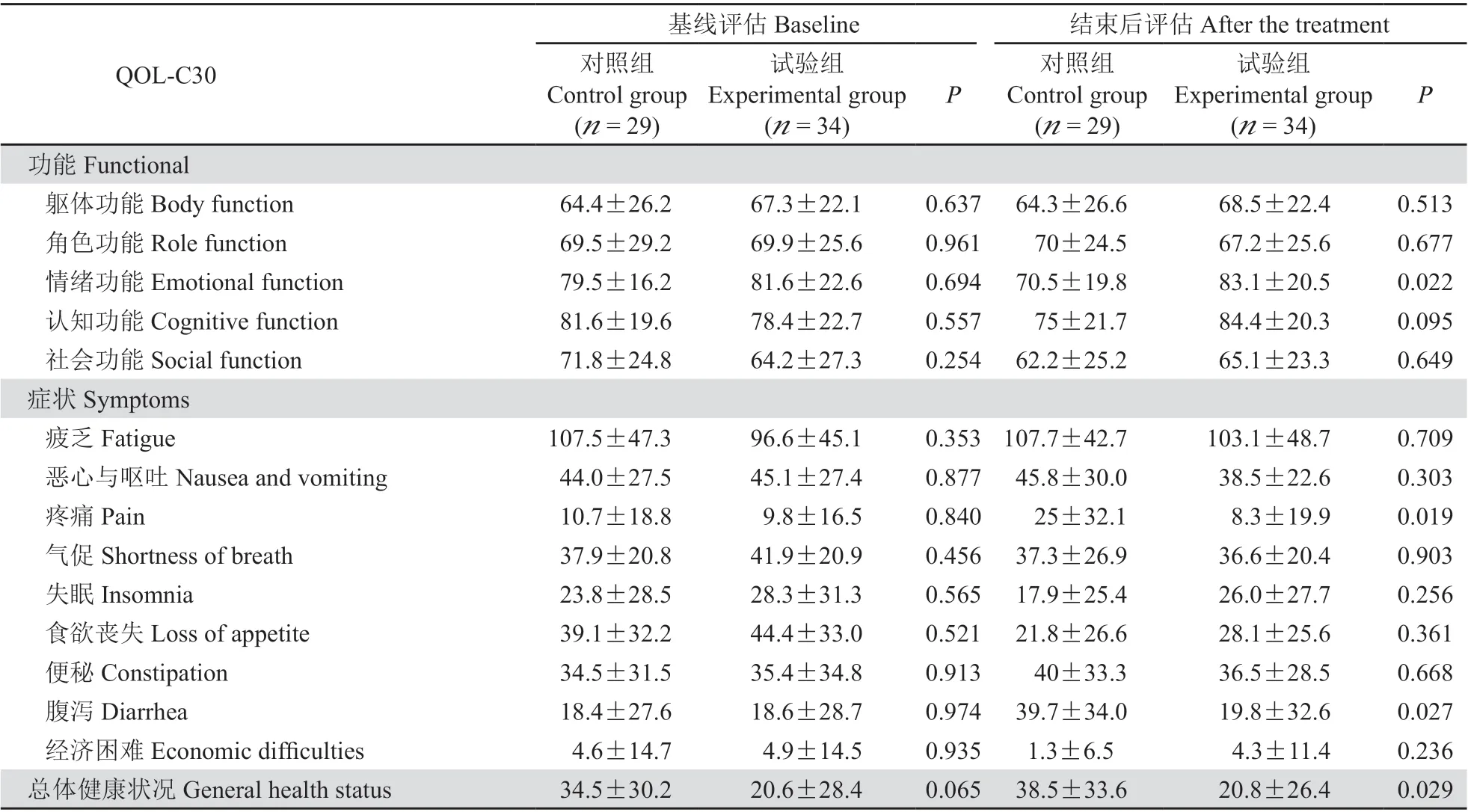
表5 中度癌痛病人治疗前后的生活质量量表比较(±SD)Table 5 Comparison of life quality scales of patients with moderate cancer before and after treatment pain (±SD)
基线评估Baseline 结束后评估After the treatment对照组Control group(n = 29)QOL-C30试验组Experimental group (n = 34)P对照组Control group (n = 29)试验组Experimental group(n = 34)P功能Functional 躯体功能Body function 64.4±26.2 67.3±22.1 0.637 64.3±26.6 68.5±22.4 0.513角色功能Role function 69.5±29.2 69.9±25.6 0.961 70±24.5 67.2±25.6 0.677情绪功能Emotional function 79.5±16.2 81.6±22.6 0.694 70.5±19.8 83.1±20.5 0.022认知功能Cognitive function 81.6±19.6 78.4±22.7 0.557 75±21.7 84.4±20.3 0.095社会功能Social function 71.8±24.8 64.2±27.3 0.254 62.2±25.2 65.1±23.3 0.649症状Symptoms 疲乏Fatigue 107.5±47.3 96.6±45.1 0.353 107.7±42.7 103.1±48.7 0.709恶心与呕吐Nausea and vomiting 44.0±27.5 45.1±27.4 0.877 45.8±30.0 38.5±22.6 0.303疼痛Pain 10.7±18.8 9.8±16.5 0.840 25±32.1 8.3±19.9 0.019气促Shortness of breath 37.9±20.8 41.9±20.9 0.456 37.3±26.9 36.6±20.4 0.903失眠Insomnia 23.8±28.5 28.3±31.3 0.565 17.9±25.4 26.0±27.7 0.256食欲丧失Loss of appetite 39.1±32.2 44.4±33.0 0.521 21.8±26.6 28.1±25.6 0.361便秘Constipation 34.5±31.5 35.4±34.8 0.913 40±33.3 36.5±28.5 0.668腹泻Diarrhea 18.4±27.6 18.6±28.7 0.974 39.7±34.0 19.8±32.6 0.027经济困难Economic difficulties 4.6±14.7 4.9±14.5 0.935 1.3±6.5 4.3±11.4 0.236总体健康状况General health status 34.5±30.2 20.6±28.4 0.065 38.5±33.6 20.8±26.4 0.029
乌头碱作为中药乌头的主要活性成分镇痛药理研究有大量报道[4],其中的草乌甲素是我国自行研发的I 类新药,最早1981 年从乌头根中分离出来的新生物碱[5],1986 年从同属植物、云南特有的滇西嘟啦中分离出来相同物质(重新命名为滇西嘟啦甲),并开发成非成瘾性镇痛药物应用[6,7],临床上广泛用于治疗多种慢性疼痛,镇痛疗效确切、不良反应小。其早期的药理机制研究表明具有抗炎、镇痛及免疫调节作用,临床多用于治疗风湿类风湿性关节炎等轻度、中度的慢性疼痛病人。近年来又发现草乌甲素可作用于离子通道,是电压门控钠通道的阻滞剂[8],同时可以调节脊髓背角神经元、小胶质细胞的功能[9,10],临床可应用于神经病理性疼痛(如带状疱疹引起的疼痛)的治疗。
已经发表的研究均提示草乌甲素在炎性疼痛、慢性疼痛、神经病理性疼痛中有效[11~14],而癌性疼痛常见的疼痛类型为混合性疼痛,草乌甲素是否可以用于癌痛的治疗尚无定论。李芳等[15]报道草乌甲素胶丸辅助硫酸吗啡缓释片治疗中重度癌痛病人,4 周之后可以减少病人服用吗啡的剂量及不良反应发生率。郑兴华[16]报道一项观察性研究,草乌甲素注射液联合使用大剂量丹参注射液治疗晚期剧烈癌痛16 例,有效率95.3%。已经报道的少量研究关注草乌甲素治疗癌性疼痛,但是整体文献质量都不高,很难提供证据支持草乌甲素治疗癌性疼痛。
轻度癌痛对病人的影响较小,可以不用药物治疗,或仅使用NSAIDs 治疗。NSAIDs 药物不良反应是其临床应用最主要的问题[17]。本研究显示轻度癌痛病人每日平均NRS 评分在对照组和试验组之间无差异,即草乌甲素片与布洛芬缓释胶囊疗效相等,同时两组不良反应发生比例相同。但是,本研究轻度癌痛病人入组例数较少,还需要扩大样本量进一步证实这一结论。
中度癌痛影响病人睡眠,对病人的生活质量会产生比较明显的影响。以曲马多为代表的弱阿片类药物由于其不良反应与强阿片类药物类似而镇痛效果明显弱于强阿片类药物,在临床使用中备受限制,近年来一直有“弱化二阶梯”的建议[18]。本研究显示中度癌痛病人每日平均NRS 评分在治疗第4 天时,对照组优于试验组,其他时间两组均无差异。在第4 天之后,两组无差异。这与我们在临床中实际观察到的比较一致,草乌甲素片治疗癌痛病人时起效比较缓慢,最佳疗效出现在第3~4 天,这可能是原因之一。另外这一现象在治疗关节炎等慢性疼痛的文献中未见报道,所以这也可能与癌痛多为混合型疼痛、与癌痛的机制不同于其他慢性疼痛有关。是否可以通过增加草乌甲素剂量来提高治疗的效果,这也是值得进一步研究的问题。在不良反应方面,草乌甲素片治疗的病人出现不良反应例次18例次、其中可能与治疗相关的为2 例次,而对照组出现不良反应例次35 次、其中与治疗相关18 例次,两者有显著差异,草乌甲素片不良反应比例明显低于曲马多缓释片。
表5 显示了中度癌痛病人治疗前后生活质量量表的评分比较,在治疗前对照组和试验组之间无差异。在治疗后,试验组情绪功能评分优于对照组。病人情绪受多种因素影响,躯体的疼痛、对药物不良反应的担心、药物不良反应对身体的影响等等均会干扰病人的情绪。症状项目里疼痛评分试验组更轻,两组之间差异有统计学意义。值得注意的是每日平均疼痛NRS 评分显示结束时使用对照药物与使用草乌甲素片治疗并无差异,都在治疗后有下降,但是生活质量量表的前后对比显示使用对照药物在治疗后疼痛症状评分比治疗前还高。出现这种结果的原因主要是由于疼痛是一种主观感受,症状对病人的影响(即症状负担)不仅仅与症状的严重程度有关,而是对病人功能、能力的综合影响[19]。对照组在治疗后情绪功能、认知功能、社会功能3 个功能领域的评分均比治疗前降低,而试验组3 个功能领域的评分在治疗后升高。控制疼痛不仅需要降低疼痛程度,也要考虑病人心理、社会、灵性,考虑生活质量改善,这也与NCCN 提出的癌痛控制目标5A 原则相一致。对照组29 例病人中出现腹泻13 例,比例为44.83%,按照研究要求全部给予相应通便治疗,试验组没有出现腹泻病例,所以对照组腹泻评分高可能与对照组出现更多药物相关性便秘、使用通便药物治疗有关。最终总体健康状况对照组更好,这可能与在治疗前试验组评分明显低于对照组,试验组在治疗前后并无明显变化。
本研究不足之处是样本量仍偏小,中心数比较少,并且各中心平衡性不佳。仍然需要进一步多中心、大样本的临床研究,以提供更有力的证据。综上所述,轻中度癌痛病人在使用第一阶梯、第二阶梯镇痛药物无效或者不耐受情况下,可以考虑选择草乌甲素片镇痛治疗。
