首次注射唑来膦酸治疗骨质疏松症所致发热及相关因素分析
2021-03-26单慧亭陈春燕吉鹏李东锋新疆医科大学第一附属医院药学部乌鲁木齐830054新疆医科大学第一附属医院风湿免疫科乌鲁木齐830054
单慧亭,陈春燕,吉鹏,李东锋*(.新疆医科大学第一附属医院药学部,乌鲁木齐 830054;.新疆医科大学第一附属医院风湿免疫科,乌鲁木齐 830054)
骨质疏松症(osteoporosis,OP)是最常见的骨骼疾病,是一种以骨量低,骨组织微结构损坏,导致骨脆性增加,易发生骨折为特征的全身性骨病[1]。随着我国人口老龄化趋势加剧,OP 患病人群逐年增加,早期筛查和治疗有助于OP 的及时防治。双膦酸盐类药物作为目前OP 治疗的一线药物,临床上常用药物有阿仑膦酸钠、唑来膦酸等[2]。唑来膦酸是目前广泛应用的静脉用含氮双膦酸盐,有研究表明患者使用唑来膦酸治疗后,急性期反应(acute phase reaction,APR)发生率较高,主要表现为发热、肌痛、流感样症状、头痛、关节痛等,国外研究报道APR 发生率约为31.6%~77.5%,国内为20.43%~100.00%[3]。不同研究结果APR 发生率不同,目前国内文献报道研究人群主要为高龄老年人或绝经后妇女,可能相关的因素有年龄、体质指数、骨吸收抑制药物使用等。本研究选取本院收治的不同人群的OP患者,作为首次使用唑来膦酸(zoledronic acid,ZOL)注射液治疗的研究对象,探讨OP 患者首次使用唑来膦酸注射液后出现发热的影响因素,为临床治疗提供参考。
1 资料与方法
1.1 研究对象
收集2017年1月至2019年12月在新疆医科大学第一附属医院风湿免疫科住院治疗的OP患者临床资料,入选标准符合原发性OP 诊疗指南(2017)骨质疏松诊断标准:① 双能X 线吸收检测法(DXA)测量的中轴骨骨密度或桡骨远端1/3 骨密度的 T 值≤-2.5;② 骨密度测量符合低骨量(-2.5 <T 值<-1)+肱骨近端骨盆或前臂远端脆性骨折;③ 既往可伴有髋部或椎体脆性骨折病史;④ 首次使用唑来膦酸注射液。排除标准:① 合并严重心、脑、肝、肾疾病等;② 内分泌疾病,如伴发甲状腺、甲状旁腺、多发性骨髓瘤等代谢类疾病;③ 恶性肿瘤病史;④ 血清钙水平低于2.1 mmol·L-1或未经治疗的低钙血症;⑤ 肌酐清除率<35 mL·min-1;⑥ 静脉滴注唑来膦酸治疗前已有发热者或有病毒感染、细菌感染病史;⑦ 对双膦酸盐成分过敏者。
合并骨质疏松性骨折定义为患者在治疗前至少发生一次骨质疏松性骨折。长期使用非甾体类药定义为治疗前曾使用该类药物时间≥3 d(依托考昔、塞来昔布、阿司匹林,入选患者因合并其他疾病需服用此类药物,最短服用时间为3 d,最长可达1年)。口服激素类药物定义为口服泼尼松片、甲泼尼龙片、地塞米松片≥7 d。使用双膦酸盐定义为口服双膦酸盐类药物≥1 个月。
1.2 给药方法
完善骨密度、生化等检查后给予入选患者唑来膦酸注射液5 mg/100 mL(诺华制药有限公司,批号:SMV10、ST049、S0764)静脉滴注,注射前给予患者萘普生片0.2 g po qd(参考说明书注射唑来膦酸后短时间内给予非甾体抗炎药可减少用药后前3 d APR 发生率),同时静脉滴注0.9%氯化钠注射液500 mL,给药后再次静脉滴注 0.9%氯化钠注射液500 mL 进行水化处理。
1.3 观察指标
观察并记录患者给药后48 h 内发热的发生情况,① 患者临床表现:包括发热(腋下体温>38 ℃);② 发热的出现时间(给药后24 h 内或给药后24~48 h);③ 血清25 羟维生素D [25(OH)D]水平判断标准:<20 ng·mL-1缺乏;≥20 ng·mL-1不足。记录患者出现发热的例数,按是否出现发热分为有APR 组和无APR组,分析比较两组的年龄、民族、腰椎骨密度T值、是否口服双膦酸盐类药物、是否长期口服非甾体类药物、是否口服激素类药物、体质指数及血钙值的差异。
1.4 统计学处理
用SPSS 22.0 软件进行统计分析,计数资料采用例数或率表示,采用卡方检验或Fisher 精确检验。样本率正态分布计量资料采用均数±标准差表示。单因素分析患者临床资料,以患者的民族、年龄、体质指数、药物使用史、血钙、血清25(OH)D 水平等作为自变量,以发生发热为因变量,差异有统计学意义的则纳入多因素分析,多因素分析采用二元非条件Logistic 回归模型。P<0.05 为差异有统计学意义。
2 结果
2.1 患者临床资料
符合入组标准的155 例患者中,男20 例、女135 例;汉族109 例,少数民族46 例(包括维吾尔族、哈萨克族、回族、柯尔克孜族、锡伯族、土家族、俄罗斯族);患者平均年龄(61.97±12.17)岁,体质指数(23.56±3.64)kg·m-2;血清钙值(2.25±0.11)mmol·L-1。
2.2 急性期反应发生情况
本研究符合入选标准的155 例OP 患者均为首次接受唑来膦酸注射液静脉滴注治疗,其中50例患者治疗后出现发热症状(体温>38℃),发热持续 1~2 d;发热患者给予对症处理后体温恢复正常;105 例患者未出现发热及其他严重不适症状。
2.3 急性期反应的影响因素
分析结果表明,患者性别、长期使用非甾体药物、血清25(OH)D 水平及是否有口服双膦酸盐治疗史与发生急性期发热有关(P<0.05),见表1。

表1 不良反应发生的单因素分析Tab 1 Single factor analysis of adverse reactions
2.4 急性期反应多因素
Logistic 回归分析以上述4 个差异有统计学意义的因素作为自变量,以是否发生急性期发热作为因变量,采用非条件多因素 Logistic 回归分析,结果显示女性是不良反应发生的危险因素,女性使用唑来膦酸后出现发热的风险是男性的7.818倍;长期使用非甾体药物(≥3 d)、口服双膦酸盐治疗史及血清25(OH)D 水平≥20 ng·mL-1是急性期反应发生的保护性因素,见表2。
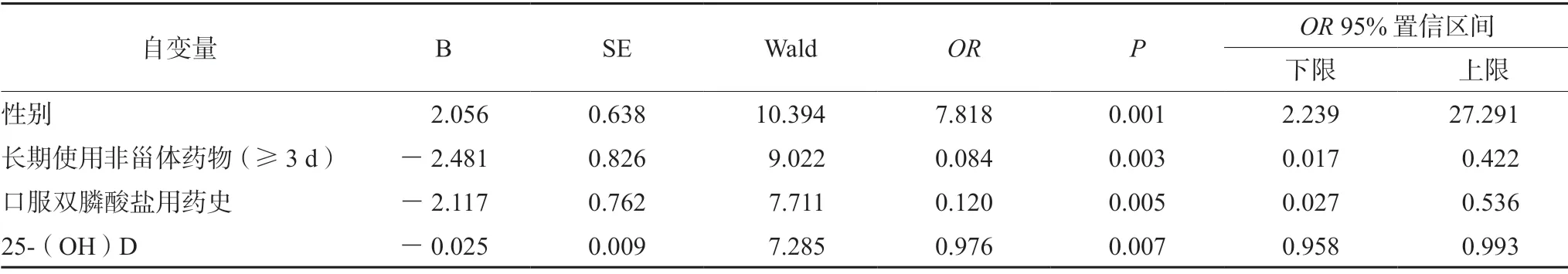
表2 不良反应发生的多因素Logistic 回归分析Tab 2 Multivariate Logistic regression of adverse reactions
3 讨论
随着我国OP 发病率及患者数量逐年增加,双膦酸盐类药物在OP 治疗中的地位和应用越发得到重视和肯定。唑来膦酸属于双膦酸盐类药物的一种,被临床定义为新一代抗骨质重吸收药物,在临床得到广泛使用。唑来膦酸注射液输注后3 d 内开始出现的反应称为APR,较为公认的5 种最常见 APR 为:发热(16.1%)、肌痛(9.5%)、流感样症状(7.8%)、头痛(7.1%)、关节痛(6.3%)[3]。因其在首次静脉注射使用过程中会出现以发热、肌痛为主要表现的APR[4](这些症状通常在输注后72 h 内出现,持续时间短暂,而且在再次使用中出现APR 的可能性比第一次输注后少得多[5],一般这些症状持续不超过1 周),其可能的机制是唑来膦酸为法尼基焦磷酸(FPP)合成酶最强有力的抑制剂,能抑制破骨细胞活性,同时也使其上游的香叶基焦膦酸和二甲基丙烯焦膦酸酯急剧堆积,并与Vγ9Vδ2T 细胞受体结合,激活T 细胞并使其增殖,释放肿瘤坏死因子-α及白细胞介素-6,激发炎症反应[6]。
在本次研究中发现,发热为主要观察到的APR。同时本次研究结果显示,非甾体药物使用情况、口服双膦酸药物治疗史和血清25(OH)D水平与 APR 的发生有关,这3 个因素均为 APR发生的保护因素。李鲲等[7]研究显示,对于静脉滴注唑来膦酸的OP 患者,常规在前3 d 给予塞来昔布口服,APR 的发生率大大降低(13.5%vs83.3%),且发热程度及肌肉疼痛程度均明显轻于未超前预防组。在日本一项多中心、随机、开放、平行分组的研究中发现,将年龄≥60 岁的原发性OP 患者(n=368)随机分为唑来膦酸+洛索洛芬组(ZOL +LOX)和唑来膦酸单药组(ZOL),给予LOX 是在唑来膦酸注射6 h后,ZOL +LOX 组和ZOL 组APRs 发生率分别为34.4%(64/186 例)和47.8%(87/182 例)(P=0.0109);两组患者体温升高(体温升高≥1 ℃和体温高于37.5 ℃)的比例相似(P=0.1186)[8]。本研究患者使用的非甾体药物包括依托考昔、塞来昔布、阿司匹林,使用时间至少为3 d,同时本研究入选患者均在静脉滴注唑来膦酸半小时前给予萘普生口服,给药次数为一次,而 APR 通常在输注唑来膦酸后3 d 内发生,考虑萘普生给药时间短,同时维持作用时间短,并未明显影响APR 的发生率,显示非甾体药物使用时长和种类对APR 的发生影响不同。因此,可根据患者情况选择适合的非甾体药物,若使用萘普生治疗建议增加给药次数。
孟佳等[9]研究显示口服双膦酸盐预治疗可减少首次应用唑来膦酸注射液治疗后不良反应的发生(包括不良反应发生率的减少和不良反应程度的减轻)。王翯等[6]发现既往有口服含氮双膦酸药物如阿仑膦酸钠用药史的患者,在首次接受静脉滴注唑来膦酸5 mg 治疗时,急性炎性发热反应发生率显著减少。Oberg 等[10]认为,口服双膦酸盐药物后患者体内γδT 淋巴细胞的激活与APR的发生有关,连续应用双膦酸盐药物可导致γδT淋巴细胞耗竭,此后应用唑来膦酸则不良反应发生率降低。本研究显示曾服用过阿仑膦酸钠的患者首次静脉滴注唑来膦酸后并未出现发热症状,与上述研究结果一致。
Crotti 等[11]研究153 名绝经后OP 患者首次接受唑来膦酸静脉滴注治疗,在确定APR 发生是否和血清25(OH)D 水平存在关联性时发现,与对照组相比,APR 患者的血清25(OH)D 水平显著低于无APR 患者[(26.3±12.7)vs(37.0±13.5)ng·mL-1,P<0.0001],并且发现血清25(OH)D 水平<30 ng·mL-1为发生APR 的高风险因素。Okimoto 等[8]在研究非甾体药物用药史对唑来膦酸治疗引起APR 的影响时,在亚组分析中发现,低血清25(OH)D 水平可作为APR 的风险因素。本研究发现患者血清25(OH)D 水平≥20 ng·mL-1为发生APR 的保护因素,与国外人群血清25(OH)D 水平存在差异,鉴于有研究发现亚洲人体内的血清25(OH)D 水平通常比其他人群低[12],虽然血清25(OH)D 水平与APR 之间的因果关系尚未得到明确的证实,但有研究证实血清25(OH)D 能够抑制适应性免疫过程,并通过产生抗菌肽来促进先天免疫。特别是已经证明在体外血清25(OH)D 可抑制T 细胞[13],同时也抑制了激活γδTCR[14]。这可以解释低血清25(OH)D 水平与首次静脉滴注唑来膦酸后发生APR 的高风险相关。
本研究发现性别为首次静脉滴注唑来膦酸发生APR 的危险因素,在相关研究报道中,APR 与年龄、种族、降钙素、他汀类药物、淋巴细胞数等因素存在相关性[15],并未涉及性别。但本次研究样本量小,且因为中国男性在各年龄段骨质疏松发病率均低于同年龄段女性[16],导致本研究男性与女性患者入组人数差异较大,导致结果与相关研究报道结果不一致。
综上所述,首次静脉滴注唑来膦酸后发生发热较为常见,但多为一过性,对症治疗后可有效缓解。预先使用非甾体药物、双膦酸盐口服用药史及患者血清25(OH)D 较高水平可减少APR 发生的风险。而对于女性患者,发生APR 的风险高于男性患者,在实际使用时应多关注此类患者的情况,若出现APR 需及时对症处理。
