镧系金属有机骨架比例荧光检测萘普生
2021-03-25张亚如陈企发
隗 玉,张亚如,陈企发,夏 炎,2*
(1.南开大学 化学学院 南开大学中心实验室,天津 300071;2.天津市生物传感与分子识别重点实验室,天津 300071)
日常生活中,药品和个人护理产品(Pharmaceuticals and personal care products,PPCPs)被广泛使用。PPCPs由于保质期很长,产品进入外界环境后,仍可持久存在[1-2]。有研究表明,废水处理厂、少数的地下水、河流和湖泊中都存在PPCPs[3-5]。据报道,PPCPs会影响鱼类的内分泌系统[6],并可能会通过危害水中的生物进而影响人体健康。萘普生属于PPCPs中的药品系列,被用于治疗发烧、发炎和疼痛等疾病,但过量的萘普生会导致心脏病和中风,而且进入环境中后,会对生态系统有一定的危害。因此,开发一种简单、快速测定萘普生的传感器非常重要。

图1 Eu-MOF检测萘普生机理图
已报道的测定萘普生的分析方法主要有:同步光谱法[7]、磷光法[8]、分光光度法[9]、伏安法[10]、毛细管电泳法[11]和化学发光法(CL)[12]。但这些方法比较耗时,不适于萘普生的快速检测。荧光检测法具有响应速度快、检测时间短和灵敏度高等优点。其中比例荧光检测方法可以克服单一荧光发射峰荧光检测法易受环境和人为因素干扰的缺点,进行高效准确检测。进行比例荧光检测时,选择的探针应具有稳定的化学性质和良好的发光性能。镧系金属有机骨架(Lanthanide-based metal-organic frameworks,Ln-MOFs)兼具镧系金属的优良发光性能和金属有机骨架的多孔性、优良的稳定性和孔径可调等优点[13-16],是一种符合上述要求的优势材料。研究者们开发了多种Ln-MOFs并将其用作比例型荧光传感器[17]。具有双荧光发射的Ln-MOFs与目标物作用后,自身的两个发射峰会发生不同变化,其颜色的变化可通过肉眼识别[18]。
本文采用超声法合成了检测萘普生的比例型荧光传感材料Eu-MOF(图1)。研究发现,Eu-MOF和萘普生之间较强的π-π相互作用增强了其对萘普生的富集能力和选择性,提高了检测灵敏度。
1 实验部分
1.1 仪器与试剂
Model D/max-2500X射线单晶衍射仪(XRD)、TG 8121热重分析仪(TGA)(Rigaku Corporation,日本);JSM-7500F扫描电子显微镜(SEM)(JEOL Corporation,日本);MAGNA-IR 560傅里叶变换红外光谱(FT-IR)(Nicolet Corporation,美国);KH-400KDH超声波仪器(昆山禾创超声仪器有限公司);FL-4500荧光光谱仪(Hitachi Corporation,日本)。
六水合硝酸铕(Eu(NO3)3·6H2O,99.99%,阿拉丁生化科技有限公司);1,3,5-苯三甲酸(BTC,98%,北京偶合科技有限公司);醋酸钠(CH3COONa,98%,天津市江天化工技术有限公司);无水乙醇(CH3CH2OH,分析纯,天津市康科德医药化工有限公司)。萘普生(Naproxen,NPX)、克林霉素(Clindamycin,CLI)、青霉素(Penicillin,PNC)、黄连素(Berberine,BER)、保泰松(Phenylbutazone,PHE)、双氯芬酸钠(Diclofenac sodium,DCF)、布洛芬(Ibuprofen,IBU)购自萨恩化学技术有限公司,纯度98%及以上。
1.2 实验方法
1.2.1 Eu-MOF的制备室温下将0.3 mmol BTC溶于15 mL无水乙醇中,记为溶液1;0.6 mmol Eu(NO3)3·6H2O、0.9 mmol CH3COONa和15 mL高纯水混合,记为溶液2。将溶液1倒入溶液2中,产生大量的白色固体,继续搅拌3 h。产物分别用无水乙醇和高纯水洗涤3次,70 ℃下真空干燥12 h[19]即得。
保持上述各物质的物质的量之比不变,采用超声合成法进行合成,设定温度为60 ℃,频率为40 kHz,超声时间分别为30、45、60、75、90、120 min。将得到的白色固体产物分别用无水乙醇和高纯水洗涤3次,70 ℃下真空干燥12 h即得。
1.2.2 Eu-MOF的荧光性质选择Eu-MOF和配体BTC的质量浓度均为0.3 mg·mL-1进行荧光光谱测定,激发波长为268 nm,狭缝为5.0 nm×5.0 nm,电压为700 V。
1.2.3 Eu-MOF比例荧光检测萘普生将Eu-MOF分别加入不同浓度(0.01~2.5 μmol/L)的萘普生溶液中,使Eu-MOF终浓度为0.3 mg·mL-1,超声5 min,采集相应的荧光光谱以考察萘普生浓度对检测的影响。
将Eu-MOF分别与一系列浓度为4.0 μmol/L的抗生素溶液和离子溶液混合,采集荧光光谱以考察Eu-MOF对萘普生的选择性。
将Eu-MOF加入含有1.0 μmol/L萘普生和4.0 μmol/L其他干扰物的混合溶液中,采集荧光光谱以考察Eu-MOF检测萘普生时的抗干扰能力。
1.2.4 实际样品检测收集不同水样,用0.45 μm的滤膜过滤后加入萘普生,使其浓度为1.0 μmol/L,再加入Eu-MOF(0.3 mg· mL-1),超声5 min混合均匀,采集荧光光谱。
2 结果与讨论
2.1 Eu-MOF的表征
如图2A~D所示,Eu-MOF呈长棒状,长短不一,较为杂乱。随着超声时间的延长,材料的形貌逐渐变得规整,当超声时间为90 min时,其长约8 μm,短小的棒状较少(图2E)。当超声120 min时,Eu-MOF的形貌与90 min时相似。不同超声时间下合成的Eu-MOF的荧光性能基本保持一致。因此,选择超声90 min得到的Eu-MOF与搅拌法合成的Eu-MOF进行晶型对比。

图2 不同超声时间下Eu-MOF的SEM图
如图3A所示,搅拌法和超声合成法合成的Eu-MOF在8°~26°之间都存在9组特征峰,与文献报道一致[20]。但超声法合成的Eu-MOF峰的强度更高更尖锐,晶型更好。两种方法合成的Eu-MOF在1 106、1 368、1 435、1 555、1 612 cm-1处有特征峰,这归因于Eu-MOF上游离羧基的伸缩振动[21](图3B)。图3C为常温搅拌合成的Eu-MOF的SEM图,可以观察到Eu-MOF为纳米棒状晶体,平均长度约为1.2 μm,形貌与超声合成法制备的Eu-MOF相似,但长度略短。由于超声合成Eu-MOF的时间更短、晶型更好,后续选取超声合成法制备的Eu-MOF作为传感器材料。从图3D中可以看出,Eu-MOF主要存在两个失重区域,分别为74~159 ℃和393~487 ℃。第一个失重区域重量损失值约22.1%,由Eu-MOF中的配位水分子受热蒸发所致,第二个失重区域重量损失值约为42.1%,是因为Eu-MOF的结构被分解和破坏。
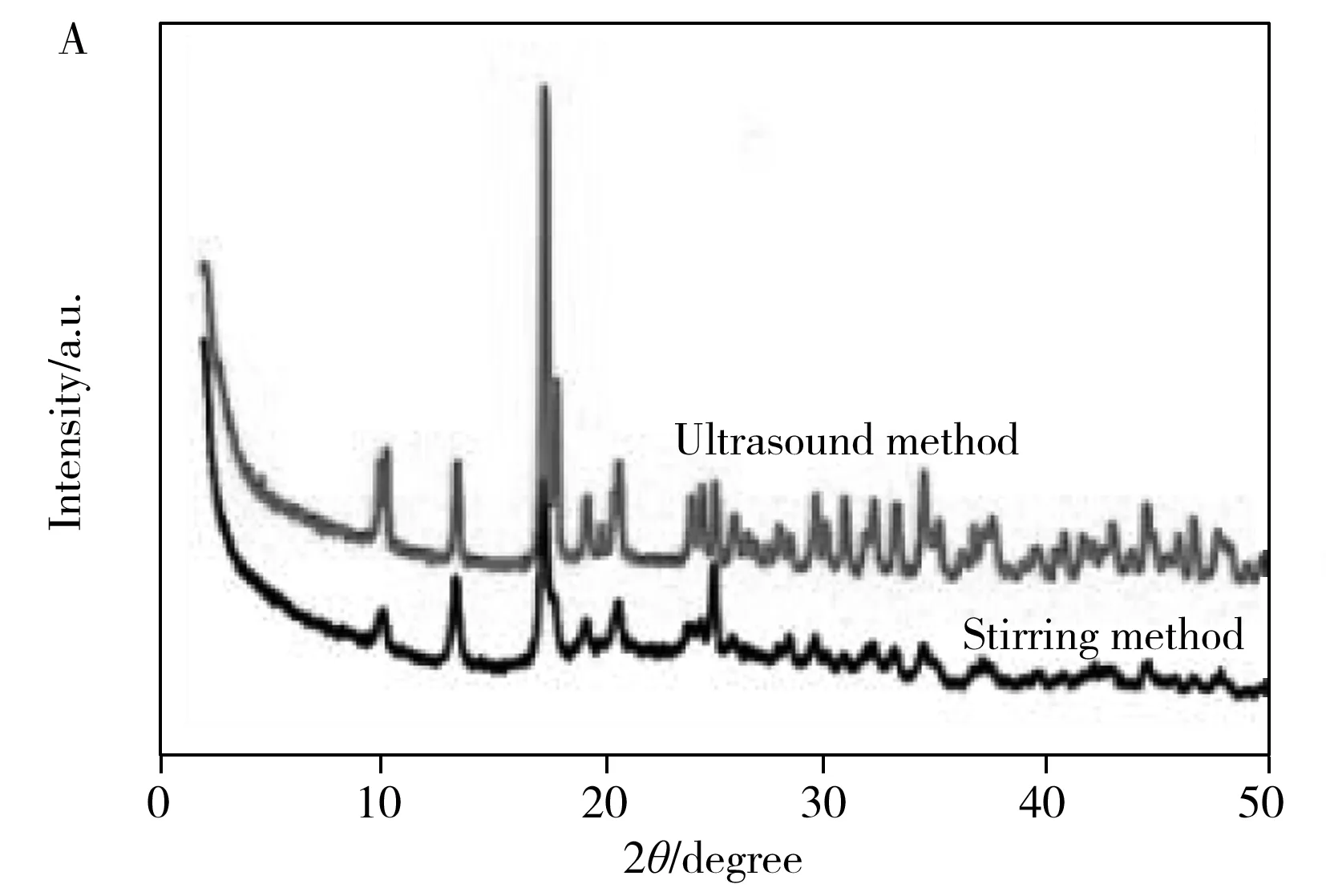
图3 Eu-MOF的XRD(A)、FT-IR(B)、SEM(C)和TGA(D)
2.2 Eu-MOF的光学性质
考察了Eu-MOF和BTC的荧光发射光谱。如图4A所示,BTC的荧光发射峰位于370 nm。单一激发光照射下,Eu-MOF呈现双荧光发射,发射峰分别位于375 nm和623 nm。可见其在375 nm处的荧光发射源于BTC,623 nm处的荧光发射源于Eu3+。Eu-MOF在375 nm处的荧光发射峰相较于游离的BTC发生红移,是因为配体BTC与中心金属Eu3+配位所致。一般情况下,Eu3+的f-f跃迁属于禁阻跃迁,这导致Eu3+吸光能力低,故采用395 nm激发光照射游离的Eu3+时,其发射峰强度非常弱(图4B)。而传感器中Eu3+显示出强烈的荧光发射,主要是因为配体向Eu3+转移了能量,增强了Eu3+的发射,即配体在激发光的照射下,电子从S0跃迁到S1,后又通过系间窜越转移至T1,最后通过能量转移过程将能量转移至Eu3+,发射出强烈的荧光。此过程又称之为“天线效应”。
研究了pH值和时间对Eu-MOF荧光稳定性的影响。结果显示,在pH 4.0~10.0范围内,Eu-MOF在水溶液中显示出良好的荧光稳定性。当溶液的酸碱度过高时,Eu-MOF的荧光性质变差。Eu-MOF的时间稳定性荧光谱图显示,其在2周内具有良好的荧光稳定性,表明Eu-MOF在水溶液中具有良好的荧光性质。
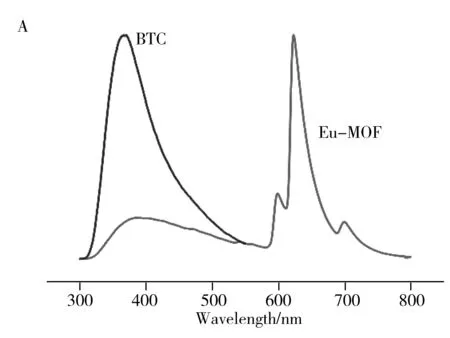
图4 配体和Eu-MOF(A)及配体和EuCl3(B)的荧光发射图

图5 I375/I623与萘普生浓度之间的点线图
2.3 Eu-MOF对萘普生的荧光检测
考察了不同浓度的萘普生对Eu-MOF荧光强度的影响。结果显示,随着萘普生的逐渐加入,Eu-MOF在375 nm处的荧光发射峰强度逐渐增强,623 nm处的峰强度逐渐减弱,可实现对萘普生的比例荧光检测。随着萘普生浓度的增加,Eu-MOF在375 nm和623 nm处荧光发射强度的比率(I375/I623)逐渐增大(图5),在0.07~2.3 μmol/L范围内,萘普生的浓度(X)与I375/I623(Y)线性相关,关系式为Y=0.677X+0.114。在信噪比为3时,检出限为0.039 μmol/L,低于已有文献的检出限(表1)。

表1 Eu-MOF与其他材料对萘普生检出限的对比
2.4 Eu-MOF对萘普生的选择性及抗干扰能力

2.5 Eu-MOF对实际样品中萘普生的检测
选取海水、湖水和地下水为实际样品,采用本文所建方法进行检测和加标回收实验,结果见表2。由表可见,实际样品的回收率为92.5%~115%,相对标准偏差为2.3%~5.5%,满足实际样品的检测需求,表明Eu-MOF可用于实际样品中萘普生的检测。

图6 Eu-MOF及各种抗生素溶液的荧光发射谱图(λex=268 nm)

图7 Eu-MOF对萘普生溶液(1.0 μmol/L)和其他离子或抗生素溶液(4.0 μmol/L)的选择性对比

表2 实际水样的加标回收结果(n=3)

图8 Eu-MOF在浸入萘普生溶液前后的XRD

图9 萘普生的紫外吸收谱图和Eu-MOF的激发光谱图
2.6 机理探究
为了探索Eu-MOF检测萘普生的机理,将Eu-MOF浸泡在萘普生溶液中24 h,图8的XRD分析结果显示,Eu-MOF的晶体结构未发生改变,说明萘普生溶液未使Eu-MOF的结构坍塌。由于萘普生与Eu-MOF在375 nm处的荧光发射相吻合,因此,随着萘普生的逐渐加入,Eu-MOF在375 nm处的荧光发射峰强度逐渐增强。而萘普生的紫外吸收光谱和Eu-MOF荧光激发光谱相重叠,使两者产生竞争吸收,发生内滤光效应(图9),并且随着萘普生浓度的增加,竞争吸收更加明显,导致Eu-MOF在623 nm处的荧光发射逐渐减弱,这使得Eu-MOF在375 nm和623 nm处的荧光发射强度比率(I375/I623)逐渐增大。此外,Eu-MOF和萘普生结构之间存在较强的π-π相互作用,这增强了Eu-MOF对萘普生的富集能力,从而进一步提高了检测灵敏度。
3 结 论
本文通过超声法合成了具有双发射的Eu-MOF,并将其用作比例型荧光传感器检测萘普生。考察了Eu-MOF的形貌特征和光学性质。由于萘普生的发射光谱与Eu-MOF的一个发射光谱位置重合,且二者之间存在竞争吸收,产生内滤光作用。故随着萘普生浓度的增加,传感器在375 nm和623 nm处的荧光发射峰发生不同的变化,其荧光发射强度比率(I375/I623)逐渐增大,进而实现了萘普生的检测。其线性范围为0.07~2.3 μmol/L,检出限为0.039 μmol/L。Eu-MOF在检测萘普生的过程中显示出良好的选择性和抗干扰能力,是检测萘普生的优势材料。