钝化材料的老化对水稻土中Cd钝化稳定性的影响
2021-03-23单志军陈勇红张丽刘岩焦位雄林大松
单志军,陈勇红,张丽,刘岩,焦位雄,林大松*
(1.农业农村部环境保护科研监测所,天津 300191;2.仙游县农业农村局农村环保能源站,福建莆田 351200)
矿业、冶金和交通运输等人类活动导致我国南方部分水稻田受重金属Cd污染[1],对人体健康具有潜在危害[2-3]。农田原位钝化修复具有修复效率高、操作简单和费用低等优点,适合我国大部分轻度、中度的农田重金属污染土壤修复[4],但是重金属的原位钝化技术只是降低Cd 的生物有效性,未能将重金属从污染土壤中去除,复杂的土壤环境和农作物生长等因素,势必对钝化材料本身的稳定性及钝化产物中Cd的重新活化产生影响。
目前,关于钝化材料的钝化效果稳定性研究多集中在老化效应对钝化材料的影响,孙良臣[5]在溶液环境中对钠基膨润土和生物质炭的热力学稳定性、化学稳定性和生物学稳定性进行了研究,以钝化材料的降解率反映钝化稳定性的强弱。梁学峰[6]在巯基改性天然海泡石吸附Pb2+性能及机理的研究中,利用X 射线衍射(X-ray diffraction,XRD)和傅氏转换红外线光谱分析仪(Fourier transform infrared spectroscopy,FTIR)对负载重金属前后的天然海泡石进行表征,发现天然海泡石上修饰的巯基对重金属具有主要的钝化作用。刘兆云[7]利用去离子水、双氧水和硝酸模拟了黑炭在环境中的短期氧化和长期氧化,初步结果表明,自然老化过程可引起黑炭孔隙结构的破坏,致使其比表面积和总孔体积减小,导致黑炭对重金属的吸附减弱。然而,有关钝化材料与土壤组分之间交互作用的报道较少,缺少对钝化修复后土壤稳定态重金属再释放机制的研究。本研究考察施用钝化材料(天然海泡石和生物质炭)后,河池、湘潭和韶关酸性水稻土中Cd形态变化,以及土壤Cd、Fe、Mn、Cu 和Zn 形态变化之间的相关性分析,以期为酸性Cd污染农田钝化修复提供技术支撑。
1 材料与方法
1.1 试验材料
钝化材料:供试天然海泡石中伴生碳酸钙含量较高,含少量白云石和滑石等杂质,pH 值为10.1,阳离子交换量(Cation exchange capacity,CEC)为18.0 cmol·kg-1,比表面积为22.3 m2·kg-1,孔径为1.4 nm。X射线荧光分析表明其主要组成为41.7% CaO、16.8%MgO、7.4% Al2O3、32.5% SiO2;玉米秸秆生物质炭在550~600 ℃缺氧条件下热解6~8 h 制备而成,pH 值为9.8,比表面积为60.1 m2·g-1,孔体积为0.028 cm2·g-1,平均孔径为3.8 nm,含碳量为52.5%。
水稻土分别取自广西河池、广东韶关、湖南湘潭Cd 污染水稻田。土壤性质及重金属Cd 污染程度见表1,水稻土Cd背景值见表2。
1.2 试验设计
田间最大持水量测定:应用环刀法[8]测定湘潭、河池和韶关三地采样点土壤田间最大持水量,分别为61.29%、81.78%和82.47%。
土壤培养试验:在河池、湘潭、韶关三类酸性水稻土中开展了温室条件下为期308 d 的土壤培养试验,每类水稻土均设置1 个对照和50 g·kg-1天然海泡石、10 g·kg-1生物质炭2 个钝化材料处理,共9 组,每组3次重复。每个实验桶装5 kg 过2 mm 筛的土壤,实验桶规格:桶高为30 cm,底面半径为15 cm。在温室条件下,通过称质量法保持70%的田间最大持水量。取样时间分别为第0、7、28、56、112 d和308 d,每份土壤样品约300 g,土壤经自然风干后,磨碎过20、100目筛,置于室温下保存备用。
土壤pH的测定:水土比2.5∶1混合,摇匀,沉淀至溶液澄清,用pH计(PB-10,Sartorius,德国)测定。
钝化材料的表征、CEC和土壤有机质均送至检测公司检测。
连续提取法(BCR):土壤酸提取态、还原态和氧化态重金属根据Alan 等[9]的方法进行提取,残渣态通过差量法测量。土壤重金属全量选用HCl-HNO3-HF体系消解,选用标准物质SRMs-2586 进行质量控制。以上土壤提取液采用ICP-MS(iCAP Q,Thermo Scien⁃tific,美国)测定重金属Cd、Fe、Mn、Cu和Zn含量。
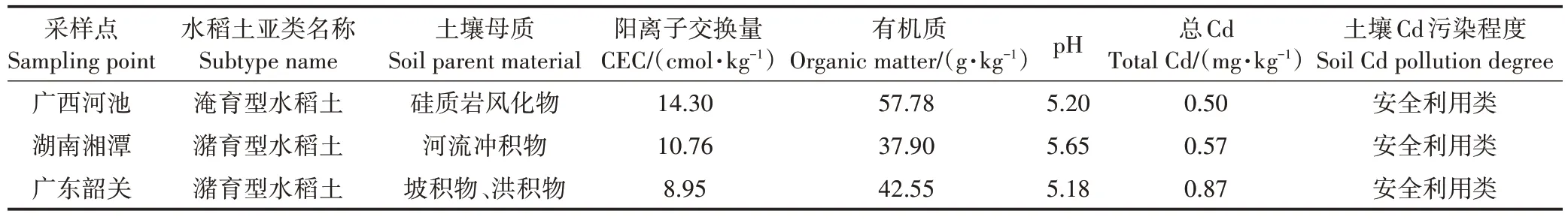
表1 土壤性质及重金属Cd污染程度Table 1 Soil properties and pollution degree of Cd
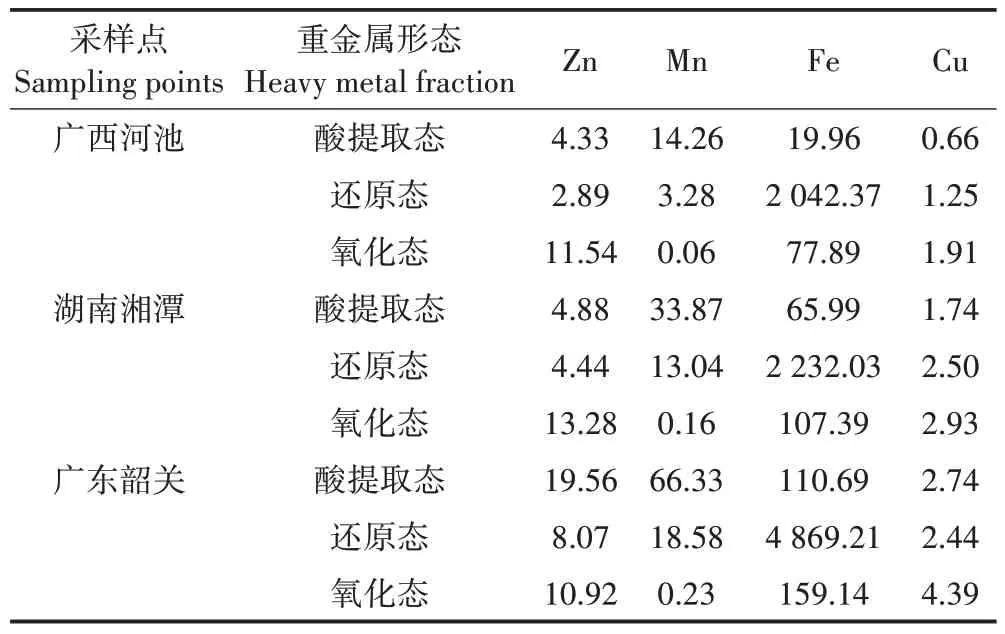
表2 水稻土重金属形态背景值(mg·kg-1)Table 2 Background values of heavy metal fraction in the experimental soils(mg·kg-1)
1.3 数据统计分析
采用Excel 2016 和Origin 2018 软件进行数据处理和图表绘制,应用R 语言进行相关性分析。采用DPS 软件进行统计分析,采用Duncan′s 多重检验分析处理间差异的统计学意义(α=0.05),数据取3 次重复的平均值。
2 结果与分析
2.1 土壤培养过程中pH的变化
图1 为施加天然海泡石或生物质炭后,河池、湘潭和韶关土壤pH 随时间的变化。与对照处理相比,施加天然海泡石或生物质炭后,河池土壤pH 值明显增加,0~28 d 土壤pH 无显著差异(P>0.05),与第28 d相比,第56 d 土壤pH 显著增加(P<0.05)。与对照处理相比,施加天然海泡石或生物质炭后,湘潭土壤pH明显增加,其土壤pH 的变化趋势类似于河池水稻土处理;与对照处理相比,施加天然海泡石或生物质炭后,韶关土壤pH 明显增加,其土壤pH 的变化趋势类似于河池水稻土处理。不同水稻土类型的对照处理pH 均呈现先增加后减小的变化趋势。施加天然海泡石或生物质炭后,不同水稻土pH变化趋势相近。
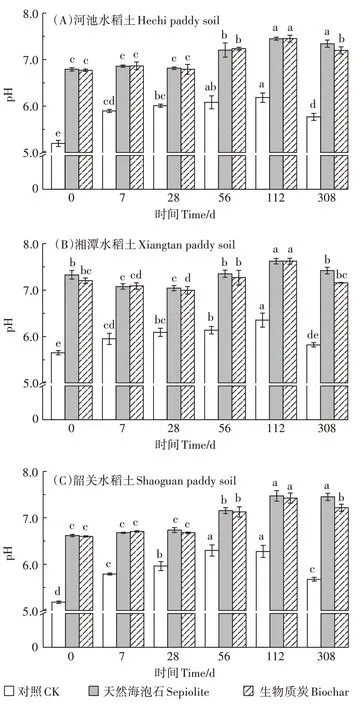
图1 河池、湘潭和韶关土壤pH随培养时间的变化Figure 1 Changes of soils pH in Hechi,Xiangtan and Shaoguan under different incubation time
2.2 不同钝化材料对土壤Cd形态变化的影响
2.2.1 河池水稻土中Cd形态变化
图2A 为施加天然海泡石或生物质炭后,河池土壤Cd形态随时间的变化。在0 d时,河池对照处理土壤中酸提取态Cd 含量占土壤中总Cd 含量的37.1%,随着老化时间的增加,土壤中酸提取态Cd 未发生显著变化(P>0.05)。
施加天然海泡石后,在土壤培养0~28 d,河池土壤中酸提取态Cd 和还原态Cd 分别减少9.0、9.9 个百分点,氧化态Cd 减少3.0 个百分点,残渣态Cd 增加21.9 个百分点;在土壤培养28~308 d,土壤中残渣态Cd 减少19.0 个百分点,酸提取态Cd、还原态Cd 和氧化态Cd 分别增加13.8、4.6 个百分点和0.6 个百分点。但是在施加生物质炭后,在土壤培养0~7 d,土壤中酸提取态Cd和还原态Cd分别减少8.1、4.5个百分点,氧化态Cd 和残渣态Cd 分别增加7.5、5.1 个百分点,在7~28 d,氧化态Cd 减少9.3 个百分点,残渣态Cd 减少11.9 个百分点;在土壤培养28~308 d,则土壤中残渣态Cd 减少14.0 个百分点,酸提取态Cd 和还原态Cd分别增加6.5、9.6 个百分点。可以看出,施加天然海泡石后,河池土壤中酸提取态Cd 占比呈先减少后增加的趋势;施加生物质炭后,土壤中酸提取态Cd占比也呈先减少后增加的趋势。因此,施加天然海泡石或生物质炭后,河池土壤Cd存在再释放现象。
2.2.2 湘潭水稻土中Cd形态变化
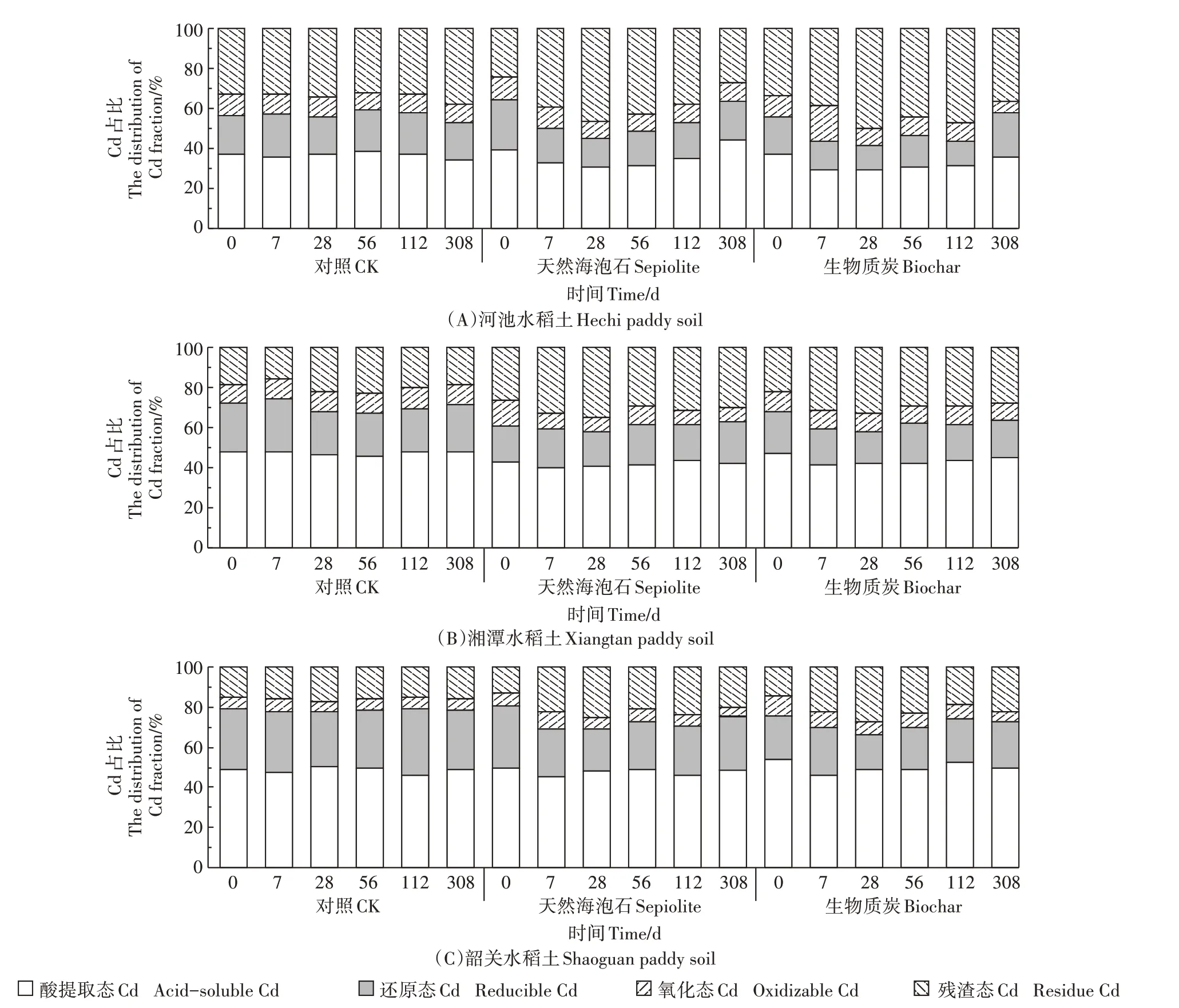
图2 不同老化时间下水稻土中Cd形态分布Figure 2 Distribution of soil Cd fraction in paddy soil under different aging time
图2B 为施加天然海泡石或生物质炭后,湘潭土壤Cd形态随时间的变化。在0 d时,湘潭对照土壤中酸提取态Cd 含量占土壤中全Cd 含量的47.7%,随着老化时间的增加,土壤中酸提取态Cd 未发生显著变化(P>0.05)。
施加天然海泡石后,在土壤培养0~7 d,湘潭土壤中酸提取态Cd 和氧化态Cd 分别减少3.2、4.9 个百分点,还原态Cd 增加1.9 个百分点,残渣态Cd 增加6.2个百分点;在土壤培养7~308 d,土壤中残渣态Cd 和氧化态Cd分别减少2.6、1.0个百分点,酸提取态Cd和还原态Cd 分别增加2.0、1.5 个百分点。施加生物质炭后,在土壤培养0~7 d,土壤中酸提取态Cd、还原态Cd和氧化态Cd分别减少5.5、2.9个百分点和1.3个百分点,残渣态Cd增加9.7个百分点;施加生物质炭后,在土壤培养7~308 d,土壤中残渣态Cd 和氧化态Cd分别减少3.6、0.8个百分点,酸提取态Cd和还原态Cd分别增加3.4、1.0 个百分点。可以看出,施加天然海泡石后,湘潭土壤中酸提取态Cd 占比呈先减少后增加的趋势;施加生物质炭后,土壤中酸提取态Cd占比也呈先减少后增加的趋势。因此,施加天然海泡石或生物质炭后,湘潭土壤Cd存在再释放现象。
2.2.3 韶关水稻土中Cd形态变化
图2C 为施加天然海泡石或生物质炭后,韶关土壤Cd形态随时间的变化。在0 d时,韶关对照土壤中酸提取态Cd 含量占土壤中全Cd 含量的49.2%,随着老化时间的增加,土壤中酸提取态Cd 未发生显著变化(P>0.05)。
施加天然海泡石,在土壤培养0~7 d,韶关土壤中酸提取态Cd和还原态Cd分别减少4.4、7.4个百分点,氧化态Cd和残渣态Cd分别增加2.0、9.8个百分点;在土壤培养7~308 d,土壤中残渣态Cd 和氧化态Cd 分别减少2.3、4.0个百分点,酸提取态Cd和还原态Cd分别增加3.5、2.8 个百分点。施加生物质炭后,在土壤培养0~7 d,土壤中酸提取态Cd 和氧化态Cd 分别减少7.8、1.8个百分点,还原态Cd和残渣态Cd分别增加1.9、7.8 个百分点,在土壤培养7~308 d,土壤中氧化态Cd 减少3.3 个百分点,酸提取态Cd 增加3.5 个百分点。可以看出,施加天然海泡石后,韶关土壤中酸提取态Cd占比呈减少(0~7 d)、增加(7~56 d)、减少(56~112 d)、增加(112~308 d)的趋势;施加生物质炭后,土壤中酸提取态Cd占比呈先减少后增加的趋势。因此,施加天然海泡石或生物质炭后,韶关土壤Cd存在再释放现象。
施加天然海泡石或生物质炭后,河池、湘潭和韶关土壤Cd 均存在再释放的现象,但是对于相同钝化材料,不同水稻土类型土壤Cd 钝化稳定性具有明显差异。施加天然海泡石后,在土壤培养0~28 d,河池土壤中酸提取态Cd 减少9.0 个百分点,0~7 d,湘潭和韶关土壤中酸提取态Cd 分别减少3.2、4.4 个百分点;在土壤培养28~308 d,河池土壤中酸提取态Cd 增加13.8 个百分点,在7~308 d,湘潭和韶关土壤中酸提取态Cd 分别增加2.0、3.5 个百分点。施加生物质炭后,在土壤培养0~7 d,河池、湘潭和韶关土壤中酸提取态Cd 分别减少8.1、5.5 个百分点和7.8 个百分点;在土壤培养7~308 d,河池、湘潭和韶关土壤酸提取态Cd 分别增加6.6、3.4 个百分点和3.5 个百分点。
2.3 土壤重金属形态变化相关性分析
图3 为施加天然海泡石后,在308 d 的土壤培养过程中,河池、湘潭和韶关土壤各形态Cd、Fe、Mn、Zn和Cu 的相关性分析结果。施加天然海泡石后,河池土壤残渣态Cd 与酸提取态Fe 呈显著负相关(P<0.05),残渣态Cd 与还原态Fe、Zn 均呈极显著正相关(P<0.01)。说明与湘潭和韶关相比,施加天然海泡石后,河池土壤Fe、Mn、Cu 和Zn 变化未导致土壤中Cd形态的变化。
由图3 可以看出,施加天然海泡石后,对于河池、湘潭和韶关土壤,仅韶关土壤还原态Cd 与还原态Cu呈显著正相关(P<0.05),韶关土壤氧化态Cd 与氧化态Cu 呈极显著正相关(P<0.01),河池、湘潭土壤中酸提取态、还原态和氧化态的Cd 与Cu、Zn 的各形态基本无相关性。
图4 所示为施加生物质炭后,在308 d 的土壤培养过程中,河池、湘潭和韶关土壤各形态Cd、Fe、Mn、Zn 和Cu 的相关性分析结果。施加生物质炭后,河池土壤酸提取态Cd 与酸提取态Zn、还原态Fe、还原态Mn、氧化态Fe 和氧化态Zn 均呈极显著正相关(P<0.05),与还原态Cu呈显著正相关(P<0.05);河池土壤还原态Cd 与酸提取态Mn、酸提取态Zn、还原态Fe、还原态Mn、还原态Cu、还原态Zn和氧化态Fe、Mn、Zn均呈现极显著正相关(P<0.05)。说明与湘潭和韶关相比,施加生物质炭后,河池土壤Fe 和Mn 变化引起土壤中Cd形态的变化。
由图4 可以看出,施加生物质炭后,河池土壤中酸提取态Cd 与酸提取态Zn 呈极显著正相关,还原态Cd 与还原态Zn、Cu、Mn、Fe 呈极显著正相关,氧化态Cd 与氧化态Cu 呈极显著正相关;湘潭土壤中酸提取态Cd 与酸提取态Zn、还原态Zn 呈显著正相关,土壤氧化态Cd 与酸提取态Cu 呈显著负相关,土壤氧化态Cd 与还原态Zn 呈显著正相关;韶关土壤中酸提取态Cd与酸提取态Zn呈显著正相关,土壤还原态Cd与还原态Fe、Mn、Cu呈显著正相关,土壤氧化态Cd与氧化态Cu呈极显著正相关。
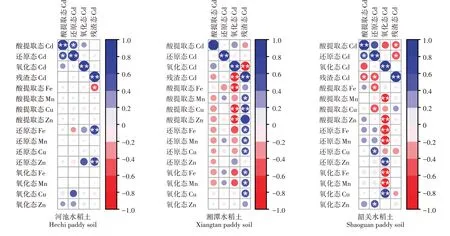
图3 施加天然海泡石土壤各形态Cd、Fe、Mn、Zn和Cu的相关性分析Figure 3 Pearson correlation analysis of paddy soil Cd,Fe,Mn,Zn and Cu fraction after applying lime sepiolite
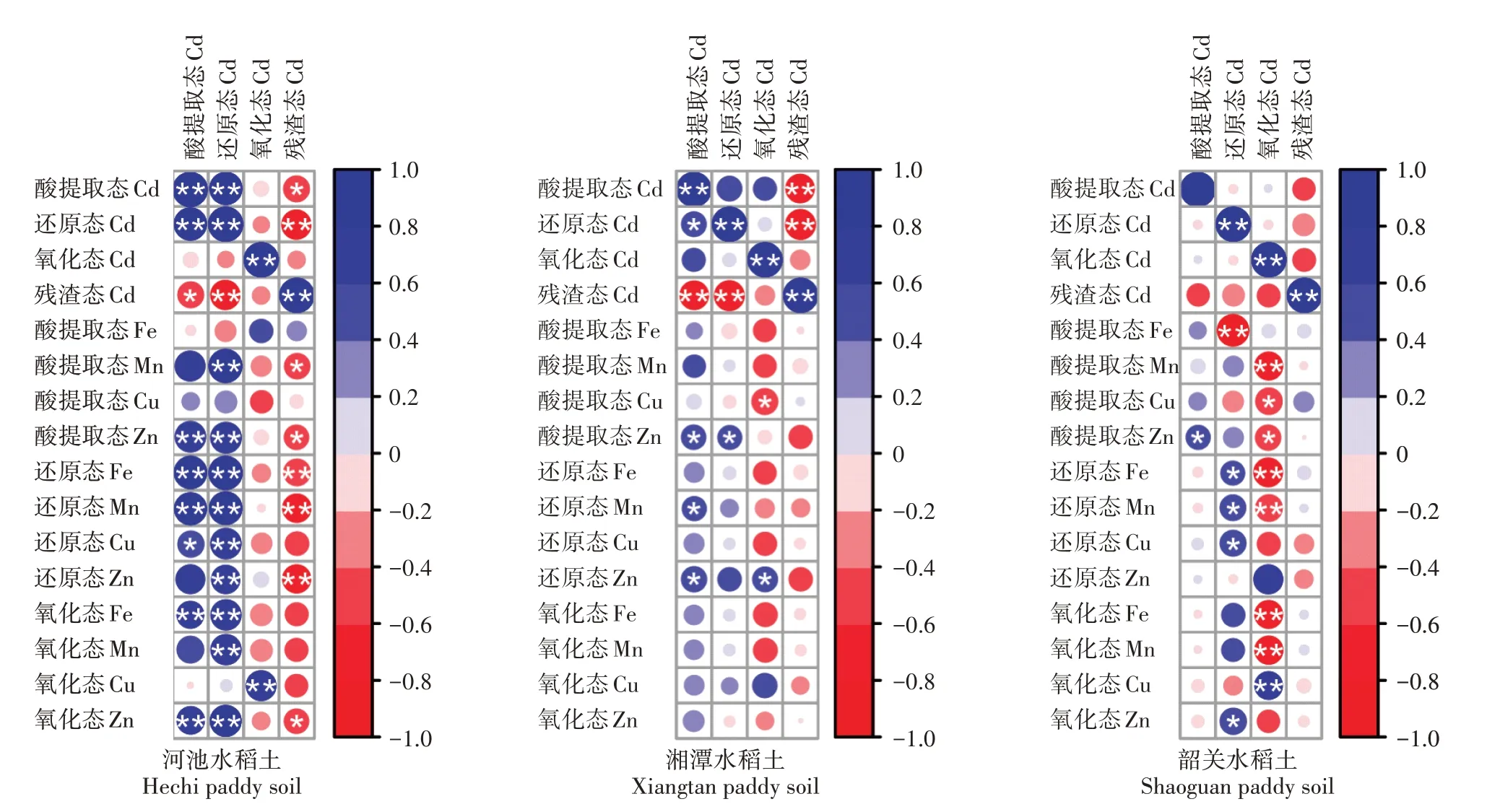
图4 施加生物质炭土壤各形态Cd、Fe、Mn、Zn和Cu的相关性分析Figure 4 Pearson correlation analysis of paddy soil Cd,Fe,Mn,Zn and Cu fraction after applying biochar
由图3 和图4 可以看出,在308 d 土壤培养过程中,与施加天然海泡石相比,施加生物质炭后,河池土壤酸提取态Cd 与酸提取态Mn、酸提取态Zn、还原态Fe、还原态Mn、还原态Zn、氧化态Mn 和氧化态Zn 均呈极显著正相关,河池土壤酸提取态Cd 与还原态Cu呈显著正相关,河池土壤还原态Cd 与酸提取态Mn、酸提取态Zn、还原态Fe、还原态Mn、还原态Zn、还原态Cu、氧化态Fe、氧化态Mn 和氧化态Zn 均呈极显著正相关。表明与施加天然海泡石相比,施加生物质炭会显著影响河池土壤中Cd、Fe、Mn、Zn 和Cu 的赋存形态。
3 讨论
土壤pH 是土壤中重金属形态的重要影响因素,在土壤培养前期,施加天然海泡石、生物质炭后,河池、湘潭和韶关的土壤pH 均增加,同时,土壤酸提取态Cd 和还原态Cd 向氧化态Cd 和残渣态Cd 转化,表明施加天然海泡石或生物质炭后,可以显著提高土壤pH 从而降低土壤Cd 活性[10-11],在淹水条件下,土壤pH 增加,与金属硫化物沉淀以及较高浓度的无定形Fe 氧化物有关[12];在土壤培养后期,施加生物质炭和天然海泡石后,在112~308 d土壤pH呈稳定的趋势。
在土壤培养过程中,施加天然海泡石或生物质炭后,河池、湘潭和韶关土壤Cd形态变化差异明显。主要原因是不同的水稻土类型,土壤Cd污染情况不同,钝化材料对重金属Cd 的钝化修复途径不同,天然海泡石属于碱性矿物材料,同时伴生碳酸钙含量比较高,碳酸钙中的CO2-3可以结合土壤中H+形成HCO-3,从而提高土壤pH[13],增强土壤胶体对重金属离子吸附,有利于生成重金属的氢氧化物或碳酸盐沉淀,从而减少土壤重金属的生物有效性和可迁移性[14-15],另外天然海泡石具有较大的比表面积,层状结构间含有大量的可交换阳离子,可以通过表面吸附和离子交换作用促进Cd由活性高的形态向活性低的形态转化[16-17];天然海泡石属于黏土矿物,具有层链结构和纤维状形态,对重金属具有吸附能力,天然海泡石与土壤组分之间进行充分的物理化学反应,土壤中可能存在与Cd2+相似的金属离子(Ca2+、Zn2+和Cu2+)与土壤稳定态Cd 竞争吸附,导致土壤Cd 再释放;生物质炭具有很高的阳离子交换量,能吸附大量可交换态重金属离子[18];生物质炭具有多孔结构和巨大比表面积,能够较好地钝化土壤中的重金属离子[19];生物质炭含有大量无机盐,可与土壤重金属形成稳定的化合物[19];而且土壤重金属形态主要受土壤性质(土壤pH[20-21]、氧化还原电位[22])、土壤组分(有机质[23]、重金属元素含量[24])等的影响。有机物对重金属活性的影响较为复杂,根据其性质的不同,它既可能通过吸附作用固定重金属,又可能通过络合作用促进土壤重金属的活化[25-27],生物质炭加入到土壤中,可能在微生物的作用下发生矿质化转化为无机物[28],导致土壤Cd再释放。
在河池、湘潭和韶关Cd污染土壤中,施加天然海泡石后,在土壤培养过程中,河池土壤各形态Cd、Fe、Mn、Cu 和Zn 之间相关性弱,是由于重金属元素在不同类型土壤中的形态分布比例差异明显[29],并且河池水稻土为淹育型水稻土,土壤质地为粉砂质黏土[30],其CEC 为57.78 g·kg-1,高于湘潭(37.9 g·kg-1)和韶关的水稻土CEC(42.55 g·kg-1),表明与湘潭和韶关水稻土相比,在加入同等剂量的天然海泡石后,河池水稻土对重金属离子的缓冲性能强,导致不同形态重金属之间的相关性不显著。不同水稻土的成土母质不同,成土母质决定土壤胶体的数量和性质[31],而土壤胶体能够与重金属等污染物质相结合,对其运移产生重要影响[32],由于河池水稻土中Fe、Mn、Cu 和Zn 有效态含量较低,土壤Cd、Fe、Mn、Cu 和Zn 形态之间相关性弱。河池土壤Cd 与Fe、Mn、Cu 和Zn 形态的相关性分析表明,与天然海泡石处理相比,施加生物质炭不仅改变河池土壤Cd形态分布,同时会影响河池土壤Fe、Mn、Cu 和Zn 形态分布。主要原因是施加生物质炭后,土壤有机质的含量明显增加,土壤中颗粒状有机质对土壤中重金属(Cd、Co、Cr、Cu、Ni、Pb、Zn 和Mn)有明显的富集作用[33],而且施加到土壤中的生物质炭发生矿化后,主要转化为腐殖质,部分分解为有机酸,其中有机酸含有羧基、羟基和氨基,能与重金属络合形成可溶态的有机金属络合物,增加土壤重金属的溶出[34],而土壤腐殖质吸附重金属,促进不溶于水的有机结合态重金属的形成[34]。不同水稻土类型土壤Cd 与土壤Fe、Mn形态之间的相关性存在一定差异,可能是生物质炭的施加显著地影响土壤Fe、Mn的赋存形态,进而影响土壤Cd的形态分布,苏园[35]研究表明游离铁和无定形铁与小麦籽粒Cd含量呈正相关;游离锰和无定形锰与小麦籽粒Cd含量呈负相关,且土壤中铁锰氧化物具有稳定的化学性质和较高的比表面积,吸附性能良好,对重金属离子迁移和沉淀有重要影响[36],铁锰淀积增强了土壤对重金属的吸附能力[37];在土壤培养过程中,水稻土中同一形态的Cd与Zn、Cu之间无显著负相关,这与水环境下重金属Cd与Zn、Cu之间存在竞争吸附关系的结论不一致[38-39],可能是由于施加生物质炭增加了土壤中可溶性有机碳含量。李妍等[40]研究表明稻草、污泥和菜叶可溶性有机碳对Zn吸附的抑制均强于对Cd吸附的抑制,进而减弱了Cd与Zn之间竞争吸附的强度。
4 结论
(1)在308 d的土壤培养期内,施加天然海泡石或生物质炭后,重金属Cd 污染程度在安全利用类范围的水稻土(河池、湘潭和韶关水稻土)中酸提取态Cd总体呈先减少后增加的趋势,即天然海泡石和生物质炭对Cd 产生钝化作用一段时间后,土壤Cd 存在再活化、再释放现象,说明天然海泡石和生物质炭的老化显著影响土壤Cd的形态分布。
(2)由于成土母质的差异,不同类型水稻土中Cd、Fe、Cu 和Zn 形态之间的相关性差异明显。施加天然海泡石后,河池水稻土(阳离子交换量高的水稻土)中Cd 与Fe、Mn、Cu、Zn 的赋存形态相关性弱;与施加天然海泡石相比,施加生物质炭后,河池水稻土中Cd与Fe、Mn的赋存形态相关性强。
(3)施加天然海泡石或生物质炭后,重金属Cd污染程度在安全利用类范围的河池、湘潭和韶关水稻土中同一形态的Cd与Zn、Cu之间相关性不同。
