氧化银沉淀- 离子色谱法测定盐湖水中的氟离子、硝酸根和硫酸根
2021-03-20崔建勇
王 利, 崔建勇, 徐 静
(核工业北京地质研究院, 北京 100029)
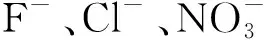
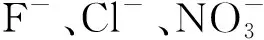
去除Cl-可通过银柱法或在溶液中引入Ag+的方式生成银盐沉淀[8-11]。当用银柱法处理盐湖水时,由于Cl-浓度较高,Cl-与Ag+生成的大量沉淀存在于柱上端,容易堵塞柱子,且银柱的价格较贵,成本较高,使用存在局限性。当加入一些可溶性的银盐去除Cl-,如硝酸银,会引入新的阴离子影响待测离子的测定,干扰实验结果。而Ag2O作为银的一种氧化物,不含有待测阴离子,溶度积常数为2.0×10-8。AgCl的溶度积常数为1.8×10-10,小于Ag2O的溶度积常数,当在溶液中加入Ag2O时,溶液中的Ag+会与Cl-形成AgCl沉淀,促进Ag2O的溶解,达到去除Cl-的效果。

1 实验部分
1.1 仪器及试剂
1.1.1 仪器
戴安ICS-1100离子色谱仪,配Chromeleon色谱工作站;0.22 μm尼龙滤膜过滤头;电热鼓风干燥箱。
1.1.2 试剂
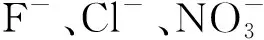
1.2 样品前处理
1.2.1Ag2O的前处理

1.2.2 树脂制备及处理
湿法填充树脂后,先用二次去离子水洗涤树脂至中性,然后用1+1 HCl洗涤树脂3~4次,用二次去离子水洗涤至中性,用1% NaOH洗涤树脂3~4次,用二次去离子水洗涤至中性,重复上述步骤酸- 水- 碱- 水2到3次以去除树脂中的杂质离子。最后用1+1 HCl洗涤,使其转换成氢型阳离子树脂,用二次去离子水洗涤至中性。
1.2.3 样品前处理
取一定体积的样品溶液,按照Cl-与Ag2O的摩尔浓度比为1∶1.5加入Ag2O,搅拌10 min。然后将溶液过阳离子交换树脂小柱,前3 mL溶液弃掉后,开始收集样品溶液,最后将滤液过0.22 μm滤膜,取续滤液,待离子色谱测定。
1.3 色谱条件
淋洗液为3.5 mmol·L-1NaHCO3和1.0 mmol·L-1Na2CO3溶液,流速1.0 mL·min-1,色谱柱为IonPac AS14 A 阴离子分析柱(4 mm×250 mm)和IonPac AG14阴离子保护柱(4 mm×50 mm)。仪器配有AERS 500型阴离子自再生抑制器(4 mm),电流强度为20 mA,定量环体积为25 μL。
1.4 标准曲线的计算

2 结果与讨论
2.1 搅拌时间对Cl-去除的影响
样品溶液中Cl-的浓度约为90 g·L-1,分别取25 mL样品两份,按照Cl-和Ag2O的摩尔浓度比1∶1和1∶1.5加入Ag2O,搅拌不同时间,过滤,测定Cl-浓度,结果如图1所示。由图1a和b可见,Cl-和Ag2O的摩尔浓度比为1∶1和1∶1.5时,当搅拌时间在10 min之内时Cl-浓度随搅拌时间的增加急剧下降,在10~15 min之间Cl-降低的速度减缓,当超过15 min后Cl-浓度几乎不随搅拌时间发生变化。初步确定Cl-和Ag2O的摩尔浓度比在1∶1和1∶1.5之间,搅拌的最佳时间为10~15 min。

图1 按1∶1(a)和1∶1.5(b)比例加入Ag2O时Cl-浓度随搅拌时间的变化图Fig.1 The variation of chloride concentration with stirring time while adding silver oxide in a ratio of 1∶1 (a) and 1∶1.5 (b)
2.2 Ag2O用量对Cl-去除的影响
为了确定最佳实验条件,分别取三份平行样品按照Cl-与Ag2O的摩尔浓度比值1∶1,1∶1.2,1∶1.5加入Ag2O,搅拌不同时间测定Cl-浓度,结果如表1所示。
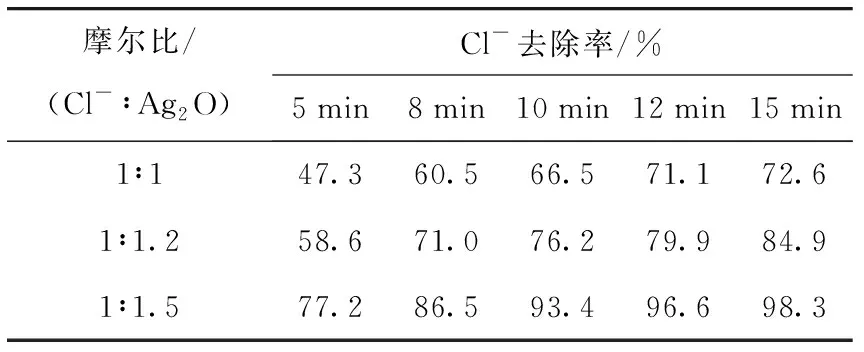
表1 Cl-去除率随摩尔比值变化Table 1 The removal rate of chloride with molar ratio
由表1可见,采用不同摩尔浓度比加入Ag2O时,随着搅拌时间增加,Cl-去除率逐渐升高,在10 min内Cl-去除率变化较大,10~15 min之间Cl-去除率变化较小,且搅拌5 min和8 min时去除率均不能满足测量的要求,与上述结论一致。当按照摩尔浓度比1∶1和1∶1.5加入Ag2O,搅拌10~15 min,去除率最高分别为72.6%和84.9%,也无法满足测量要求。如果按照1∶1.5加入Ag2O搅拌10 min,Cl-去除率为93.4%,可满足离子色谱测定的条件,且考虑到时间成本,可确定实验条件为按照摩尔浓度比1∶1.5加入Ag2O并搅拌10 min。
2.3 溶液pH的变化
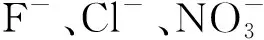
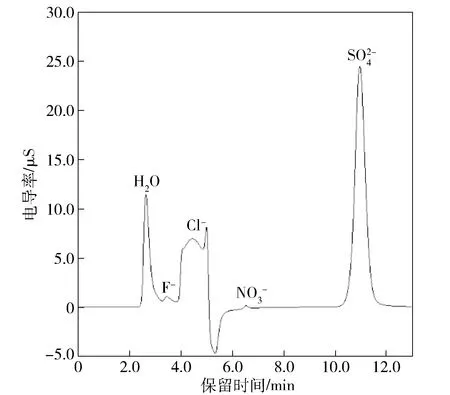
图2 加入Ag2O后样品溶液的离子色谱图Fig.2 Ion chromatogram of sample solution after adding silver oxide
通过对加入Ag2O前后溶液pH值的测定,结果表明,加入Ag2O后,溶液的pH值由8.03变为12.0,呈碱性。采用Ag2O去除Cl-存在如下反应,如式(1)~(3)。离解出的大量OH-使溶液的pH增大,将样品进样到离子色谱时,溶液的电导率升高,出现水的正峰。此外,溶液较高的pH也会对色谱柱造成损伤,影响色谱柱的使用寿命,因此有必要降低溶液的pH。

(1)

(2)

(3)
2.4 溶液pH的调节

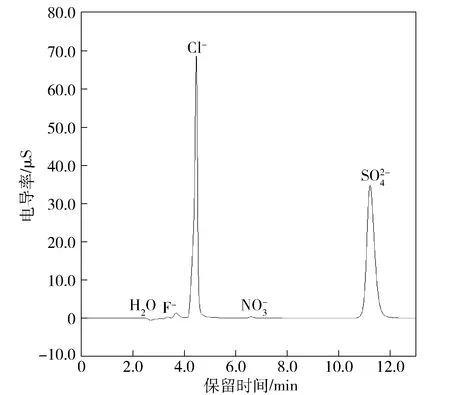
图3 加入Ag2O并过树脂柱后样品溶液的离子色谱图Fig.3 Ion chromatogram of sample solution after adding silver oxide and passing through a resin column
2.5 Ag2O的加入对的影响


2.6 精密度

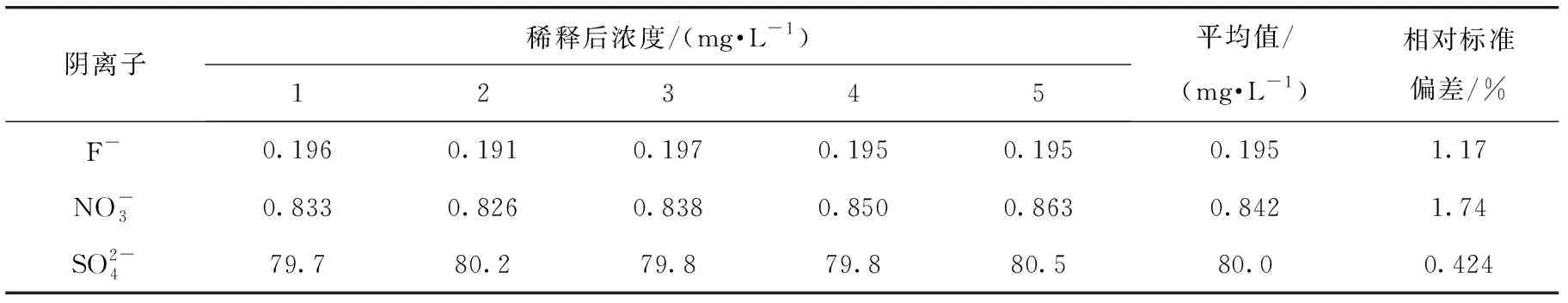
表2 Ag2O法测定水样中各离子质量浓度结果Table 2 The result of parallel measurement of anions in salt water sample
2.7 准确度
2.7.1 基质溶液加标回收率的测定
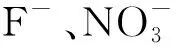

表3 1% KCl溶液中各离子质量浓度测定结果Table 3 The result of anions in 1% KCl solution
2.7.2 样品溶液加标回收率的测定

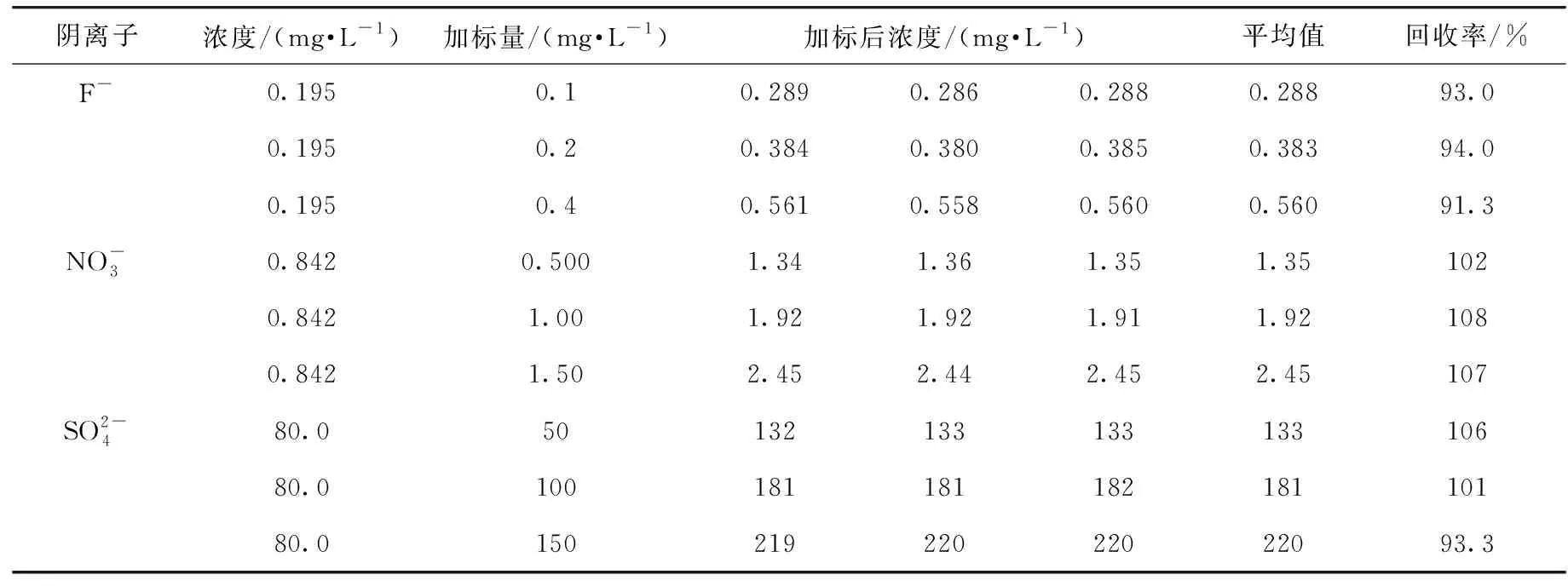
表4 样品溶液回收率结果Table 4 The result of recovery rate of anions in salt water sample
2.8 检出限

3 结 论

