二尖瓣置换在二尖瓣关闭不全中的临床效果
2021-03-18
(皖南医学院附属弋矶山医院胸心外科,安徽 芜湖 241000)
心脏瓣膜病主要由风湿热[1]、结缔组织疾病[2]、退行性改变及缺血[3]或先天异常等众多因素引起的瓣膜开关功能障碍的疾病。心脏瓣膜病发病率为2.5%[4],其中以二尖瓣最为多见,二尖瓣关闭不全(Mitral regurgitation,MR)在二尖瓣疾病中占据很大一部分。笔者从2016年1月1日—2019年5月31日收集我院MR患者的资料,行二尖瓣置换(Mitral valve replacement,MVR)术共98例(失访5例),其中包括53例机械瓣膜置换和40例生物瓣膜置换者,通过对比术前、术后及术后随访6个月的患者的相关情况,了解行MVR对MR患者的治疗及预后情况。
1 资料与方法
1.1 一般资料 收集2016年1月1日—2019年5月31日在我院行MVR治疗MR患者共计98例作为研究对象。其中失访5例,53例机械瓣膜置换和40例生物瓣膜置换。患者纳入及排除标准:①术前均行心脏彩超确诊二尖瓣中度及中度以上反流或轻中度反流伴有严重的症状者;②由同一组医生行手术治疗,均为首次心脏手术;③根据术中患者自身及瓣膜情况与手术术者的相关经验,术中食管超声检测瓣膜情况选择行MVR或二尖瓣成形中转为MVR,行MVR同期可行三尖瓣成形(主要以患者预计寿命作为更换机械瓣膜与生物瓣膜的主要依据);④排除有严重心功能不全者(EF<30%经药物治疗不能得到改善者),恶病质者,合并其他脏器严重的功能不全者或严重其他疾病无法耐受手术者,合并有二尖瓣狭窄或其他瓣膜、大血管病变与微创手术的患者。持续随访患者共93例(基本信息见表1)。
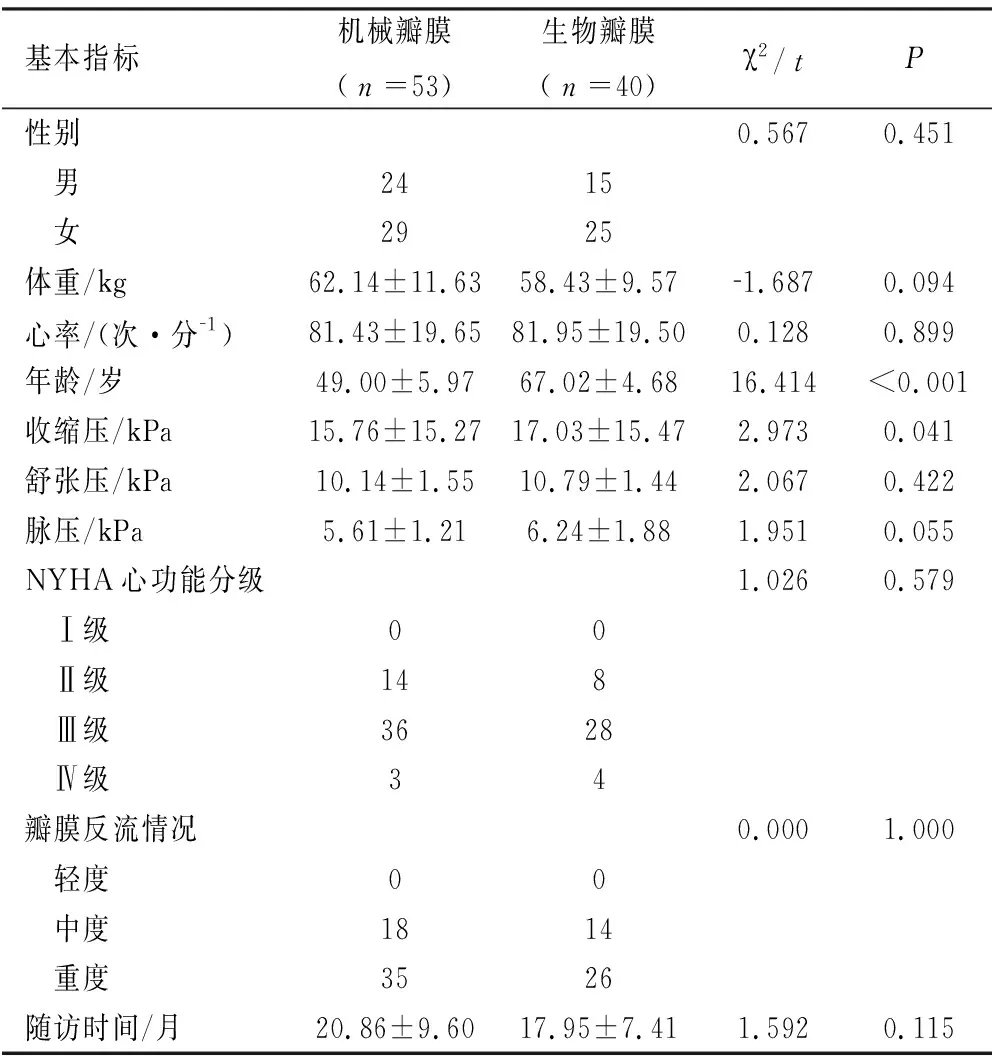
表1 二尖瓣置换基本情况对比
1.2 手术方法 患者均在麻醉会诊下麻醉,行胸骨正中切口,锯开胸骨,切开并悬吊心包,插管建立体外循环,依次阻断下腔静脉、上腔静脉、升主动脉,主动脉根部灌冷停跳液,心脏停跳满意,切开右心房,卵圆窝前方打开房间隔,观察二尖瓣病变情况。根据术中及患者相关病变情况,选择MVR或成形术效果不佳中转MVR,检查置换瓣膜开闭情况探查三尖瓣情况,如有病变同期行三尖瓣成形。连续缝合房间隔,复温,左房及升主动脉根部排气,开放升主动脉,缝合右房切口,待充分辅助循环后停机通过TEE探查瓣膜情况,无明显反流,确切止血放置心包纵隔引流管,关胸转入ICU。
1.3 观察指标 对比患者入院时候的基本指标:体重、年龄、血压、脉压;心脏超声检查术前及术后随访的指标:射血分数(EF值)、左心房内内径、心室舒张末期内径、左心室缩短分数(FS)、术后并发症及中远期抗凝相关并发症。
1.4 随访 入选的患者出院后均持续保持随访,通过门诊、通讯信息或电话咨询等方式对患者心脏功能相关情况进行记录,对比1个月后、3个月后、6个月后的相关指标,了解患者出院后心脏情况及术后并发症情况。

2 结果
93例行MVR的患者均未出现死亡,术后6个月内随访中患者共有9例并发症:术后切口延迟愈合2例,低心排出量1例,血栓栓塞2例(术后6个月内),出血3例,术后钢丝取出术1例;长期持续随访中,7例术后6个月出现脑血管栓塞(机械瓣膜组共5例)。术后持续随访中,记录患者术后1个月、3个月、6个月的心脏相关情况:心功能、左房内径、左室舒张末期内径、EF值、FS(见表2、表3)。术后随访MVR的患者心脏相关功能均较术前有所改善(P<0.05),左心房、左心室较术前均有所缩小(P<0.05),机械瓣膜组与生物瓣膜组患者术后心脏相关指标差异无统计学意义。
3 讨论
MR是瓣膜病中较为常见的一种。在西方国家的一般人群和75岁以上的人群中,MR的发生率分别接近1.7%和10%[5]。二尖瓣能正常开闭主要依赖瓣叶、瓣环、腱索、乳头肌、左心室这5个部分的完整结构和正常功能,如果其中一部分受到损伤都将影响二尖瓣的正常功能。急性的MR多见于外伤或其他原因引起的腱索断裂、缺血性的腱索乳头肌功能异常,患者症状较为明显,及时手术预后较好。慢性的因素导致MR较为常见,慢性患者中一部分人小叶与腱索功能、形态正常,在慢性缺血性因素导致的MR或一些特发性心肌病引起的MR,常常会同时伴随着左室功能不全。慢性MR一般症状出现较晚,具有逐渐加重的趋势,反流量增加左心室前负荷,使得心室进行性扩张顺应性下降,左心室收缩功能障碍。在MR中左房的增大会影响左室的功能,降低射频消融恢复窦性心律的可能性[6],及时的干预可以增加复率的机会,降低血栓形成的风险。

表2 二尖瓣置换组患者相关数据

表3 机械瓣膜置换和生物瓣膜置换患者相关数据
MVR与二尖瓣成形是治疗MR常见的手术方式。成形可以使用在绝大多数MR的患者中,但也有四分之一的此类患者必须实行MVR[7],此类患者可能出现大面积纤维化,小叶游离缘的钙化或者腱索的融合,乳头肌或瓣环严重纤维化钙化都会增加修复难度,行MVR的可能性加大。MVR的患者年龄较大,病情较重[8],瓣膜病变更为复杂,包括瓣叶和环状钙化以及瓣叶受限或纤维化[9],这对修复提出特殊的挑战。对瓣膜结构损伤严重无法修复者或者术中修复不佳者都可行MVR,一些高龄合并高风险的患者,为了降低术后死亡率与相应的并发症,也可行MVR,保留瓣下结构对其术后生存率有益[10]。MR应首选成形术[11],其中包括以下因素考虑行MVR:①接诊患者中风湿性病变较多,瓣叶出现中重度的钙化,瓣叶下的相关结构病变较为严重,瓣膜的活动度受到严重的破坏;②患者左心功能因长期病变影响出现明显的功能不全;③患者自身条件较差,考虑患者不能耐受成形手术可能出现较长的手术时间与体外循环时间;④成形术未能治疗MR的,术中打水测试反流情况与术中食管超声检查显示瓣膜仍然出现明显的反流情况,中转行置换术。经导管的二尖瓣置换术(TMVR)已进入临床,在未来置换术中扮演重要的角色,其中最为重要的障碍:左室流出道梗阻风险问题尤为突出[12],TMVR引起的左室流出道梗阻风险的不确定性以及出现并发症的高死亡率[13],是TMVR发展的一个重要难题。
综上所述,MVR常用于上述几类MR的患者。MVR能有效地改善MR患者的心脏舒缩功能,心房、心室能有所缩小,心功能明显得到提高[14],提升患者术后生活质量。机械瓣膜与生物瓣膜对心脏功能恢复都有明显的效果[15],但两组无明显的差异。由于机械瓣膜需终生抗凝,术后继发抗凝相关并发症较高,及时的手术干预,可以终止瓣膜问题导致的心房、心室扩大,心功能失代偿;较早诊断MR,可以争取成形手术的机会,保留自身瓣膜,减少术后相关并发症的发病率[16]。
