重症急性胰腺炎合并感染耐碳青霉烯类肠杆菌科细菌的危险因素分析
2021-03-17牛司强夏吉荣
陈 嵌,牛司强,邱 菊,夏吉荣
重庆医科大学附属第一医院检验科,重庆 400016
近年来,随着人们生活水平提高,伴随一些不健康的饮食和生活习惯,急性胰腺炎发病率呈逐年上升的势态[1],而此疾病又常伴随较多并发症和严重感染,临床转归效果较差,特别是重症急性胰腺炎(SAP)病情发展迅速,病死率较高,尤其在病程晚期合并感染,其病死率可达30%[2-3],因此寻找具有针对性的临床干预措施来降低SAP病死率已是急待解决的问题。据研究报道SAP死亡大多由并发感染引起的,感染的病原菌主要是革兰阴性菌,其中主要是肠杆菌科细菌[4-5]。目前全球耐药菌泛滥,SAP合并感染的耐药菌中又以多重耐药革兰阴性菌感染为主。耐碳青霉烯类肠杆菌科细菌(CRE)因其对大多数抗菌药物耐药率高而备受关注[6-7]。CRE是一类对碳青霉烯类抗菌药物耐药的肠杆菌科细菌[8-9]。近年来,随着CRE感染率逐年增长,给临床治疗带来了巨大挑战,但目前对SAP合并感染CRE的临床特点和危险因素分析的报道较少。因此,本文对此问题进行了流行病学相关分析和探讨,以期为预防和减少SAP合并感染CRE,降低其病死率提供临床循证依据。
1 资料与方法
1.1一般资料 通过重庆医科大学附属第一医院电子病例系统和临床微生物数据库,收集2011年4月至2019年12月在院治疗的105例非重复性SAP患者的临床资料,按是否合并感染CRE,分为试验组(35例)和对照组(70例)。同一病例住院后多次检出CRE,纳入第1次检出结果。SAP纳入标准:(1)符合SAP临床诊断标准[10];(2)临床资料完整;(3)住院时间>2 d。CRE的判断标准:仪器法药敏试验的耐药折点是亚胺培南或美罗培南≥4 μg/mL,厄他培南≥2 μg/mL。纸片扩散法的抑菌圈直径耐药折点是亚胺培南或美罗培南≤19 mm,厄他培南≤18 mm。
1.2方法 回顾性分析所有患者的临床资料,以下列参数作为潜在危险因素进行比较分析:(1)一般住院资料和基础疾病,包括患者总住院天数、检出CRE前的住院时间、重症监护室(ICU)住院时间、抗菌药物使用史等,以及胃肠系统疾病、心血管系统疾病等;(2)住院期间合并的感染包括尿路感染、呼吸道感染、腹腔内感染、血流感染、皮肤及软组织感染;(3)侵入性操作包括外科手术干预、穿刺引流术、经内镜逆行性胰胆管造影术(ERCP)、导尿管、气管切开、血液滤过;(4)检出CRE前的抗菌药物使用情况。
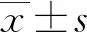
2 结 果
2.1两组患者年龄、性别比较 试验组35例,其中男22例、女13例,年龄30~75岁,平均(50.29±12.45)岁。对照组70例,其中男45例、女25例,年龄20~87岁,平均(53.34±16.88)岁。两组患者性别、年龄比较,差异无统计学意义(P>0.05),具有可比性。
2.2SAP合并感染CRE的情况及特征 试验组的标本类型中以腹腔引流液为主[17(48.57%)]、其次为血液[7(20.00%)]、痰液[4(11.43%)]等。试验组感染的CRE以肺炎克雷伯菌(42.86%)和大肠埃希菌(31.43%)为主,其次为阴沟肠杆菌(20.00%)和弗氏柠檬酸杆菌(5.71%)。
2.3SAP合并感染CRE的相关危险因素分析 对试验组和对照组进行单因素分析,结果显示,检出CRE前的住院天数,伴胃肠、肾脏等疾病,合并腹腔内感染、皮肤及软组织感染、休克、腹腔积液等并发症,进行气管切开、穿刺引流术、血液滤过等侵入性操作治疗,差异均有统计学意义(P<0.05),见表1。进一步多因素分析,结果显示,腹腔内感染、皮肤及软组织感染和血液滤过是SAP合并感染CRE的独立影响因素(P<0.05),见表2。
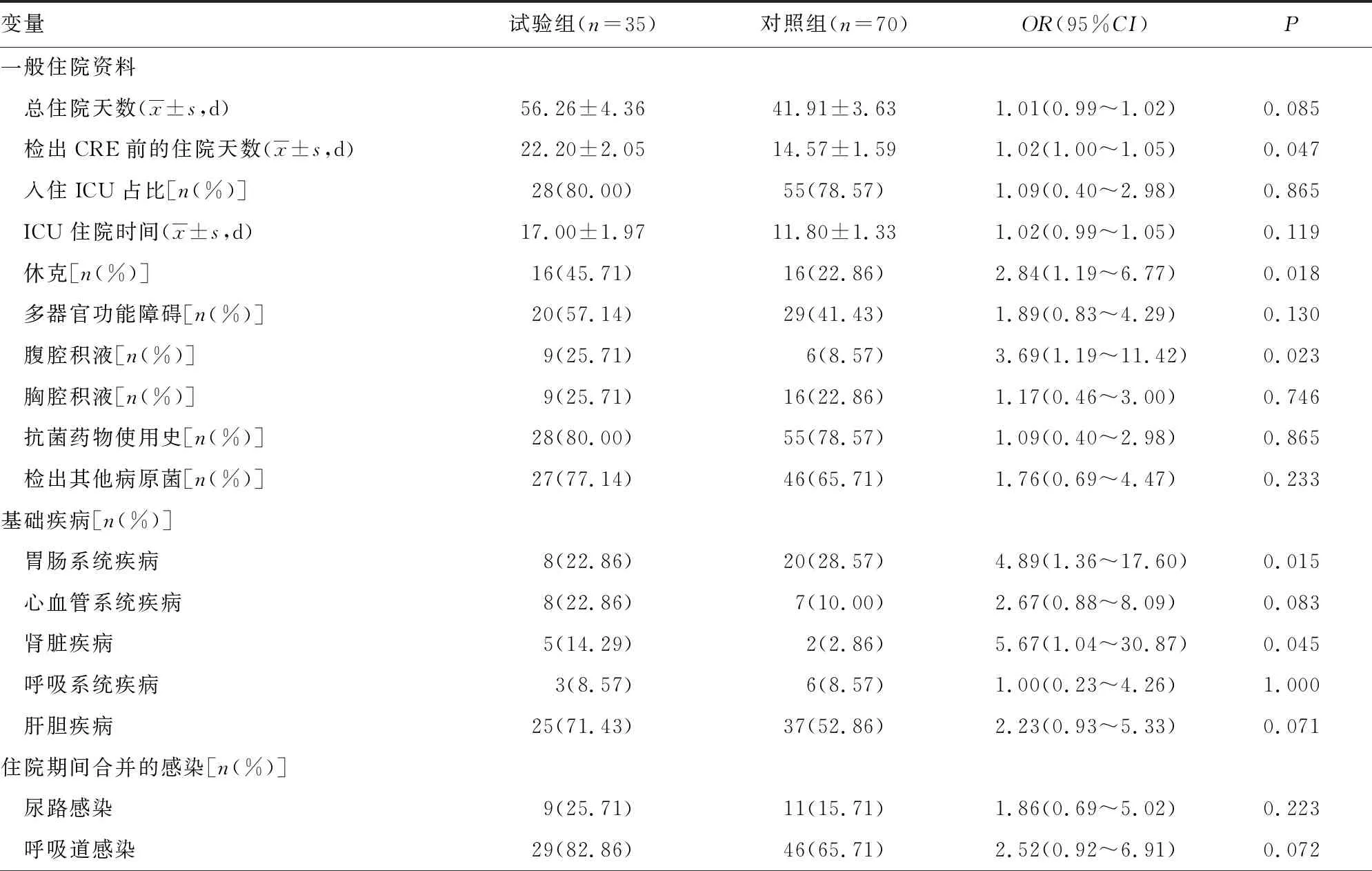
表1 SAP合并感染CRE的单因素分析
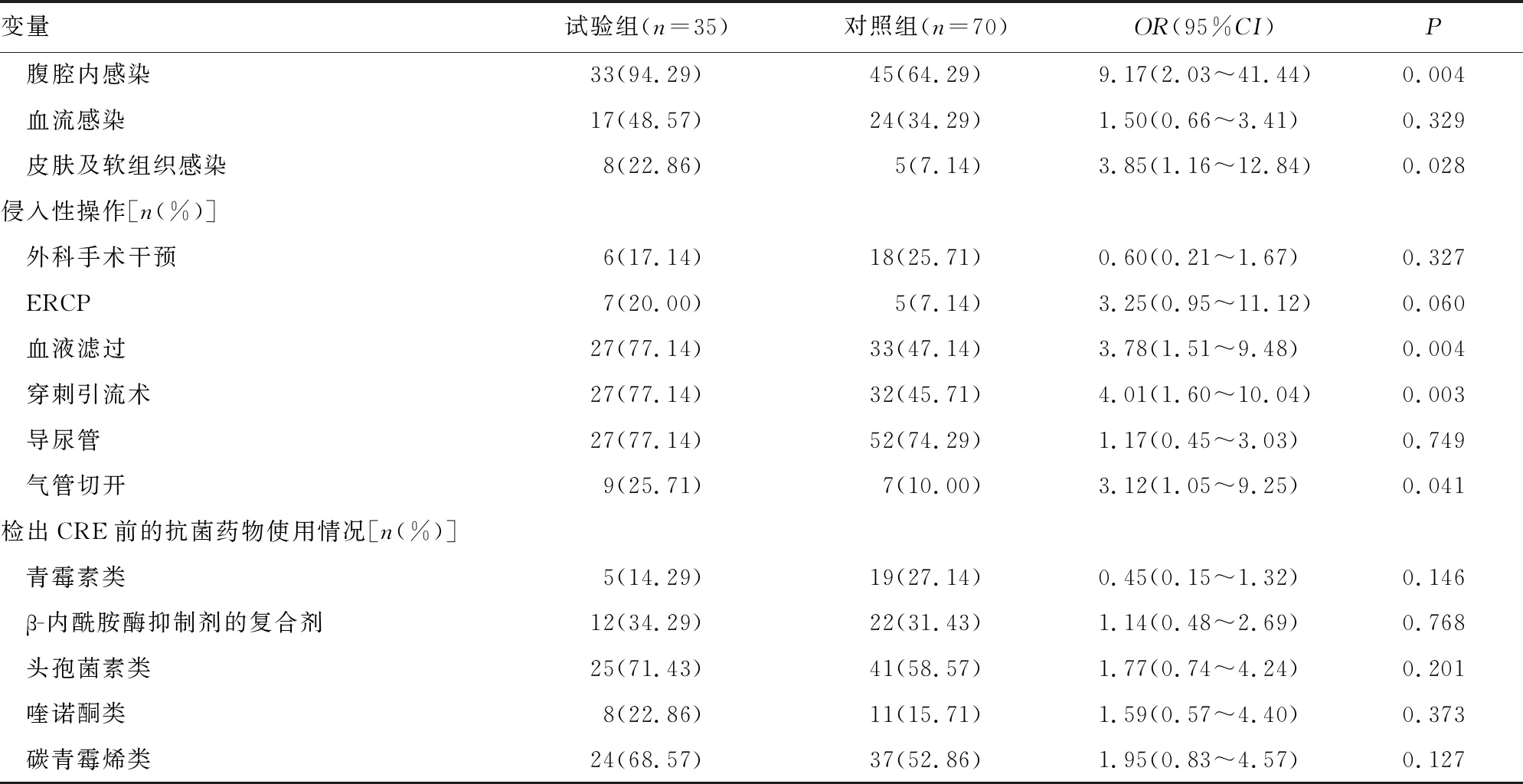
续表1 SAP合并感染CRE的单因素分析
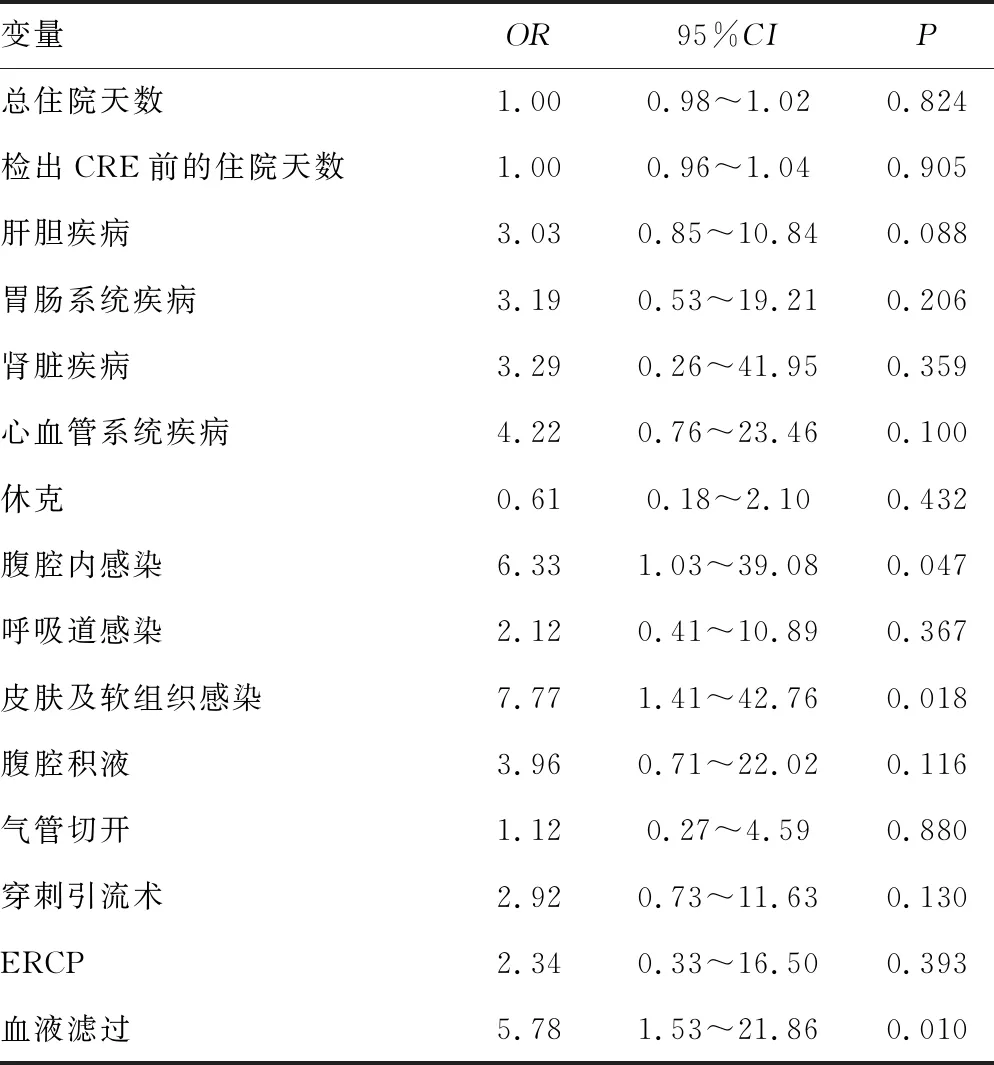
表2 SAP合并感染CRE的多因素分析
3 讨 论
SAP是一类临床常见消化系统的严重急腹症,病情非常复杂,具有并发症多、风险大等特征[11],尤其在疾病后期发生感染的概率和病死率均较高[12]。SAP患者合并感染的病原菌以革兰阴性菌为主,其中肠杆菌科细菌居多,其可引起呼吸道、泌尿道、腹腔和手术切口等多部位的感染,在临床分离的阴性菌中占比最高[13]。碳青霉烯类抗菌药物作为治疗多重耐药肠杆菌科细菌感染的首选药物,已在临床治疗上广泛使用,近年来由于耐碳青霉烯酶基因的出现和播散,给临床抗感染治疗带来了很大困难。
本研究中,SAP合并感染CRE患者中检出的细菌多来源于腹腔引流液,其中肺炎克雷伯菌最多(42.86%),大肠埃希菌次之(31.43%),与文献[14]报道结果较一致,也与中国CRE的流行情况一致[15-16]。根据2019年中国细菌耐药监测网数据显示,2005—2019年,肺炎克雷伯菌对美罗培南和亚胺培南的耐药率分别从2.9%和3.0%上升至26.8%和25.3%,这可能与其耐药机制有关,它可在质粒间传播,甚至可在不同菌株,不同地区与不同患者之间广泛传播[17]。
本研究的单因素分析中,SAP合并感染CRE与患者检出CRE前的住院天数,合并胃肠、肾脏基础性疾病,进行气管切开、穿刺引流术等治疗操作,以及并发休克、腹腔积液等密切相关,是CRE感染的危险因素。但在本研究的多因素分析中显示上述变量均不是SAP合并感染CRE的危险因素(P>0.05),这可能与样本量少及患者的个体差异等原因有关。
多因素分析的结果显示,SAP合并感染CRE的独立危险因素主要有3个:(1)SAP合并腹腔内感染。产生的原因可能是SAP患者发病早期存在局部炎性反应导致机体有血容量不足的情况发生,从而对体内脏器功能造成损伤,严重影响胃肠道的正常功能[18];同时在治疗期间的禁食禁饮等治疗方式极易增强患者肠壁通透性,可引发肠道黏膜萎缩、绒毛脱落等,导致大肠杆菌等常驻菌群发生移位进入腹腔,引起腹腔内感染,对患者的机体造成更严重的损伤[19-20];由于机体经过重创后,免疫力也下降,也更增加了CRE感染概率。(2)SAP合并皮肤及软组织感染。本研究发现几乎所有皮肤及软组织感染的SAP患者,均同时伴随腹腔内感染的发生。(3)进行血液滤过治疗。炎性因子“瀑布样”级联反应是SAP病程进展的关键[21],在临床治疗中,血液滤过因可有效清除大量炎性介质,恢复机体促抗炎平衡,是抢救SAP合并肾脏损伤主要方法[22]。但血液滤过治疗属于侵入性有创操作,需要进行穿刺插管建立有效的体外循环,而侵入性操作则极大增加了暴露于耐药菌的风险[23-24]。此外,SAP合并肾脏损伤的患者病情严重,自身免疫抵抗力较低,这些都增加了感染CRE的概率。
综上分析,为避免SAP合并感染CRE的发生,应尽早针对腹腔内感染,皮肤及软组织感染和血液滤过这些危险因素采取一系列保护措施,制订避免继发感染的有效治疗策略和适宜的护理方法,同时严格执行有创操作的适应证和无菌技术,使患者避免处于器械相关感染风险之中,是有效降低SAP合并感染发病率的重要举措。
