苯多羧酸分子标志物对生物炭吸附磷行为的表征
2021-03-15张军周丹丹常兆峰王薇李芳芳刘洋储刚古正刚
张军,周丹丹*,常兆峰,王薇,李芳芳,刘洋,储刚,古正刚
(1.昆明理工大学环境科学与工程学院,昆明650500;2.云南省土壤固碳与污染控制重点实验室,昆明650500;3.昆明理工大学建筑工程学院,昆明650500)
目前磷肥的过量施用加速土壤酸化,降低作物产量,造成水体污染及富营养化,并对生物多样性及人类健康构成威胁[1]。生物炭(Biochar)是生物质原料在无氧或缺氧的条件下热解形成的含碳量高的固态物质[2],因其具有比表面积大、表面官能团丰富、阳离子交换量较大且具有芳香性,能有效吸附重金属(Cu、Pb、Zn等)、N、P和有机污染物。因此,生物炭特性对其吸附污染物的行为至关重要。生物炭一旦施用于土壤中,并经过物理、化学及生物老化过程后,难以将其从土壤颗粒中分离出来。目前常用于生物炭特性定性或定量表征的方法(如扫描电镜−能谱、元素分析、核磁共振以及傅里叶红外光谱等[3]),难以从生物炭−土壤复杂混合体系中描述生物炭特性,成为动态表征生物炭环境效应的障碍。
分子标志物已被广泛应用于土壤及沉积物中碳行为研究,是有机地球化学研究领域的重要技术手段。其中,苯多羧酸(Benzene polycarboxylic acids,BPCAs)分子标志物已成功用于描述土壤中炭黑的来源和特性[4],为复杂体系中碳行为的研究提供了重要的技术方法。BPCAs分子标志物主要是通过对研究对象进行氧化处理,破坏浓缩度高的芳香结构而形成单个相对稳定的小芳香结构,如苯三甲酸(Benzene tricarboxylic acid,B3CA)、苯四甲酸(Benzene tetracarboxylic acid,B4CA)、苯五甲酸(Benzene pentacarboxylic acid,B5CA)等。一般认为,羧基取代的量越多,其芳香缩合度越高。B6CA/BPCA值可作为表征生物炭芳香族缩合或芳香性的指标,较高的B6CA/BPCA值通常具有较高的芳香性或缩合度[5]。因此,通过各个BPCAs单体分子的相对含量能够得到炭黑的性质和来源。这个技术的引入为复杂混合体系中生物炭特性描述提供重要的技术手段,从而有利于动态表征生物炭对污染物的吸附行为。本研究选择烟秆和松木为原料,在200~600℃下限氧制备生物炭,通过批量吸附实验,探讨了B6CA/BPCA值与生物炭吸附磷行为的联系。本研究将有助于动态表征生物炭施入土壤后对磷的吸附行为。
1 材料与方法
1.1 生物炭制备
制备生物炭所用的生物质原料:松木采自昆明市周边木材加工厂,烟秆采自楚雄某烟草种植区。将松木和烟秆于烘箱中60℃烘干,研磨粉碎后过60目筛,置于马弗炉中,通入氮气,在不同温度(200、400、600℃)下热解4 h制得生物炭。冷却至室温后装入瓶中保存待用,生物炭分别标记为WBC0、WBC200、WBC400、WBC600和TBC0、TBC200、TBC400、TBC600,WBC0和TBC0分别代表松木和烟秆,数字代表相应热解温度。
1.2 生物炭表征
称取0.4 g生物炭放于40 mL瓶中,加入40 mL去离子水,静置过滤,测定滤液的pH值[3];采用元素分析仪(Elementar Vario Micro Cube,Germany)测定生物炭中C、N、H、S和O元素的含量,并计算H/C、O/C和(N+O)/C原子个数比;比表面积(BET−N2)采用比表面积分析仪(JW−BK132F)进行表征;傅里叶红外光谱分析(FTIR)采用溴化钾压片法,生物炭样品与KBr以质量1∶1 000充分研磨混合并压片,并利用傅里叶红外光谱仪(Varian 640−IR)进行表征,其扫描区域为4 400~400 cm−1,分辨率4 cm−1,扫描次数为100次;样品于马弗炉中800℃加热4 h[6]测定其灰分含量。利 用Zeta分 级 器(BI−870,Brookhaven Instruments Corporation)测定生物炭Zeta电位[7]。
1.3 生物炭苯多羧酸分子标志物(BPCAs)的测定
根据Brodowski等[8]方法分析生物炭中的BPCAs,取5 mg生物炭放入反应釜中,加10 mL 4 mol·L−1三氟乙酸(TFA)溶液,105℃加热4 h。随后取出抽滤并用去离子水反复冲洗,40℃烘干。把滤渣放入反应釜中,加入2 mL 65%的HNO3,170℃加热8 h,冷却室后加10 mL去离子水过滤。取2 mL滤液,加入10 mL去离子水和100μL柠檬酸,混合均匀过阳离子交换层析柱(Dowex 50 WX8,200~400目),收集液体冷冻干燥。将处理过的含水样品冷冻干燥并重新溶解于甲醇中,并加入100μL联苯−2,2′−二羧酸酯,氮气吹扫干燥,然后加入100μL无水吡啶和100μL BSTFA+TMCS,烘箱80℃反应2 h,进行衍生化处理。冷却至室温后放入冰箱冷藏24 h,进气相色谱−质谱联用仪(Agilent,7890A GC equipped with a 5975C quadrupole mass selective detector)测定BPCAs。
1.4 批量吸附实验
利用KH2PO4在去离子水中配制浓度为50 mg·L−1的P标准储备溶液(以分子式中P含量计算),其中KH2PO4为优级纯。将储备液用去离子水稀释成浓度范围为1~20 mg·L−1P溶液。每个吸附曲线包括8个浓度,每个浓度进行两个重复实验。根据预实验结果,本实验按照固液比为1∶100(m∶m),称取40 mg生物炭放入40 mL螺口玻璃样品瓶中,分别加入40 mL浓度为1~20 mg·L−1的P溶液,于20℃下以120 r·min−1振荡7 d,悬浊液以2 500 r·min−1离心10 min,过0.45μm微孔滤膜,采用钼酸铵分光光度法(GB 11893—1989)测定P的浓度,通过方程(1)计算在不同初始浓度下,生物炭对P的吸附量。
式中:Qe为吸附平衡时生物炭对P的吸附量,mg·kg−1;C0和Ce分别为初始和吸附平衡时溶液中P的浓度,mg·L−1;V为溶液体积,mL;m为生物炭质量,mg。
1.5 数据分析
借助Excel 2013进行数据处理,使用Langmuir(公式2)和Freundlich(公式3)模型拟合吸附等温线,并使用SigmaPlot 10.0进行数据拟合,公式如下:
式中:Qe和Qm分别为平衡吸附量和吸附容量,mg·kg−1;Ce为平衡溶液中P的浓度,mg·L−1;KL为Langmuir模型吸附系数,L·kg−1;KF为Freundlich模型吸附系数,(mg·kg−1)·(mg·L−1)−n;n为Freundlich常数。
单点吸附系数(Kd,L·kg−1)可以表征生物炭对P的吸附量大小,Kd值越大,吸附量越大,其公式为:
由于数据点的数量和模型中系数的数量不相同,常用的决定系数R2不能直接进行比较。通过公式(4)将R2转化为R2adj进行比较[9]:
式中:m为用于拟合的数据点数量;b为方程中系数的数量。
2 结果与讨论
2.1 生物质及生物炭的特性
生物质及生物炭的理化性质见表1。因松木中木质素含量高于烟秆[10],在热解过程中木质素含量对焦炭产物的贡献率较高[11],从而导致松木生物炭产率高于烟秆生物炭产率。随着热解温度的升高,生物炭中C含量增加,而O和H含量降低,这是由于生物质在热解过程中发生脱水、脱羧基和脱氢等作用,其所含饱和脂肪烃向不饱和脂肪烃和芳香烃转化而产生[6]。烟秆生物炭的N含量明显高于松木生物炭,这与烟秆在种植过程中施加大量氮肥使得大量氮素在烟秆中累积[12]所致。生物质和200℃生物炭的H/C均较高(H/C>1.0),这与生物质和200℃生物炭中含有大量原始有机物,如聚合物?H2、脂肪酸、木质素(芳香核心)和一些纤维素(极性部分)有关[13]。热解温度升高,生物炭中H/C和O/C急剧下降,表明高温使得生物炭炭化程度增加,并使其疏水性[13]及芳香化程度增强[3]。
生物炭比表面积随热解温度升高而增大,热解温度在200~400℃时,生物炭比表面积增加比较缓慢,当热解温度达到600℃时,比表面积迅速增加。这可能是因为热解温度升高至600℃时,生物炭中所含的挥发性有机物迅速增加并随通入的氮气排出,使其在生物炭中的残留量减少,进而促使生物炭孔隙结构发育得更好[14]。另外,热解温度低于600℃时,烟秆生物炭比表面积高于松木生物炭。这与该热解温度下生物质中半纤维素和纤维素比木质素更容易迅速分解,使得生物炭孔隙结构发育得更好[15]有关。
随热解温度的升高,生物炭中灰分含量和pH值不断增加,这表明热解过程中生物质中大部分无机矿物成分不断积累并保留在生物炭中[14]。
2.2 BPCA分子标记对生物炭属性的描述
两类生物炭中BPCAs的含量均随热解温度的增加而增加。如松木原生质中BPCAs含量为21.41 mg·g−1C(WBC0),600℃松木生物炭中BPCAs含量为397.32 mg·g−1(WBC600),增加了近18倍(图1)。随着热解温度的升高,BPCAs的含量明显增加,而H/C呈减少趋势(表1),BPCAs和H/C的变化趋势均说明生物炭中形成了不饱和碳结构,如芳香环结构[5]。另外,对比两类生物质及其制备的生物炭发现,松木及其制备的生物炭BPCAs含量>烟秆及其制备的生物炭,可能原因是松木比烟秆含有更多的木质素成分,而芳香环结构主要由木质素贡献[3]。
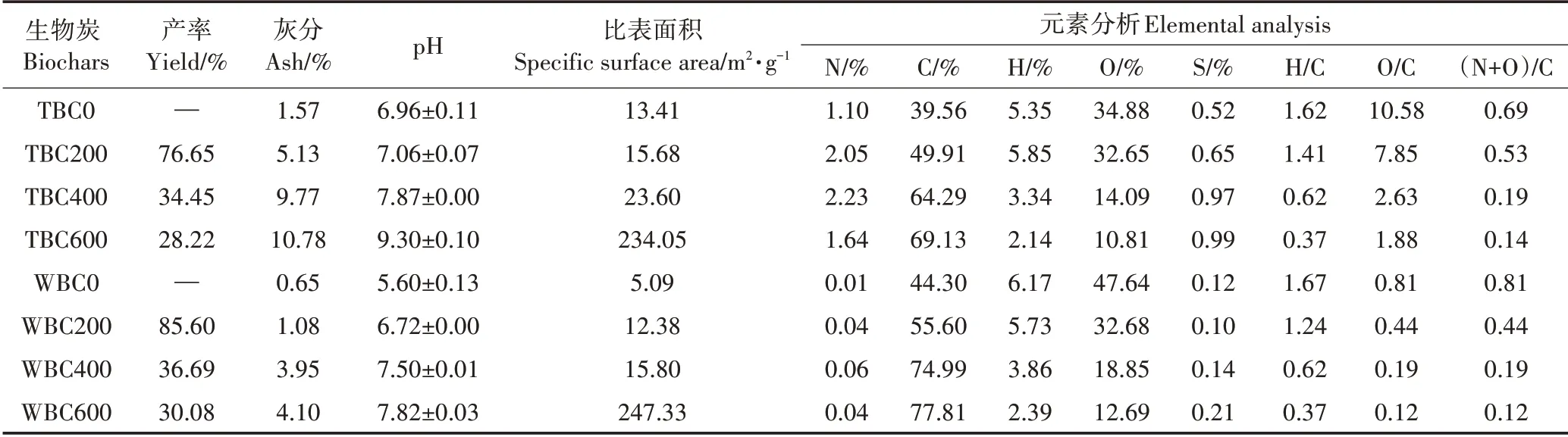
表1 生物炭的物理化学性质Table 1 Physical and chemical properties of biochars
通常用单个BPCA分子标记的贡献来推断芳香簇的大小,特别是B6CA的含量[16]。随着温度的升高,特别是从400℃到600℃,B6CA的相对含量随之增加,分别从58.24 mg·kg−1C(TBC400)增加到238.18 mg·kg−1C(TBC600)和从65.40 mg·kg−1C(WBC400)增加到216.34 mg·kg−1C(WBC600)(图1)。两类生物炭中B6CA对BPCA的贡献率随热解温度的升高而增加,如热解温度≤400℃制备的生物炭中B6CA含量介于15%~31%,而600℃生物炭中B6CA含量增至54%~62%,600℃生物炭中B6CA对BPCA的贡献率均高于50%(图2),这表明生物炭的芳香缩合度随热解温度升高不断增强[5],这与元素分析中H/C的结果一致。
2.3 生物炭的FTIR光谱图
图3 为生物质及生物炭的FTIR光谱图。随着热解温度的升高,在3 400 cm−1附近的羟基[6]伸缩振动峰减小,这是因为在炭化过程中,生物质发生脱水和脱羟基作用,使得羟基大量减少,吸收峰明显变弱[14]。2 975、2 886 cm−1为存在于脂肪族和脂环族化合物中的CH或CH3伸缩的峰,1 051 cm−1处为脂肪族CO伸缩的峰,当热解温度≥400℃时,CH伸缩振动峰消失,表明随着热解温度的升高,生物炭中的非极性脂肪族官能团不断减少。对于TBC0样品,在1 720 cm−1处发现COOH的CO伸缩峰在随热解温度的升高后消失,在松木生物炭中也发现类似的结果,可能是因为含氧官能团被热解分裂导致羧基的减少和消失。CO键在高热解温度(≥600℃)下易被热解生成气体或液体产物,所以1 616 cm−1处酮类中的CO键于600℃后显著减少。波数位于1 385 cm−1处的酚羟基的OH伸缩振动,在TBC中表现出随热解温度的升高逐渐减弱,而在松木生物炭中没有明显变化。结果表明,随热解温度的升高,含氧官能团等含量呈下降趋势,热解温度升高可能降低官能团活性[17]。
2.4 生物炭的Zeta电位
两类生物炭的Zeta电位均为负值且随热解温度的升高呈现逐渐下降趋势(图4),烟秆生物炭和松木生物炭的Zeta电位分别从−17.63 mV和−14.47 mV降至−43.36 mV和−22.93 mV。生物炭表面的羟基和羧基官能团是其表面带负电荷的主要因素[18],热解温度升高,羟基和羧基官能团的去质子化增强,生物炭表面负电荷量增加[19],从而使生物炭的Zeta电位降低。
2.5 生物炭对P的吸附等温线
由于WBC0前4个浓度点吸附出现负值导致WBC0无法拟合,这可能是WBC0吸附量较低所致。除了WBC0外,利用Freundlich和Langmuir对两类生物质及其制备的生物炭吸附P的等温线进行拟合(图5),其拟合参数见表2。Langmuir对烟秆及其制备的生物炭吸附P的等温线拟合,其调整后可决系数(Radj2,0.739~0.962)大于Freundlich的(0.748~0.953),说明Langmuir更适合描述烟秆及其制备的生物炭对P的吸附。对松木及其制备的生物炭来说,Freundlich对其吸附P的等温线拟合,其调整后可决系数(Radj2,0.810~0.976)大于Langmuir的(0.726~0.975),表明Freundlich更适合描述松木生物炭对P的吸附。由表2可以看出,松木200℃生物炭的非线性较弱(n值为0.94),但随热解温度的升高,n值逐渐降低,达到600℃时,n值降低为0.17,显示出明显的非线性吸附特征。然而,烟秆生物炭却表现出相反结果,随热解温度升高,n值逐渐升高,非线性吸附特征逐渐减弱。相关研究认为,n值大小可反映出吸附位点的能量分布,n值越小,吸附位点能量分布范围越大[20]。通过n值与生物炭性质的关系(图6)可发现,随热解温度增加,Freundlich模型的非线性因子n值与WBC的B5CA/B6CA及H/C原子比均呈显著正相关(P<0.01),而TBC反之。土壤中测得的H/C不仅来源生物炭,还有可能来源于其他有机组分,而BPCA可识别炭黑的来源和性质,生物炭具有与炭黑相似的结构单元。因此,可将BPCA分子标志物法用于生物炭定性和定量分析中[5]。相关性分析表明,如获得并组合更多数据,则可建立B5CA/B6CA和n值之间的定量关系。

表2 Freundlich模型和Langmuir模型吸附等温线拟合参数Table 2 Freundlich and Langmuir isotherm fitting results of phosphorus adsorption
通过计算不同浓度P(1、10 mg·L−1)条件下,生物炭对P吸附的吸附系数(Kd,见表2)发现,随着P浓度的增加,Freundlich中两类生物炭的Kd值均有所下降,这是因为生物炭对P的吸附为非线性吸附(图5)。表2显示了烟秆和松木生物炭对P酸盐的最大吸附量Qm值,两类生物炭对磷酸盐的Qm值差别较大。随热解温度的升高,烟秆生物炭对P的吸附呈现先增大后减小的趋势,其拐点出现在热解温度为400℃时,其Qm=583.51 mg·kg−1。这种现象可以从3个方面进行解释。其一,随热解温度升高,烟秆生物炭比表面积的增加能够为P提供更多的吸附位点,从而促进生物炭对P的吸附;其二,当热解温度≥400℃时,烟秆生物炭表面含氧官能团下降以及B6CA含量增加,导致生物炭吸附P的位点减少,进而使生物炭对P的吸附量降低。其三,热解温度≥400℃时,体系中pH为7.80~9.30,P的主要形态主要为HPO2−4,呈负电性[21],且Zeta电位为−42.36 mV,从而使生物炭与P之间的静电斥力大量增加,吸附量降低。
松木生物炭的Qm值随热解温度的升高而降低,200℃生物炭对P的吸附量最大为921.11 mg·kg−1。这可能与两个方面因素有关。一是随着热解温度的升高,生物炭表面含氧官能团减少,B6CA含量增加,从而使P在生物炭上的吸附量降低。二是松木生物炭Zeta电位范围为−22.93~−14.47 mV(图4),体系pH值范围为5.00~8.00,P的主要形态为H2PO−4,使得生物炭表面与P形成静电排斥而减少其对P的吸附。
烟秆生物炭对P的吸附量高于松木生物炭,这与生物炭中B6CA含量有关。烟秆生物炭中B6CA含量明显低于松木生物炭(图1),从而使得烟秆生物炭芳香化程度低于松木生物炭,进而使烟秆生物炭对P的吸附高于松木生物炭。
生物炭对P的吸附量随着初始浓度的增加而增加,烟秆生物炭对P的吸附量略大于松木生物炭,这与烟秆生物炭的比表面积高于松木生物炭有关(表1)。对烟秆生物炭来说,生物炭对P的吸附量随热解温度的升高呈现先增加后降低的趋势,拐点出现在热解温度为400℃时,TBC400对P的吸附量最大为583.51 mg·kg−1,可能是因为从400℃到600℃,生物炭表面官能团减少(图3),使得600℃生物炭吸附量降低,这与Chang等[5]的研究结果一致。
此外,松木不能从较低浓度P溶液中吸附P(即较低浓度时出现负值),而在较高浓度溶液中发现少量P吸附(图5),这可从3个方面进行解释。其一,松木比表面积较低(5.09 m2·g−1)且Zeta为−14.47 mV,从而导致P的吸附量很低或者没有吸附;其二,松木本身含有一定的P,且生物炭中的P主要以无机P形式存在,在吸附过程中,生物炭中的有效P不断解吸出来[22],从而增加了溶液中P的浓度;其三,高浓度的P有较低的pH值(图7),允许P与其他阴离子(如硝酸盐、硫酸盐)发生静电交换[23],使得高浓度的P能吸附在生物炭上。
3 结论
(1)随着热解温度的升高,生物炭的比表面积不断增大,O和H含量、H/C、O/C和(N+O)/C的比值均逐渐降低,说明生物炭芳香性逐渐增强,极性逐渐降低,含氧官能团不断减少。
(2)BPCA分子标志物对生物炭性质研究表明,生物炭的芳香缩合度随热解温度升高不断增强。烟秆生物炭中B6CA含量明显低于松木生物炭,使烟秆生物炭芳香化程度低于松木生物炭,进而使烟秆生物炭对P的吸附高于松木生物炭。
(3)Langmuir模型更适合描述烟秆及其制备的生物炭对P的吸附,而Freundlich模型更适合描述松木生物炭对P的吸附。从吸附性能上看,生物炭中表面含氧官能团的减少和静电排斥作用降低了生物炭对P的吸附,而比表面积大使烟秆生物炭的吸附量高于松木生物炭。
