真空蒸馏法脱除区熔锗渣中杂质的研究
2021-03-11崔丁方廖吉伟王艺曌恒2斌2
崔丁方,廖吉伟,王艺曌,熊 恒2,,杨 斌2,
(1.云南驰宏国际锗业有限公司,云南 曲靖 655000;2.昆明理工大学复杂有色金属资源清洁利用国家重点实验室,云南 昆明 650093;3.昆明理工大学真空冶金国家工程实验室,云南 昆明 650093;4.昆明理工大学云南省有色金属真空冶金重点实验室,云南 昆明 650093;5.昆明理工大学 冶金与能源工程学院,云南 昆明 650093)
锗是一种稀散金属,没有独立的矿床,在半导体[1]、太阳能光伏电池[2-5]、光纤通讯[6]、红外光学材料[7,8]、有机保健食品[9]、聚酯PET催化剂[10]等领域应用广泛。我国是最大的初级锗产品生产国,但高端的生产技术仍被发达国家所垄断[11]。目前,锗是以现有锗资源为原料来制取,包括含锗烟尘和炉渣、锌冶炼副产品等[12],长期以往,会造成锗资源稀缺,且资源开采对环境也会造成一定的破坏,不利于循环发展。为了应对未来资源和环保问题,找到一种高效处理区熔锗渣的方法至关重要,迫在眉睫,也是大势所趋。
如今,社会对半导体新材料的要求远胜从前,对金属锗纯度有着极高的要求,但用化学法难以实现生产高纯锗,采用物理法提纯锗将作为高纯、超高纯锗生产的重要方法。美国劳伦斯伯克利国家实验室1978年以本征锗为原料,镀二氧化硅膜石英舟为容器,通过区熔提纯,可以得到净电活性杂质浓度|NA-ND|≤2×1010 cm-3的高纯锗材料[13],国内超高纯锗的提纯研究报道较少,1988年白尔隽等[14,15]利用国产材料进行锗提纯,得到了~1010cm-3纯度的超高纯锗材料。Yang G等[16]也在南达科他大学进行了高纯锗的区熔提纯研究,采用两步提纯(石墨舟内提纯和石英舟内提纯),得到了大约1011cm-3纯度的超高纯锗材料。
对于生产高纯、超高纯锗,真空蒸馏是其他方法无法代替的,其原理是在高温和真空条件下利用金属蒸气压的差异性来实现有效分离。每种金属在特定的温度范围下有一定的蒸气压和蒸气分子结构,在温度不变的情况下,环境的气体压强会影响金属的蒸发温度、饱和蒸汽压以及挥发速率,这些对金属的真空蒸馏有直接的作用[17]。真空蒸馏具有流程短、污染小、金属回收率高、加工费用低的优势。对于处理火法炼锌的副产物硬锌,有人曾用真空蒸馏法实现锗与其他金属分离,控制适当的蒸馏温度,可以使绝大部分的铅、锌、砷挥发,而绝大部分的锗将与铜、铁一起留于残渣中,达到锗与大部分杂质分离的目的[18]。本研究拟采用真空蒸馏和区域熔炼两种物理的方法实现锗合金的高效处理,旨在为高效、绿色制取高纯锗提供支持。
1 锗与十二种主要杂质挥发反应的热力学分析
根据经典热力学计算获得不同压力条件下Ge及Mg、Al、Ca、Fe、Co等十三种物质纯金属挥发反应的理论开始反应温度,结果如表1所示。

表1 不同压力条件下纯金属挥发反应的理论开始反应温度/K
由表1可以看出,不同压力条件下十三种物质随蒸馏温度升高的挥发先后顺序为 :In、Zn、Mg、As、Ca、Pb、Al、Cu、Fe、Ni、Co、Ge、Si。理论计算可知In的挥发反应很容易发生,105Pa条件下,温度低于800K挥发反应就能发生,因此表1中没有列出对应的数值。
十二种纯金属与纯Ge挥发反应的理论开始反应温度比值如表2所示。在相同压力条件下,理论开始反应温度比值小于1的物质,随温度升高,优先于锗挥发进入气相;反之亦然。

表2 不同压力条件下12种物质与Ge理论开始反应温度的比值
由表2通过比较可以得出,Mg、Ca、Zn、Pb、As比值比1小且比值偏离1较多,这5种元素将优先于锗挥发进入气相;Al、Cu比值小于1且接近1,这2种元素与锗分离相对困难;Fe、Co、Ni、Si比值大于1,难于锗挥发。
2 实验
2.1 研究目标
以区熔锗渣为原料,开展百克级真空蒸馏实验,考察不同蒸馏温度、蒸馏时间条件下,区熔锗渣中Mg、Al、Ca、Fe、Co、Ni、Cu、Zn、In、Pb/Bi、As、Si十二种杂质元素的去除效果与规律。
2.2 研究内容
(1)真空条件下,Ge、Mg、Al、Ca、Fe、Co等十三种元素挥发反应的热力学计算分析。查阅并收集Ge、Mg、Al、Ca、Fe、Co等十三种物质挥发反应的热力学数据,以经典热力学方法计算对应挥发反应的-T关系,计算不同压力条件下十三种物质对应反应的理论开始反应温度,获得十三种物质真空条件下挥发的先后顺序。
(2)开展区熔锗渣百克级真空蒸馏实验,获得Mg、Al、Ca、Fe、Co等十二种杂质元素的去除效果和规律。
2.3 实验原料
本次实验原料区熔锗渣GD-MS分析结果如表3所示。
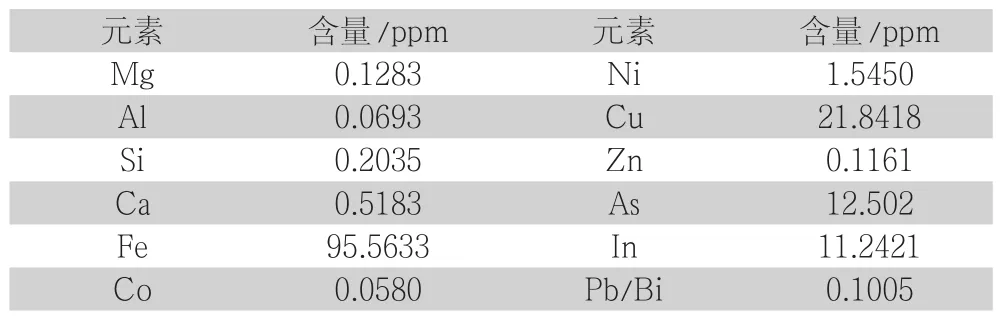
表3 区熔锗渣GD-MS分析结果
2.4 实验设备
真空蒸馏实验设备如表4所示。

表4 真空蒸馏实验设备
真空蒸馏炉、辉光放电质谱仪如图1、2所示。

图1 真空蒸馏炉

图2 辉光放电质谱仪(GD-MS)
2.5 实验步骤
2.5.1 准备阶段
实验前对样品、石墨坩埚、冷凝盖和冷凝盘和真空炉内壁用酒精清理。
2.5.2 操作步骤
(1)准确称量实验样品、石墨坩埚、冷凝盖和冷凝盘;
(2)将样品放入石墨坩埚内,置于真空炉内,保证石墨坩埚处于炉子中央恒温区,将冷凝盘逐一叠放并放入真空炉盖上冷凝盘放置区域,关闭真空炉盖,锁上炉体锁扣;
(3)开启冷却水,检查水路;
(4)设置控温程序;
(5)检查放气阀是否关死,打开真空泵,抽真空;
(6)炉内残压<30Pa时打开加热开关并运行控温程序;
(7)按实验方案进行升温、保温,实验结束后关闭加热电源,将真空炉内温度冷却至室温;
(8)开启放气阀,待炉内压力升高至室温后,打开炉盖,取出蒸馏残留物和挥发物,盖上炉盖,再次将炉子抽至真空状态,关闭冷却水,关闭电源;
(9)准确称量石墨坩埚、冷凝盖和冷凝盘,将蒸馏残余物取出后,再次称量石墨坩埚、冷凝盖和冷凝盘,并将数据准确无误的记录在实验记录本上。
2.6 试验方案
由于真空炉预实验结果压力为(4~8)Pa,且锗的熔点为1211K,根据表1、表2热力学分析,设计了如表5的式样方案。第一阶段考察温度、蒸馏时间对杂质脱除的影响;第二阶段进一步验证蒸馏时间对十二种杂质元素的脱除的影响;第三阶段考察区熔锗渣挥发的最低温度。设计了第二阶段的实验。

表5 实验方案
2.7 数据分析方法
本次实验经真空蒸馏后获得的残留锗(后称蒸馏残留物),将与经提纯的三组6N区熔锗锭样品化学成分平均值作为参照,三组样品GD-MS分析结果如表6所示。

表6 区熔锗锭化学成分/ppm
3 结果分析与讨论
3.1 第一阶段实验结果分析与讨论
(1)实验结果
第一阶段实验结果如表7所示M投-30、M投-180、分别表示区熔锗渣30min、180min投入量,M产-30、M产-180分别表示30min、180min蒸馏残留物质量,GD-MS分析如附表1~8所示,以下结果分析均以平均含量为依据讨论。
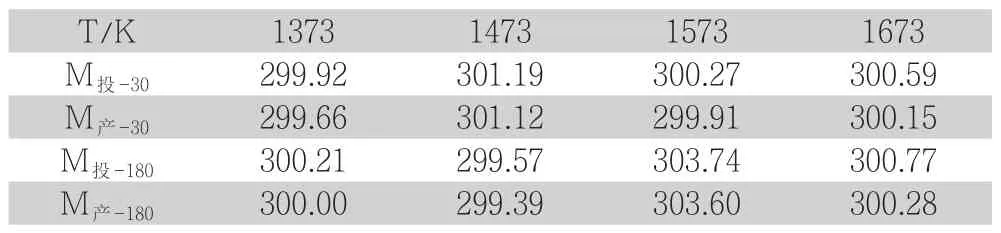
表7 实验结果/g
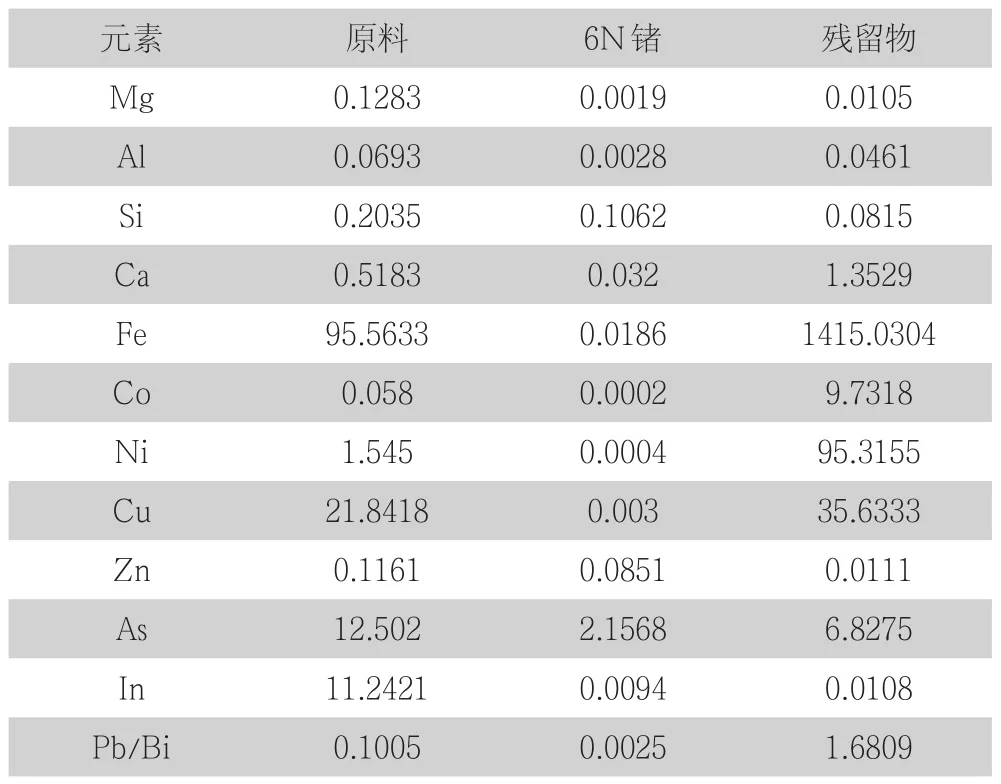
表8 残留物、原料、6N锗中元素成分/ppm
(2)分析与讨论
依据附表1~8的实验结果,绘制了不同蒸馏温度和蒸馏时间条件下,原料、6N锗与Mg、Al、Si、Ca等十二种不同杂质元素蒸馏残留物的关系图,如图3~14所示。

图3 原料、6N锗与区熔锗蒸馏残留物中Mg的含量关系
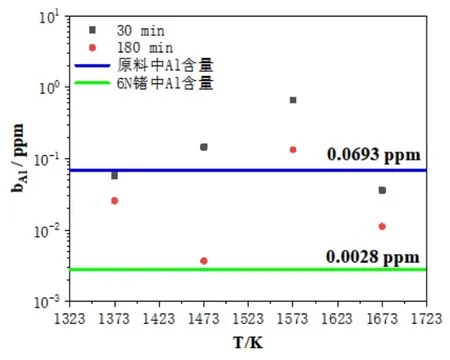
图4 原料、6N锗与区熔锗蒸馏残留物中Al的含量关系
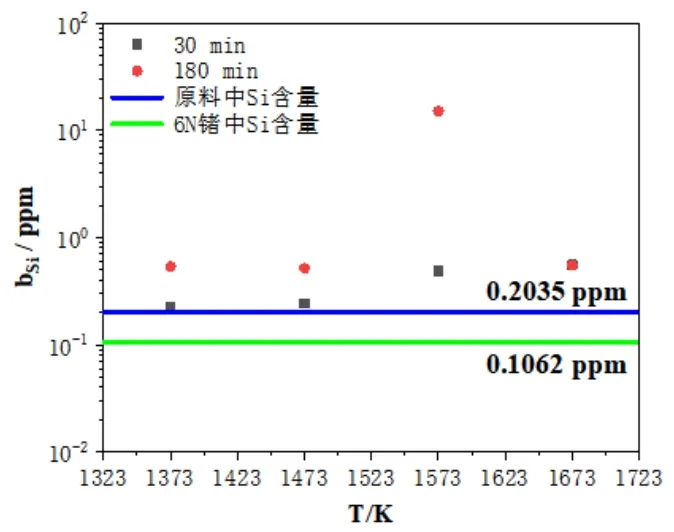
图5 原料、6N锗与区熔锗蒸馏残留物中Si的含量关系
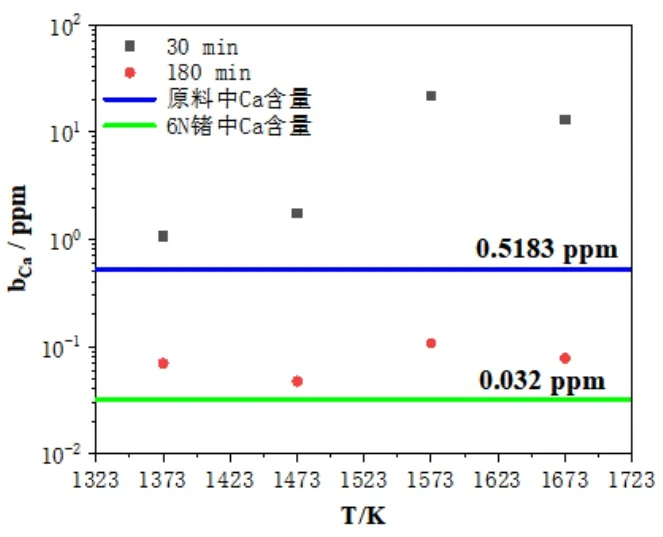
图6 蒸原料、6N锗与区熔锗蒸馏残留物中Ca的含量关系
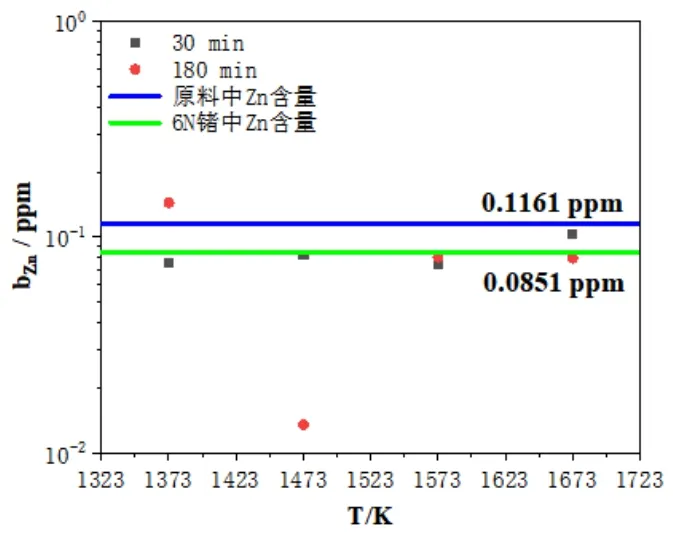
图7 原料、6N锗与区熔锗蒸馏残留物中Zn的含量关系

图8 原料、6N锗与区熔锗蒸馏残留物中As的含量关系
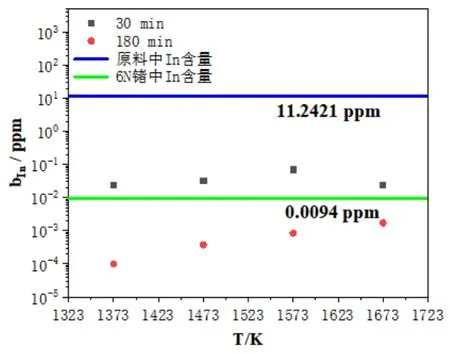
图9 原料、6N锗与区熔锗蒸馏残留物中In的含量关系

图10 蒸原料、6N锗与区熔锗蒸馏残留物中Pb/Bi的含量关系

图11 原料、6N锗与区熔锗蒸馏残留物中Fe的含量关系

图12 原料、6N锗与区熔锗蒸馏残留物中Co的含量关系

图13 原料、6N锗与区熔锗蒸馏残留物中Ni的含量关系
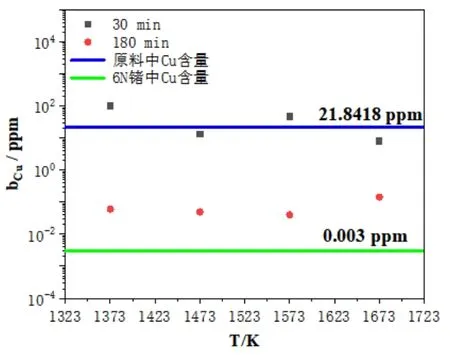
图14 原料、6N锗与区熔锗蒸馏残留物中Cu的含量关系
由图3可以看出,在蒸馏温度(1373~1573)K,蒸馏时间30min条件下,区熔锗蒸馏残留物中Mg含量较原料有所降低,达不到6N锗产品标准,降低了近一个数量级,当温度高于1673K,Mg的含量达到6N锗产品标准;在蒸馏温度(1373~1673)K,蒸馏时间180min条件下,Mg脱除至6N锗产品标准以下。
由图4可以看出,在蒸馏温度(1373~1673)K,蒸馏时间30min条件下,区熔锗蒸馏残留物中Al含量变化不大;蒸馏时间延长至180min,Al由一定脱除效果。
由图5可以看出,在(1373~1673)K,蒸馏时间(30~180)min范围内,区熔锗蒸馏残留物中Si富集,无法进行脱除。
由图6可以看出,在(1373~1673)K,蒸馏时间30min条件下,区熔锗蒸馏残留物中Ca富集,无法进行脱除;保温时间延长至180min,区熔锗蒸馏残留物中Ca含量较原料有所降低,但达不到6N锗产品标准。
由图7可以看出,在(1373~1673)K,蒸馏时间(30~180)min条件下,区熔锗蒸馏残留物中Zn含量较原料有所降低,部分实验数据表明Zn含量达到6N锗产品标准。
由图8可以看出,在(1373~1673)K,蒸馏时间30min条件下,区熔锗蒸馏残留物中As含量变化不大,保温时间延长至180min,区熔锗蒸馏残留物中As含量较原料有所降低,达到6N锗产品标准。
由图9可以看出,在蒸馏温度(1373~1573)K,蒸馏时间30min条件下,区熔锗蒸馏残留物中In含量较原料有所降低,达不到6N锗产品标准,降低了近两个数量级,当温度高于1673K,In的含量达到6N锗产品标准;在蒸馏温度(1373~1673)K,蒸馏时间180min条件下,In脱除至6N锗产品标准以下。
由图10可以看出,在蒸馏温度(1373~1573)K,蒸馏时间30min条件下,区熔锗蒸馏残留物中Pb/Bi得到了富集;保温时间延长到180min,Pb/Bi完全脱除。
由图11~14可以看出,在蒸馏温度(1373~1673)K,蒸馏时间30min和180min条件下,Fe、Co、Ni、Cu变化和规律一致,相同温度条件下蒸馏时间延长含量降低。根据理论计算,在此条件下Fe、Co、Ni、Cu均无法挥发,含量应比原料中各自元素的含量高,与实际情况不符。
3.2 第二阶段实验结果分析与讨论
由图15可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,区熔锗蒸馏残留物中Mg含量有所降低,较原料降低了近2个数量级;对比图3分析,Mg的含量可达到6N锗产品标准。
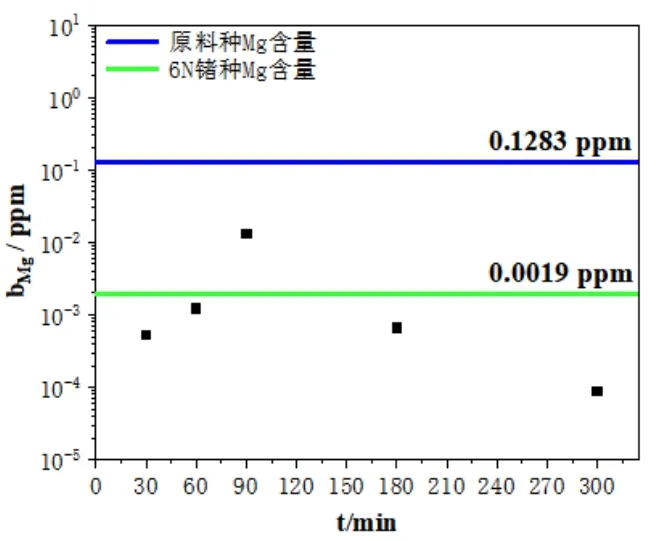
图15 原料、6N锗与区熔锗蒸馏残留物中Mg的含量关系
由图16可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,区熔锗蒸馏残留物中Al含量变化不大,对比图4分析,Al不能脱除;

图16 原料、6N锗与区熔锗蒸馏残留物中Al的含量关系
由图17可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,区熔锗蒸馏残留物中Si得到了富集,对比图5分析,Si不能脱除;

图17 原料、6N锗与区熔锗蒸馏残留物中Si的含量关系
由图18可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,区熔锗蒸馏残留物中Ca得到了富集,对比图6分析,Si不能脱除;

图18 原料、6N锗与区熔锗蒸馏残留物中Ca的含量关系
由图19可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,Zn含量可以达到6N锗产品标准,图7也证明了这一事实。
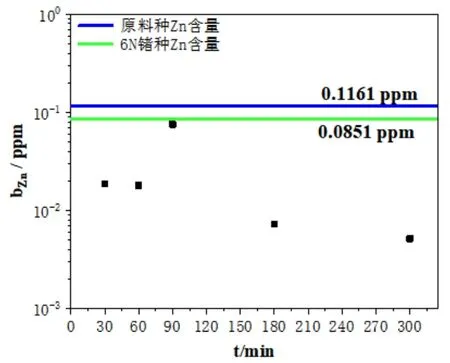
图19 原料、6N锗与区熔锗蒸馏残留物中Zn的含量关系
由图20可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,随着时间的延长,As的含量先降后升,60min达到6N锗产品标准;其余条件As含量均高于原料。

图20 原料、6N锗与区熔锗蒸馏残留物中As的含量关系
由图21可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,区熔锗蒸馏残留物中In含量有所降低,区较原料降低了近2个数量级;比图9分析,In的含量可达到6N锗产品标准。
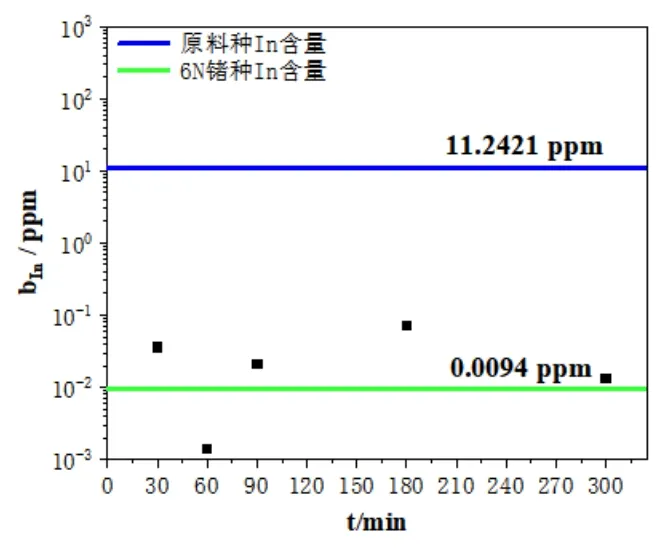
图21 原料、6N锗与区熔锗蒸馏残留物中In的含量关系
由图22可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,区熔锗蒸馏残留物中Pb/Bi的含量达到6N标准;比图10分析,蒸馏时间超过60min Pb/Bi脱除效果很好。

图22 原料、6N锗与区熔锗蒸馏残留物中Pb/Bi的含量关系
由图23~26可以看出,在蒸馏温度1673K,蒸馏时间(30~300)min条件下,区熔锗蒸馏残留物中Fe、Co、Ni、Cu得到了富集;对比图11~14分析,实际与理论计算相符。

图23 原料、6N锗与区熔锗蒸馏残留物中Fe的含量关系

图24 原料、6N锗与区熔锗蒸馏残留物中Co的含量关系

图25 原料、6N锗与区熔锗蒸馏残留物中Ni的含量关系

图26 原料、6N锗与区熔锗蒸馏残留物中Cu的含量关系
3.3 第三阶段实验结果分析与讨论
蒸馏温度为1273K、蒸馏时间180min、压力(4~8)Pa的真空蒸馏实验,真空蒸馏残留物GD-MS检测结果如附表14,将其整理为残留物、原料、6N锗中元素成分如表8所示。
由表8可以看出,蒸馏温度为1273K、蒸馏时间180min、压力(4~8)Pa的真空蒸馏实验,对比原料化学成分Ca、Fe、Co、Ni、Cu、Pb/Bi得到了富集 ;Mg、Al、As有一定脱除效果,Si、Zn、In脱除效果明显。对比6N锗化学成分Ca、Mg、Al、As达不到6N锗标准;Si、Zn、In达到6 N锗标准。
根据一、二阶段的实验结果分析可知,表8中Si的含量存在错误,蒸馏温度为1273K低于Pb/Bi的有效挥发温度。
4 结论
以上三个阶段区熔锗渣真空蒸馏十二种杂质的脱除效果、对应的条件分析如表9所示,可以得出,区熔锗渣真空蒸馏,系统压力(4~8)Pa条件下,蒸馏温度低于1673K,蒸馏时间小于300min,Si、Ca、Fe、Co、Ni、Cu不能脱除;蒸馏温度高于1273K,蒸馏时间大于30min,Mg、As有脱除效果;蒸馏温度高于1673K,蒸馏时间大于300min,Mg可以达到6N锗标准;蒸馏温度高于1673K,蒸馏时间大于180min,Al有脱除效果;蒸馏温度高于1273K,蒸馏时间大于30min,Zn、In可以达到6N锗标准;蒸馏温度高于1373K,蒸馏时间大于60min,Pb/Bi可以达到6N锗标准。

表9 真空蒸馏的脱除分析情况
