广藿香油中1个新的愈创木烷型倍半萜
2021-03-09周勤梅
黄 露,马 川,熊 亮,彭 成,郭 力*,周勤梅,
1.成都中医药大学药学院 教育部中药材标准化重点实验室,四川 成都 611137
2.成都中医药大学 西南特色药材创新药物成分研究所,四川 成都 611137
3.成都中医药大学 中医药创新研究院,四川 成都 611137
神经退行性疾病的发病率与年龄密切相关,随着世界人口老龄化的加速,其发病率呈现明显上升趋势[1]。在《世界老年痴呆症报告》中指出,未来15年阿尔兹海默病患者人数会增长50%~110%[2]。患者发病后病情呈现进行性加重,逐渐丧失独立生活能力,最终因并发症而死亡[3]。中药挥发油类物质具有上行于窍,开窍的作用,中医上也认为“芳香药行散走窜、芳香上达”[4-5],现代研究证实芳香类药物针对神经性疾病具有较好的疗效[6-11]。
广藿香是芳香中药的代表,为唇形科(Lamiaceae)刺蕊草属PogostemonDesf.植物广藿香Pogostemon cablin(Blanco) Benth.的干燥地上部分[12]。国内外研究者已从广藿香中分离得到90 余个单体化合物,其主要的结构类型包括黄酮类、苯丙素类、萜类、甾体类、生物碱类以及脂肪酸类等[13-17]。而广藿香油作为广藿香的主要活性组分,具有抗菌[18]、抗病毒[19]、神经保护[20]等多种药理活性。Perry 等[21]在芳香疗法中发现广藿香精油具有安神、保护神经的作用,对于防治神经性疾病有着独特的优势。前期研究发现,广藿香油中分离得到的愈创木烷型倍半萜对具有较好的神经细胞保护活性[20]。因此,本实验继续深入分离广藿香中倍半萜化合物,得到2个愈创木烷型倍半萜,分别鉴定为 (+)-(1S,4S,5S,7R,10R)-愈创木烷-5,15-环氧-11-烯-10-醇[(+)-(1S,4S,5S,7R,10R)-guaiacane-5,15-epoxy-11-ene-10-ol,1]、patchouliguaiol C(2)。其中化合物1 为新化合物,命名为环氧愈创木醇。并对获得的化合物进行神经保护作用筛选,结果发现化合物2 具有显著的神经保护活性。
1 仪器与材料
Bruker D8 QUEST X 单晶衍射仪(德国Bruker公司);Waters Synapt G2 高分辨质谱仪(Waters 公司);安东帕MCP 200 旋光仪(美国安东帕有限公司);Agilent Cary 600 FTIR 显微镜和成像系统(美国Agilent 公司);Bruker-600 核磁共振仪(德国Bruker 公司);圆二色谱仪(Chirascan CD 光谱仪);Búchi Gradient Former B-687 中压液相色谱仪(Rp C18,43~60 μm)、Búchi Rotavapor R-205 旋转蒸发仪(瑞士BUCHI 公司);Shimadzu UV-260 型紫外光谱仪(日本岛津公司);色谱柱:Agilent C18(250 mm×9.4 mm,5 μm,安捷伦公司);Sephadex LH-20(Amersham Pharmacia 公司);GF254薄层色谱硅胶(青岛海洋化工厂);醋酸乙酯均购自成都科龙试剂厂;色谱甲醇购自天地试剂公司。
DMEM 高糖培养基(Gibco 公司);胎牛血清(Gibico 公司);细胞培养板(Costar 公司)。Water Jacket CO2孵箱(Thermo Scientific 公司);Series II Allegra X-12R 离心机(Beckman Coulter 公司);AE 2000 电子显微镜(Motic 公司);Sunrise 酶标仪(TECAN 公司);甲基噻唑蓝(MTT,Sigma 公司)。SH-SY5Y、PC12 神经细胞株购自江苏凯基生物细胞库。
广藿香药材于2017年12月采自广东省阳春县广藿香种植基地,经成都中医药大学中药鉴定教研室高继海副教授鉴定为唇形科刺蕊草属植物广藿香P.cablin(Blanco) Benth.的全草。标本(SGHX-20171205)现存于成都中医药大学。
2 提取与分离
取干燥的广藿香药材地上部分80 kg,采用水蒸气蒸馏装置进行提取,收集得到挥发油,然后用无水硫酸钠干燥除水,最终得到广藿香挥发油405 g。采用硅胶柱色谱(100~200 目)对挥发油进行薄层色谱分离,以石油醚-醋酸乙酯(100∶0~0∶100)为流动相进行梯度洗脱,洗脱液经薄层色谱检测,合并组成相似的流分,回收溶剂得到21 个洗脱部分(F1~F21)。F18(15.5 g)部分通过反相中压液相色谱以40%~100%甲醇溶液进行梯度洗脱,洗脱液经薄层色谱检测,合并组成相似的流分,得到14份洗脱部分F18-a~F18-n。F18-f部分采用Sephadex LH-20 柱色谱进行分离,以石油醚-氯仿-甲醇(5∶5∶1)为流动相,分离得到3 个亚组分F18-f-1~F18-f-3。对F18-f-1采用Sephadex HW-40F 柱色谱进行分离,以80%甲醇水为洗脱剂进行洗脱,最后经制备薄层色谱,石油醚-醋酸乙酯(7∶1)展开,得到含化合物1 的混合物,再经过反相半制备高效液相色谱,以69%的甲醇溶液为流动相进行分离纯化,最终得到化合物1(6.5 mg,tR=73 min,体积流量1 mL/min)。F18-h部分采用硅胶柱色谱进行分离,以石油醚-醋酸乙酯(100∶1~1∶1)梯度洗脱,得到12 个亚组分(F18-h-1~F18-h-12),F18-h-10通过采用反相半制备高效液相色谱法(78%甲醇水溶液)处理组分F18-h-11得到化合物2(10.3 mg,tR=54 min,体积流量1 mL/min)。
3 结构鉴定
化合物1 的1H-1H COSY 谱显示H2-6/H-7/H2-8/H2-9、H-4/H3-14/H-1/H2-2/H2-3 的相关信号,揭示出1 个连续的质子偶合体系(图1)。HMBC 谱中,Me-14 与C-3、C-4、C-5 相关;H-1 与C-2、C-3、C-10 相关;H-15 与C-1、C-5、C-9、C-10 相关;H-7 与C-6 和C-8 相关;H-12 与C-7 和C-11相关,表明含氧季碳取代于C-10 位,且C-15 与C-5之间形成1 个五元环醚。
化合物1 的相对构型通过NOESY 谱确定,其中H-1 与H-6a 和H-9a 相关;H-15 与H-3a、H-6b和H-9b 相关;H2-12 与H-9b 相关,H-3a 与H3-14相关(图1),说明H-6a、H-1、OH-10、H-4 和H-7位于环系的同侧;H3-14 与H-15 和isopropenyl-7 位于另外一侧。同时对该化合物进行了单晶测定,见图2。进一步通过计算ECD 确定化合物1 的绝对构型。在乙腈中使用等电聚焦连续极化(IEF-PCM)溶剂化模型针对 1a (1S,4S,5S,7R,10R) 和 1b(1R,4R,5R,7S,10S) 在CAM-B3LYP/DGDZVP 级计算得到的ECD 光谱。通过ECD 光谱比较,计算得出的1a (1S,4S,5S,7R,10R) ECD 谱与实验ECD 谱非常吻合。因此,将化合物1 的绝对构型确定为1S,4S,5S,7R,10R。最终化合物鉴定为(+)-(1S,4S,5S,7R,10R)-愈创木烷-5,15-环氧-11-烯-10-醇。
化合物1 的X-ray 单晶衍射数据:C15H24O2,M=236.34 g/mol,单斜晶系(monoclinic),手性非心空间群(P21);a=7.048(4)×10−7mm,b=10.887(4)×10−7mm,c=9.457(5)×10−7mm,α=90°,β=102.96(3)°,γ=90°,V=707.2(6) ×10−7mm3,T=298(2) K,Z=2,μ(Cu Kα) =0.558 mm−1,12 502 次单晶反射收集的数据(reflections measured),其中收集到的2285 个数据为较完整的可用数据(independent reflections);Rint=0.037 7,R1=0.036 4 (I>2σ(I)),wR(F2)=0.092 6(I>2σ(I)),R1=0.041 6 (all data),wR(F2)=0.097 1(all data),F2=1.084,Flack parameter=−0.20(15)。
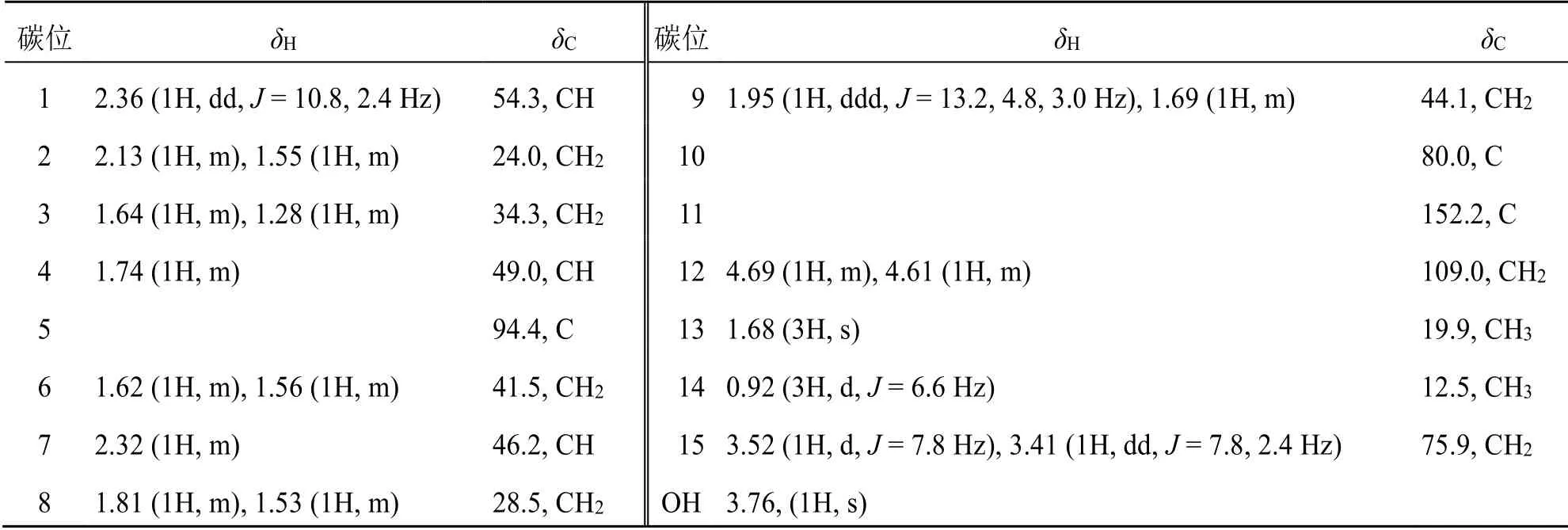
表1 化合物1 的碳、氢核磁共振波谱数据Table 1 1H-NMR (600 MHz,acetone-d6) and 13C-NMR (150 MHz,acetone-d6) data of compound 1

图1 化合物1 的结构及主要的1H-1H COSY、HMBC 和NOESY 信号Fig.1 Structure and key correlations of 1H-1HCOSY,HMBC and NOESY of compound 1
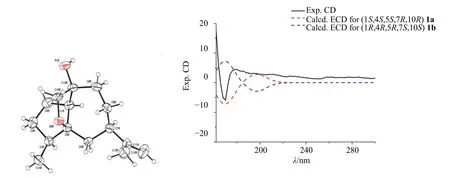
图2 化合物1 的X-ray 单晶衍射结构 (左) 和ECD 图 (右)Fig.2 X-ray crystal structure (left) and ECD (right) of compound 1
化合物2:白色粉末,10%硫酸乙醇显紫色;HR-ESI-MSm/z:259.168 5 [M+Na]+(计算值259.167 4,C15H24O2Na);1H-NMR (600 MHz,Acetone-d6)δ:5.17 (1H,brs,H-15a),4.91 (1H,brs,H-15b),4.65 (1H,brs,H-12a),4.59 (1H,brs,H-12b),4.46 (1H,q,J=6.6 Hz,H-2a),2.49 (1H,m,H-4),2.47 (1H,m,H-9a),2.22 (1H,ddd,J=13.2,6.0,4.2 Hz,H-9b),2.09 (1H,m,H-7),2.05 (1H,m,H-5),1.87(1H,m,H-8a),1.80 (1H,ddd,J=12.6,7.8,6.6 Hz,H-3a),1.68 (3H,brs,H3-13),1.67 (1H,ddd,J=12.6,7.8,6.6 Hz,H-3b),1.50 (1H,brd,J=13.8 Hz,H-6a),1.36 (1H,m,H-8b),1.12 (1H,ddd,J=13.8,12.0,10.8 Hz,H-6b),0.87 (3H,d,J=7.2 Hz,CH3-14);13CNMR (150 MHz,Acetone-d6)δ:154.7 (C-10),152.5(C-11),111.9 (C-15),108.6 (C-12),84.4 (C-1),74.0(C-2),54.6 (C-5),49.7 (C-7),41.4 (C-3),38.0 (C-8),32.9 (C-9),32.8 (C-4),31.9 (C-6),20.5 (C-13),16.8(C-14)。以上数据与文献报道基本一致[20],故鉴定化合物2 为patchouliguaiol C。
4 神经保护作用筛选
采用MTT 法测定化合物1 和2 对β 淀粉样蛋白1-42(amyloid β-protein,Aβ1-42)损伤人神经母细胞瘤细胞SH-SY5Y 和H2O2损伤PC12 细胞的作用[22-23]。
SH-SY5Y 细胞接种于DMEM 培养液中,37 ℃、5%CO2培养至对数生长期,取出离心。接种SH-SY5Y 细胞于96 孔板中,每孔1×105个细胞,其中DMEM 含有10%胎牛血清(100 μL)。将SH-SY5Y 细胞与样品一起预孵育24 h,最终浓度为3.125、6.25、12.5、25 和50 μmol/L,然后分别用25 μmol/L Aβ1-42处理4 h。培养期后,向各孔中加入20 μL MTT(5 mg/mL),培养4 h。以0.1%DMSO为对照,50 μmol/L 维生素E 用作阳性对照,使用酶标仪在490 nm 处测量吸光度(A)。每个测定重复3 次,计算细胞存活率。
当PC12 细胞处于对数生长期进行收集,PC12细胞接种于DMEM 培养液中,37 ℃、5%CO2培养至对数生长期,取出离心。接种PC12 细胞于96 孔板中,每孔1×105个细胞,其中DMEM 含有10%胎牛血清(100 μL)。将PC12 细胞与样品一起预孵育24 h,最终浓度为3.125、6.25、12.5、25 和50 μmol/L,然后分别用400 μmol/L H2O2处理4 h。培养期后,向各孔中加入20 μL MTT(5 mg/mL),培养4 h。以0.1%DMSO 为对照,50 μmol/L 维生素E用作阳性对照,以使用酶标仪在490 nm 处测定A,每个测定重复3 次,按照以下公式计算细胞存活率。
细胞存活率=A给药/A对照
由图3、4 可知,化合物2 在50 μmol/L 浓度下,对Aβ1-42损伤SH-SY5Y 细胞和H2O2损伤PC12神经细胞具有显著的保护作用,存活率分别为(79.57±4.33)%和(69.14±2.55)%。而化合物1 在3.13~50 μmol/L 浓度内,对Aβ1-42 损伤SH-SY5Y 细胞和H2O2损伤PC12 神经细胞未表现出明显作用。
5 讨论
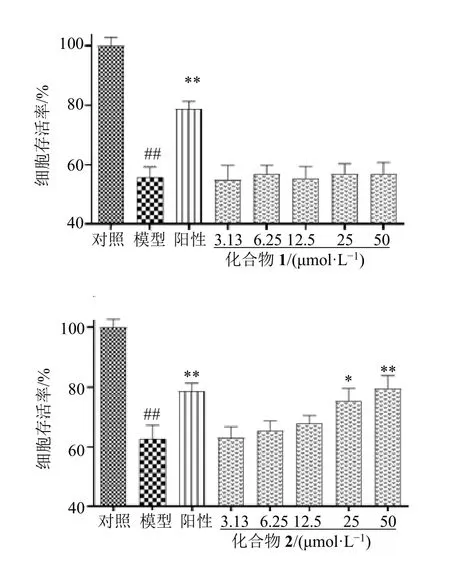
图3 化合物1 和2 对Aβ1-42 损伤SH-SY5Y 神经细胞的影响Fig.3 Effect of compounds 1 and 2 against Aβ1-42-damage in SH-SY5Y cells

图4 化合物1 和2 对H2O2 损伤PC12 神经细胞的影响Fig.4 Effect of compounds 1 and 2 against H2O2-damage in PC12 cells
神经退行性疾病是由神经元和(或)其髓鞘的丧失所致,随着时间的推移而恶化,出现功能障碍的一种老年人常发疾病[24],作为当今研究的重点,科学家尚未发现疗效很好的药物。结合中医药“芳香药行散走窜、芳香上达”的理论,选择芳香中药的代表广藿香为研究对象,从中探索对神经性疾病具有较好作用的物质。通过对广藿香的挥发性成分进行分离纯化以及活性筛选,发现化合物2 对Aβ1-42损伤SH-SY5Y 和H2O2损伤PC12 神经细胞均表现出显著的保护作用,为现代药物的研究与开发提供参考。
广藿香油中含有丰富的愈创木烷型倍半萜,同时该类型化合物也是自然界中存在的重要天然产物类型,受到广大医药研究者的密切关注[25]。愈创木烷型倍半萜含有多个手性中心,其绝对构型的确定成为该类型成分结构鉴定的难点。本研究联合HR-ESI-MS、NMR、ECD 以及X 单晶衍射等多种技术手段对新化合物1 进行结构鉴定。不仅丰富了广藿香油的化学组成,同时也为愈创木烷型倍半萜的结构鉴定提供可靠的数据。
利益冲突所有作者均声明不存在利益冲突
