基于A型塞内卡病毒VP3蛋白间接ELISA抗体检测方法的建立
2021-03-09申水莹闫若潜雷从从王淑娟马震原赵雪丽谢彩华吴志明
申水莹,闫若潜,雷从从,王淑娟,马震原,刘 影,赵雪丽,谢彩华,吴志明
(1 河南农业大学 牧医工程学院,河南 郑州 450002;2 河南省动物疫病预防控制中心,河南 郑州450008;3 西北农林科技大学 动物医学院,陕西 杨凌 712100;4 河南省兽药饲料监察所,河南 郑州 450002)
A型塞内卡病毒(SVA)可引起猪原发性水疱病,即塞内卡病毒病。SVA感染初期,病猪出现精神萎靡、进食困难、体温升高等症状,随后鼻、舌和蹄冠等部位出现水疱样病变,严重时会蔓延至蹄底部,使病猪出现跛行的症状[1]。母猪感染SVA后虽然死亡率极低,但其发病率可达90%,会造成产奶减少甚至停止、饿死乳猪等生产性能上的危害。1~3日龄新生仔猪感染SVA后体态瘦弱,贪睡,不愿进食,死亡率可达 30%~70%[2-3],给养猪行业带来了巨大的潜在隐患。首例SVA毒株(SVV-001)于2002年由美国科研人员从细胞培养基污染物中发现并分离得到[4-5];2002-2013年,SVA主要在美国和加拿大呈零星发生;2014-2016年,巴西、哥伦比亚和泰国均发现了猪SVA感染[6-9]。2015-2017年,塞内卡病毒病在我国广东、福建、辽宁、湖北、河南、黑龙江等地相继确诊[10-12],目前国内尚无针对SVA的商品化疫苗,也无特效的治疗方法,一旦SVA大面积爆发必然给养殖产业带来极大的影响。
SVA为单股、正链、RNA病毒[13],属塞内卡病毒属Senecavirus),与心病毒属(Cardiovirus)成员的亲缘关系较近[4,14-15]。SVA基因组含有7 280个核苷酸,包括666个核苷酸的非编码区和一个包含6 543个核苷酸的开放阅读框。SVA有4种衣壳蛋白:VP1、VP2、VP3和VP4[16],其中VP1、VP2和VP3位于蛋白衣壳的外部,VP4位于蛋白衣壳的内部[17],且VP1和VP3是主要的抗原表位区域,可刺激机体产生中和抗体[4,18]。Maggioli等[19]研究发现,在SVA感染的急性期,机体产生的抗体主要是抗VP2和VP3的特异性IgM;在康复期,机体产生的抗体主要是抗VP1、VP2、VP3 的特异性IgM和IgG[6],说明VP3蛋白在感染早期就能产生中和抗体,可作为塞内卡病毒病早期检测的靶标抗体。
猪感染SVA的症状与口蹄疫、水泡性口炎和水疱性疹等水泡类疾病的症状十分相似,临床上难以区分[1],国内对SVA的检测主要以RT-PCR为主,但ELISA方法既能达到与病毒中和试验、间接免疫荧光等方法高度一致,又可实现SVA的快速、简便、敏感的诊断要求,可用于大规模的流行病学研究或监测[20]。本课题组已建立了基于VP1蛋白的SVA间接ELISA检测方法[21],本试验旨在进一步建立基于VP3蛋白的SVA间接ELISA检测方法,比较基于不同蛋白建立的SVA间接ELISA检测方法的差异,为SVA感染的临床诊断检测及未来疫苗免疫效果评价提供技术支撑。
1 材料与方法
1.1 材 料
1.1.1 病毒与血清 SVA毒株及87份SVA阴性猪血清(采自健康猪,SVA荧光PCR检测阴性)、113份SVA阳性血清(采自SVA灭活疫苗免疫的猪,病毒中和试验检测阳性)和160份猪血清(20头SVA灭活疫苗免疫猪免疫后第14,21,28,35,42,49,56,63天的血清),均由河南省动物疫病预防控制中心提供。O型和A型口蹄疫病毒 (FMDV)阳性血清,为兰州兽医研究所生产的阻断ELISA检测试剂盒中所配备。猪伪狂犬病毒(PRV) 、猪繁殖与呼吸障碍综合征病毒(PRRSV)和猪瘟病毒(CSFV)阳性血清,均为美国爱德士(IDEXX)公司生产的ELISA检测试剂盒中所配备。
1.1.2 主要仪器和试剂 洗板机,瑞士Tecan Austria GmbH公司产品;BioTek-ELx808酶标仪,美国伯腾公司产品;蛋白超滤离心管,购于Millipore公司。病毒DNA/RNA提取试剂盒(CDC),购于西安天隆科技有限公司;5×PrimeScript RT Master Mix、Agarose Gel DNA Extraction Kit、Plasmid Purification Kit,购于TaKaRa公司;BCA蛋白质量浓度测定试剂盒,购于碧云天生物技术公司;pGEM-T Easy Vector,购于Promega公司;JM109、BL21 (DE3),购于康为世纪生物科技有限公司;pQE-30,购于优宝生物公司;T4连接酶、BamH Ⅰ和SacⅠ限制性内切酶、TaqDNA 聚合酶,购于宝生物工程(大连)有限公司;10×PBST、TMB单组份显色液、Western Blot试剂盒,购于Solarbio公司;山羊抗猪HRP-IgG(H+L),购于Proteintech公司;包涵体蛋白溶解及复性试剂盒,购于天恩泽生物科技公司。
1.2 SVA VP3基因的扩增及重组表达质粒的构建
参照GenBank中登录的SVAVP3基因序列(GenBank登录号为:MN885796),设计1对特异性引物,P1:5′-TCAGGATCCCTGAACGCGAGAACCTCTAC-3′,下划线部分为插入的BamH Ⅰ酶切位点;P2:5′-TCAGAGCTCCAAGCCTATGTCCCAAATAGA-3′,下划线部分为插入的SacⅠ酶切位点。引物由英潍捷基(上海)贸易有限公司合成,预期扩增出的目的片段长度为717 bp。
使用病毒DNA/RNA提取试剂盒(CDC)提取SVA的总RNA,用5×PrimeScript RT Master Mix将RNA反转录为cDNA,备用。以合成的cDNA为模板PCR扩增VP3基因,设以ddH2O代替模板的处理为阴性对照。PCR反应体系为:Premix Taq 12.5 μL,ddH2O 8.5 μL,上下游引物各0.5 μL,c-DNA模板3 μL。反应程序为:94 ℃预变性4 min;94 ℃ 45 s,56 ℃ 45 s,72 ℃ 45 s,35个循环;72 ℃ 10 min,4 ℃停止。PCR产物经1%琼脂糖凝胶电泳后使用Agarose Gel DNA Extraction Kit回收目的片段。
将VP3基因与pGEM-T Easy载体连接,构建重组质粒rT-VP3,进行蓝白斑试验筛选。对筛选出的阳性重组质粒进行PCR和测序鉴定,设以ddH2O代替模板的处理为阴性对照。将鉴定正确的重组质粒和pQE-30载体进行BamH Ⅰ和SacⅠ双酶切,回收两者的目的片段,用T4连接酶在4 ℃条件下过夜连接,构建重组表达质粒rpQE30-VP3。将rpQE30-VP3转入大肠杆菌BL21(DE3)感受态细胞,对质粒进行PCR及BamH Ⅰ和SacⅠ双酶切鉴定,将鉴定正确的重组质粒送英潍捷基(上海)贸易有限公司测序。
1.3 重组VP3(rVP3)蛋白的表达、纯化及抗原性鉴定
选取鉴定过的阳性菌落,1∶100接种到LB(含氨苄青霉素100 μg/mL)培养液,在37 ℃下180 r/min培养约2 h,测定600 nm处吸光值(OD600)为0.5~0.6时(即达到对数生长期),加入IPTG使终浓度为0.3 mmol/L,诱导6 h。取1 mL菌液4 ℃下8 000 r/min离心5 min,取沉淀进行SDS-PAGE电泳,观察rVP3蛋白是否表达。将菌液于4 ℃下8 000 r/min离心30 min,收集菌体,于-80 ℃冻融后用裂解液重悬,超声波裂解(功率320 W,工作3 s间歇7 s,重复至菌体完全破碎),4 ℃下8 000 r/min离心30 min,收集上清和沉淀进行SDS-PAGE电泳,分析rVP3蛋白是否可溶性表达。按照包涵体蛋白溶解及复性试剂盒说明书对包涵体溶解、洗涤及复性,之后用10 K蛋白超滤管5 000 r/min离心20 min进行浓缩,按照BCA蛋白质量浓度测定试剂盒说明书测定浓缩后蛋白的质量浓度。
采用Western Blot法鉴定rVP3蛋白的抗原特异性。将经过SDS-PAGE鉴定的样品重新进行SDS-PAGE,同时设置pQE-30转化的产物为阴性对照,然后电转印至硝酸纤维素膜(NC膜)。将NC膜置于封闭液(含50 g/L脱脂奶粉的PBST)中,4 ℃封闭过夜。将NC膜取出后用PBST洗膜3次,每次5 min;加入灭活的SVA阳性血清(1∶200稀释)37 ℃孵育1 h,PBST洗膜3次,每次5 min;加入山羊抗猪 HRP-IgG(H+L)(1∶5 000稀释)37 ℃孵育1 h,PBST洗膜3次,每次5 min;用ECL底物显色试剂盒显色。
1.4 间接ELISA方法工作条件的优化
采用矩阵法,分别对包被液[pH 7.2的PBS、pH 9.6的碳酸盐缓冲液(CB)]、纯化的rVP3蛋白包被浓度(1,2,4 μg/mL)、封闭液(10 g/L BSA、50 g/L脱脂奶粉和5 g/L Casein)、封闭条件(37 ℃下2 h、4 ℃过夜)、样品稀释倍数(1∶25,1∶50,1∶100,1∶200)、TMB室温下作用时间(5,10,15 min)、山羊抗猪 HRP-IgG(H+L)稀释倍数(1∶2 500,1∶5 000,1∶7 500)和作用时间 (15,30,60 min)等条件进行优化。
1.5 间接ELISA方法临界值的确定
采用上述最优条件检测SVA阳性对照(经3次重复检测确定P值)和200份临床猪血清样品(87份SVA阴性猪血清和113份SVA阳性血清)。采用SPSS 16.0软件对200份血清样品在450 nm处的吸光值(OD450)进行分析。以敏感性为纵坐标,1-特异性为横坐标,使用非参数构建受试者工作特征曲线(ROC),以Youden指数(敏感性-(1-特异性))最大点作为阴阳性判断的临界点,确定间接ELISA方法的判定标准。
1.6 间接ELISA方法的特异性、敏感性、重复性和稳定性检测
1.6.1 特异性 采用已建立的间接ELISA方法分别对SVA阴性血清、SVA阳性血清以及FMDV(O/A型)、PRV、PRRSV、CSFV阳性血清进行检测,同时设置SVA阳性对照,重复3次,分析该方法的特异性。
1.6.2 敏感性 随机选取SVA阳性血清10份,进行病毒中和试验;同时,对血清进行2倍倍比稀释(1∶2,1∶4,1∶8,…,1∶512)后,采用已建立的间接ELISA方法进行检测,分析该方法的敏感性。
1.6.3 重复性和稳定性 随机选取SVA阴性、阳性血清共10份。用3个批次rVP3蛋白包被的ELISA反应板进行检测;同时,采用同一批次rVP3蛋白包被的ELISA反应板,分别在3个不同的时间点进行检测。上述试验每份血清平行重复3次,测定OD450值。3次平行重复结果取其平均值,计算批内和批间的变异系数(CV),分析该方法的重复性和稳定性。
1.7 血清样品的检测
分别采用本试验建立的方法和课题组已建立的基于VP1蛋白的SVA间接ELISA检测方法[21],对SVA灭活疫苗免疫猪不同时期的160份血清进行检测,以SVA阴、阳性血清为对照,计算SVA抗体阳性率,分析两方法间的差异。
2 结果与分析
2.1 SVA VP3基因的扩增及rpQE30-VP3的构建
PCR产物经琼脂糖凝胶电泳,结果显示,在717 bp处获得一条特异性片段(图1-A)。筛选出的阳性重组质粒rT-VP3经PCR扩增,获得一条717 bp的特异性条带(图1-B);测序结果证实,rT-VP3构建成功。构建的重组表达质粒rpQE30-VP3经PCR鉴定后,获得一条717 bp的特异性PCR扩增条带(图1-C),BamH Ⅰ和SacⅠ双酶切鉴定获得了3 461和717 bp的条带,与预期结果相符(图1-D)。经测序对比分析,结果显示目的序列无碱基插入、突变或缺失,表明重组质粒rpQE30-VP3构建成功。

A.VP3基因PCR扩增结果;B.rT-VP3质粒PCR扩增结果;C.rpQE30-VP3质粒PCR扩增结果;D.rpQE30-VP3质粒双酶切鉴定结果。M.DNA Marker;1,3.阴性对照;2.VP3基因PCR扩增产物;4.rT-VP3质粒PCR扩增产物;5~6.rpQE30-VP3质粒PCR扩增产物;7~8.rpQE30-VP3质粒双酶切产物A.PCR amplification results of VP3;B.PCR amplification results of rT-VP3;C.PCR amplification results of rpQE30-VP3;D.Identification of rpQE30-VP3 plasmid digested.M.DNA Marker;1,3.Negative control;2.PCR amplification products of VP3;4.PCR amplification products of rT-VP3;5-6.PCR amplification products of rpQE30-VP3;7-8.Enzyme-digested product of rpQE30-VP3图1 SVA VP3基因及rT-VP3质粒和rpQE30-VP3质粒的鉴定结果Fig.1 Identification of SVA VP3 gene,rT-VP3 plasmid and rpQE30-VP3 plasmid
2.2 rVP3蛋白的表达、纯化及抗原性鉴定
rpQE30-VP3经IPTG诱导,表达出32 ku的rVP3蛋白(图2-A)。诱导表达产物经超声破碎后离心,取沉淀和上清进行SDS-PAGE鉴定,结果显示目的蛋白主要存在于沉淀中,表明rVP3以包涵体的形式表达。纯化的rVP3蛋白分子质量约32 ku(图2-B)。经Western Blot鉴定约32 ku处有特异性条带(图2-C),表明rVP3蛋白能与SVA阳性血清发生特异性反应,具有较好的反应原性。经BCA试剂盒检测,该蛋白的质量浓度为1.54 mg/mL。

A.rVP3蛋白SDS-PAGE;B.rVP3蛋白纯化后SDS-PAGE;C.rVP3蛋白Western Blot。M.蛋白质标准分子量;1,6.pQE-30空载体诱导表达对照;2.未诱导的rVP3蛋白;3.IPTG诱导的rVP3蛋白;4,5,7.纯化后的rVP3蛋白A.The SDS-PAGE results of rVP3;B.The SDS-PAGE results of purified rVP3;C.The Western Blot of purified rVP3.M.Protein Marker;1,6.Induction of pQE-30 empty vector;2.Uninduction of rpQE-30-VP3;3.Induction of rpQE-30-VP3;4,5,7.Purification of rpQE-30-VP3图2 rVP3蛋白的表达、纯化及抗原性分析Fig.2 Expression,purification and antigenicity analysis of rVP3 protein
2.3 间接ELISA方法最佳工作条件的优化
矩阵法试验结果显示,间接ELISA的最佳工作条件为:抗原2 μg/mL,碳酸盐缓冲液(pH 9.6)在4 ℃下包被14~16 h,5 g/L Casein在4 ℃下封闭14~16 h,1∶100稀释样品在37 ℃下反应1 h,1∶5 000稀释山羊抗猪HRP-IgG(H+L)在37 ℃下反应30 min,TMB在室温避光条件下反应10 min。
2.4 间接ELISA方法的判定标准
利用SPSS 16.0软件对200份血清样品的OD450检测结果进行分析,绘制的ROC曲线见图3。结果显示,SPSS 16.0软件数据分析Youden指数最大时所对应的OD450值,即临界OD450为0.276,3次重复测定阳性对照的OD450为2.0。临界OD450/阳性对照OD450= 0.138,因此,本方法的判定标准定为:样本OD450(S)/阳性对照OD450(P)>0.138为SVA抗体阳性,反之则为阴性。

图3 基于VP3蛋白的SVA间接ELISA检测方法的ROC曲线Fig.3 ROC curve of SVA indirect ELISA method based on VP3 protein
2.5 间接ELISA方法的特异性、敏感性、重复性和稳定性
2.5.1 特异性 特异性检测结果(表1)显示,rVP3蛋白与FMDV(O/A型)、PRV、PRRSV、CSFV病原阳性血清均为阴性(S/P≤0.138),仅能与SVA阳性血清发生反应,表明本检测方法特异性较好。

表1 基于VP3蛋白的SVA间接ELISA检测方法的特异性Table 1 Specificity of SVA indirect ELISA method based on VP3 protein
2.5.2 敏感性 敏感性检测结果(表2)显示,有6份血清样品的结果与中和试验一致,4份样品最高稀释度倍数比中和试验仅低1个稀释度。病毒中和试验能够检测出的平均最高稀释度为1∶150.4,而本方法能够检测出的平均最高稀释度为1∶113.6。结果表明,本研究建立的间接ELISA检测方法虽比中和试验结果略低,但依旧有较好的敏感性。
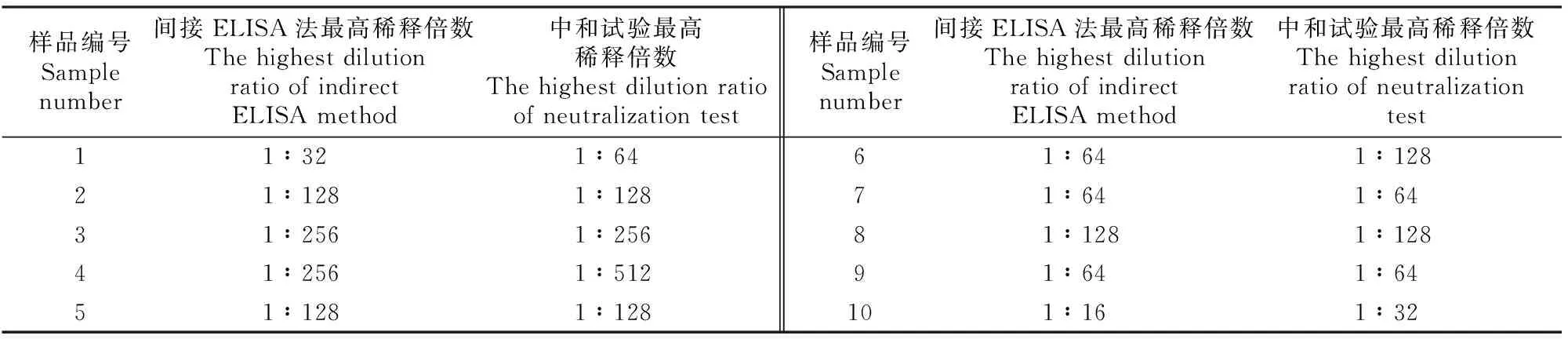
表2 基于VP3蛋白的SVA间接ELISA检测方法的敏感性Table 2 Sensitivity of SVA indirect ELISA method based on VP3 protein
2.5.3 重复性和稳定性 将选取的10份猪血清分别进行批内和批间重复性检测,其变异系数(CV)分别为1.0%~3.8%和3.0%~8.0%,批内小于4%,批间小于9%(表3),表明该检测方法重复性和稳定性较好。
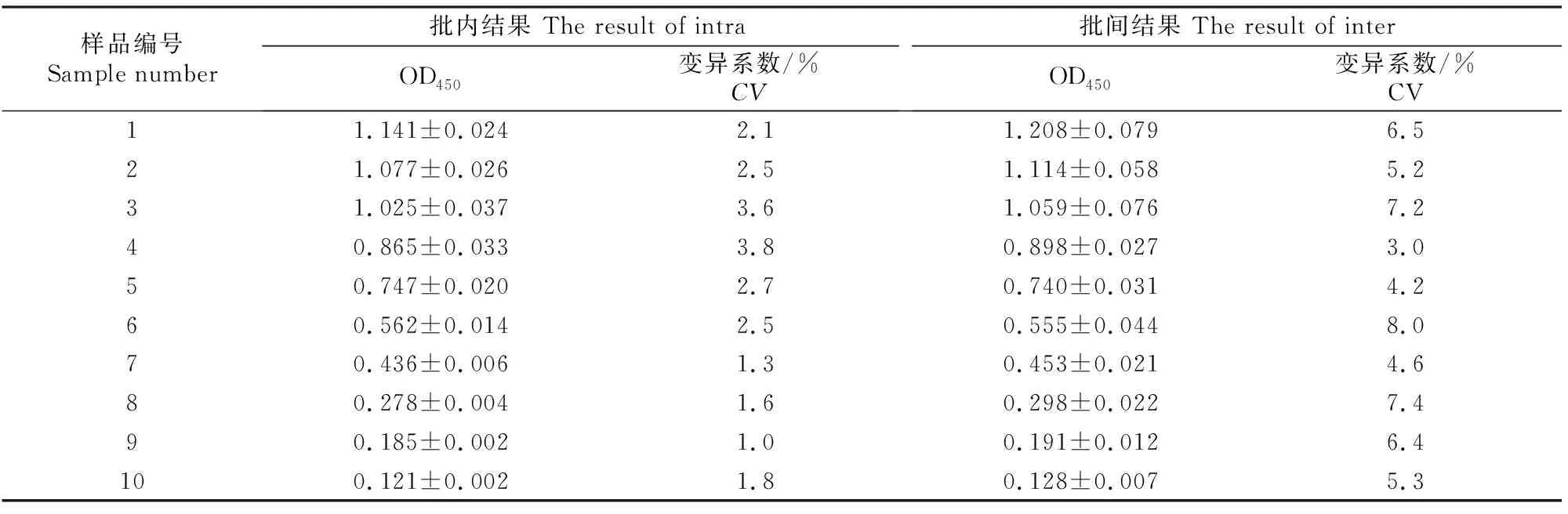
表3 基于VP3蛋白的SVA间接ELISA检测方法的重复性Table 3 Repeatability of SVA indirect ELISA method based on VP3 protein
2.6 基于VP3,VP1蛋白的SVA间接ELISA法免疫血清检测结果比较
采用两种方法对SVA灭活疫苗免疫猪不同时期的160份血清进行检测。结果显示,在免疫后的第14,21,28,35,42,49,56和63天,VP1抗体的阳性率分别为30.00%,70.00%,90.00%,100.00%,90.00%,90.00%,85.00%和80.00%;VP3抗体的阳性率分别为35.00%,70.00%,80.00%,100.00%,90.00%,100.00%,95.00%和95.00%(图4),表明两种方法均能在不同时期检测出抗体,但抗体阳性检出率略有差异。

图4 基于VP3、VP1蛋白的SVA间接ELISA检测方法的检测结果对比Fig.4 Comparison of detection effects of indirect ELISA based on VP3 and VP1 protein
3 讨 论
2015年初,我国与SVA相关的水疱病暴发并开始增多,且与新生仔猪死亡率的升高密切相关[5,22]。2015年我国广东、福建、河南、湖北[23-24]等地陆续检出SVA,隐性感染率极高,给我国养猪行业带来了潜在的危害。SVA与其他水疱病在临床症状上难以区分,还需要依靠实验室诊断技术。目前国内外尚无SVA疫苗的应用,ELISA检测出抗体阳性即为感染。而间接ELISA方法具有敏感度高、特异性强、重复性和稳定性好以及成本低、操作简单等优点,适用于基层的检测。目前,已有针对VP1和VP2蛋白建立的间接ELISA抗体检测方法[21,25-26],但市场上仍缺少商品化可用试剂盒。本研究以VP3蛋白作为包被抗原,建立了检测SVA抗体的间接ELISA方法。本方法与常发猪病毒病阳性猪血清无交叉反应,对检测SVA阳性血清具有特异性;阳性血清检测结果与中和试验基本一致,具有良好的敏感性;批内和批间的变异系数均在9%以内,具有良好的重复性和稳定性。为临床血清SVA抗体检测提供了成本低、操作简单的技术手段,同时也为不同蛋白所建立的间接ELISA方法的对比奠定了基础。评估本研究方法的敏感性时发现,其敏感性略低于中和试验,可能是中和试验检测所有的中和抗体,而本方法检测的是VP3单一蛋白的IgG抗体[6],因而两种试验会产生一定差别,但是本研究建立的间接ELISA方法仍具有较高的敏感性。
采用本研究建立的基于VP3蛋白的间接ELISA方法和本实验室已建立的基于VP1蛋白的间接ELISA方法,分别对SVA灭活疫苗免疫猪不同时期的160份血清进行检测。结果显示,两种方法均能在不同时期检测出抗体,但抗体阳性检出率略有差异,免疫后第14天到第35天,VP1较VP3检测出的抗体阳性率略高;从第42天至第63天,VP3比VP1检测出的抗体阳性率略高。目前本实验室正在进行VP2蛋白间接ELISA方法的建立,以期进行不同抗体水平的检测。
