CO2高值化利用:CO2加氢制甲醇催化剂研究进展
2021-03-08徐敏杰朱明辉陈天元徐晶杨子旭韩一帆
徐敏杰,朱明辉,陈天元,徐晶,杨子旭,韩一帆,2
(1 化学工程联合国家重点实验室,华东理工大学,上海200237;2 先进功能材料制造教育部工程中心,郑州大学,河南郑州450001)
自工业革命开始以来,人类蓬勃发展的生产力伴随着不断增长的能源需求,化石燃料燃烧过量排放导致空气中的二氧化碳(CO2)浓度连年攀升,引发了全球变暖、海水酸化、土地沙漠化等一系列环境问题。为了降低大气中CO2含量,改善温室效应,人们提出了碳捕获利用与封存(carbon capture,utilization and storage,CCUS)策略,该策略的核心思想是将生产过程中排放的CO2进行利用,以减少碳循环中新增的CO2排放。该策略中的最优方案不是简单地封存CO2,而是将CO2资源化、能源化,同时能产生经济效益[1-2]。
甲醇是重要的化工原料,广泛用于有机合成、农药、医药、涂料、汽车和国防等工业中,同时甲醇也是重要的能源物质,可发展替代传统化石燃料[3-4]。目前工业上合成甲醇仍旧依赖化石燃料,主要采用合成气催化转化路线,以煤炭经过气化后通过合成气(CO+H2)制备甲醇。CO2加氢制甲醇,指通过电解水、光解水等可再生途径产生的氢气(H2)以及炼焦工业副产氢,在一定温度、压力下,将CO2催化还原生成甲醇,是一项十分具有应用前景的CCUS技术[5-6]。
因此,开发CO2加氢制甲醇技术既能解决温室效应等环境问题,又能有效提高资源的利用率。本文对CO2加氢制甲醇的热力学分析、反应机理研究与催化剂结构表征方法进行了综述,重点介绍了近年来对铟基催化剂的研究进展,并对未来发展方向进行了展望。
1 热力学分析
CO2是有十六电子的直线型分子,碳原子的两个sp杂化轨道分别与两个氧原子生成σ键,碳原子上两个未参与杂化的p 轨道与sp 杂化轨道呈直角,并且在侧面同氧原子的p轨道分别肩并肩发生重叠,生成两个三中心四电子的离域π键,如图1所示。

图1 CO2电子结构
CO2分子中,碳原子处于最高氧化态+4 价,CO2的标准吉布斯自由能(ΔfG0m)为-394.38kJ/mol。CO2分子化学性质稳定,在通常条件下为惰性分子。因此,CO2的活化通常需要催化剂,且需要在较高的温度和压力下以克服热力学能垒。H2是一种高能分子,来源广泛,被广泛地应用于化学工业中。H2同时也被视为活化CO2分子的理想高能分子,一旦突破电(光)解水效率瓶颈,CO2加氢的经济性将会大大提高。CO2加氢催化转换途径包括热催化、光催化、电催化和生物催化等,其中热催化可在高温高压下进行,CO2加氢转化效率相对较高。此外,目前世界及我国已有完善的热催化化工产业链,因此该路径最具有工业化前景,其核心仍是发展高效的CO2转化催化剂。
CO2加氢催化的产物有很多种,依据碳链长度分类可分为C1产品(如甲醇、CO、甲烷)和C2+化学品;若依据含官能团分类可分为含氧类产物,如甲醇、二甲醚、低碳醇等,烯烃类产物如低碳烯烃,烷烃产物如汽油等。CO2加氢反应路径如图2所示,CO2转化成不同的产品主要是从甲醇路径、逆水气变换(RWGS)结合费-托反应路径(FT)和CO2直接费-托三类路径生成[7]。
CO2加氢生成甲醇和CO 是最重要的两个基本反应,其反应如式(1)和式(2)所示,其中RWGS 可以继续加氢生成甲醇,如式(3)所示。

由式(1)~式(3)可知,CO2加氢生成甲醇是一个分子量降低的放热反应。因此,从热力学角度上分析,CO2加氢生成甲醇适宜在低温高压下进行反应,而高温下更利于CO 的生成。CO2加氢生成甲醇及CO在不同温度下的化学平衡产率如表1和表2所示(H2∶CO2=3)[8]。
2 CO2加氢制甲醇催化剂
CO2加氢制甲醇的相关研究报道首次出现在20世纪40 年代。1945 年研究人员制备了一系列不同的Cu-Al催化剂,并在此基础上研究了不同反应温度、压力及反应气氛对CO2加氢制甲醇的影响[9]。20世纪80年代初期,Halder Tøpse公司利用石油炼化废气中的CO2及H2进行了CO2加氢反应的尝试,生产了甲醇为主的一系列含氧化合物。之后,东京瓦斯公司、德国鲁奇公司及德国南方化学公司也相继在CO2加氢催化剂和相关反应器上进行研究,并逐步优化工艺条件[10]。

图2 CO2加氢制备高附加值化学品的反应路径[7]
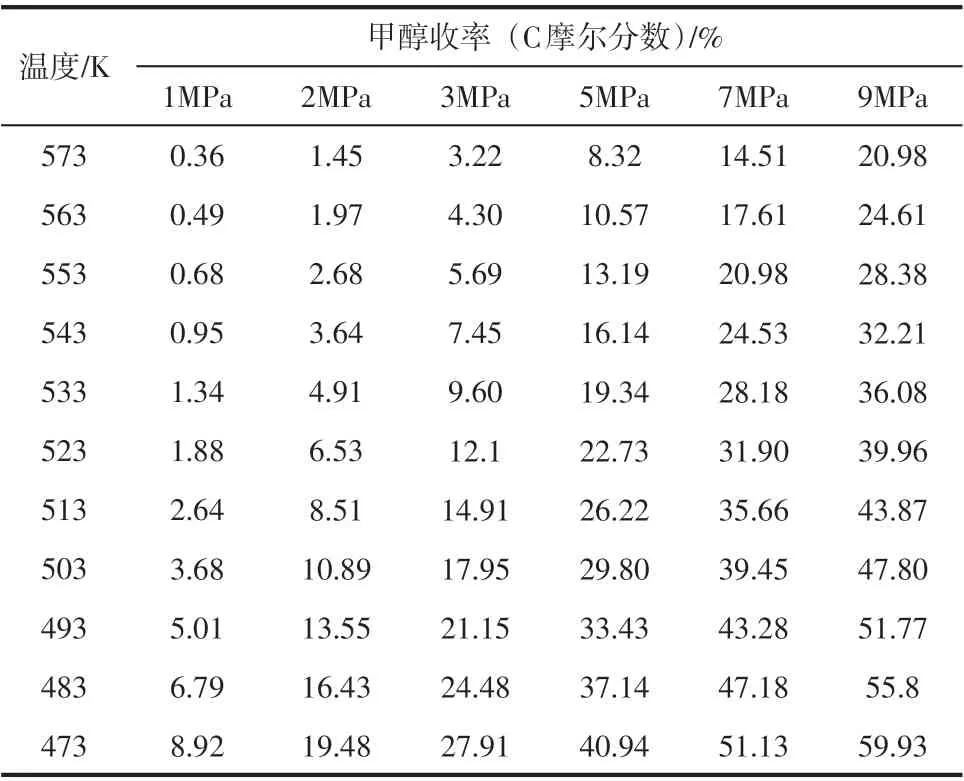
表1 不同温度压力下CO2加氢生成甲醇的平衡产率

表2 不同温度压力下CO2加氢生成CO的平衡产率
此后,CO2加氢制甲醇的催化剂研究日益受到广泛关注。目前,CO2加氢制甲醇催化剂主要包含以下三种体系:①铜基催化剂,以铜作为催化剂的主要活性成分,最典型的是Cu/ZnO/Al2O3体系;②负载型贵金属催化剂,如Pd/ZrO2、Pd/Ga2O3催化剂等;③具有半导体性质的金属氧化物,如ZnO-ZrO2、In2O3等。
2.1 铜基催化剂
Cu基催化剂上的研究主要是针对Cu-ZnO催化剂进行改性,包括改变载体、添加助剂、优化制备方法等,从而改进催化剂的结构和性能。近期部分载体改性的Cu 基催化剂及助剂改性的催化剂性能分别如表3、表4所示。
Bansode等[11]使用Cu/ZnO/Al2O3催化剂在36MPa和H2∶CO2=10的条件下,CO2加氢的甲醇选择性达到77.3%,时空收率达到7729gMeOH/(kgcat·h)。然而该反应条件过于苛刻,不具有可推广的工业应用价值。Angelo 等[12]使用共沉淀法制备了一系列Cu/ZnO/MOx催化剂,并对催化剂制备条件及反应条件进行了优化。实验发现ZrO2掺杂且在400℃煅烧的催化剂具有最高的甲醇生成活性,在280℃、5MPa、GHSV=10000h-1的条件下甲醇产率达到331gMeOH/(kgcat·h)。
Liao 等[13]制备了不同形貌的ZnO,然后使用物理研磨的方法将Cu颗粒与ZnO混合,实验发现ZnO的形貌对Cu/ZnO 催化剂的CO2加氢性能有巨大影响,其中使用平板状ZnO(platelike ZnO)具有最高的甲醇选择性。在270℃、543K、H2∶CO2=2.2、4.5MPa 的条件下CO2转化率为10.9%,甲醇选择性高达72.70%。而相同条件下的棒状ZnO 选择性仅42%。该实验说明特定的ZnO晶面可是实现更优化的ZnO-Cu 相互作用,从而提高CO2加氢的甲醇选择性。

表3 载体改性的CO2加氢制甲醇的Cu基催化剂
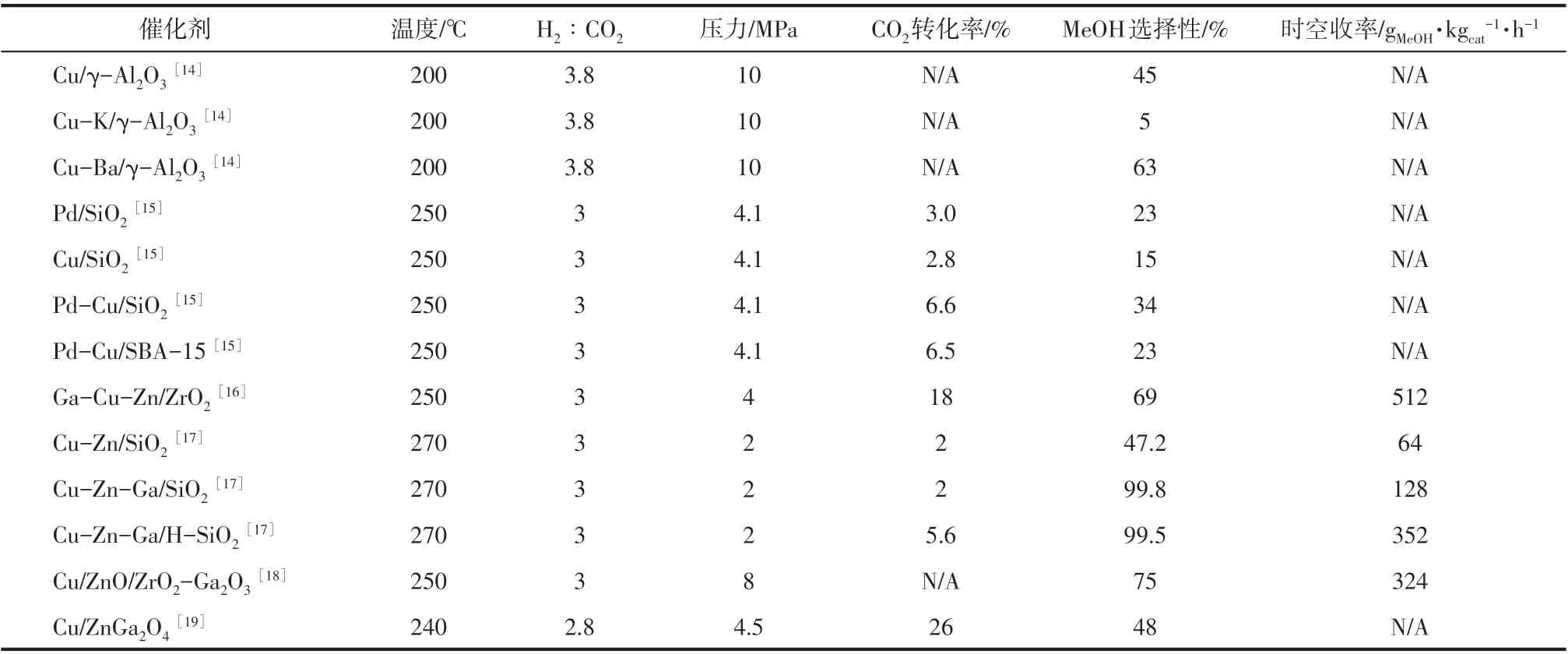
表4 助剂改性的CO2加氢制甲醇的Cu基催化剂
此外,载体和Cu-Zn 催化剂之间存在的金属-载体相互作用对于调控催化性能也发挥了独特的作用。Arena 等[20]分别使用Al2O3、ZrO2和CeO2对Cu-ZnO催化剂进行改性。研究发现不同的载体影响了催化剂表面金属的暴露程度,同时影响了CO2的吸附,两者的协同作用在用ZrO2作为载体时达到最佳。在5MPa、513K、H2∶CO2=10条件下甲醇收率达到1200gMeOH/(kgcat·h)。实验同时发现CO同时由甲醇分解和RWGS反应生成。
Witoon 等[21]使用了不同种类的ZrO2载体制备了Cu/a-ZrO2、Cu/t-ZrO2及Cu/m-ZrO2催化剂,发现Cu/a-ZrO2、Cu/t-ZrO2较Cu/m-ZrO2催化剂有更大的比表面积和更强的Cu-ZrO2相互作用。该相互作用强度影响了Cu 上的氢溢流,从而导致了不同的甲醇产率,其中Cu/a-ZrO2催化剂有最高的甲醇产率,而Cu/t-ZrO2有最高的甲醇转化频率(turnover frequency, TOF)。 Phongamwong 等[14]在Cu/ZnO/ZrO2催化剂中添加了质量分数0~5%的SiO2,制备了一系列CuO-ZnO-ZrO2-SiO2。研究发现添加了质量分数1%的SiO2后,甲醇的生成活性提升了26%,SiO2提高了催化剂活性位点分布,且提高了催化剂的稳定性。
除了对Cu 基催化剂的载体进行改性外,研究者们还对不同助剂对Cu 基催化剂CO2加氢性能的影响进行研究。Bansode 等[15]研究了K 和Ba 改性的Cu/γ-Al2O3催化剂,发现在10MPa、473K 的条件下,Ba的添加将甲醇的选择性从46%提升至62%,而K 的添加极大地提升了RWGS 的活性,CO 选择性高达96%。同时,Ba 和K 的添加都抑制了二甲醚的生成。实验证明K 的添加覆盖了Cu 和Al 表面的与甲醇生成相关的活性位,并稳定了CO 生成的中间物种;而Ba 的添加仅覆盖了Al 的表面,并促进了Cu的还原,因此提高了甲醇的选择性。
Jiang等[16]研究了一系列SiO2载体上的Pd-Cu双金属催化剂,实验发现Pd 的添加可以提高Cu/SiO2催化剂CO2加氢制甲醇的选择性,高分散的Pd-Cu合金被认为是甲醇生成的活性位。该研究认为在低转化率下CO2是甲醇的碳源,而高转化率下CO 也会参与反应生成甲醇。Ladera 等[17]使用共沉淀法制备了Ga 改性的Cu/Zn 催化剂,实验发现Ga 的添加提高了甲醇的生成速率,其原因为Ga 的添加强化了Cu 的分布,使催化剂表面暴露了更多的金属Cu。此外,动力学研究发现,在高H2分压下生成甲醇和RWGS反应属于竞争关系。
Jamil等[18]使用浸渍法制备了一系列Ga-Cu-Zn/SiO2催化剂,发现添加Ga 抑制CO 和烃类的生成,且甲醇选择性达到了99%,甲醇的产率也有很大提升。经过表征发现,催化剂表面生成的Ga2O3粒径及其对Cu的相互作用至关重要。Ga2O3颗粒影响了Cu 的电子结构,使之处于Cu0和Cu2+间的Cu+态。同时,该研究发现疏水SiO2(H-SiO2)可以有效提升甲醇的产率。
Słoczyński 等[19]使用共沉淀法和柠檬酸盐分解法制备了一系列Ga、B、In、Gd、Y、Mn、Mg 掺杂的CuO/ZnO/ZrO2催化剂,并评估了其CO2加氢制CH3OH 性能。研究结果表明,添加了助剂后,甲醇和CO 的活化能都发生了改变,说明助剂的添加改变了催化反应的活性位点,其中Ga 对甲醇生成的提升效果最为明显。助剂的添加提高了Cu 的分布,提高了表面ZrO2的相对表面浓度,同时提高了催化剂表面的疏水性。这些影响提高了甲醇的生成速率并抑制了CO的生成。
Li 等[22]使用共沉淀法制备了一系列Cu/ZnO-Ga催化剂,实验发现Ga3+的加入使得ZnO 更容易被还原,部分ZnO 被还原成了金属Zn,从而形成了Zn-Cu 合金。同时Ga3+还形成了ZnGa2O4尖晶石结构,该结构形成了ZnO-MGa2O4(M=Zn 或Cu)电子异质结,如图3所示。该Ⅱ型电子异质结有利于ZnO 的还原,增加了Zn0的数目且稳定了CuZn 合金,从而有利于*HCO(formyl,甲酸基)、*H2CO(bidentate-acetal, 双 齿 甲 缩 醛) 和*H3CO(methoxy,甲氧基)三种中间体的生成,并且降低了CH3OH生成的能垒,从而促进了CH3OH的生成。
由上文综述可知,Ga助剂对Cu基催化剂制备甲醇性能的提升最为明显。其主要从结构和电子两方面优化了Cu基催化剂。从Ga的几何结构改性上看,Ga的加入形成了表面Ga2O3,促进了Cu物种的分布,同时覆盖了催化剂表面RWGS的活性位,稳定了生成甲醇的中间物种;从Ga 的电子改性角度而言,Ga的存在改变了催化剂表面Cu、Zn的配位状态,促进了Cu、Zn 的还原,加强了氢溢流,从而提高了甲醇的选择性。
2.2 贵金属基催化剂
除了Cu 基催化剂以外,贵金属的CO2加氢过程也受到了广泛的关注,相关工作如表5所示。
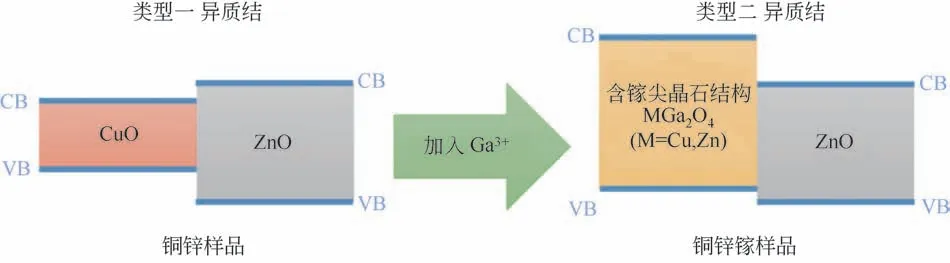
图3 Cu/ZnO-Ga催化剂中能级平面示意图[23]

表5 CO2加氢制甲醇的贵金属催化剂
贵金属催化剂一般均为负载型催化剂,与Cu基催化剂类似,使用不同的载体以及助剂改性能够显著提高催化剂的性能。Kusama 等[23]分别使用了二十多种元素对Rh/SiO2催化剂进行改性,并对其CO2加氢反应进行了评估。实验发现添加了Sn 的Rh-Sn/SiO2具有相对较高的甲醇选择性。Kong等[24]使用沉淀法将Pd/CNT 与PdZnO 催化剂结合到了一起,发现掺杂了Pd/CNT 的催化剂有较高的甲醇选择性。动力学显示掺杂了Pd/CNT 的PdZnO 催化剂甲醇活化能并未改变,因此Pd/CNT 的加入主要加强了催化剂上的氢溢流,促进了PdZnO 上Pd0的形成,增强了CO2的加氢过程。Qu等[25]也做了类似的尝试,使用共沉淀法将Pd/CNT与PdGa2O3催化剂结合到了一起,甲醇的选择性也得到了提升。
Venugopal 等[26]通过浸渍法制备了Pd-Ga2O3/SiO2催化剂,同时也使用浸渍法分别制备了Pd/SiO2、Ga2O3/SiO2催化剂,然后将其物理研磨混合。发现通过浸渍法制备的Pd-Ga2O3/SiO2催化剂具有最佳的甲醇选择性,而将Pd/SiO2、Ga2O3/SiO2两种催化剂混合后,甲醇的选择性较单独使用Pd/SiO2或Ga2O3/SiO2有较大提升,同时在反应过程中观察到了甲酸中间物种。实验说明甲醇在Pd-Ga2O3基催化剂上由双活性中心形成,Pd上的氢溢流对甲醇的影响较大,并且氢溢流的作用可以通过物理研磨可以实现。Song等[27]使用浸渍法制备了Pd/MCM-41催化剂用于CO2加氢,并使用Ca、La、Ga 等对其改性。实验发现通过添加金属氧化物能提高甲醇的选择性和CO2的转化率,在反应条件下会形成Pd6Ca3合金,且高分散的Pd 和CaO 起到了协同作用,分别提供加氢和CO2吸附活性位。
由上文综述可知,负载型贵金属催化剂CO2加氢机理基本符合双活性位机理。Pd 等贵金属在反应过程中提供氢气解离和溢流作用,而金属氧化物助剂或氧化物载体提供CO2吸附活性位,两种活性位的协同作用实现了CO2加氢,从而进一步生成甲醇。基于该反应机理,对负载型贵金属催化剂的改性主要是提高表面金属分散和稳定性以促进氢气解离溢流,亦或是强化CO2吸附和加强两种活性位的亲密程度。
2.3 金属氧化物催化剂
由于Cu 基催化剂在反应过程中结构不稳定,容易在水的影响下发生表面羟基过量、Cu 烧结团聚、Cu 氧化态发生改变等多种状况,从而导致失活[28]。而贵金属催化剂价格昂贵,没有大规模工业化应用前景。因此除了Cu 基催化剂和负载型贵金属催化剂外,金属氧化物用于CO2加氢的研究也开始受到了广泛的关注,相关研究如表6所示。
近期,李灿院士团队[29]通过共沉淀法制备了13%ZnO-ZrO2双金属固溶体氧化物催化剂,如图4所示,该催化剂在320℃具有90%的甲醇选择性和近10%的CO2转化率。而且该催化剂具有非常好的稳定性,在工业条件下连续反应500h 并未出现催化剂失活的迹象。此外,该催化剂具有良好的抗飞温和抗中毒性质。床层温度上升至400℃后甲醇选择性降低,保持24h 后降温回到320℃,甲醇选择性回到初始水平并无失活迹象。反应过程中加入50μL/L SO2及H2S 气体并不影响催化剂活性,该催化剂有良好的应用前景。
另一类金属氧化物催化剂,In基催化剂制备甲醇的相关研究可追溯至In2O3在乙醇和甲醇蒸汽重整(MSR)中的应用。Umegaki 等[30]报道了蠕虫状In2O3上的乙醇重整产物有较高的CO2选择性,推断In2O3抑制了反应中可能存在的逆水气变换反应(RWGS)。Lorenz 等[31]报道了在In2O3催化剂上的甲醇重整反应,CO2选择性接近100%。因此,研究者们开始关注In2O3催化剂制备甲醇的可能性。
刘昌俊等[32]对In2O3进行了CO2加氢的活性测试,结合TGA、XRD 和HR-TEM 等表征手段,发现In2O3有良好的热稳定性。通过建立微观动力学模型,发现升高反应压力有利于提升甲醇产率。在270℃、4MPa、H2/CO2=3 时,CO2转化率为1.1%,甲醇选择性为54.9%。
2016年,Martin等[33]首次报道了In2O3/ZrO2催化剂,相比于已得到工业应用的Cu-ZnO-Al2O3催化剂,该催化剂的优势在于可以达到接近100%的甲醇选择性以及非常好的稳定性,如图5,在5MPa、300℃下运行1000h 未出现失活。相比TiO2、ZnO、Al2O3等其他载体,当ZrO2作为载体时,甲醇的单位时间产率最高,因此ZrO2和In2O3的相互作用被认为是高甲醇选择性的关键。
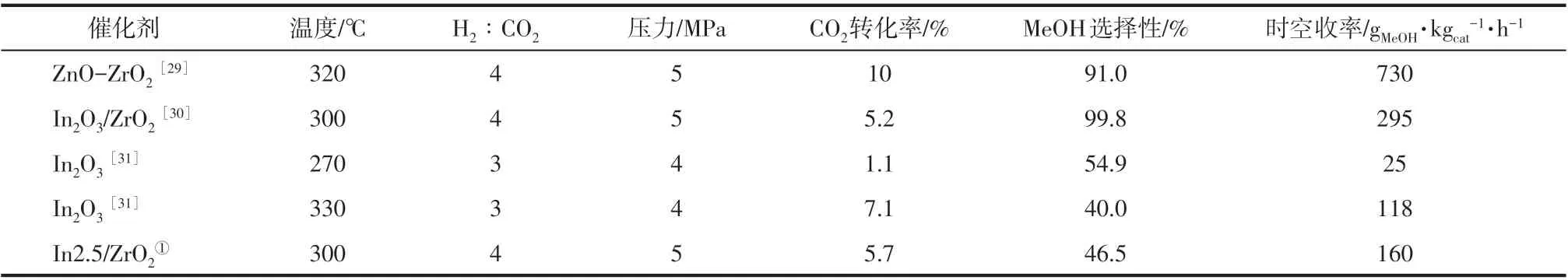
表6 CO2加氢制甲醇的氧化物催化剂

图4 ZnO-ZrO2上CO2加氢性能随Zn比例、温度、反应时间和有害气体添加的变化[29]

图5 In2O3/ZrO2上CO2加氢性能及与Cu-ZnO-Al2O3稳定性对比[33]
3 铟基催化剂
氧化铟(In2O3)作为一种新型n型半导体功能材料,在光电催化、氮氧化物还原[34]、气体传感器等领域得到广泛研究和应用。如上一节所述,相比传统Cu 基催化剂,In 基催化剂具有在高温条件下能高效生成甲醇的优势。因此,近年来对In2O3在二氧化碳热催化领域的表征应用吸引了越来越多研究者的关注。
3.1 反应机理
叶静云等[35]对CO2在In2O3上加氢进行了理论计算和实验研究。DFT 研究认为In2O3(110)表面可以非均相裂解H2,即形成InOH和InH中间过渡物种。InH 可以对In2O3(110)表面吸附的CO2加氢,从而形成甲酸盐物种*HCOO,且In2O3表面有很强的疏水性。此外,他们还对In2O3(110)表面不同Ov(氧空缺)上的CO2加氢活性进行了研究,其中Ov4可以将CO2加氢生成*HCOO 物种,并持续加氢生成甲醇。其中,*H2CO 生成*H3CO 是反应的控速步骤[36]。此外,叶静云等[37-38]还在Pd/In2O3催化剂上CO2加氢进行了DFT计算,计算结果表明甲醇主要由*HCOO路径生成。
Frei 等[39]随后对In2O3进行了微观动力学研究,发现In2O3上生成甲醇的活化能和RWGS 的活化能分别为103kJ/mol 和117kJ/mol。该团队同时通过DFT计算比较了不同的甲醇生成路径。计算结果表明,在表面产生*H2COOH 后,生成甲醇是热力学能量更低的反应路径。张敏华等[40-41]建立了Zr修饰的In2O3(110)表面,通过DFT 计算模拟In-ZrO2界面及Zr 对反应的影响。结果表明Zr 的掺杂削弱了Ov的生成能力,而In-ZrO2界面处的CO2吸附能力得到了增强。此外,ZrO2的掺杂抑制了*HCOO、*H2CO 及*H3CO 三种重要的甲醇生成中间体的分解,提高了甲醇的选择性。Dou 等[42]发表了类似的报道,建立了CO2和CO 在缺陷ZrO2负载In2O3(110)面上加氢的DFT模型。
Tsoukalou 等[43]结 合Operando XAS-XRD 和In situ TEM等技术,研究了In2O3催化剂在CO2加氢反应整个生命周期中动态结构转变与对应甲醇产率的变化。如图6,他们观察到在活化阶段In2O3结晶度没有显著变化,但被逐渐还原,氧空穴增多;在甲醇产率达到最大值的稳定阶段,In2O3占比为50%~40%,无定形的In2O3-x占比为50%~60%,且两者结构在不断发生着动态转换;随着反应的继续进行,过度还原的In0含量增多,结晶度下降了60%,从而导致了催化剂的失活。反应后的催化剂在CO2或空气中也只能被部分氧化,并且无法恢复到新鲜催化剂的粒径。因此,作者认为In2O3-x是活性相,而In0是失活相。
Chen 等[44]研究了不同晶型In2O3的催化效果。首先他们通过水热法以薄毡Al2O3/Al 纤维作为载体,成功负载了六方晶型In2O3(H-In2O3),发现水热制备过程中尿素和In的比例为4.5时,氧空位数量最多,表面碱性最强,催化剂性能相应也最优异。使用该催化剂在325℃、4.0MPa的反应条件下能得到67.6%的甲醇选择性,同样以薄毡Al2O3/Al纤维为载体,通过以浸渍法制备的立方晶型In2O3(C-In2O3)上甲醇选择性仅为36.8%。通过原位FTIR证实了反应中间体为甲酸盐物种(HCOO)。
3.2 铟与载体间相互作用
正如上一节提到的,In2O3/ZrO2上能高选择性地生成甲醇,因而许多研究者从不同方面来揭示In-Zr 之间独特的相互作用。陈天元等[45]制备了不同In负载量的In/ZrO2催化剂来研究In-Zr之间特殊的相互作用,发现In 的负载量能有效调控产物CO和甲醇的选择性,在负载量质量分数从0.1%上升到5%的过程中甲醇选择性逐渐提高。HADDFSTEM光谱技术以及对应的EDX元素映射表明低负载量(In0.5/ZrO2)时In2O3均匀分布在ZrO2表面,而高负载量(In5/ZrO2)时In2O3发生团聚,颗粒变大,说明不同负载量的催化剂表面In的种类存在差异。再结合原位DRIFTS 和TPD-MS 分析,提出In的作用提供解离吸附的H以及*HCOO和*H3CO的生成位点,ZrO2的主要作用是稳定HCOO 中间体。In负载量质量分数小于0.5%时,InOx高度分散,存在大量的In-Zr 界面,HCOO 很容易进入ZrO2上分解生成CO;In 负载量质量分数提高到2.5%~5%时,Zr 修饰的In2O3晶体能够促进*HCOO 进一步加氢,最终生成甲醇,反应路径示意见图7。
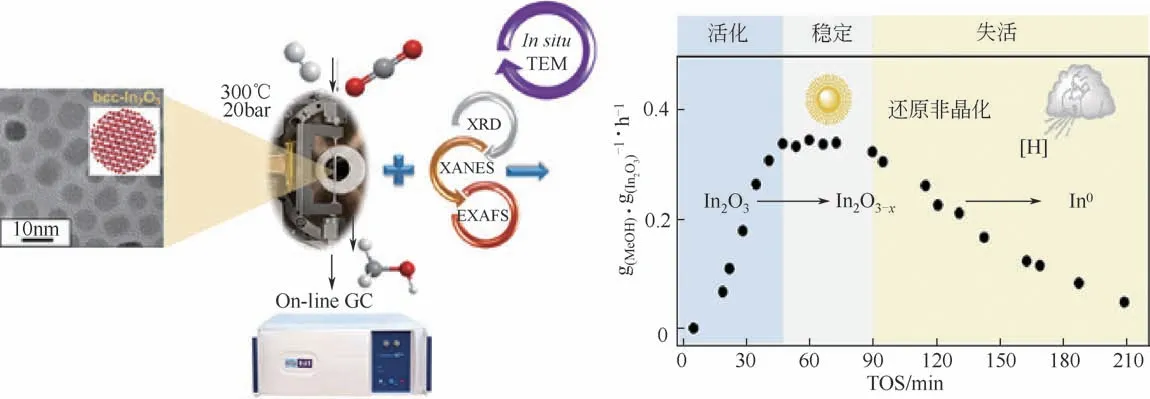
图6 CO2加氢反应活化、稳定和失活阶段In基催化剂相结构变化[43](1bar=105Pa)
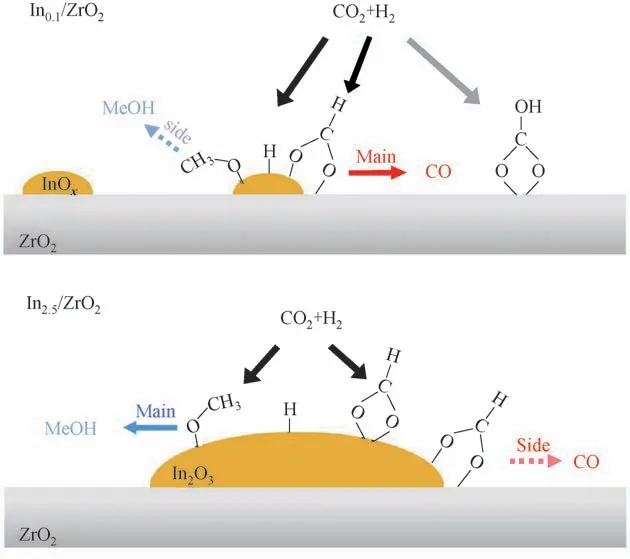
图7 In0.1/ZrO2和In2.5/ZrO2在CO2加氢反应中的反应路径和结构性能关系[45]
Frei 等[46]从电子效应、几何效应和界面效应这几方面来研究In-Zr之间的特殊作用。为了使In-Zr达到最大程度接触,他们首先用共沉淀法制备了不同比例的In2O3-ZrO2,发现相比于纯ZrO2,即使少量的In 也会使ZrO2变成亚稳态的四方晶型结构,证明In-Zr 之间存在强电子作用。而催化剂性能相比纯In2O3并无显著提高,甚至有些比例还有下降,从而排除了电子效应。接着他们又分别在相同负载量下比较单斜晶型ZrO2(m-ZrO2)、四方晶型ZrO2(t-ZrO2)、CeO2和Al2O3作为载体,发现m-ZrO2上单位时间甲醇产率远超其他载体。他们把这归功于In2O3和m-ZrO2外延对齐提高了分散性以及两者晶格匹配不佳,有利于生成更多独特的氧空位。
曹晨熙等[47]研究了不同载体对于负载型铟基催化剂的影响,发现仅ⅣB 族元素(Ti、Zr、Hf)氧化物作为载体时,In基催化剂表现出明显的CO2加氢活性,其中In/HfO2和In/ZrO2具有较高的甲醇选择性,而In/TiO2上主要生成CO。通过设计稳态动力学实验、TP实验以及高压原位DRIFTS表征,发现在反应条件下In/HfO2和In/ZrO2的表面物种是甲酸盐和甲氧基,In/HfO2解离加氢能力更强,有利于甲醇生成。他们的工作揭示了In-Hf之间也存在着类似In-Zr的相互作用。
3.3 助剂作用
Cu、Co、Ni 等过渡金属以及Pd 本身就具有CO2加氢反应的催化活性,将它们与In2O3结合引入额外的活性位,从而提升催化剂性能,也成为了改性In 基催化剂的重要思路。Shi 等[48]采用水热法合成了InCu@SiO2核壳催化剂,在280℃、3.0MPa 反应条件下,其单位时间甲醇的产率达到了6.55mmolCH3OH/(h·gcat),显著优于单一金属的Cu@SiO2、In@SiO2核壳催化剂以及浸渍法制备的CuIn/SiO2负载型催化剂。进一步研究发现Cu-In之间的相互作用有利于催化剂还原并形成更多的氧空位,Cu2In合金和In2O3之间的界面位对于CO2的活化起到了关键作用。
有研究使用水热法制备了In-Co催化剂,发现在应用于CO2加氢反应中,不同于纯Co3O4几乎只生成甲烷,纯In2O3转化率很低且主要生成CO,In-Co 上生成甲醇的选择性能超过80%的选择性[48]。In-Co 催化剂上单位时间的甲醇产率为0.45gMeOH/(h·gcat),超 过 了 传 统Cu-ZnO-Al2O3上 的0.27gMeOH/(h·gcat),且副反应RWGS 更少。他们通过ADF-STEM imaging和EELS在反应后的催化剂上发现厚度在1~4nm的In2O3-Co结构,认为这是活性相。通过DFT计算证实了In2O3-x和Co之间存在电荷转移,增加了表面氧空位,进而增强了In2O3-x活性。Snider等[49]制备了一系列不同In/Pd比例的双金属负载型催化剂(In-Pd/SiO2)。证实了Pd的加入能提高催化剂活性和甲醇选择性,其中In/Pd比例为2∶1时催化剂性能最优。他们建立In-Pd双金属DFT理论模型,并结合原位XAS等表征技术,如图8所示,发现活性相来源于In在表面富集的In-Pd合金与In2O3的相互作用。此外,他们进一步推广他们的工作,发现Ni的加入能起到和Pd类似的作用。

图8 In-Pd/SiO2催化剂在CO2加氢反应中的结构[50]
Frei等[50]进一步研究了Pd对In2O3在CO2加氢制甲醇的作用,他们分别以共沉淀法和浸渍法的方式引入Pd,由于Pd具有解离H2并产生氢溢流效应的作用,两者均能提高甲醇的产率,但浸渍法制备的Pd-In2O3稳定性较差。接着他们使用固态115In NMR技术等手段以揭示Pd-In2O3上氧空位的形成和短程结晶度,并结合理论模拟,发现在共沉淀法制备的催化剂上,Pd 嵌入In2O3晶格中限制Pd 团簇的生长,有利于H2O 的脱附,避免In2O3烧结;而对于浸渍法制备的催化剂,Pd 分布在In2O3表面,容易团聚,氢溢流效应过强,导致催化剂过度还原,并引发晶体聚集。他们的工作为In 基催化剂的结构设计提供了新的思路。
其他助剂也被运用于In 基催化剂的改性。为了扩大In 基催化剂在高温(320~400℃)下催化CO2加氢生成甲醇的优势,Akkharaphatthawon 等[51]通过共沉淀法引入Ga 制备了不同In-Ga 比例的GaxIn2-xO3催化剂,发现Ga 的加入提高了催化剂的比表面积,减小了粒径,更重要的是通过电子作用增强了高温下对H2和CO2的吸附。当Ga/In=1/4时,甲醇产率达到最大值,而且继续增加Ga 比例会使对CO2和H2的吸附过强,导致甲烷大量生成。Chou等[52]尝试在负载型In2O3/ZrO2上继续添加Y 和La 两种稀土元素作为助剂,发现Y 或La 的加入均增加了表面CO2吸附位点,并且相比于未添加助剂的催化剂,在保持甲醇总产率基本不变的情况下,提高了大约20%的甲醇选择性。
此外,还有一些研究者们开始将In 基催化剂上CO 或CO2加氢制甲醇,与甲醇在分子筛上进一步碳-碳偶联生成烃类产物这两个反应进行耦合。例如,高鹏等[53-54]将In2O3与ZSM-5 和SAPO-34 耦合用于CO2加氢催化制备液态燃料和烯烃,Dang等[55]研究了Zr 在In 基催化剂和SAPO-34 双功能体系中发挥的作用。
4 结语
CO2加氢制甲醇技术对于解决环境问题、提供新型清洁能源、生产高附加值化学品具有重要意义。本文综述了CO2加氢制甲醇反应的热力学分析,Cu 基催化剂和贵金属催化剂应用于该反应的重要工作以及近几年兴起的对于In 基催化剂的研究进展。但目前CO2加氢制甲醇催化剂仍然存在着单程转化率不高、RWGS等副反应降低了碳原子利用率、催化剂易失活、反应机理不明确等问题。未来的发展中,以下几方面的研究尤为关键:①目前对改性In 基催化剂的研究尚不充分,通过引入新的助剂或额外的活性金属,调控载体物理化学性质,进一步提升甲醇产率,限制副反应;②设计特殊结构的催化剂,建立原子尺度调控活性相和助剂分布的技术,来提高在反应过程中的稳定性;③深入研究反应机理,采用原位表征技术,检测反应条件下催化剂结构的动态变化,反应物及中间体的吸附形式,进一步辅助催化剂的设计;④加速与分子筛上甲醇制备烃类反应的耦合研究,特别是利用好In基催化剂在高温下活性好和醇制烯烃过程的反应温度更匹配这一优势,建立并完善双功能催化剂体系,实现从CO2一步制备高附加值化学品。
