水系钠离子电池Na0.44MnO2正极的制备及性能研究
2021-03-07汪慧明陈重学
薛 晴, 李 慧, 汪慧明, 徐 丽, 陈重学
(1.全球能源互联网研究院有限公司,先进输电技术国家重点实验室,北京102209;2.武汉大学动力与机械学院水力机械过渡过程教育部重点实验室,湖北武汉430072)
近年来,随着动力电池以及移动电子设备行业的迅猛发展,具有明显能量密度优势的锂离子电池又掀起一股研究热潮。然而,锂在地壳中的储量有限(含量约0.006 5%)且分布不均(主要在南美洲地区),严重限制了其在大规模储能领域的应用。而Na 与Li 处在同一主族,具有相似的物理化学性质,此外钠元素在地壳中储量颇丰(含量约2.74%)、分布广泛均匀,基于脱嵌机制的钠离子电池与锂离子电池体系类似,而水系电池具有绿色安全、无污染且价格低廉等突出优势,这使得水系钠离子电池吸引了广泛关注,被视为下一代规模储能体系的理想选择[1]。
正极材料是决定水系钠离子电池成本和性能的关键,被视为电池体系中最重要的组成部分。水系钠离子电池常用的正极材料包括锰基氧化物、普鲁士蓝类和聚阴离子型化合物等[2]。而锰基氧化物中的Na0.44MnO2电极材料因其特殊的隧道结构吸引了诸多研究者的兴趣。在Na0.44MnO2结构中,MnO5四面体和MnO6八面体连接构成特殊的三维框架结构,该骨架存在两种形式的隧道结构,即较大的S 形隧道和较小的五边形隧道[3]。这一特殊的隧道使得Na+在其中进行可逆脱嵌的同时,Na0.44MnO2电极材料依然可维持良好的结构稳定性,且Na0.44MnO2电极材料具有资源丰富、价格低廉、环境友好等突出优点而成为水系钠离子电池正极材料的研究热点[4-6]。我们通过溶胶凝胶法获得的Na0.44MnO2循环1 000次容量保持率达91.7%[5,7]。Whitacre 课题组研究了不同Na/Mn 对目标产物的影响,结果表明Na/Mn 化学计量比为0.55 时,贫钠杂质α-Mn2O3和富钠杂质β-Na0.7MnO2生成量较少[8]。Zhan 等在不同温度下(600、700、750、800 ℃)分别合成具有不同储钠性能的电极材料,结果显示750 ℃的样品具有更好的循环稳定性和倍率性能[9]。Chen 等研究了不同锰源对尖晶石LiMn2O4电化学性能的影响[10]。可见,电极的形貌与其性能有着密切的联系,而不同的前驱体盐会影响电极材料的形貌[11-12]。
在本工作中,我们分别以C4H6MnO4·4 H2O、MnCO3、50%Mn(NO3)2溶液作为锰源,通过固相球磨法制备了Na0.44MnO2电极材料,并研究了锰源对Na0.44MnO2晶体结构、形貌及其在水系钠离子电池中电化学性能的影响。在此基础上,分析了Na0.44MnO2在水系电池中的反应机理。
1 实验
固相法合成Na0.44MnO2:按Na/Mn 相应的摩尔比称取Na2CO3(国药、分析纯)和锰源[分别为C4H6MnO4·4H2O、MnCO3、50%Mn(NO3)2溶液(均国药、分析纯)],置于玛瑙球磨罐中,加入一定量球磨珠,再加入适量丙酮(国药、分析纯)分散剂,于球磨机中以300 r/min 的转速机械球磨混合3 h,将混合均匀的样品置于鼓风干燥箱中在80 ℃下干燥6 h,随后将干燥后的前驱体粉体置于马弗炉中,在850 ℃煅烧15 h 得到Na0.44MnO2产物,三种产物分别命名为MCHO、MCO、MNO。
采用X 射线衍射仪(德国布鲁克公司,D8 Advance)研究样品的晶体结构,衍射仪配备Cu 靶作为光源,Kα波长为0.154 nm,扫描范围为10°~60°,扫描速率为4(°)/min。采用扫描电子显微镜(卡尔蔡司公司,ULTRA/PlUS ZEISS)观察样品的微观形貌结构。采用比表面及孔径分析仪(精微高博,JWBK200C)研究样品的比表面积。
有机体系测试:按照Na0.44MnO2电极材料、导电碳(Super P)和聚偏氟乙烯(PVDF)粘接剂质量比8∶1∶1 的比例先称取一定量的Na0.44MnO2和Super P 并充分研磨混匀,再称取PVDF并加入适量溶剂N-甲基吡咯烷酮(NMP)一并置于离心管中,在匀浆机中充分研磨形成浆料,随后采用线棒涂布器将浆料均匀涂覆在铝箔上,再放入真空干燥箱中于80 ℃下干燥12 h。最后将干燥好的电极用切片机冲成直径为12 mm 的圆片,即为工作电极。以该电极为工作电极,直径为19 mm 的聚丙烯(PP)微孔膜为隔膜,擀磨光亮的钠片为负极,1.0 mol/L NaClO4/碳酸乙烯酯(EC)+碳酸二乙酯(DEC(体积比为1∶1)+5%氟代碳酸乙烯酯(FEC)为电解液,在无水无氧手套箱中组装成扣式2032 电池。在电池测试系统(LAND,CT-2001)上进行充放电测试,充放电电压范围为2~4 V。
水体系测试:先按质量比{ω(Na0.44MnO2电极材料)∶ω[导电碳(Super P)]∶ω[聚四氟乙烯(PTFE)]=8∶1∶1}称取一定质量的Na0.44MnO2和Super P 充分研磨,再称取PTFE 于小杯中并加入适量异丙醇破乳,再加入混合均匀的复合材料,在红外灯下充分搅拌并在对辊机上碾压成膜,将膜片置于80 ℃的真空干燥箱中干燥约6 h,而后用模具冲压制成直径6 mm 的圆片,最后将其在8~10 MPa 的压力下压在不锈钢网集流体上,即为工作电极。将此工作电极、6 mol/L NaOH 溶液为电解液、新打磨光亮的锌片为对电极和参比电极在空气中用U 型玻璃管组装成水系三电极电池。在电池测试系统(LAND,CT-2001)上进行充放电测试,充放电电压范围为1.1~1.9 V。
2 结果与讨论
图1 为MCHO、MCO 和MNO 三种样品 的XRD 谱图和BET 比表面曲线。通过图1(a)对比发现,三个样品均与Na0.44MnO2的标准谱图(Pbam 空间群, JCPDS No. 27-0750)十分吻合,而经过仔细对比发现MNO 和MCHO 样品均在32°附近出现了Mn2O3的杂质特征峰(PDF:24-0508),MNO 样品杂质峰的出现归因于硝酸锰溶液中水不易挥发导致其与钠盐混合不均匀,进而生成杂相。而MCHO 杂质峰的出现主要是因为采用C4H6MnO4·4 H2O 作为锰源具有较大黏度,导致原材料混合不均匀而产生少量杂质相。相较之下,MCO 样品未出现任何杂质峰,表明合成了单一相的隧道型Na0.44MnO2材料。比表面测试结果如图1(b)所示。经过计算,MCHO、MCO、MNO 的比表面积分别为1.269、1.862、1.273 m2/g,较大的比表面积有助于促进Na+和电子在相界面之间的转移,提高电极材料的储钠性能。
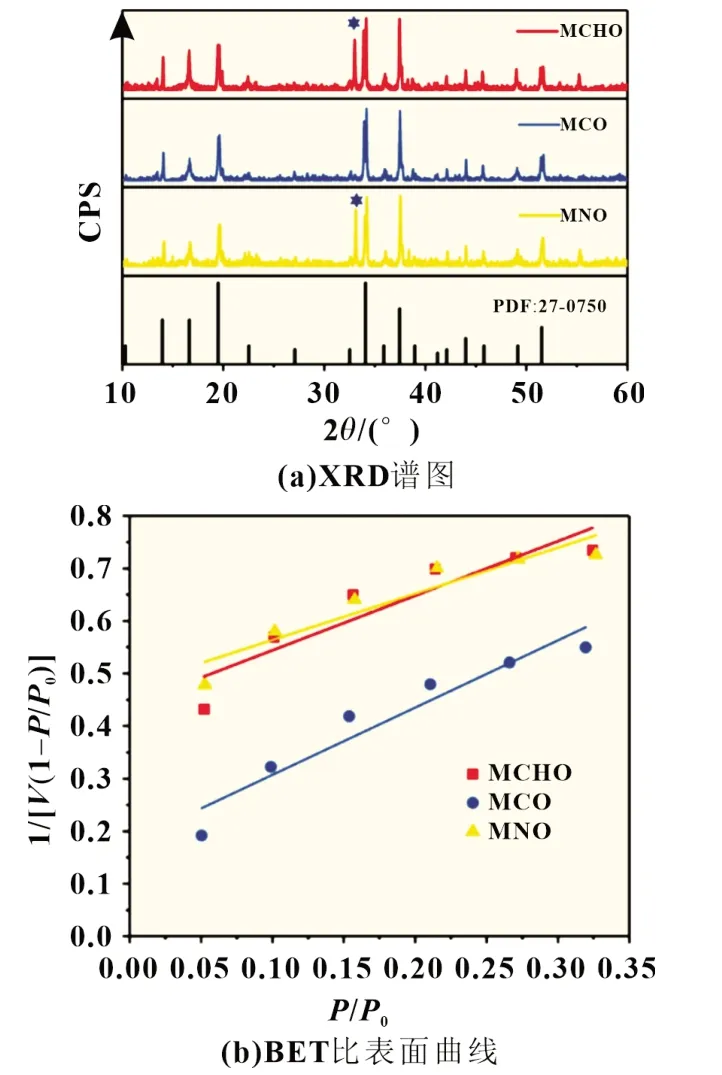
图1 MCHO、MCO和MNO三种样品的XRD 谱图和BET比表面曲线
图2 为三种样品的SEM 图。我们可以看出目标产物Na0.44MnO2均具有明显的纳米棒状结构,但是不同样品的Na0.44MnO2纳米棒尺寸有较大差别,这与不同材料在固相球磨时的机械过程和热处理过程中的化学行为有关。MCHO样品的纳米棒直径约400~600 nm[图2(a)],且表面存在碎屑小颗粒,归因于醋酸盐黏度较大且结晶水含量高,导致前驱体混合不均匀。MCO 样品呈直径较小(约200~400 nm)且形貌均一的纳米棒状结构[图2(b)]。而MNO 样品纳米棒状结构不明显,主要为短小的片状并且有明显的一次颗粒聚集现象[图2(c)],颗粒直径均大于350 nm,大部分直径大于0.5 μm。这是因为硝酸锰溶液中水含量高且不易挥发,在机械球磨过程中与钠盐混合不均匀导致Na0.44MnO2生长不完全。

图2 不同锰源合成样品的SEM 图
图3(a)为三种样品在有机电解液中的充放电曲线,电流密度为20 mA/g。MCHO、MCO 和MNO 样品的可逆放电比容量分别为96.6、107.5 和70.1 mAh/g。其中MCHO 和MCO样品的平均放电电压为2.81 V 左右,而MNO 样品的平均放电电压仅有2.67 V。通过图3(b)的长周期循环曲线可以看到,MCHO、MCO、MNO 样品在120 mA/g 的电流密度下的首次放电比容量分别为91.8、104.5 和61.2 mAh/g,经过500 次循环后三者的容量保持率分别为89.3%、87.6%和75.0%。MCO纳米棒状形貌均一,且具有较大的比表面,因而表现出最优的储钠性能,此结果与XRD、BET 和SEM 的测试结果一致。综上,我们认为MnCO3为固相法制备Na0.44MnO2的最佳锰源。
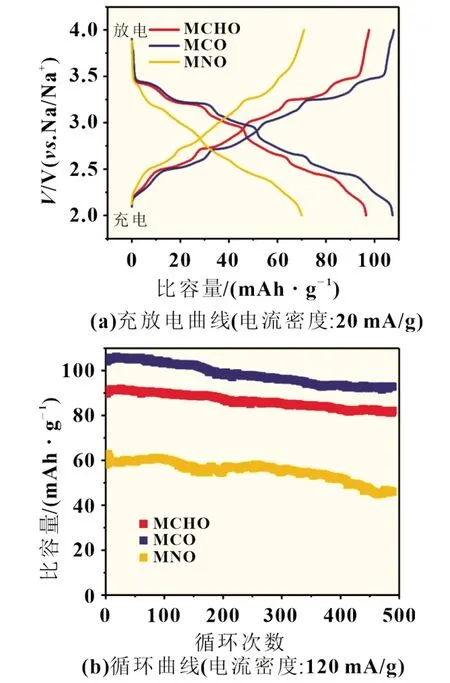
图3 MCHO、MCO和MNO 在有机电解液中的充放电曲线和循环曲线
随后我们研究了MCO 在6 mol/L NaOH 水溶液中的储钠性能。图4(a)的充放电曲线显示MCO 样品在120 mA/g 电流密度下的放电比容量为64.4 mAh/g,且具有多对充放电电压平台,对应于Na0.44MnO2在Na+脱出/嵌入过程中经历的多个相变反应。与在有机电解液中的充放电相比,Na0.44MnO2在水溶液中的充放电容量降低,且电压平台数减少,其原因可能是充放电电压窗口变窄,导致Na+未能完全脱出。图4(b)为MCO 在1 200 mA/g 大电流密度下的长循环曲线和库仑效率,首次放电比容量为56 mAh/g,经过1 000 次的循环后容量保持率高达82%,且该Na0.44MnO2在水体系中的库仑效率均大于99%,表明Na0.44MnO2在脱嵌钠过程中具有良好的可逆性和优异的循环稳定性。
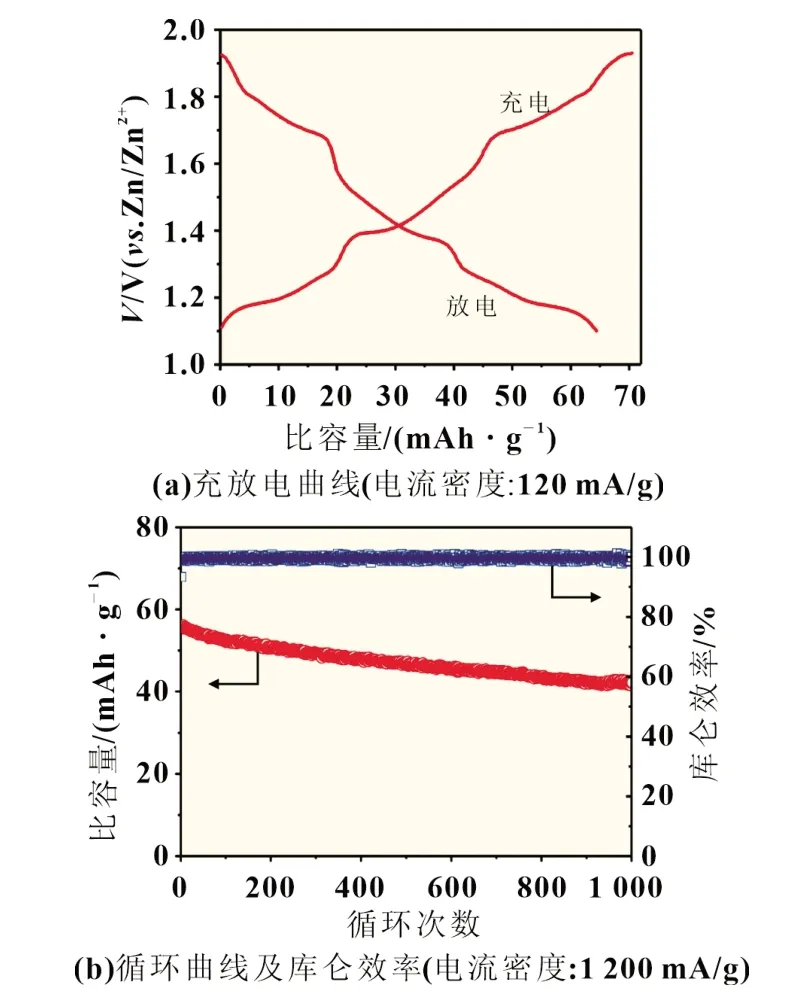
图4 MCO在6 mol/L NaOH水溶液中的充放电曲线和循环曲线及库仑效率
最后,我们研究了MCO 在脱嵌钠过程中的结构变化。图5 为不同充放电态Na0.44MnO2电极材料的非原位XRD 谱图。在Na0.44MnO2的首次脱钠(充电)过程中,XRD 谱峰均向高角度方向发生偏移,表明样品晶格参数变小,归因于Na+脱出导致的晶面间距变小。在Na0.44MnO2的嵌钠(放电)过程中,XRD 谱峰均向小角度方向移动,对应于Na+的嵌入造成的晶格参数增大。经过对比可以发现,Na0.44MnO2在脱嵌钠的过程中结构没有发生变化,表明没有新相的生成,其在水体系中具有良好的结构稳定性。
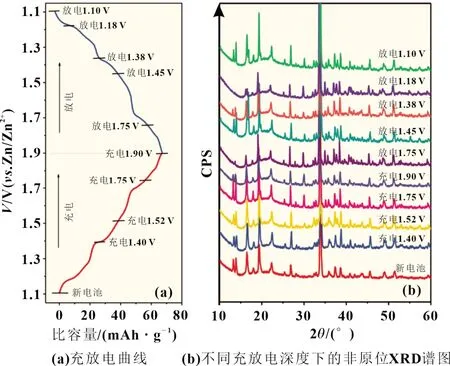
图5 MCO在6 mol/L NaOH水溶液中的非原位XRD测试
3 结论
我们分别以C4H6MnO4·4 H2O、MnCO3和50%Mn(NO3)2溶液为锰源制备了三种Na0.44MnO2材料,并研究了不同锰源对Na0.44MnO2电极材料的形貌、结构及储钠性能的影响。结果显示,当采用碳酸锰作为锰源时,所得Na0.44MnO2为结晶良好、形貌均一的纳米棒,直径约为200~400 nm,且具有较大的比表面积(1.862 m2/g),这将有助于促进Na+和电子在相界面之间的传递和转移,从而提高Na0.44MnO2的储钠性能。在有机体系中,Na0.44MnO2在120 mA/g 的电流密度下首次放电比容量达到104.5 mAh/g,循环500 次后容量保持率高达87.6%。水体系中,Na0.44MnO2在120 mA/g 电流密度下的放电比容量达到64.4 mAh/g,循环1 000 次后容量保持率高达82%。本工作可为Na0.44MnO2电极材料的规模生产制备提供基础数据,并有助于推进水系钠离子电池在规模储能系统中的应用。
