金属锂电池的热失控与安全性研究进展
2021-03-05张世超沈泽宇陆盈盈
张世超,沈泽宇,陆盈盈
浙江大学化学工程与生物工程学院,杭州 310027
1 引言
近年来,锂离子电池由于具备能量密度高、循环寿命长、无记忆效应和安全性较好等优点,已在便携式电子产品和电动汽车中得到了广泛应用,对现代社会产生了深远的影响1-3。然而,电池安全问题逐渐受到广泛关注,笔记本电脑和手机中锂离子电池爆炸事故时有发生4,以及多起新能源汽车起火事故,严重阻碍了它们的进一步实际应用5。目前,使用石墨负极的锂离子电池的比能约为260 Wh·kg-1,接近理论能量密度极限6,而电动汽车及储能市场迫切需要更高的比能量(≥ 500 Wh·kg−1)并扩展行驶距离(≥ 500 km)7-9。金属锂理论容量高达3860 mAh·g−1,具有最低的还原电位(−3.04 V,相对标准氢电极(SHE))以及较小的密度(0.53 g·cm−3),是未来锂电池负极材料的最终选择10,11。使用金属锂作为负极的金属锂电池理论比能极高,如锂氧电池和锂硫电池的比能分别高达3582和2567 Wh·kg−1,发展潜力巨大12-14。
遗憾的是,相比于锂离子电池,金属锂电池面临着更为严峻的安全问题。除了非水系电池体系常见安全问题外(如电解质的高度可燃性、隔膜材料的热收缩性、液态电解质易泄漏等),不可控的锂金属沉积/剥离更使安全风险激增。具体来说,金属锂的反应活性极高,与电解质副反应加剧,形成异质固态电解质界面膜(SEI),复杂化界面过程,导致枝晶状锂沉积;金属锂固有的体积效应使得SEI容易破裂,无法阻止电解质的侵蚀,导致SEI或死锂的堆积与电极的粉化,带来了不可逆的容量损失、库伦效率(CE)降低和电解质消耗等一系列问题15。更可怕的是,尖锐的针状锂枝晶可能会刺穿隔膜使电池内部短路,产生热量导致内部温度升高,引发一系列放热反应,最终发生热失控,出现起火爆炸等灾难性事故。据报道,较高的能量密度和容量会导致更早和更严重的热失控反应16,因此实用化金属锂电池的安全问题更为复杂。最近针对锂离子电池热失控和安全性的综述和评论已有多篇报道17-21,还有针对热失控过程的热传播建模研究22、排气分析23,24、喷射出的粉尘分析25和检测与监测方法26,而针对金属锂电池的综述却很少。
锂电池的热失控问题主要与电解质的化学稳定性、电化学稳定性以及电解质与隔膜的热稳定性差有关,深入理解热失控过程和提高电池热安全性,成为研究热点之一。近年来已有一些提高电解质安全性的研究成果,包括阻燃剂电解质、离子液体、高浓电解质、局域高浓电解质和热响应聚合物电解质等,另外在提高隔膜材料的热稳定性、设计热响应隔膜、阻燃性隔膜和智能型隔膜方面也取得了巨大进展。这些策略在一定程度上提高了电池的安全性,然而复杂的热失控问题依然很突出,有待进一步地研究和解决。
本文从金属锂电池的热安全角度出发,首先分析电池热失控的诱因及过程,然后介绍在材料层面上提升电池热安全性的多种策略,最后展望了安全型金属锂电池未来的发展方向和研究前景,这篇综述为研究者理解金属锂电池的热失控特征及设计更安全的锂电池提供了一定的参考价值。
2 金属锂电池的热失控过程分析
2.1 金属锂电池的安全性
电池的安全性与隔膜的热稳定性和液态电解质的可燃性密切相关,因为电池的起火爆炸可能是由隔膜在受热时体积收缩而导致的电池内部短路27和易燃液态电解质的剧烈燃烧28引起的。大部分商业化的锂离子电池所用的液态电解质仍适用于金属锂电池。表1为锂电池所用传统液态电解质中常见碳酸酯类和醚类溶剂的熔点、沸点和闪点,可见传统碳酸酯类溶剂的沸点和闪点很低,具有高度易燃性,所以电池的运行温度被限制在60 °C以下29。而与金属锂负极相容性更好的醚类溶剂的沸点和闪点则更低30,因此商业锂电池的工作温度一般限制在20-55 °C范围内31。当超过该温度范围时,SEI会发生分解,引起一系列自加速放热反应,包括电解质与负极之间的界面反应、正极分解析氧、电解质氧化分解等,造成隔膜收缩与熔化和气体粉尘排出,带来了极大的火灾和爆炸的安全隐患,在触发热失控的情况下尤其容易出现灾难性事故32-35。

表1 锂电池常用碳酸酯类和醚类电解质溶剂熔点、沸点和闪点对比29Table 1 Comparison of melting point, boiling point and flash point of carbonate and ether electrolyte solvents commonly used in lithium batteries 29.
产气是铅酸电池、钛酸锂电池等电池系统中的一种普遍现象36。然而实验室条件下,金属锂扣式电池由于存在较大的封装压力,其产气问题往往被忽视。当金属锂电池从扣式电池形式放大到软包电池时,任何微小的缺陷都会加剧,使产气问题成为实用化高能量密度金属锂电池在未来发展中无法回避的话题37。锂电池热失控过程产生的气体有两个来源,第一是升温导致的有机溶剂的汽化;第二是电解质氧化和SEI分解等副反应的气体产物。大量的气体增加了内部压力,很容易使电池体积膨胀甚至破裂,排出的易燃气体与空气中的氧气混合引发火灾,具有较高的可燃爆炸危险性。另外,由层状正极材料分解释放的氧气易与挥发性溶剂和易燃气体剧烈反应,引发和加剧热失控过程18,38。Gao等37观察了使用金属锂负极和LiNi0.5Co0.2Mn0.3O2(NCM523)正极的软包电池的产气现象,发现金属锂与电解质之间的寄生反应是导致产气的主要原因,并通过构建多功能硅烷化界面(MSI)层有效抑制了产气。不仅如此,传统LiPF6/碳酸酯电解质热分解产生的气体还具有毒性,未来必须充分考虑各种电解质热分解产生的气体副产物的物理危害和健康危害17。
2.2 锂离子电池热失控的过程
热失控是由各种滥用触发的,如图1a,包括机械滥用(如碰撞、挤压、穿刺)、电滥用(如过充电、过放电、短路)和热滥用(如局部过热)等,在循环期间的一些潜在缺陷也可能演变为诱因19,20。热滥用往往由机械滥用和电滥用演变而来,很少独立存在,却往往是触发热失控的直接原因。内部短路(ISC)在超过90%的滥用条件下都会发生,一般来说,它是由于电池隔膜的故障而使正极和负极直接接触引起的,可能由以下原因导致:(1)机械滥用,隔膜因穿透或挤压而破裂;(2)电滥用,隔膜被生长的枝晶刺穿;(3)热滥用,隔膜在高温下收缩熔化而塌陷19。如图1b所示,Feng等20将ISC分为三个级别,在I级时,电池自放电缓慢且无明显发热,具有自熄灭特征;在II级时,电压下降和温度上升明显加快;在III级时,由于隔膜塌陷,热失控进程无法停止而产生大量热量。

图1 (a)锂离子电池热失控相关滥用条件示意图;(b)内部短路的三个级别20Fig. 1 (a) Schematic diagram of abuse conditions related to thermal runaway of lithium ion battery;(b) three levels of internal short circuit 20.
在此基础上,Feng等19利用加速量热(ARC)技术,在绝热测试环境中探究了电池层面上的热失控机理,将锂离子电池的热失控分为三个阶段。如图2a所示,他们将电池热失控的共同特性概括为{T1,T2,T3}和max{dT·dt−1},其中T1代表异常发热的开始温度,即ARC系统从电池内的副反应检测到明显发热的时刻,SEI分解,电池开始失去热稳定性;T2是电池不可控反应开始引发热失控的触发温度,是平缓升温区与急剧升温区之间的临界点;T3是热失控期间的最高温度,决定了热失控行为的严重程度;max{dT·dt−1}反映了热失控期间的最大放热速率,与电池的能量密度呈正相关39。对比图1b和图2a,可以发现ISC的三个级别和热失控的三个阶段是对应的,说明提高SEI、电解质和隔膜的热稳定性,可以增大T1、T2并减小T3和max{dT·dt−1},进而缓解热失控。
金属锂电池与锂离子电池热失控的机理有所不同。Puthusseri等40采用差示扫描量热法(DSC)探讨了锂硫电池和Li-LiNi0.5Co0.2Mn0.3O2(NCM523)电池的热安全性。如图2b,c,对比使用石墨负极的锂离子电池,量热结果表明隔膜熔化导致ISC和以锂负极为中心的热降解反应(锂硫电池体系为金属锂与硫在180 °C的放热反应;Li-NCM523电池体系为金属锂与电解质的反应)是它们热失控的主要机制。建模模拟结果也表明隔膜的热稳定性和锂负极与电解质的寄生反应(更高的动力学参数,包括反应热、反应速率)决定了金属锂电池热失控的临界起始温度。此外,电池容量、正负极负载比(N/P)对两种体系的金属锂电池最高温升的影响进行定量研究,为高安全金属锂全电池设计参数提供一定的理论指导。
全固态金属锂电池潜在的热失效安全问题近期也被得到证明。Chen等38使用ARC技术和密度泛函理论(DFT)计算研究了四种常见无机氧化物固态电解质(ISEs)的热稳定性,即Li1.5Al0.5Ge1.5(PO4)3(LAGP)、Li1.4Al0.4Ti1.6(PO4)3(LATP)、Li3xLa2/3−xTiO3(LLTO)和Li6.4La3Zr1.4Ta0.6O12(LLZO),结果如图2d所示。理论计算与实验结果表明,金属锂的高反应活性以及在高温下产生的氧气与熔融金属锂发生的放热反应为无机氧化物固态金属锂电池热失控的主要原因。其中,对锂本质稳定的LLZO与锂接触时没有明显的热释放。而对于对锂不稳定的Ti/Ge基ISEs,锂熔化后的高温和紧密的界面接触会加速界面反应,其产生的热量进一步促进ISEs的分解和氧气的产生,锂与氧气反应产生大量热量最终引起热失控。因此,全固态金属锂电池热失控反应过程需要得到更多重视和深入研究。针对全固态金属锂电池,通过引入合适的界面层作为物理屏障阻止锂与ISEs的直接接触,或者合理设计电池结构来减少负极侧氧气的释放,可以有效防止热失控。
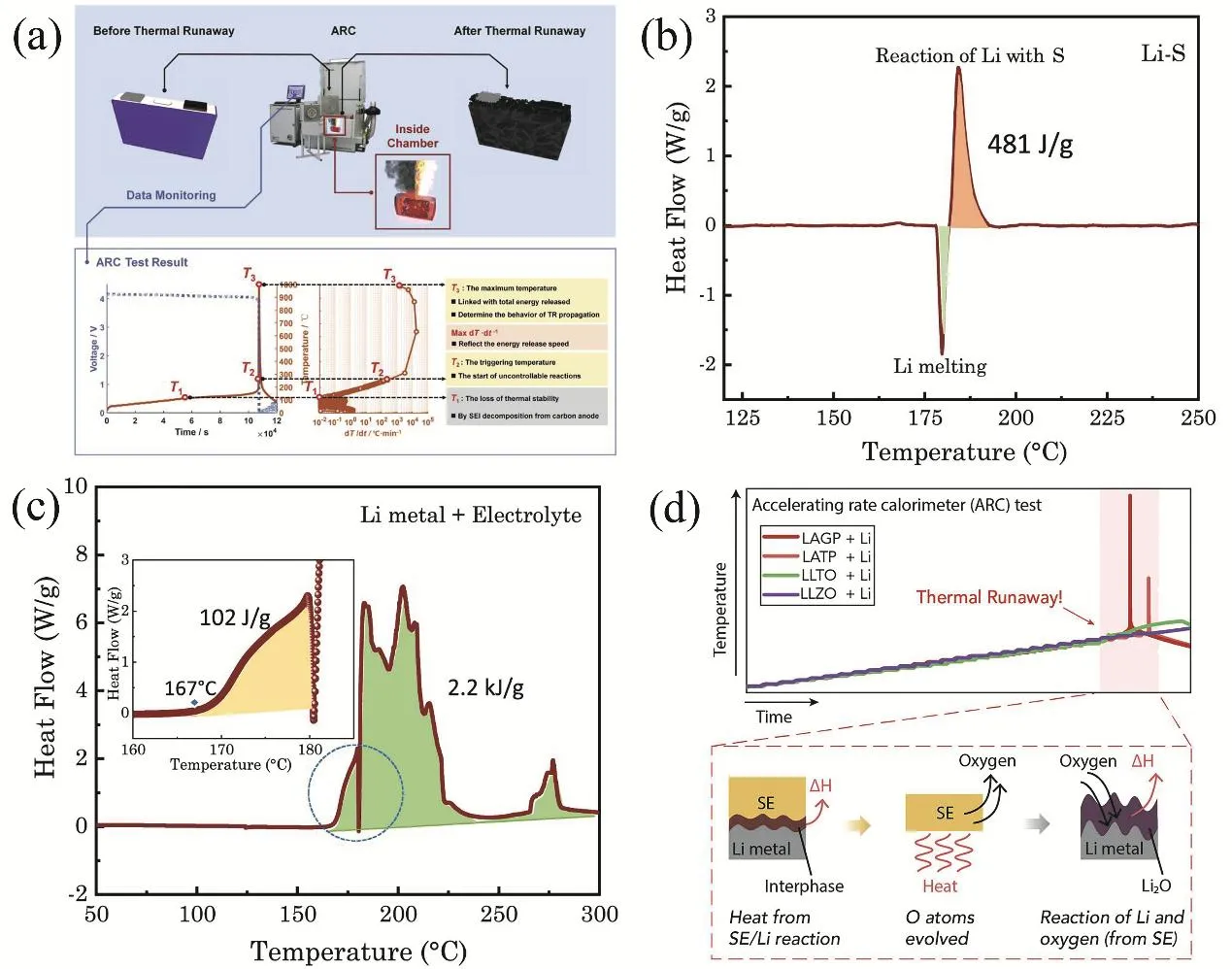
图2 (a)锂离子电池热失控的普遍特征19;(b)锂金属与硫的DSC加热曲线40;(c)在1 mol·L−1 LiPF6/(EC + DEC)电解质中锂金属的DSC曲线40;(d)锂金属与四种ISEs的ARC测试曲线及热失控原因示意图38Fig. 2 (a) The general characteristics of thermal runaway of lithium ion batteries 19; (b) DSC heating curve of lithium metal and sulfur 40; (c) DSC curve of lithium metal in 1 mol·L−1 LiPF6/(EC + DEC) electrolyte 40; (d) ARC test curve of lithium metal and four ISEs and schematic diagram of the cause of thermal runaway 38.
2.3 热力学对锂枝晶成核和生长的影响
枝晶生长是铜、镍、锌等金属在电镀过程中常见的电沉积现象41,已被人们所熟知,由于这种沉积一般是一次性的,因而在工业上并不是一个问题。然而对于多次充放电循环的金属锂电池,经过反复的电化学剥离与沉积,这些锂枝晶可能持续生长而刺穿隔膜,成为导致电池内部短路并引发热失控的一个重要原因42。
一般认为,在较高的电流密度下,枝晶问题会更严重。然而,Li等43报道了一种独特的锂枝晶演化机制,他们发现较高的电流密度会使枝晶产生自热愈合效应,可加快锂原子在表面的大面积扩散,从而修复枝晶并使得金属锂表面光滑。如图3a, 随 着 电 流 密 度 从 0.75 mA·cm−2增 加 到 9 mA·cm−2,锂枝晶的直径减小但堆积密度显著增加,当增大到15 mA·cm−2时,锂枝晶完全融合在一起,转化为相对光滑且致密的锂层。他们采用经典的成核和生长理论来模拟这种现象,预测结果表明过电位随电流密度的增加而增大,较高的过电位会减小成核半径,并增加枝晶的成核速率和成核密度。锂枝晶与高电流密度一起产生大量焦耳热,热模型预测15 mA·cm−2下枝晶升温大约40-60 °C,该自热效应处于安全水平,不会使电解质击穿或者隔膜受热损坏,但足以促进锂的表面扩散。在锂硫电池中的测试结果表明,有限的时间内以高电流密度(9 mA·cm−2)进行周期性操作足以修复锂负极表面形貌,并显著改善电池库伦效率。
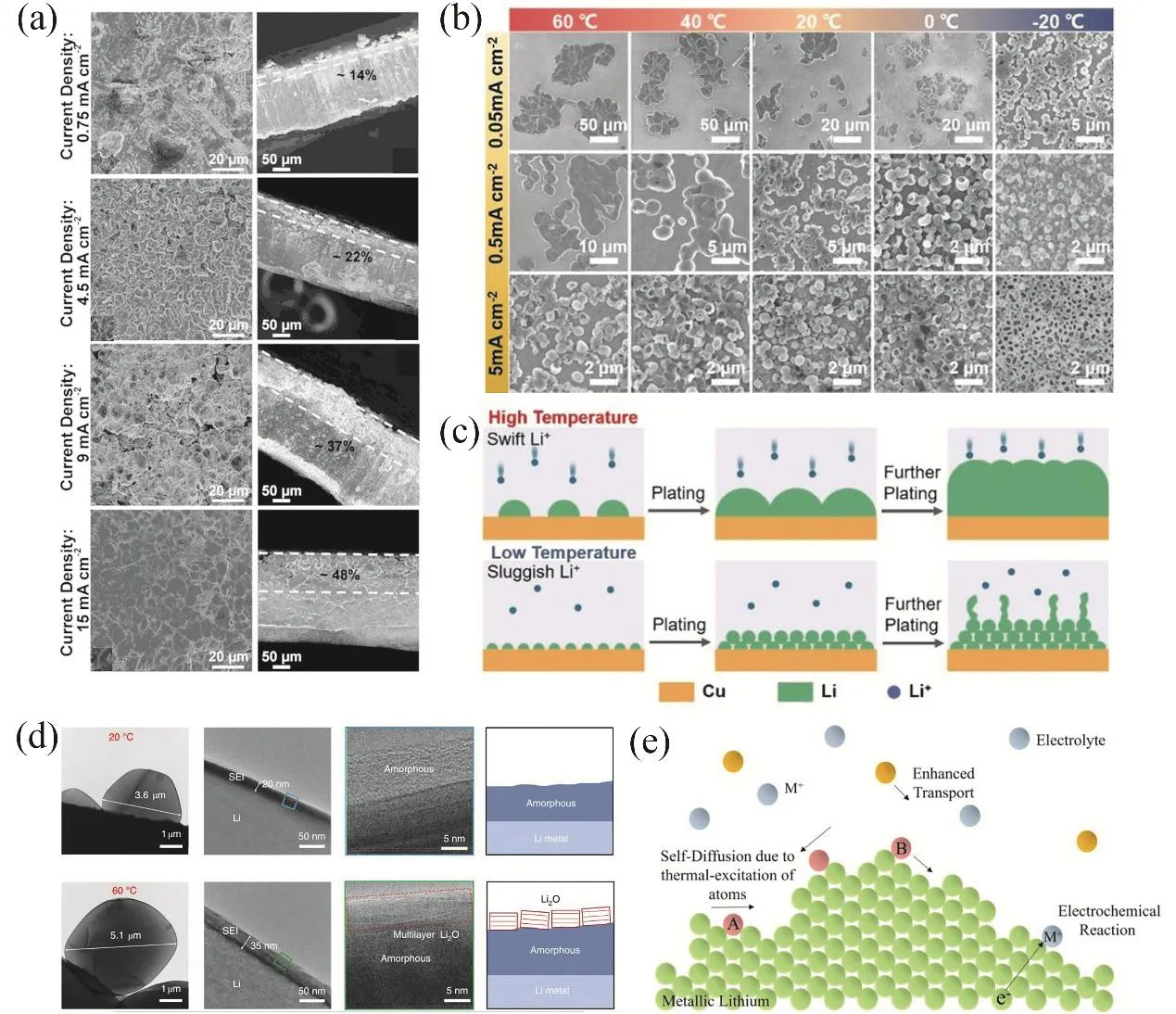
图3 (a)不同电流密度下锂锂对称电池中锂枝晶形态演化的扫描电镜(SEM)图43;(b)不同电流密度和温度下锂层的SEM图49;(c)高温和低温下锂成核和沉积过程原理示意图49;(d) Cryo-EM显示了在低温和高温下形成的SEI纳米结构的不同50;(e)锂离子电沉积过程中的三个基本过程示意图53Fig. 3 (a) SEM images of the morphological evolution of lithium dendrites in lithium-lithium symmetric batteries under different current densities 43; (b) SEM images of the lithium layer under different current densities and temperatures 49;(c) schematic diagram of the principle of lithium nucleation and deposition processes at high and low temperatures 49;(d) cryo-EM shows the difference in SEI nanostructures formed at low and high temperatures 50;(e) three basic processes in the process of lithium ion electrodeposition Schematic diagram 53.
在此基础上,Hundekar等44结合第一性原理的DFT计算和计算机热建模,发现了表面扩散速率与温度的强烈相关性。计算热模型证实大于10 mA·cm−2的电流密度可以产生足够的温度升高,以实现自扩散辅助的枝晶修复。他们进一步证明,锂枝晶在由磷酸铁锂(LiFePO4)/碳复合正极和金属锂负极组成的二次电池中可以被由电流控制的电池自加热成功修复。该加热会导致表面原子从锂枝晶尖端移出,因而使表面光滑,说明该愈合机制在实际的金属锂全电池中仍然适用。
然而,有些研究发现温度升高会加速锂枝晶生长或者降低电池性能45,其他一些研究却表明高温下电池性能会得到改善46,47,因此温度变化对锂枝晶生长和电池性能的影响无法确定。Hong等48认为,电池温度的升高会增加锂离子在电解质中的扩散系数、电化学反应速率和表面扩散,进而影响电沉积过程。为了揭示自热愈合机理,他们建立了一个热耦合相场模型,发现电化学反应势垒是决定高速率/高温下枝晶生长机制的关键参数。通常,当该势垒比扩散势垒小时,在高过电位/电流下的自加热会导致离子迁移大大增加,可以使界面生长速度均匀化,从而抑制枝晶的生长并实现稳定的电沉积;然而在较大的电化学反应势垒下,电沉积速率的增加会超过离子迁移速率的提高,大大增加枝晶的生长速率。
Yan等49从实验角度研究了操作温度对锂成核和生长行为的影响。如图3b,在同一温度下,随着电流密度的增加,锂核尺寸显著减小而成核密度显著增加;在同一电流密度下,相比于20、60 °C时锂核的尺寸增大而密度减小。通过系统观测、原位表征和理论模拟,他们发现高温增强了集流体的亲锂性和锂离子的迁移率,使集流体界面处锂离子的浓度升高,快速移动的锂离子在减少成核位点数量的同时增大了锂核尺寸(如图3c)。随着沉积的继续进行,大而稀疏的锂核逐渐生长并与相邻锂核融合,最终形成致密平滑的锂沉积层。
此外,研究表明升高温度可以改变SEI组成结构模式,进而从根本上调节锂沉积行为。Wang等50对比了使用醚基电解质的Cu/Li电池在20和60 °C的性能,发现60 °C时电池具有异常高的库伦效率和循环稳定性。如图3d,冷冻电镜(Cryo-EM)观察发现,20 °C时形成的非晶态聚合物SEI厚度较薄,而且其中的有机成分可溶于电解质使SEI极易破裂,在循环过程中重复的SEI修复/破裂导致了连续的副反应;而60 °C时形成的SEI具有有序分层的纳米结构和较大的厚度,外层为多层Li2O无机层,因此具有更好的机械强度和循环稳定性。
然而,电池内部不均匀的局部热点却极大可能触发内部短路并引起热失控。Zhu等51使用激光在电池内部产生局部高温,利用显微拉曼光谱进行测量,发现与周围较低温度区域相比,由于局部增强的表面交换电流密度,热点上的锂沉积速率提高了几个数量级,这将诱导明显的锂枝晶生长并导致电池内部短路,继而进一步升高局部温度。锂枝晶生长与局部温度升高之间的双向关系,揭示了锂枝晶生长的正反馈机制。另外升温还会触发电解质与活性材料和SEI的放热反应,进一步加剧热失控的风险。Golozar等52对全固态聚合物金属锂电池失效机理的分析结果,也表明局部温度升高和热失控有助于锂枝晶的形成。
综上所述,温度对锂枝晶的生长具有双重效应。Vishnugopi等53针对该问题提出了一个全面的论述,使用粗粒度动力学蒙特卡罗(KMC)模型捕获了锂离子电沉积过程的动态演变。如图3e,电沉积过程中发生了三个基本过程:锂离子(蓝色)在电解质中传输、锂离子在电极/电解质界面处发生电子转移和锂原子(绿色)在电极表面上扩散。其中原子A和B分别呈阶梯状和层间扩散,锂离子(黄色)和锂原子(红色)表示受热激发后其在电解质中传输和电极表面扩散速率分别增强。因此,使用均匀的热场(自加热和电池外部加热)可以同时增强锂离子在电解质中的传输和锂原子在电极表面的扩散,获得均匀的锂沉积;局部热点的存在会增加交换电流密度从而提高局部反应速率,局部优先的成核和沉积触发了锂枝晶的生长,可能穿透隔膜而导致电池短路。因此,采用均匀热场的电池的运行状况将优于常温下运行的电池,这为提高金属锂电池的循环性能和安全性提供了一种新的改进思路。
3 提升金属锂电池热安全性的策略
在材料层面缓解电池热失控的策略主要包括以下几个方面,首先是液态电解质改性,包括阻燃剂电解质、离子液体电解质、高浓电解质和局域高浓电解质等不易燃电解质体系。其次是隔膜材料改性,主要包括开发高热稳定性隔膜、热响应隔膜、阻燃性隔膜和具有枝晶检测预警与枝晶消除功能的智能型隔膜。最后是热响应聚合物电解质的应用。
3.1 液态电解质改性
3.1.1 阻燃剂电解质
添加阻燃剂是降低液态电解质可燃性最简便的策略,常用的阻燃添加剂包括磷酸盐、氟化物、氟化磷酸盐和氟化磷腈54。有机磷酸盐的存在能够抑制火焰的传播55,具有低粘度、对锂盐的溶解度高和宽的电化学窗口等优点,常被作为电解质的添加剂或助溶剂广泛使用,如磷酸三甲酯(TMP)、磷酸三乙酯(TEP)、磷酸三苯酯(TPP)等。
然而,含磷阻燃剂容易被还原分解,对锂金属反应活性高,形成的SEI不稳定,使电池的性能下降,因此常常需要添加与锂金属能够形成稳定SEI的成分作为共溶剂,来有效保护金属锂负极。Yang等56在锂硫电池TEP溶剂中引入氟化碳酸乙烯酯(FEC)作为成膜添加剂,利用FEC在金属锂负极表面的优先还原作用来抑制TEP的分解。他们发现添加30%体积比的FEC可以最大程度平衡电池的安全性与电化学性能。TEP能产生自由基(如PO·),有效捕获电解质燃烧时释放的H·、OH·等自由基,具有较好阻燃性能。如图4a,点火实验结果表明,TEP/FEC (体积比为7 : 3)溶剂不能完全点燃,而EC/DMC (体积比为1 : 1)溶剂极易点燃并且会持续燃烧。该电解质系统在不牺牲锂硫电池倍率性能的前提下,保证长循环性能和高度的安全性。此外,相同体系电解质被证明有更宽的电化学窗口(最高5 V),可普遍适用于使用LiNi0.8Co0.1Mn0.1O2(NCM811)、LiNi0.6Co0.2Mn0.2O2(NCM622)和LiCoO2(LCO)等4 V级正极的金属锂电池57。
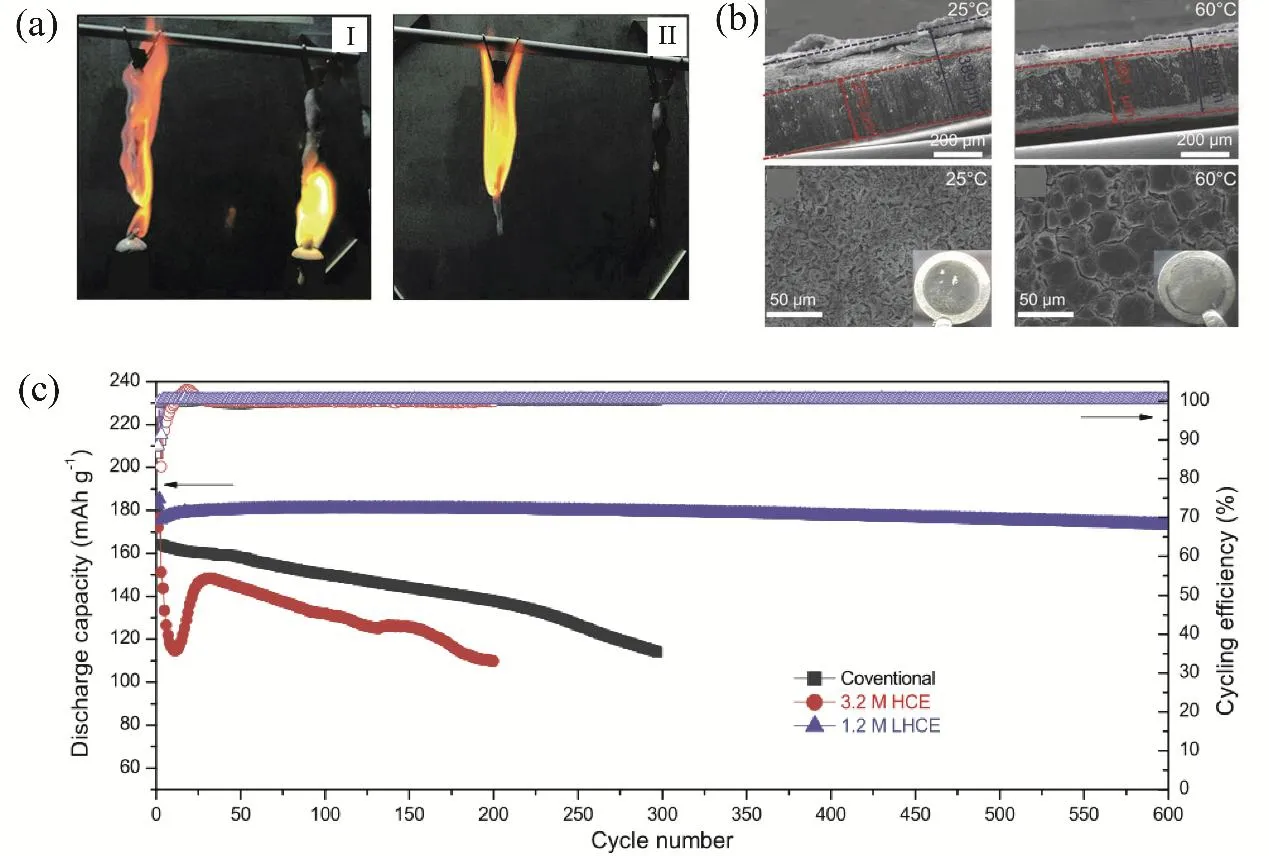
图4 (a)存在外源火(I)和没有外源火(II)时,EC + DMC溶剂(左)和TEP + FEC溶剂(右)的燃烧现象对比56;(b) 25和60 °C下50次循环后的锂沉积层横截面和俯视SEM图像47;(c)使用常规电解质、HCE和LHCE的电池循环效率和稳定性对比58Fig. 4 (a) Comparison of the burning phenomenon of EC + DMC solvent (left) and TEP + FEC (right) with an external fire(I) or without external fire (II) 56; (b) 25 and 60 °C cross-section and top SEM image of the lithium deposition layer after the next 50 cycles 47; (c) comparison of battery cycle efficiency and stability using conventional electrolyte, HCE and LHCE 58.
提高溶质锂盐的浓度,能够改变锂离子溶剂化结构及SEI组成,进而能够提高磷基电解质与锂金属的适配性,为开发高能量密度金属锂电池的安全电解质系统开辟了一条新途径。Yang等47使用双(氟磺酰)亚胺锂(LiFSI)、TEP和1,1,2,2-四氟乙基-2,2,3,3,-四氟丙基醚(TTE),制备了一系列锂盐浓度在1.1-3.8 mol·L−1范围的锂硫电池本征阻燃(IFR)电解质。如图4b,高浓IFR电解质在高温下(60 °C)能够实现微米级致密锂沉积,且在正极侧形成富含Li3PO4和LiF的界面(CEI)可抑制电解质与含硫物的副反应,实现锂硫电池的稳定循环。Chen等58报道了一种可用于4 V级金属锂电池的局域高浓磷基电解质 (1.2 mol·L−1LiFSI-TEP/双(2,2,2-三氟乙基)醚(BTFE)),具有较高的锂库伦效率(99.2%),大大提高了Li-NCM622电池的循环稳定性(如图4c)。
3.1.2 离子液体电解质
传统的易燃和腐蚀性有机液态电解质存在严重的安全问题。离子液体(IL)是一种仅由离子组成的溶剂,它的构成为有机阳离子和有机或无机阴离子。IL电解质具有优异的离子传导能力、电化学稳定性和热稳定性,并且可燃性极低,不挥发,具有较宽的电化学窗口(高达5-6 VvsLi+/Li),安全性好,是金属锂电池电解质体系的理想选择之一59。然而,IL电解质的高粘度和疏水性使它们无法完全润湿商用聚烯烃隔膜,并且严重降低了离子电导率,成为IL电解质的主要缺点60。
IL电解质能够改善金属锂负极表面SEI。Zheng等61采用离子液体N-甲基-N-丁基吡咯烷双(三氟甲基磺酰基)酰亚胺(Py14TFSI)作为助溶剂加入常规锂硫电池电解质中,诱导形成高质量的致密SEI,大大减少了多硫化物与锂金属之间的副反应。当离子液体含量为75%时,电池表现出很高的库伦效率和循环性能(如图5a)。另外,Py14TFSI含量的增加显著降低电解质的可燃性,提高安全性。此外,通过加入合适的稀释剂可以有效解决离子液体的粘度高的问题。Lee等62介绍了一种使用氢氟醚稀释剂(TTE)的离子液体(1-甲基-1-丙基吡咯烷双(氟磺酰基)酰亚胺(P13FSI))局域高浓电解质(LCIL)。如图5b所示,TTE降低了电解质粘度并显著增强了对隔膜的润湿性,促进了锂离子的迁移。由于IL和TTE固有的阻燃性,该电解质可以有效防止电池起火。此外,双阴离子(FSI−/TFSI−)之间的协同作用有助于修饰SEI,形成更薄的平滑致密沉积层(如图5c),提高锂库伦效率和抑制锂枝晶生长。该电解质相比常规IL电解质明显提高了Li-LCO电池的循环性能。

图5 (a)不同IL添加量的电池循环性能和库伦效率对比61;(b) DIL(稀释离子液体)、CIL(高浓离子液体)和LCIL对隔膜的润湿性和接触角对比图62;(c) DIL、CIL和LCIL中形成的SEI俯视和剖面SEM图62Fig. 5 (a) Comparison of battery cycle performance and coulombic efficiency with different amounts of IL addition 61;(b) comparison of wettability and contact angle of separator with DIL (diluted ionic liquid), CIL (highly concentrated ionic liquid) and LCIL 62; (c) top and cross-sectional SEM images of SEI formed in DIL, CIL and LCIL 62.
3.1.3 高浓电解质和局域高浓电解质
高浓电解质(HCE)能够改变锂离子溶剂化结构,大大减少自由态溶剂分子的数量,提高阻燃性能。此外,其诱导的SEI主要是由阴离子(如FSI−、TFSI−)还原分解形成的富无机物SEI,能够有效减少界面处的副反应,抑制锂枝晶的生长。然而,盐浓度的提高会导致粘度增加、成本升高、对隔膜润湿性差等问题。氢氟醚类(HFEs),例如TTE、2,2,2-三氟乙基醚(BTFE),因其粘度低、不可燃性、对锂离子的溶解能力可忽略不计(即不参与锂离子溶剂化结构)的优点,常用作稀释剂来构建局域高浓电解质(LHCE)。
高浓电解质和局域高浓电解质能够抑制正极活性物质或中间产物(例如多硫化锂)的溶解63,因此显著延长金属锂电池的循环寿命。然而电解质中阴阳离子与溶剂之间的溶剂化能力的差异可能会造成溶剂和离子的交换,导致多硫化锂重新形成。如图6a所示,高浓度锂盐倾向于形成接触离子对(CIP)和阳离子-阴离子聚集体(AGG),而不是溶剂分离的离子对(SSIP)。其中TFSI−和Sx2−与醚类溶剂分子之间的溶剂化能力较差,会导致溶剂-离子交换(SIE)过程,使溶剂化的Sx2−重新形成。Amine等64通过使用硅氧烷高浓电解质,有效消除隐藏的SIE过程,从而限制多硫化物的溶解和锂枝晶的生长。同时游离的溶剂分子大大减少,使得该高浓电解质无法点燃,具有极高的安全性。
此外,由于自由溶剂分子的减少,高浓电解质和局域高浓电解质能够具有更宽的电化学窗口,同时优化SEI和CEI组成结构,因此能够有效保护高压正极材料,减少电解质的侵蚀程度。Fan等65报道了一种由1 mol·L−1六氟磷酸锂(LiPF6)和FEC/4-三氟甲基碳酸乙烯酯(FEMC)/1,1,2,2-四氟乙基-2’,2’,2’-三氟乙基醚(HFE) (质量比为2 : 6 : 2)组成不易燃全氟电解质,形成富含LiF的SEI和以含氟复合物为主的CEI,可大大缓解锂金属体积膨胀与粉化(如图6b),并可稳定循环NCM811正极(库伦效率约99.93%)和5 V正极LiCoPO4(LCP) (库伦效率约99.81%)。此外,更宽的适用温度范围被得到证明,加速了电池实用化进程。Fan等66以4.2 mol·L−1LiFSI-FEC/FEMC和2.33 mol·L−1双(五氟乙烷磺酰基)亚胺锂(LiBETI)-FEC/DEC作为两种氟化电解质模型,使用四氟-1-(2,2,2-三氟乙氧基)乙烷(D2)和甲氧基全氟丁烷(M3)两种非极性溶剂制备了超级电解质。如图6c所示,非极性溶剂破坏了高极性分子之间的强相互作用,但与锂离子的相互作用远弱于锂离子和含氟碳酸酯的相互作用,全氟电解质的溶剂化结构得以保留。该电解质可以在0−5.6 V的宽电压范围和−125 - 70 °C的宽温度范围内使用。
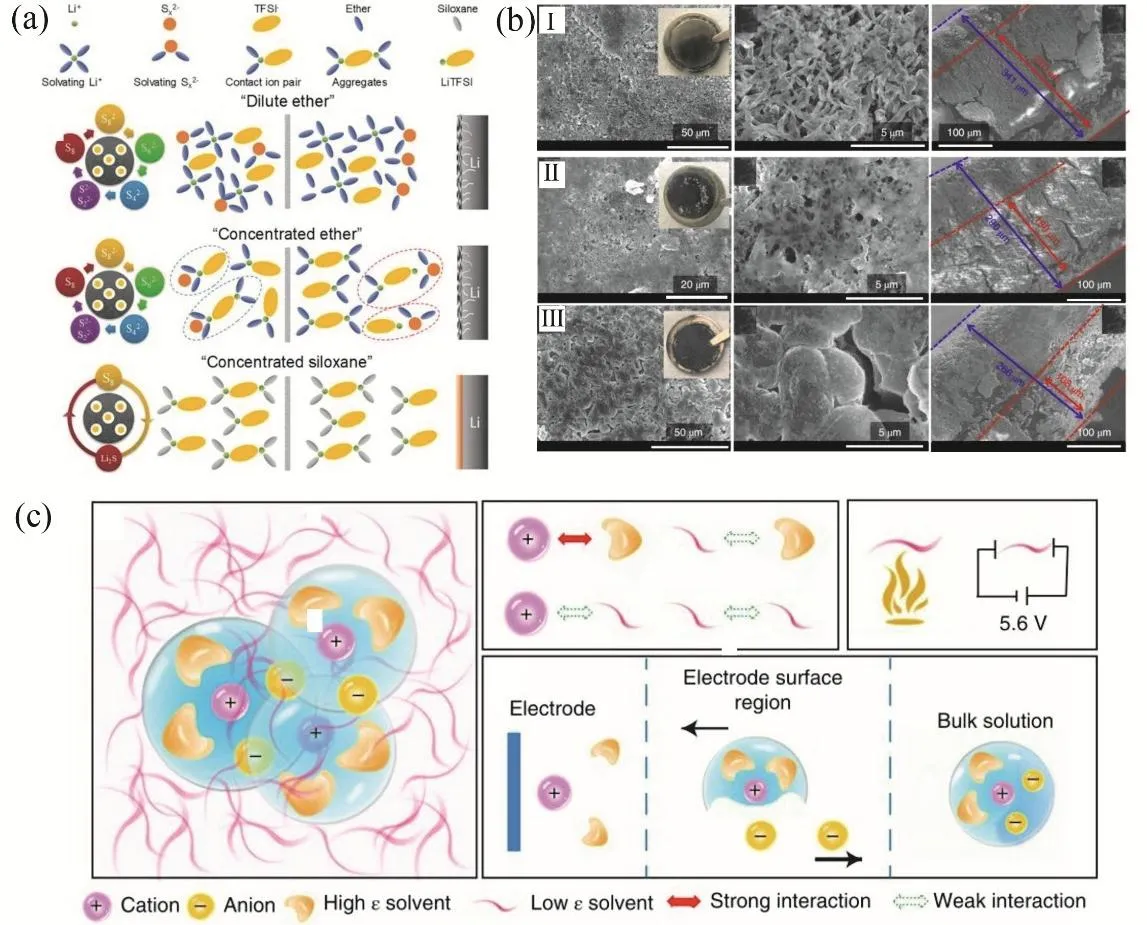
图6 (a)电解质中的常见物质及稀醚、浓醚、浓硅氧烷电解质中锂离子溶剂化结构图示64;(b) 100个循环后不同电解质(I、II、III中溶剂分别为EC/DMC、DMC/FEC和FEC/FEMC/HFE)中锂金属形态的SEM图65;(c)使用非极性溶剂的超级电解质原理图示66Fig. 6 (a) Common substances in electrolytes and diagrams of lithium ion solvation structure in dilute ether, concentrated ether, and concentrated siloxane electrolytes 64; (b) different electrolytes after 100 cycles (the solvents in I, II, and III are respectively EC/DMC, DMC/FEC and FEC/FEMC/HFE) SEM images of lithium metal morphology 65;(c) schematic diagram of super electrolyte using non-polar solvent 66.
3.2 隔膜材料改性
3.2.1 高热稳定性隔膜
传统聚烯烃隔膜熔点较低,热稳定性差,当电池内部温度高于其熔点时会产生较大的热收缩,使得正负极直接接触引起内部短路而导致热失控。使用陶瓷颗粒或者高熔点聚合物制作耐热涂层,是提高聚合物隔膜热稳定性最常见的做法。类似研究已有广泛报道,例如Al2O3/SiO2复合涂层隔膜67、酚醛树脂改性的陶瓷涂层隔膜68、等离子体处理Al2O3陶瓷涂层隔膜69等。然而,使用涂层往往需要加入聚合物粘结剂,不仅增加了成本,而且涂层很可能会改变隔膜的孔结构和离子通道,影响电池性能70。Lee等71首次报道了利用射频(RF)磁控溅射将无粘结剂的Al2O3涂层引入商用PE隔膜的可行性,然而超过10 min的溅射时间不能满足商业化应用的要求。Lee等72引入聚多巴胺(PDA)表面热阻涂层,制备的PDA/Al2O3涂层PE隔膜热稳定性优异(在145 °C下暴露30 min,尺寸保持率67%,而PE仅为9%) (图7a),同时极大地缩短了溅射加工时间(从40到2 min),具有大批量商业化生产前景。另外亲水性PDA和Al2O3涂层创建了理想的离子通道,在不堵塞隔膜微孔的情况下,改善了隔膜对极性有机电解质的润湿性。
生物材料和仿生材料具有良好的纳米结构,能够有效改善聚烯烃隔膜对电解质润湿性不足和孔隙率低等缺陷。如图7b,Ma等73基于原始蛋壳膜(ESM)制备出平整的三维纳米多孔柔性再生ESM(RESM),保留了原始ESM高亲水性、孔分布均匀和高热稳定性等优点。ESM和RESM具有大量高极性和亲水性的含氮官能团,与锂离子亲和力很强,相互连接的微纤维形成丰富的纳米孔,有效抑制锂枝晶的生长。与在150 °C时即收缩明显的商业化Celgard隔膜相比,ESM和RESM在180 °C下尺寸收缩极小,热稳定性优异,在Li-LiFePO4电池中也显示出明显改善的性能。此外,可生物降解的材料逐渐受到关注。如图7c,Song等74将天然粘土矿物凹凸棒石(ATP)纳米纤维与从褐藻中提取的可生物降解多糖海藻酸钠(SA)通过相转化工艺制备了SA/ATP多孔隔膜。ATP纤维赋予了材料阻燃性、高热稳定性和机械强度,在250 °C加热2 h后仍能保持其尺寸。高表面积和纳米级孔隙赋予隔膜优异的电解质润湿性和电解质保留率(液态电解质吸收率高达420%)。此外,隔膜可以在土壤中降解而不会引起任何污染,环保无毒,展现了可降解生物材料在电池应用中的良好前景。
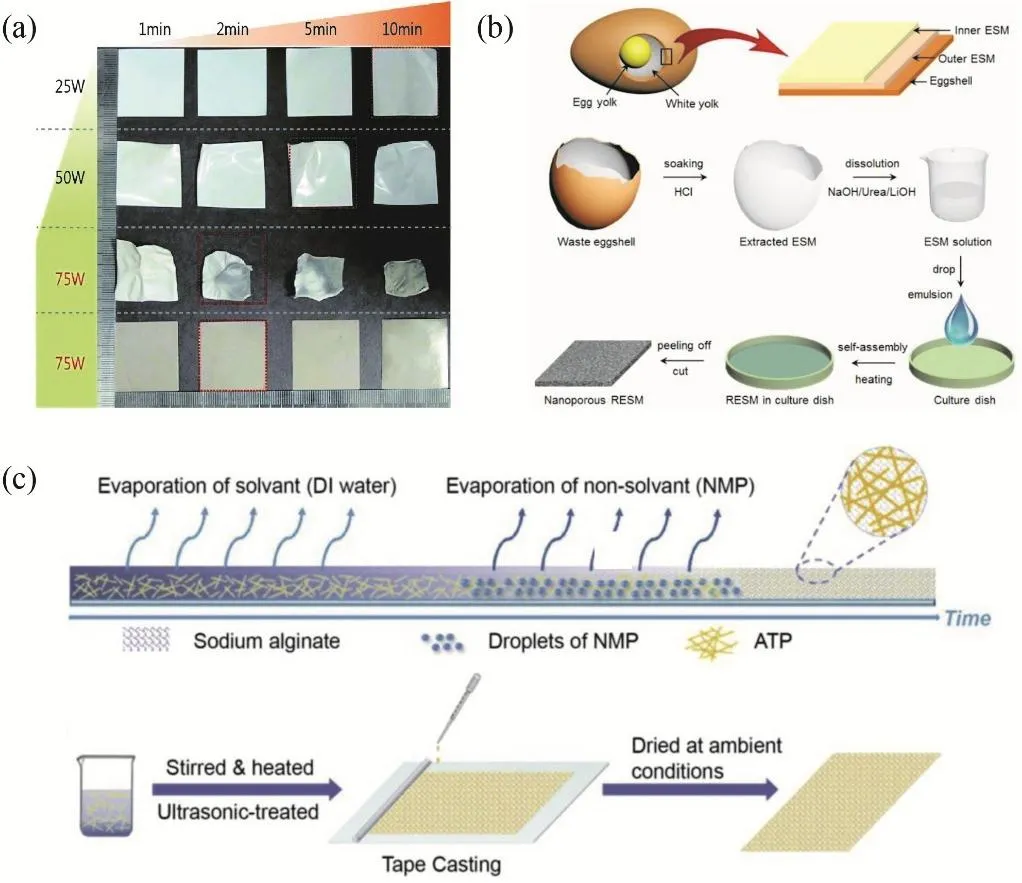
图7 (a)裸PE隔膜(从上到下前三个)和PDA涂层(第四个)PE隔膜在不同射频溅射功率和时间下的数码照片72;(b)鸡蛋和蛋壳结构以及RESM制备过程示意图73;(c)相转化法机理和材料制备的总体过程示意图74Fig. 7 (a) Bare PE separator (the first three from top to bottom) and PDA coating (fourth) ) digital camera images of PE separator under different RF sputtering power and time 72; (b) schematic diagram of egg and eggshell structure and RESM preparation process 73; (c) schematic diagram of phase inversion method mechanism and overall process of material preparation 74.
3.2.2 热响应隔膜
商业化隔膜主要成分为PE和PP,两者熔点分别约为120和160 °C,以PP/PE/PP三层复合隔膜为例,若热失控时电池内部温度在120-160 °C之间,外部的PP层可以维持隔膜尺寸几乎不变,内部的PE层熔融会堵塞隔膜的微孔,阻碍了离子在液态电解质中的传输,使电池阻抗增加,防止电池的进一步反应,这种机制被称为热关闭。然而,当电池温度高于160 °C时,三层隔膜受热熔化而严重收缩变形,可能会使得正负极直接接触而发生内部短路,失去热关闭的保护作用75,因此提高两侧材料的热稳定性至关重要。
聚对苯二甲酰对苯二胺(PPTA)具有高热稳定性、电化学稳定性和对液态电解质的润湿性76,可用作隔膜外侧的保护层。Zhang等77采用低温共聚的方法合成了低分子量PPTA,然后用浸渍包覆和相分离的方法将其引入到完整的PE网络表面,制备出具有热关闭功能的热稳定隔膜。如图8a,p-PE-1 (改性复合隔膜)具有显著的热稳定性。极性PPTA涂层增强了隔膜对液态电解质的润湿性,对隔膜固有孔隙率几乎无影响,使用该隔膜的Li-LCO电池放电容量和倍率性能良好。与之类似,He等78采用自组装过程成功制备高耐热性的PPTA@PP复合隔膜。
可再生材料纤维素纳米纤维(CNFs)具有较高的热稳定性。Pan等79采用简单的造纸层压工艺,将从藻类中提取的CNFs直接层压在经等离子体处理后的具备亲水性的PE隔膜两边,设计了一种CNFs/PE/CNFs三层(CPC)隔膜(如图8b)。CNFs层内部均匀的纳米通道可以有效均匀化锂离子流,在200 °C的高温下暴露60 s后,内部PE层熔融堵塞隔膜微孔,阻碍了离子传输(如图8c)。CNFs可以在330 °C以下保持其尺寸稳定,因此CPC隔膜整体尺寸不变,从而提供了热关闭功能。

图8 (a)两种隔膜在不同温度下暴露0.5 h的热收缩行为对比图77;(b) CPC隔膜制作过程示意图79;(c) CPC隔膜原始状态和在200 °C下起到热关闭作用的SEM对比图79Fig. 8 (a) Comparison of thermal shrinkage behavior of two kinds of membranes exposed to different temperatures for 0.5 h 77; (b) schematic diagram of CPC membrane production process 79; (c) original state of CPC membrane comparison with SEM which has a thermal shutdown effect at 200 °C 79.
3.2.3 阻燃性隔膜
溴化聚苯醚(BPPO)是一种常见的卤系阻燃剂。Woo等28设计了一种基于BPPO的阻燃隔膜(FRS),如图9a所示,FRS显著降低了液态电解质的可燃性。BPPO具有由苯环和溴组成的结构,其中苯环提高了热稳定性,溴降低了隔膜的可燃性。随着温度升高,BPPO释放出溴自由基(Br·),可与高反应性H·反应形成低反应性的HBr,从而阻碍了引起燃烧反应的自由基链反应80。此外,由于BPPO的高热稳定性,即使温度达到200 °C,FRS仍可以保持尺寸的稳定81,使用FRS的Li-LiFePO4电池显示出改善的循环性能。
将阻燃剂封装于隔膜纤维内部实现自控释放,可以减少其对电池性能的负面作用。Liu等82通过静电纺丝技术设计了一种具有热触发阻燃性能的新型核壳微纤维隔膜,外壳是聚偏氟乙烯-六氟丙烯(PVDF-HFP),阻燃剂TPP封装在壳内部。如图9b所示,壳结构阻止了阻燃剂直接暴露于电解质并大大减缓了其溶解,从而防止阻燃剂对聚合物电化学性能的负面影响。另外,PVDF-HFP的熔点相对较低(约160 °C),因此可以在燃烧之前或燃烧初期熔化,阻燃剂释放到电解质中发挥阻燃作用。

图9 (a) FRS和PE/PP隔膜中液体电解质燃烧的时间对比28;(b)核壳结构阻燃隔膜原理示意图82Fig. 9 (a) Comparison of the burning time of liquid electrolyte in FRS and PE/PP separators 28; (b) schematic diagram of the principle of the flame retardant separator with a core-shell structure 82.
3.2.4 智能型隔膜
极端条件下运行的电池仍可能暴露在枝晶生长和内部短路的风险之中,将枝晶检测、短路预警、枝晶消除等功能集成到隔膜上,可以更好地提高电池的安全性。Wu等83报道了一种聚合物-金属-聚合物三层结构的双功能隔膜,既可以物理上隔离正负极,又提供了新颖的电压感应功能。如图10a所示,当锂枝晶刺穿隔膜聚合物层并将中间金属层与负极相连时,外部电路可以检测到明显的电压降,从而预告危险。然而,由于传统隔膜的厚度一般小于12 μm,因此从检测到安全隐患到发生内部短路的时间可能只有几秒钟,无法提供足够的时间阻止灾难的发生。Moon等84在两层隔膜之间夹入石墨设计了一种辅助电极,它不仅可以作为安全传感器实时预警,而且石墨层能够快速吸收锂离子,清除一定量的锂来抑制枝晶进一步生长,从而提供足够时间关闭电路。
在隔膜中引入可与锂金属反应的填料,或者改变锂枝晶生长方向,可以消除锂枝晶并实现超长循环寿命。Liu等85将SiO2纳米颗粒夹在两层商业化聚烯烃隔膜之间,如图10b所示,当锂枝晶生长到刺穿隔膜时,锂金属与SiO2接触发生固相转化反应而被腐蚀,减慢了锂枝晶渗透速率,将金属锂电池使用寿命延长约5倍。另外,通过在隔膜负极侧涂覆固定有锂离子的功能化纳米碳(FNC),可以控制锂枝晶的生长。如图10c,电池运行期间来自FNC层和负极的锂同时生长,相遇时会改变方向从而形成致密锂层,延长电池使用寿命86。使用固定化阴离子的隔膜也可以改善锂金属的电沉积稳定性,有利于在高电流密度下使用87。

图10 (a)智能电池设计和制造原理示意图83;(b) SiO2夹层隔膜消除锂枝晶示意图85;(c)智能隔膜改变锂枝晶生长方向原理示意图86Fig. 10 (a) Schematic diagram of the design and manufacturing principle of smart batteries 83; (b) SiO2 sandwich separator to eliminate lithium dendrites Schematic diagram 85; (c) schematic diagram of the principle of the smart separator changing the growth direction of lithium dendrites 86.
3.3 热响应聚合物电解质
与易燃、易泄露的液态电解质不同,聚合物电解质由于其特殊的结构和组成,具有质量轻、柔韧性好和易于加工等特点88-90,很容易添加上应变功能。设计具有热关闭功能的热响应电解质,可以有效防止电池的热失控91。
热响应聚合物电解质使全固态金属锂电池具备自保护功能。Zhou等92通过聚1,3-二氧戊烷(PDOL)和聚烯丙基硫化锂(PLAS)的共聚反应,设计了一种高离子电导率的非水热响应固态聚合物电解质(TSPE)。如图11所示,TSPE显示出对温度变化的自主准确感应。当电池温度升高到70 °C时,电解质将停止锂离子的运输并永久和不可逆地关闭电池,消除了燃烧和爆炸的可能性,对大型电池组的安全使用具有重要意义。
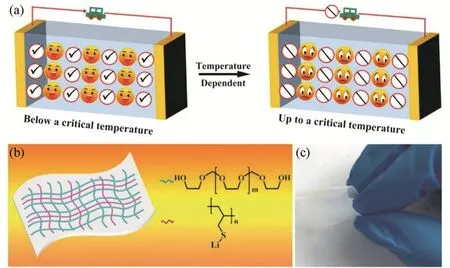
图11 (a)热响应聚合物抑制离子传导示意图;(b) TSPE (PDOL和PLAS)组成的示意图;(c)获得的TSPE膜的数码照片92Fig. 11 (a) Schematic diagram of thermally responsive polymer inhibiting ion conduction; (b) schematic diagram of the composition of TSPE (PDOL and PLAS); (c) digital photo of the obtained TSPE film 92.
将共聚物与低聚物共混,可以在高温下形成交联结构实现热关闭。Cheng等75通过将PVDFHFP共聚物与聚乙二醇二甲基丙烯酸酯(PEGDMA)低聚物共混,制备了具有热关闭功能的聚合物电解质。在成膜过程中,交联的低聚物提供了机械强度,而未交联的低聚物充当增塑剂。与聚烯烃隔膜的熔融机理不同,当温度升高到120 °C以上时,未交联的低聚物开始反应并在电解质中形成交联结构。这种致密的结构阻碍了锂离子的迁移,导致电池的阻抗增加,从而避免了自发热和热失控。另外,在高温下,交联的PEGDMA网络也显示出良好的尺寸稳定性。
4 总结与展望
金属锂负极由于其极高的能量密度成为锂电池负极材料的最终选择,然而锂的高反应活性和不可控的枝晶生长,带来了严重的安全隐患和热失控的风险,阻碍了金属锂电池商业化的道路。如何提高电池的安全性,成为一个亟待解决的问题。本文针对金属锂电池的安全性,首先介绍了热失控的原因及基本过程,然后在阻燃剂电解质、离子液体电解质、(局域)高浓电解质、高热稳定性隔膜、热响应隔膜、阻燃性隔膜、智能隔膜和热响应聚合物电解质等方面,对近年来的研究成果进行综述,总结了提高金属锂电池热安全性的多种策略。总的来说,能量密度的增加势必会降低电池的安全性,因此电池的安全性是相对的。
提高热安全是金属锂电池进一步发展以及最终实现商业化的关键因素,结合目前的研究现状分析,未来需要在以下几个方面进行深度研究。
(1)发展先进的表征技术来观测锂枝晶的生长、SEI结构和电池内部温度,例如冷冻电镜技术50,93,94、氢气捕集法检测枝晶95,利用磁场96、电场97等抑制锂枝晶的生长,利用显微拉曼光谱感应检测金属锂电池内部局部高温51,利用同步加速成像技术观察金属锂负极微观结构与温度的依赖关系98,利用超声检测电池内部状况99-101等。
(2)缓解热失控应包含多个层面的手段,比如材料、电池单体、电池组系统。有以下几个缓解步骤,即减少滥用条件的发生、一旦发生立即消除滥用条件、提高电池材料的热稳定性、减少热失控期间释放的能量、识别潜在的热失控并及时预警和减少电池组中热量传播的危害19。
(3)进一步研究高性能阻燃剂对离子溶剂化结构及SEI的影响,使之在发挥阻燃作用的前提下不影响电池循环性能;研究热响应材料和正温度系数材料,开发智能电池;研究更先进的电池热检测和热管理系统。
相信在研究者的共同努力下,未来高能量密度金属锂电池的热安全性必将得到进一步的提高,并最终实现商品化和实用化。
