腹腔镜下根治性膀胱切除+小切口辅助尿流改道术临床应用24例报告
2021-03-02廖明朗季辉华张正龙王天宝张少峰李云飞
许 杰,廖明朗,甘 伟,季辉华,陈 胜,张正龙,王天宝,高 钇,刘 云,张少峰,李云飞
(湖北医药学院附属人民医院泌尿外科,湖北十堰 442000)
在全球范围内,膀胱癌发病率为最常见肿瘤的第9位,死亡率居第14位,2012年世界膀胱癌年龄标准化发病率男性为9.0/10万,女性为2.2/10万[1-2]。根治性膀胱切除术(radical cystectomy,RC)+尿流改道是肌层浸润性膀胱癌和高危非肌层浸润性膀胱癌治疗的主要方法,该手术是泌尿外科操作过程最复杂、耗时最长且并发症最多的手术[3-4]。近20年来,随着腹腔镜技术的成熟和腔镜器械的改进,腔镜手术与传统开放手术相比,具有手术创伤小、术野清晰、术中出血少、术后恢复快等诸多优势[5-6],在许多单位中逐渐取代了开放手术。湖北医药学院附属人民医院于2015年9月至2019年6月针对24例肌层浸润性膀胱癌患者行腹腔镜下根治性膀胱切除(laparoscopic radical cystectomy,LRC)+尿流改道术,手术效果满意,现报告如下。
1 资料与方法
1.1 临床资料2015年9月至2019 年6月湖北医药学院附属人民医院共行LRC+回肠通道术21例,LRC+原位回肠新膀胱术3例,男性22例,女性2例,平均年龄68(56~72)岁。体重指数(body mass index,BMI)21.4±5.3,美国麻醉医师协会(American Society of Anesthesiologists,ASA)评分1分15例,2分9例。术前经膀胱镜肿瘤活检病理诊断为膀胱尿路上皮癌者23例、膀胱腺癌1例;低级别11例、高级别13例;T1期3例、T2期16例、T3期4例、T4期1例。术前可疑淋巴结转移2例,所有患者术前评估排除肺部及骨骼等远处转移。主刀均由同一术者完成。所有患者签署了知情同意书,该研究方案得到湖北医药学院附属人民医院伦理委员会的批准,术前已向患者及其亲属详细说明病情并获得患者及亲属的知情同意,术前3 d流质饮食,术前1 d禁食、口服抗生素及术前清洁灌肠。
1.2 手术方法
1.2.1患者体位及Trocar布局 患者气管插管全身麻醉生效后,仰卧位,头低脚高位20°~30°。于脐部上缘刺入气腹针,建立人工气腹,压力12~15 mmHg(1 mmHg=0.133 kPa)。套管放置均采用5孔法,脐上缘置入10 mm Trocar,放置30°观察镜,直视下分别在左、右腹直肌外缘置入12 mm Trocar,然后在左、右髂前上棘水平内侧2指处分别置入5 mm Trocar。
1.2.2膀胱切除 术前留置F16尿管,经尿管注入吉西他滨2.0 g+体积分数为0.9%的氯化钠溶液至50 mL保留膀胱灌注。具体手术操作步骤如下:①游离输尿管中、下段。切开侧腹膜,游离输尿管至膀胱,注意保留输尿管周围脂肪组织。②离断膀胱侧蒂。以骼内动脉为标志,依次离断脐动脉,膀胱上、下动脉等支配膀胱及前列腺的血管。③游离狄氏(Denonvilliers)间隙。以输精管为标志,将其远端在近内环口处离断,提起近端向下游离出输精管壶腹及精囊,上提精囊及输精管,显露Denonvilliers筋膜并在精囊稍下方将其打开,进入Denonvilliers间隙。④缝扎阴茎背深静脉复合体(deep dorsal vein complex,DVC)。打开盆底筋膜,2-0倒刺线缝扎DVC。⑤离断前列腺侧血管蒂。有性功能需求和原位新膀胱术行保留性神经的筋膜内前列腺切除,其他患者行筋膜外前列腺切除。⑥离断尿道。游离前列腺尖部尿道,拔除尿管,远端尿道夹闭,完整切除膀胱、前列腺、精囊腺及部分输精管。⑦淋巴结清扫。行标准淋巴结清扫,其范围上至髂总动脉分叉处,下至旋髂静脉,外至生殖股神经,内至膀胱壁。具体包括远端的髂总淋巴结,髂内、外淋巴结及闭孔淋巴结。⑧左侧输尿管从腹膜后移位至右侧。注意腹膜后通道应足够宽,保证输尿管无扭曲及成角,建议以右侧骼总动脉为标志逆行游离至腹主动脉分叉处,则可见到预先游离的左侧输尿管。用4-0可吸收线在距回肠末端20~25 cm处缝合标记回肠和双侧输尿管末端,便于从切口中拉出行尿流改道(图1)。回肠通道术具体步骤参见文献[7]。

A:游离输尿管中下段;B:游离及离断膀胱血管蒂;C:分离Denonvilliers间隙;D:结扎阴茎背深静脉丛;E:分离及离断前列腺血管蒂;F:游离及离断尿道;G:盆腔淋巴结清扫;H:4-0可吸收线标记双侧输尿管及末端回肠(左侧输尿管已从腹膜后移至右侧)(a:输精管;b:输尿管;c:脐动脉;d:精囊;e:狄氏间隙;f:结扎DVC;g:前列腺血管蒂;h:结扎尿道;i:闭孔神经;j:髂外静脉;k:髂外动脉;l:左输尿管;m:右输尿管;n:末端回肠)。图1 腹腔镜下膀胱肿瘤切除及周围淋巴结清扫
1.2.3截取肠管及构建Studer新膀胱 作脐下正中切口5~7 cm,取出标本,于标记的回肠末端截取长约55 cm带有1~2根肠系膜动脉供应血供的肠袢,恢复肠管的连续性,并关闭肠系膜缺口。保留近心输入端10 cm肠管不去管化,将余下45 cm肠段用电刀沿对系膜缘去管化,随后用3-0可吸收线连续缝合肠片后壁成U形再对折肠片前壁缝合成近似球形,前壁近心端暂不缝合;劈开输尿管末端约1.5 cm,5-0可吸收线连续黏膜对黏膜吻合输尿管和输入袢肠段末端,内置入F8单J管,最后关闭新膀胱前壁近心端(图2A)。
1.2.4新膀胱尿道吻合 回纳新膀胱至腹腔,关闭腹部正中切口,重新建立气腹。将新膀胱推入膀胱窝内,采用3-0倒刺线连续吻合新膀胱尿道周围,留置F18尿管(图2B)。
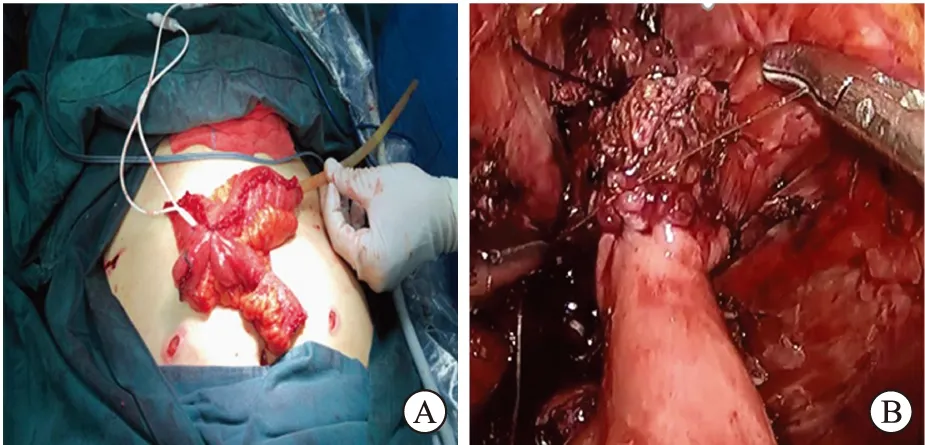
A:体外缝制Studer新膀胱;B:腹腔镜下新膀胱与尿道吻合。图2 体外新膀胱的重建和与尿道吻合
2 结 果
24例患者中男性22例,女性2例,平均年龄(68.4±5.5)岁;BMI为21.4±5.3,24例手术均获成功,无中转开放手术病例。平均气腹时间182(90~320)min,平均尿流改道时间220(72~260)min,平均术中出血量150(100~420)mL,围手术期输血2例(8.3%)。平均术后进食时间6.5(4~23)d,平均住院时间12.8(7~29)d。原位新膀胱术后1周开始膀胱训练,术后3周拔出输尿管支架管,术后4周拔除导尿管。中位随访时间8(2~34)个月,近期(<30 d)术后并发症4例,其中肠梗阻(Clavien-Dindo Ⅱ级)2例、淋巴漏(Clavien-Dindo Ⅰ级)1例,均经保守治疗治愈;1例死于心肌梗死(Clavien-Dindo Ⅴ级)。远期并发症(≥30 d)3例,左肾轻度积水1例(Clavien-Dindo Ⅰ级),随诊观察;2例急性肾盂肾炎(Clavien-Dindo Ⅰ级),经保守治疗治愈。原位膀胱癌患者膀胱充盈良好,容量均>300 mL,日间尿控均正常,2例夜间轻度尿失禁(Clavien-Dindo Ⅰ级),见图3。

A:Studer新膀胱术后3个月CT冠状面;B:Studer新膀胱术后3个月CTU。图3 术后3个月的新膀胱CT和CTU
3 讨 论
LRC+尿流改道术指征包括肌层浸润性膀胱癌(T2~4、N0~X、M0),高危复发的非肌层浸润性膀胱癌,卡介苗(bacillus calmette-guérin,BCG)治疗复发、耐药及无反应的膀胱癌和经尿道膀胱肿瘤切除术(transurethral resection of bladder tumor,TURBT)无法控制的广泛乳头状病变[8-9]。近年来的研究表明,LRC与开放手术比较不仅具有出血少、术后痛疼轻及住院时间短的优点,并在近期总体并发症方面也从开放手术的72%下降到26%[10-11]。随着腹腔镜技术的发展及成熟,这一术式近年来越来越受到术者的青睐。
我们采用LRC,总结经验如下:①以输精管为标志切开腹膜,这样有2个目的,其一是在输精管近内环口处可迅速找到脐外侧正中韧带深面的脐动脉,沿脐动脉处理膀胱侧蒂可有效阻断膀胱血供,有助于减少术中出血及降低后续操作难度。其二可沿输精管向下游离直至与精囊汇合的输精管壶腹部,可快速找到及显露精囊,在整个RC过程中,识别及良好的精囊腺显露对整个手术至关重要,是决定RC能顺利完成的关键。②缝扎DVC,我们采用2-0倒刺线,无需打结,结扎可靠并降低手术难度,尤其对DVC宽大合并骨盆狭小患者最为适应,有效控制DVC降低术中手术出血,使术野清晰,更有利于性神经保留的精准操作。③离断尿道注意无瘤技术,其一在手术开始前经尿道灌注化疗药物,可有效降低癌细胞的种植能力[12];其二,在离断尿道前我们充分游离尿道,在靠前列腺部用Hem-O-lock夹闭尿道后离断,以防止含有癌细胞的尿液外渗种植;其三,若术中发现尿道游离后宽大,估计Hem-O-lock难以闭合尿道的情况下,我们的经验是用2-0可吸收线在靠近前列腺部尿道进行缝合结扎近端尿道,这样离断后同样也可避免尿液外渗。④游离Denonvilliers间隙,该间隙是否顺利进入决定标本能否切除,我们总结有3种方法进入此间隙,其一顺行方法(最为常用),通常为精囊显露满意,以精囊为标志,在其稍下方切开Denonvilliers筋膜,钝性结合锐性分离,见到黄色脂肪证实进入该间隙层面正确。需注意的是,若太靠近精囊切开Denonvilliers筋膜则常常进入到前列腺筋膜内,此时出血较多,见不到直肠前黄色脂肪证明进入Denonvilliers间隙不正确,可继续往下方重新切开Denonvilliers筋膜进入正确层面[13];其二逆行方法,采用此方法一般膀胱肿瘤巨大或有侵犯前列腺的情况发生,精囊无法显示,此时应先游离膀胱前方,打开膀胱前间隙,游离及离断尿道后进入Denonvilliers间隙,逆行切除前列腺及膀胱;其三侧方入路法,无法顺和逆行进入时可考虑从前列腺侧方进入Denonvilliers间隙,此法要领为辨清前列腺组织轮廓切开前列腺侧蒂进入该间隙,必须保持术野清晰,否则易损伤直肠。值得注意的是,上述3种方法,若遇到复杂情况,并不是按部就班,可根据术中具体情况互相交替进行,各自弥补。
从本研究结果来看,术后肠梗阻2例,考虑是由于手术创伤或盆腹腔内炎性介质等原因引起广泛的肠壁水肿粘连和肠腔内渗出增多,从而形成机械性与动力性同时存在的一种炎性肠梗阻,据文献报道,保守治疗的有效率在87.5%~98.0%之间,而行手术解除梗阻的病例,病死率高达29.4%[14]。值得注意的是,炎性肠梗阻病程个别病例较长,本研究中有1例原位新膀胱患者,我们坚持对其实行非手术治疗(禁食、胃肠减压、全胃肠外营养、生长抑素、中药促进胃肠蠕动等综合治疗)23 d后患者腹胀消失、肛门排气及排便,进食后无肠梗阻表现而治愈。从尿流改道的方式来看,我们选择小切口辅助(脐下正中5~7 cm切口),而非完全腹腔镜,因为通过小切口取出标本后行尿流改道并不增加创伤。其次,完全腹腔镜下尿流改道术可能导致肠内容物进入腹腔,增加腹腔感染机会。最后,完全腹腔镜手术增加手术时间及手术费用[15-16]。
综上所述,LRC+小切口辅助尿流改道是一种治疗高危非肌层浸润性膀胱癌及肌层浸润性膀胱癌安全、有效的手术方法,其具有手术创伤小、出血少,术后恢复快,术后疗效确切、并发症发生较少等优点,值得临床推广应用。
