Cobas c 501和BNⅡ两种系统检测类风湿因子的性能分析*
2021-02-23王建伟谢海花孙嘉峰
王建伟,谢海花,孙嘉峰
福建省立金山医院检验科,福建福州 350008
类风湿因子(RF)是一种抗人或动物IgG分子Fc片段抗原决定簇的抗体,是以变性IgG为靶抗原的自身抗体。RF是临床诊断类风湿关节炎(RA)的重要依据之一[1-4]。RF常见的检测方法有乳胶凝集法、酶联免疫吸附试验(ELISA) 法和免疫散射比浊法等,目前临床上多采用免疫散射比浊法和免疫透射比浊法检测RF[5]。由于乳胶颗粒增强免疫技术的灵敏度较高,全自动生化分析仪功能日趋完善,而且免疫透射比浊法应用在全自动生化分析仪上的精密度高、检测速度快、消耗成本低,越来越多的实验室采用自动生化分析仪检测RF[6-8]。本研究拟对罗氏全自动生化分析仪Cobas c 501(以下简称Cobas c 501)和西门子全自动特定蛋白分析仪BNⅡ(以下简称BNⅡ)两种系统检测RF的部分性能进行分析,并探讨二者检测结果之间的相关性。
1 材料与方法
1.1标本来源 43份血清标本来自2018年6月1日至8月31日本院收治的43例患者。
1.2仪器与试剂 Cobas c 501;BNⅡ。适用于Cobas c 501的试剂:RF检测试剂盒(批号:2297701)、RF定标品(批号:28558201)、RF质控品(批号:277021/277022)来自德国罗氏诊断有限公司。适用于BNⅡ的试剂:RF检测试剂盒(批号:48274)、RF定标品(批号:18390B)来自德国西门子医学诊断产品(上海)有限公司;液体免疫学和蛋白质控品(批号:66372/66373)购自美国伯乐生命医学产品(上海)有限公司。
1.3检测方法 各项操作均严格按照试剂盒说明书进行,相应质控品、标准品均与标本同时检测,均符合试剂盒质控要求。
1.3.1检测原理 BNⅡ检测RF:采用免疫散射比浊法进行检测,当包被由人-γ-球蛋白/绵羊抗人-γ-球蛋白组成的免疫复合物的聚苯乙烯颗粒与含有RF的标本混合时,这些颗粒会凝集起来,光线通过悬浊液发生散射,散射光的强度与标本中相关蛋白水平呈正比,与已知的标准水平对比可得出结果。Cobas c 501检测RF:采用免疫散射比浊法进行检测,结合有热灭活IgG的乳胶与标本中RF-抗体发生凝集反应形成抗原抗体复合物。
1.3.2精密度评价 按照美国临床和实验室标准化协会(CLSI)EP15-A2标准:2个水平,5 d试验,每天一批,每批每个水平重复检测3次。
1.3.3正确度评价 根据《临床化学定量检验程序性能验证指南》(CNAS-GL037),实验室可采用偏倚评估、回收试验、与参考方法比对等方式进行正确度的验证。本研究通过偏倚评估进行正确度的验证:对2017、2018年中华人民共和国国家卫生和计划生育委员会临床检验中心和福建省临床检验中心提供的室间质评质控品20份进行检测,比较回报靶值和实验室检测结果,计算偏倚及平均偏倚。 偏倚(%)=[检测值-参照值(靶值)]/参照值(靶值)×100%,平均偏倚(%)=[偏倚(绝对值)/数据个数]×100% 。 如果平均偏倚小于1/2 PT(生物学变异与分析质量要求允许总误差10%),说明该检测系统的正确度在允许的误差范围内。
1.3.4相关性评价 对本院检验科免疫室2018年6月1日至8月31日收到的43份检测RF的标本同时采用Cobas c 501和BNⅡ进行检测,将结果进行相关性分析。
1.4统计学处理 采用SPSS20.0统计软件及Excel2019统计软件进行数据处理及统计分析。检测结果小于检测下限的结果归化为1。
2 结 果
2.1精密度验证 采用Cobas c 501检测RF,其批内精密度(低、高水平)均<1/4TEa,批间精密度(低、高水平)均<1/3TEa,见表1。采用BNⅡ检测RF,其批内精密度(低、高水平)均<1/4TEa,批间精密度(低、高水平)均<1/3TEa。见表2。

表1 Cobas c 501精密度验证结果

表2 BNⅡ精密度验证结果
2.2正确度验证 采用Cobas c 501检测RF的正确度验证结果,平均偏倚为3.67%,小于1/2 PT,该检测系统的正确度在允许的误差范围内。采用BNⅡ检测RF的正确度验证结果,平均偏倚为4.46%,小于1/2 PT,该检测系统的正确度在允许的误差范围内。
2.3两种方法检测结果的相关性分析 以采用Cobas c 501检测的结果为X轴,以采用BNⅡ检测的结果为Y轴,分析结果显示二者具有良好的相关性(Y=1.057 9X+0.526,R2=0.990 6),见图1。
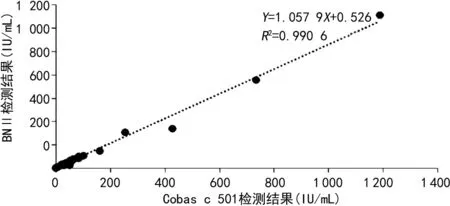
图1 两种检测系统检测结果相关性分析
3 讨 论
RF无明显的种属特异性,是由感染因子刺激机体产生的一种自身抗体,以变性IgG为抗原。RF主要存在于RA及某些风湿免疫性疾病患者的血清和关节液中,RF有IgG、IgM、IgA、IgD和IgE等5种抗原[9-12]。当前临床检验技术不断发展,RF的检测出现了许多新的方法,其中全自动生化分析仪检测越来越受到临床实验室的青睐。全自动生化分析仪功能日趋完善,而且具有自动化程度高、检测速度快、消耗成本低等特点。
本研究严格按照CLSI文件中的要求对两台仪器的精密度、正确度进行验证。结果显示两台仪器的低、高水平批内精密度均<1/4TEa(实验室允许不精密度为6.25%),批间精密度均<1/3TEa(实验室允许不精密度为8.33%)。正确度验证结果显示,采用Cobas c 501和BNⅡ两种系统的平均偏倚分别为3.67%、4.46%,正确度均较高。同时,本研究对相同标本同时在两种系统上的检测结果进行相关性分析,结果显示两种检测系统相关性良好。实际工作中发现,BNⅡ配套RF试剂开瓶后稳定时间较短,当天开瓶试剂未使用完,待后面检测时,对检测结果影响较大,易出现室内质控失控现象。
综上所述,Cobas c 501和BNⅡ均适用于临床进行RF的检测,然而BNⅡ试剂开瓶后稳定性时间较短,更适用于标本量较大的实验室;Cobas c 501上机稳定时间较长,适用于标本量较少的实验室。