《AHA冠状动脉非阻塞性心肌梗死诊断和管理科学声明》解读
2021-02-23李祎铭姜厚望李海燕张玲霞王云潇王相宝
李祎铭,姜厚望,李海燕,张玲霞,王云潇,王相宝,王 显
冠状动脉非阻塞性心肌梗死(myocardial infarction in the absence of obstructive coronary artery disease,MINOCA)治疗和管理与冠状动脉阻塞性急性心肌梗死(acute myocardial infarction with obstructive coronary artery disease,AMI-CAD)截然不同,许多心脏中心的治疗尚不规范。目前,我国尚无相关管理指南。2016年,欧洲心脏病协会(European Society of Cardiology,ESC)首先制定了MINOCA诊疗建议[1]。2019年,美国心脏协会(American Heart Association,AHA)发布了《AHA冠状动脉非阻塞性心肌梗死诊断和管理科学声明》[2],纳入了近年来的最新研究证据,为MINOCA的临床诊断和管理提供参考。
1 流行病学
接受冠状动脉造影的急性心肌梗死(acute myocardial infarction,AMI)病人MINOCA的发病率为5%~6%[3],在不同的人群中,MINOCA的发病率为5%~15%[4-5]。在人口统计学分布方面,MINOCA病人的平均年龄更小、女性占比更高[6],MINOCA病人较少具有传统的冠心病危险因素,如血脂异常、高血压、糖尿病、吸烟、冠心病家族史等[7]。
2 定义与诊断
2016年,ESC在国际上首次提出了MINOCA诊断标准:①AMI符合《第三版心肌梗死全球定义》;②符合现有冠状动脉造影指南非阻塞性冠状动脉的定义,即主要心外膜血管不存在>50%的狭窄;③没有任何明显的其他原因可导致病人出现目前的临床表现。但是,2018年发布的《第四版心肌梗死全球定义》改变了AMI诊断标准,即缺血因素导致的心肌损伤才能诊断为AMI。因此,根据这一定义AHA提出了新的MINOCA诊断原则,即缺血因素导致的心肌损伤,且无明显阻塞冠状动脉的病人才能被诊断为MINOCA。在做出MINOCA诊断之前,需排除以下几种情况:①其他临床疾病导致的肌钙蛋白升高(如脓毒血症、肺栓塞等);②临床上被忽略的冠状动脉阻塞性疾病(如由于斑块破裂或血栓栓塞导致的细小冠状动脉分支完全闭塞,或被忽略的冠状动脉远端狭窄>50%等);③临床上造成类似于AMI心肌损伤的隐匿非缺血性机制(如心肌炎等)。另外,由于斑块负荷较重的病人相对预后较差[8],根据造影结果将病人分为3组:正常冠状动脉(造影未见狭窄)、轻微冠状动脉管腔不规则(造影可见狭窄<30%)、中等程度的冠状动脉粥样硬化病变(30%<狭窄<50%)。鉴于部分冠状动脉狭窄30%~50%的病人实际上会出现有临床意义的功能性冠状动脉狭窄,因此,行冠状动脉血流储备分数(fractional flow reserve,FFR)检查的病人,FFR>0.8方能诊断为MINOCA。
AHA提出的MINOCA诊断标准:①急性心肌梗死(修改自《第四版心肌梗死全球定义》指定的标准)时,肌钙蛋白动态演变且至少1次>参考值上限99个百分位,且明确的至少有一种如下梗死临床证据:a)心肌缺血症状;b)新发的缺血性心电图改变;c)出现病理性Q波;d)经过影像学检查证实的缺血原因导致的存活心肌减少或新发室壁运动异常;e)造影或尸检证实存在冠状动脉内血栓。②造影证实冠状动脉呈非阻塞性病变,定义为造影显示主要心外膜血管无阻塞性病变(即无任何一条主要冠状动脉狭窄>50%)包括如下几类病人,即a)正常冠状动脉(造影未见狭窄);b)轻微冠状动脉管腔不规则(造影可见狭窄<30%);c)中等程度的冠状动脉粥样硬化病变(30%<狭窄<50%)。③对于目前的病情没有其他可替代的诊断,可替代的诊断包括但不限于例如脓毒血症、肺血栓栓塞症或心肌炎等非缺血性病因。
MINOCA的诊断流程相对于AMI-CAD较为复杂(见图1)[2]:①对于没有阻塞性冠心病的AMI病人,首先应该考虑可能会引起心肌损伤这一临床并发症的其他疾病,在医生对病人的临床资料进行谨慎的分析后,往往就能避免将非缺血因素导致的心肌损伤误诊为AMI;②如果经过上述过程后还能维持AMI的临床诊断,那么临床医生应该通过复习病人的造影结果防止在首次阅片过程中被忽略的冠状动脉阻塞,并考虑通过进一步的影像学检查排除临床上易被混淆的非缺血机制导致的心肌损伤,在这一步中,推荐进行心脏磁共振检查(cardiac magnetic resonance imaging,CMRI),CMRI除了可以排除心肌炎、应激性心肌病(takotsubo syndrome)和其他原发性心肌病等疾病外,可以对AMI进行确诊;③在排除了上述疾病后,可做出MINOCA的临床诊断,对于大的心脏中心,在做出MINOCA的诊断后还可进行进一步的检查以明确MINOCA的病因。需要注意的是,对于MINOCA诊断并不能够总是按照本流程图推荐的顺序进行,例如某些心脏中心可能不具有CMRI条件,在临床应用中需根据各中心的客观实际进行调整。
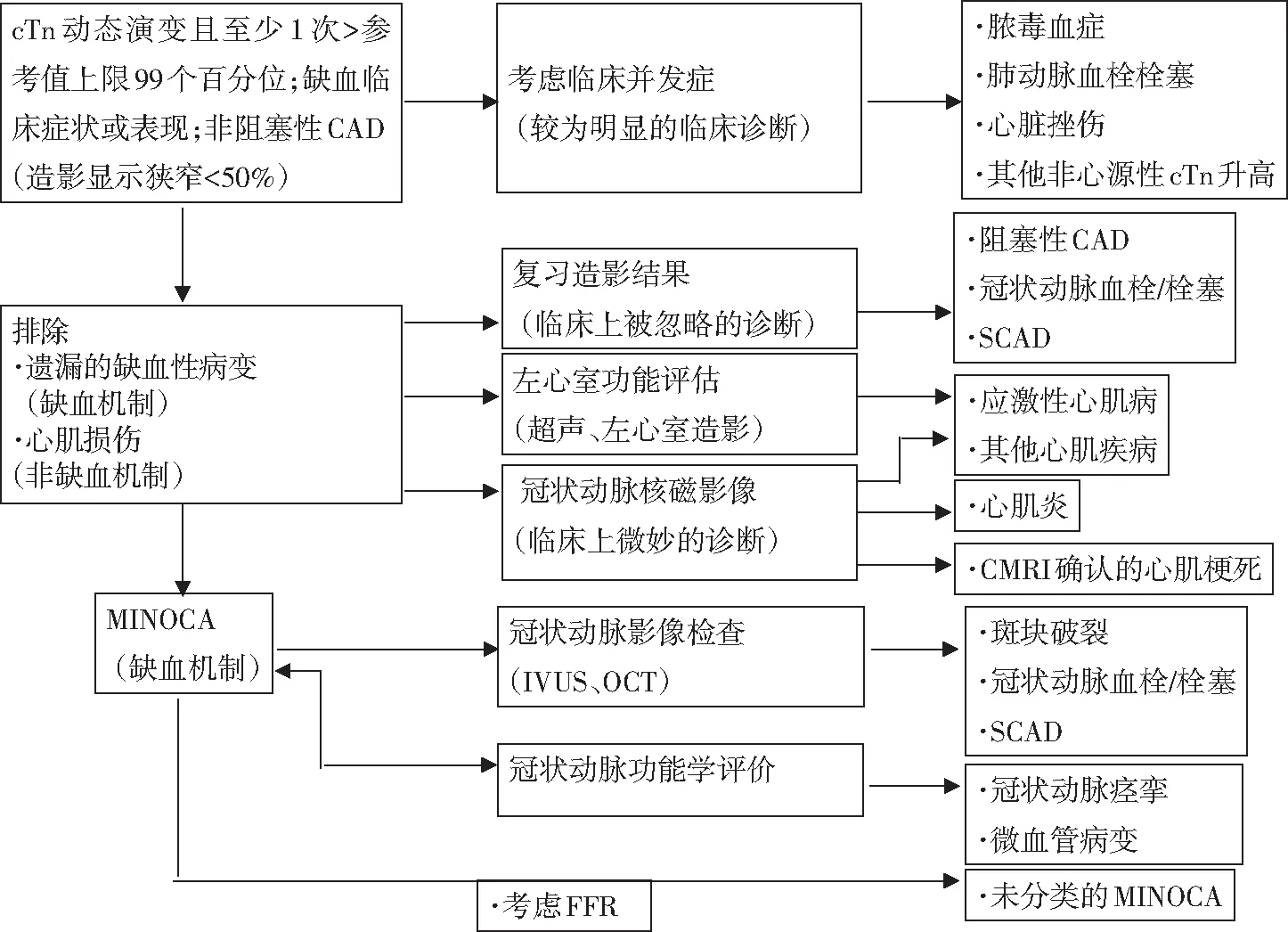
图1 MINOCA诊断流程图[CAD为冠状动脉粥样硬化性心脏病;cTn为肌钙蛋白;IVUS为血管内超声;OCT为光学相干断层成像;SCAD为自发性冠状动脉夹层。资料来源:TAMIS-HOLLAND J E,JNEID H,REYNOLDS H R,et al.Circulation,2019,139(18):e891-e908]
3 病 因
MINOCA的病因主要分为冠状动脉粥样硬化因素造成的心肌坏死(如斑块破裂)和非冠状动脉粥样硬化因素造成的心肌坏死(如心外膜冠状动脉痉挛、冠状动脉微血管功能障碍、冠状动脉血栓/栓塞、自发性冠状动脉夹层、心肌氧供需失衡等)。
3.1 斑块破裂 斑块破裂包括了斑块破裂、侵蚀和钙化结节,约有37%的MINOCA病人表现为斑块破裂[9]。斑块破裂可引起冠状动脉内血栓形成,栓子脱落栓塞冠状动脉远端,同时冠状动脉痉挛造成AMI;而在另一些病人中则表现为暂时性的冠状动脉完全被血栓阻塞,随后出现自发性的血栓溶解。造影表现为冠状动脉影像模糊或充盈缺损,确诊斑块破裂需要腔内影像学技术如OCT或IVUS。
3.2 心外膜冠状动脉痉挛 心外膜冠状动脉痉挛是指造成冠状动脉血流减少的强烈血管收缩(>90%)。自发性冠状动脉血管紧张度调节功能障碍,或药物或毒物(如可卡因)造成的冠状动脉平滑肌高反应性都可造成冠状动脉痉挛。短时间的冠状动脉痉挛可造成静息型心绞痛,长时间的冠状动脉痉挛则会造成MINOCA。冠状动脉激发试验对于诊断冠状动脉痉挛非常重要,在接受该试验的MINOCA病人中,46%出现了冠状动脉痉挛[10],亚洲人群出现冠状动脉痉挛的比例更高[11]。目前,推荐冠状动脉内高剂量乙酰胆碱弹丸式注射(5 mL含20~100 μg乙酰胆碱的溶液于20 s内冠状动脉内注射)作为冠状动脉激发试验的最佳方案[12]。
3.3 冠状动脉微血管功能障碍 虽然在传统冠状动脉造影中无法评价冠状动脉微循环(血管直径<0.5 mm),但是冠状动脉微循环提供了大约70%的冠状动脉血流阻力[13]。冠状动脉微血管功能障碍可通过内皮依赖性或非内皮依赖性机制成为MINOCA的潜在病因。同时具有缺血性胸痛、非阻塞性冠状动脉和冠状动脉血流受阻的病人可被诊断为微血管性心绞痛[14]。满足下列条件之一即可认为冠状动脉血流受阻:①使用如腺苷等血管舒张药后冠状动脉血流储备(coronary flow reserve,CFR)<2.0;②乙酰胆碱激发试验过程中病人出现胸部不适和缺血性心电图改变,且未出现心外膜冠状动脉痉挛,可诊断为冠状动脉微血管痉挛;③经过校正的TIMI血流分级评价,冠状动脉血流受阻。冠状动脉微血管功能障碍在女性病人和伴有心血管危险因素的病人中更为常见。需要注意的是,冠状动脉微循环功能障碍既可以是AMI的病因,也可能是AMI的并发症,因此,MINOCA与冠状动脉微循环障碍的关系尚待进一步研究。
3.4 冠状动脉血栓/栓塞 冠状动脉血栓或栓塞影响冠状动脉微循环,或心外膜冠状动脉血栓部分溶解表现为非阻塞性病变,都可以成为MINOCA的病因。遗传性或获得性的高凝状态都可以导致冠状动脉内血栓形成。获得性高凝状态包括血栓形成性血小板减少性紫癜(thrombotic thrombocytopenic purpura,TTP)、抗磷脂综合征、肝素诱导性血小板减少症(heparin-induced thrombocytopenia,HIT)和骨髓增殖性肿瘤,对于这类病人的诊断需要与血液科和风湿免疫科等学科密切合作。
3.5 自发性冠状动脉夹层 自发性冠状动脉夹层(spontaneous coronary artery dissection,SCAD)是非动脉粥样硬化因素导致的AMI罕见病因,但是在50岁以下女性AMI病人中较为常见[15]。虽然大部分的SCAD病人表现为阻塞性病变,但也有部分SCAD病人因冠状动脉直径逐渐变细,表现为冠状动脉正常或接近正常,因此,SCAD是MINOCA的可能原因。SCAD病人冠状动脉中外膜分离,壁内血肿突入冠状动脉管腔,造成血流受阻。精神紧张、剧烈运动和拟交感药物等引起儿茶酚胺分泌过多,可诱导潜在的血管病变恶化,出现SCAD[16]。由于分辨率较高,推荐使用OCT对疑诊为SCAD的MINOCA病人进行诊断[17]。
3.6 心肌氧供需失衡 由心肌氧供需失衡导致的MINOCA包含于《第四版心肌梗死全球定义》中缺血事件引起的心肌梗死范围内。冠状动脉痉挛、冠状动脉血栓栓塞和导致氧供需失衡的系统性疾病,如快速性心律失常、贫血、低血压、甲状腺功能亢进等均可能成为其潜在病因。与快速性心律失常有关的AMI在临床上较为常见[18],然而鉴别快速性心律失常是MINOCA的原因或是结果较为困难。对于这类病人的MINOCA诊断应该极为慎重,在缺乏临床、造影和冠状动脉腔内影像学证据支持的诊断其他类型AMI的情况下,方可做出诊断。
4 管理策略
目前尚无前瞻性随机对照试验对MINOCA管理提供指导,其他相关文献意义也较为有限。专家组为MINOCA的治疗拟定了下列基本原则:急诊支持治疗;对于病人的评估和诊断在整个救治流程中持续进行;无论病人的MINOCA为何种原因,均进行心肌保护治疗;针对病因进行治疗。
4.1 急诊支持治疗 由于发病机制不同,无法对MINOCA病人进行再血管化治疗以稳定病情。因此,临床医师需要考虑MINOCA的可能病因和病人的临床表现,迅速处理恶性心律失常或心源性休克等事件。
4.2 持续的诊断和评估 对于MINOCA病人病因和病情的诊断评估应该贯穿整个治疗过程,这主要包括两个方面:排除其他类似于AMI的疾病;识别MINOCA的病因。这一步骤可依照MINOCA诊断流程图进行(见图1)。
4.3 心肌保护治疗 AMI-CAD病人需要进行心血管病二级预防,包括药物治疗[双联抗血小板聚集治疗、他汀类、血管紧张素转换酶抑制剂(ACEI)/血管紧张素Ⅱ受体拮抗剂(ARB)、β受体阻滞剂]、控制危险因素和心脏康复。这些治疗主要针对动脉粥样硬化性心血管疾病,但是MINOCA病人动脉粥样硬化负荷较小,因此,传统心血管病二级预防治疗应根据MINOCA病人的具体病因进行选择,例如对于斑块破裂的MINOCA病人强烈推荐抗血小板聚集治疗,对于冠状动脉痉挛的病人β受体阻滞剂则是禁忌。既往针对SWEDENHEART注册的数据分析显示,MINOCA病人使用二级预防药物(除抗血小板聚集药物外)可能获益[5]。
4.4 病因治疗
4.4.1 斑块破裂 由于发病机制的原因,对于斑块破裂的病人使用阿司匹林抗血小板治疗是合理的。对未区分病人冠状动脉是否阻塞的AMI病人使用P2Y12受体拮抗剂效果良好[19],因此,可以考虑在MINOCA病人中使用双联抗血小板聚集治疗。不推荐对这类病人常规置入支架治疗。
4.4.2 心外膜冠状动脉痉挛 钙离子阻断剂可以缓解冠状动脉痉挛病人的心绞痛症状,不使用钙离子阻断剂是血管痉挛性心绞痛病人发生心血管事件的独立危险因素[20]。长效硝酸酯类药物对这类病人的疗效并不明显[12]。
4.4.3 冠状动脉微血管病变 钙离子阻断剂和β受体阻滞剂可以缓解这类病人的临床症状,硝酸酯类药物疗效较差[13]。一些小样本随机对照试验显示,改善内皮功能药物(如他汀类[21]、依那普利[22])、扩张微血管药物(如双嘧达莫[23])、内脏解痉药物(如氨茶碱[24])可能有效。
4.4.4 冠状动脉血栓/栓塞 对于这类病人终生使用抗凝药或抗血小板聚集药有待进一步分析讨论,特定病因的冠状动脉血栓/栓塞病人需要特殊治疗,例如血小板减少症(HIT)病人需要避免再次使用肝素。其他血液系统疾病则需要血液病学专家会诊。
4.4.5 自发性冠状动脉夹层 急性期应避免对SCAD病人行介入治疗,因为介入治疗可能造成夹层或壁内血肿范围扩大。药物治疗方面,使用阿司匹林和β受体阻滞剂可能是合理的,观察性研究发现β受体阻滞剂可降低临床风险[15],抗凝药和双联抗血小板聚集治疗尚有争议。
4.4.6 心肌氧供需失衡 主要需针对造成心肌氧供需失衡情况的病因进行治疗,其他药物需根据病人临床状况选用。
5 预 后
MINOCA的预后取决于其潜在病因,大部分研究显示MINOCA相对AMI-CAD预后较好[4,25],但是也有一些研究表明MINOCA病人预后并不优于AMI-CAD病人[7]。MINOCA病人心血管事件发生率高于普通人群[26],而与AMI-CAD病人相近[27]。MINOCA病人与AMI-CAD病人院内死亡危险因素相同(年龄、cTn水平较高、肾功能不全、心率、血压、外周动脉疾病)[28],其院内死亡率约为1%。
6 结 论
多种病理生理学机制可能造成MINOCA的发生,对MINOCA的正确认识、诊断和管理至关重要。缺血原因导致的,无冠状动脉阻塞证据的AMI可诊断为MINOCA。对于MINOCA病人需针对病因采取个性化治疗,从而改善病人预后。
