LC-MS-MS法测定人血浆中阿托伐他汀、邻位阿托伐他汀和对位阿托伐他汀的浓度
2021-02-16易志恒李筱旻申秋莹潘琳王珊向圆圆李岱戴伊歆徐素梅中南大学长沙41008湖南迪诺制药股份有限公司长沙4101中南大学湘雅医院期临床试验研究中心长沙410008国家老年疾病临床医学研究中心湘雅长沙410008
易志恒,李筱旻,申秋莹,潘琳,王珊,向圆圆,李岱,戴伊歆,徐素梅*(1.中南大学,长沙 41008;. 湖南迪诺制药股份有限公司,长沙 4101;. 中南大学湘雅医院Ⅰ期临床试验研究中心,长沙 410008;4. 国家老年疾病临床医学研究中心(湘雅),长沙 410008)
阿托伐他汀(atorvastatin,AT)是一种选择性3-羟基-3-甲基戊二酰辅酶A(HMG-CoA)还原酶抑制剂,其主要作用机制是通过抑制HMGCoA 还原酶,减少胆固醇和脂蛋白的前体物质甲羟戊酸的形成,从而显著降低胆固醇、低密度脂蛋白及三酰甘油水平[1]。同时,阿托伐他汀还具有降低血小板活化和聚集的作用,临床常用于高脂血症的治疗和心脑血管疾病的防治[2-4]。
阿托伐他汀有明显的首过效应,主要由肝脏的CYP3A4 酶代谢成邻位羟基代谢物(orthohydroxy atorvastatin,o-AT)和对位羟基代谢物(para-hydroxy atorvastatin,p-AT),两者的药理活性与阿托伐他汀相当[5]。而阿托伐他汀、o-AT、p-AT 又可动态转化成相应的非活性内酯衍生物[6]。因此,阿托伐他汀及其活性代谢产物o-AT和p-AT 的血浆浓度低,对其药代动力学研究提出了挑战[7]。目前已报道多种分析方法可用于单独测定阿托伐他汀,或同时测定阿托伐他汀及其活性代谢物,如GC-MS、LC-MS/MS[8-14],但有前处理繁琐、灵敏度较低或分析时间长等缺陷。
本研究旨在建立一种快速、灵敏、准确、操作简便的HPLC-MS/MS 法,同时测定阿托伐他汀、o-AT、p-AT,以满足药代动力学研究的需要。
1 材料
1.1 仪器
低温离心机(TDL5M,盐城凯特);HPLC系统(ExionLC);串联四极杆质谱(AB Sciex Triple Quad5500);数据采集和处理硬件(Analyst 1.6.3,AB Sciex)。
1.2 试药
阿托伐他汀(批号:8-SCC-42-1,含量:96.0%)、邻位阿托伐他汀(批号:13-AUG-16-37,含量:94.8%)、对位阿托伐他汀(批号:13-AUG-16-36,含量:96.1%);阿托伐他汀-d5(批号:2-OMK-4-1,含量:96.0%)、邻位阿托伐他汀-d5(批号:39-GHZ-67-1,含量:94.0%)、对位阿托伐他汀-d5(批号:39-GHZ-67-1,含量:95.0%)(对照品,Quality Control Chemicals Inc)。
甲酸(HPLC 级,ROE);甲醇、乙酸乙酯、乙腈(HPLC 级,Burdick & Jackson); 甲基叔丁基醚(HPLC 级,J.T. Baker);水(HPLC 级,DUKSAN);乙酸铵(分析纯,国药集团化学试剂有限公司)。
2 方法
2.1 色谱条件
色谱柱:Zorbax SB-C18(2.1 mm×150 mm,5 μm,Agilent); 流动相A:5 mmol·L-1的乙酸铵(含0.1%甲酸的水溶液),流动相B:5 mmol·L-1的乙酸铵(含0.1%甲酸的甲醇溶液);柱温:40℃;自动进样器温度:5℃;进样体积:30.0 μL。
2.2 质谱条件
ESI+方式进行离子监测;源喷射电压:5500.00 V;源温度:550℃;离子源气体1:35 psi;离子源气体2:35 psi;碰撞气:4.0 psi;气帘气:20 psi;阿托伐他汀、邻位阿托伐他汀、对位阿托伐他汀、阿托伐他汀-d5、邻位阿托伐他汀-d5、对位阿托伐他汀-d5在ESI+源电离方式下主要生成[M +H]+峰分别为m/z559.5、575.20、575.40、564.50、580.3 和580.2,以此离子作为母离子,对母离子进行碰撞碎裂,碎裂后子离子分别为m/z440.3、440.4、440.30、445.40、445.40 和445.60。阿托伐他汀、邻位阿托伐他汀、对位阿托伐他汀、阿托伐他汀-d5、邻位阿托伐他汀-d5、对位阿托伐他汀-d5的碰撞能量均为34 eV,去簇电压分别为103 eV、100 eV、100 eV、121 eV、100 eV、112 eV。
2.3 对照品溶液的配制
称量约1.00 mg 阿托伐他汀钙、邻位阿托伐他汀、对位阿托伐他汀(对位阿托伐他汀按校正系数来计算实际质量,不同来源对照品的校正系数可能不同),转移至20 mL 聚丙烯闪烁瓶中,以适量50%甲醇溶解,得到质量浓度为100 μg·mL-1的阿托伐他汀钙,邻位阿托伐他汀,对位阿托伐他汀溶液(约10.0 mL)。置于-80℃冰箱保存。
以50%甲醇稀释配制以下质量浓度的阿托伐他汀、邻位阿托伐他汀、对位阿托伐他汀标准系列溶液(1.00、2.00、5.00、20.00、40.00、100.00、200.00、300.00 和400.00 ng·mL-1)。
2.4 内标溶液的配制
分别称量约1.00 mg 阿托伐他汀-d5、邻位阿托伐他汀-d5、对位阿托伐他汀-d5,经校正后计算实际质量(不同来源标准品的校正系数可能不同)。转移至20 mL 聚丙烯闪烁瓶,以适量50%甲醇溶解,得到质量浓度为100 μg·mL-1的阿托伐他汀-d5、邻位阿托伐他汀-d5、对位阿托伐他汀-d5储备液(约10.0 mL)。放置于-80℃冰箱保存。
取100 μL 储备液,用50%甲醇配得1.00 μg/mL 的中间工作溶液。放置于-80℃冰箱保存。
用加样器转移1.00 mL 1.00 μg·mL-1的中间工作溶液至装有9.00 mL 50%甲醇稀释液的20 mL 聚丙烯闪烁瓶,混匀后得到100 ng·mL-1的工作溶液。放置于-80℃冰箱保存。
2.5 样品制备方法
取血浆样品200 μL 至玻璃小管内,加入10 μL 100 ng·mL-1内标工作溶液,加入200 μL 6 mol·L-1的乙酸铵水溶液,10.0 μL 50%甲醇,再加入1.00 mL 甲基叔丁基醚和1.00 mL 乙酸乙酯,机械震荡5 min,离心(4000 r·min-1)3 min 后,放于-80℃冰箱冷冻水层,将上层有机层液体倒入标记的玻璃管中,用氮吹仪在40℃(氮气压力10 ~15 psi)吹干,再加入200 μL 6 mol·L-1的乙酸铵水溶液重新溶解样品,涡旋混匀,将样品转至2.0 mL 聚丙烯小管中,高速离心2 min,转移上层澄清样品溶液至进样小瓶,30 μL 进样,LC-MS-MS 法进行分析。
3 结果
3.1 方法专属性
分别制备空白血浆、空白血浆加阿托伐他汀、邻位阿托伐他汀、对位阿托伐他汀和内标的血浆样品,进行LC-MS-MS 分析,获得色谱图(见图1)。在本实验条件下,所有空白样品均未见干扰峰,各成分均有效分离。
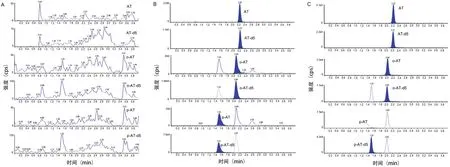
图1 血浆中阿托伐他汀、邻位阿托伐他汀、对位阿托伐他汀及其内标的色谱图Fig 1 Chromatogram of atorvastatin,ortho-hydroxy atorvastatin and para-hydroxy atorvastatin and its internal standard in human plasma
3.2 线性范围及定量下限(LLOQ)
取标准系列溶液10 μL,加入空白血浆190 μL,配制系列浓度血浆样品,按“2.7”项下操作,配制质量浓度为0.050、0.100、0.250、1.00、2.00、5.00、10.0、15.0 和20.0 ng·mL-1的阿托伐他汀、邻位阿托伐他汀、对位阿托伐他汀系列标准溶液,每一浓度进行3 样本处理分析,以待测物质量浓度为横坐标,待测物与内标的峰面积比值为纵坐标。采用加权最小二乘法(权重因子1/χ2)进行线性回归,结果阿托伐他汀、邻位阿托伐他汀、对位阿托伐他汀的回归方程分别为Y=1.230X+7.35×10-5(r=0.996),Y=0.604X+4.12×10-4(r=0.997),Y=1.400X+4.92×10-4(r=0.997),线性范围均为0.05~20.0 ng·mL-1。三者的LLOQ 均为0.05 ng·mL-1。
3.3 准确度和精密度
配制定量下限、低、中、高4 种浓度质控样品(阿托伐他汀,邻位阿托伐他汀,对位阿托伐他汀血浆浓度分别为0.050、0.150、1.50 和16.0 ng·mL-1)各6 份,测定日内准确度和精密度;另配制阿托伐他汀,邻位阿托伐他汀,对位阿托伐他汀血浆浓度分别为0.050、0.150、1.50 和16.0 ng·mL-1的质控样品,每一浓度进行6 样本分析,连续测定3 个分析批,分别计算阿托伐他汀,邻位阿托伐他汀,对位阿托伐他汀的日间准确度及精密度,准确度均在80%~120%,RSD均小于15%。
3.4 提取回收率
取空白血浆,制备血浆质量浓度分别为0.150、1.50 和16.0 ng·mL-1的阿托伐他汀,邻位阿托伐他汀,对位阿托伐他汀质控样品,按“2.5”项下操作,每一浓度进行6 样本分析,获得相应的峰面积;空白基质提取后用质量浓度为0.150、1.50 和16.0 ng·mL-1的阿托伐他汀,邻位阿托伐他汀,对位阿托伐他汀的纯溶液复溶样品,测定峰面积。分析批中质控样品的峰面积除以相应浓度的空白样品提取液加入纯溶液峰面积用来计算各质控样品的回收率。阿托伐他汀,邻位阿托伐他汀和对位阿托伐他汀的提取回收率分别为64.3%~67.0%(RSD为3.94%~13.20%),78.3%~100.0%(RSD为8.9% ~19.80%),64.3% ~71.4%(RSD为4.30%~6.0%)。
3.5 基质效应
取血浆样品200 μL 至玻璃小管内,处理后进样分析,每一浓度进行6 样本分析;另取相同浓度的标准溶液20 μL 和内标溶液50 μL,涡旋混匀,氮气吹干,加入200 μL 流动相溶解,涡旋震荡3 min,13 000 r·min-1离心5 min,30 μL 进样分析。
对于每批基质,通过计算基质存在下的峰面积与不含基质的相应峰面积比值,计算阿托伐他汀、邻位阿托伐他汀、对位阿托伐他汀和内标的基质因子(MF)和内标归一化基质因子(ISnormalised MF),结果见表1。

表1 LC-MS/MS 法测定人血浆中阿托伐他汀,邻位阿托伐他汀及对位阿托伐他汀的基质效应(n =6)Tab 1 Matrix effects of LC-MS-MS method for determination of atorvastatin,ortho-hydroxy atorvastatin,para-hydroxy atorvastatin in human plasma (n =6)
3.6 样品稳定性试验
配制质量浓度为0.150、16.0 ng·mL-1的阿托伐他汀,邻位阿托伐他汀,对位阿托伐他汀质控样品,分别考察待测物在下述条件下的稳定性:① 冻融稳定性;② 生物样品前处理过程中的稳定性(室温储存25 h);③ 生物基质中待测物的长期稳定性(-80℃冷冻储存288 d);④重新进样稳定性。结果见表2。

表2 LC-MS/MS 法测定血浆中阿托伐他汀,邻位阿托伐他汀及对位阿托伐他汀样品稳定性(x±CV,%)Tab 2 Stability of LC-MS-MS method for determination of atorvastatin,ortho-hydroxy atorvastatin,para-hydroxy atorvastatin in human plasma (x ±CV,%)
3.7 临床应用
本文所建立的阿托伐他汀及代谢物血药浓度测试方法已成功应用于阿托伐他汀钙片在中国健康受试者中的生物等效性研究。本研究分为两部分:空腹服药试验和餐后服药试验,各纳入32 例受试者。每部分均采用随机、开放、两制剂、四周期、全重复试验设计。于每周期给药前10 ~40 min 和给药后0.25、0.5、0.75、1、1.5、2、3、4、6、8、12、24、48、72 h 采集受试者上肢静脉血,每次采血约4 mL 至含有肝素钠负压真空采血管中,4℃以3500 r·min-1离心10 min,分离血浆,测定阿托伐他汀、邻位阿托伐他汀和对位阿托伐他汀的浓度。空腹和餐后口服单剂量药物后阿托伐他汀及代谢物的主要药代动力学参数分别见表3 和表4。
表3 空腹口服受试制剂或参比制剂后阿托伐他汀,邻位阿托伐他汀及对位阿托伐他汀的药代动力学参数( ±s)Tab 3 Mean pharmacokinetics parameters of atorvaststin,ortho-hydroxy atorvaststin and para-hydroxy atorvaststin after the administration reference and test products under fasting condition ( ±s)

表3 空腹口服受试制剂或参比制剂后阿托伐他汀,邻位阿托伐他汀及对位阿托伐他汀的药代动力学参数( ±s)Tab 3 Mean pharmacokinetics parameters of atorvaststin,ortho-hydroxy atorvaststin and para-hydroxy atorvaststin after the administration reference and test products under fasting condition ( ±s)
参数阿托伐他汀邻位阿托伐他汀对位阿托伐他汀受试制剂参比制剂受试制剂参比制剂受试制剂参比制剂tmax/h0.50(0.25,3.00)0.50(0.25,4.00) 0.75(0.50,8.00)1.00(0.50,6.00) 1.50(0.25,24.00)2.00(0.25,24.00)Cmax/(ng·mL-1)16.09±7.5913.81±6.9914.26±6.1012.82±5.84 0.41±0.19 0.40±0.22 AUC0 ~t/(ng·h·mL-1) 63.03±32.12 65.08±31.58120.81±39.94125.04±41.3910.04±6.2110.70±6.54 AUC0 ~∞/(ng·h·mL-1) 64.60±32.09 66.41±31.68123.44±38.61126.70±41.3713.73±6.4114.98±7.73 t1/2/h 9.44±2.98 9.62±2.8410.91±2.6110.65±2.43 30.67±16.69 33.24±34.72
表4 餐后口服受试制剂或参比制剂后阿托伐他汀,邻位阿托伐他汀及对位阿托伐他汀的药代动力学参数( ±s)Tab 4 Mean pharmacokinetics parameters of atorvaststin,ortho-hydroxy atorvaststin and para-hydroxy atorvaststin after the administration reference and test products under fed condition ( ±s)

表4 餐后口服受试制剂或参比制剂后阿托伐他汀,邻位阿托伐他汀及对位阿托伐他汀的药代动力学参数( ±s)Tab 4 Mean pharmacokinetics parameters of atorvaststin,ortho-hydroxy atorvaststin and para-hydroxy atorvaststin after the administration reference and test products under fed condition ( ±s)
注(Note):tmax 以中位数(最小值,最大值)表示[tmax is expressed with median(minimum, maximum)]。
参数阿托伐他汀邻位阿托伐他汀对位阿托伐他汀受试制剂参比制剂受试制剂参比制剂受试制剂参比制剂tmax/h2.00(0.50,6.00)1.50(0.50,6.00) 6.00(0.50,12.00)6.00(0.75,12.00) 8.00(4.00,24.00)8.00(3.00,12.00)Cmax/(ng·mL-1) 7.81±3.30 8.28±5.00 94.56±27.32 98.12±41.39 8.95±3.42 9.05±4.45 AUC0 ~t/(ng·h·mL-1) 61.90±17.23 61.90±17.23 96.55±27.45 100.03±41.7413.03±4.2213.11±5.41 AUC0 ~∞/(ng·h·mL-1) 63.34±17.27 65.57±27.36 6.38±2.23 6.49±2.67 0.34±0.12 0.34±0.15 t1/2/h10.22±3.8310.284±4.1413.217±3.5112.928±3.41 30.55±12.40 28.37±10.92
4 讨论
本研究采用同位素氘标作为内标,与待测化合物性质相近,可校正其他因素对待测物测定结果的影响,提高检测的精密度和准确性,这也是近年来开展药代动力学研究或药物一致性评价的原形药物或其代谢产物研究采用较多的方法[15-16]。同时,本研究使用甲基叔丁基醚进行液液萃取,运用梯度洗脱的方法,建立了快速、灵敏、准确、操作简便的HPLC-MS/MS 法,为阿托伐他汀及其主要代谢物人体药代动力学研究提供了依据。
