UHPLC法同时测定并比较不同厂家、不同剂型益心舒制剂中7种成分含量
2021-02-03雷晓晴王亚丹乔三洋吴宏伟杨洪军
雷晓晴,王亚丹,乔三洋,吴宏伟,杨洪军,李 耿
1.首都医科大学附属北京世纪坛医院 临床合理用药生物特征谱学评价北京市重点实验室,北京 100038
2.中国食品药品检定研究院,北京 100050
3.北京中医药大学中药学院,北京 100029
4.中国中医科学院 中药研究所,北京 100700
5.中日友好医院,北京 100029
益心舒制剂为临床治疗冠心病心绞痛的常用中成药,系国家医保目录、国家基本药物目录收录品种。其组方由人参、麦冬、五味子、黄芪、丹参、川芎和山楂组成,系由经典名方生脉散为核心,在合用升陷汤重用黄芪之意的基础上,加用了活血之川芎、丹参和山楂,具有益气复脉、活血化瘀、养阴生津之功效[1]。目前,市场上的益心舒制剂有4个剂型11 种产品,胶囊、丸、颗粒和片剂分别有1家、1 家、2 家和7 家企业生产。其中益心舒胶囊曾连续多年入围《中药大品种科技竞争力报告》[2]。
《中国药典》2020年版[3]收载了益心舒丸、益心舒片、益心舒胶囊、益心舒颗粒。其中,益心舒胶囊标准仅有人参皂苷Rg1、Re 和丹酚酸B 3 种成分的含量测定,益心舒丸、益心舒片和益心舒颗粒标准中还规定了人参皂苷Rb1的含量限度;鉴别项下均包括黄芪、麦冬、五味子的薄层鉴别,未涉及川芎和山楂。此外,目前对益心舒制剂质量研究的文献多集中于对人参皂苷的含量测定[4-7],另外还有杨小孟[8]采用高效液相色谱法测定了益心舒胶囊中黄芪甲苷的含量,王绍志等[9]采用HPLC 法测定了益心舒胶囊中丹参素、原儿茶醛、阿魏酸、丹酚酸B 的含量;其他益心舒制剂质量研究还涉及丹参酮、五味子甲素、五味子醇甲等成分[10-20],本课题组此前采用UHPLC-Q/TOF-MS 技术鉴定识别了益心舒胶囊中的276 种化学成分,初步掌握了益心舒胶囊化学成分的种类[21],但要全面研究益心舒胶囊质量,比较不同厂家、不同剂型益心舒产品的物质基础差异,仍有待获取更多的量化化学信息。
全面研究中药质量要素的形成和传递过程,构建过程化质量控制体系,是突破中药质量瓶颈的关键。获取足够多的量化信息,是研究中药质量要素形成的前提,对于中药质量研究意义重大。通过建立中成药产品的检测方法,可为今后基于药典标准建立优质中成药产品质量标准奠定基础;有利于研究从药材、饮片到提取物、中间体,再到中成药的关键质量属性传递过程;有利于全面了解不同剂型产品的物质基础及质量水平;也有利于中药质量大数据的积累,为实现智能化生产奠定基础。为了更全面的评价和控制益心舒制剂质量,本研究在药典检测方法的基础之上,进一步拓展定量检测范围,建立可以同时检测益心舒制剂中阿魏酸、迷迭香酸、紫草酸、洋川芎内酯I、丹酚酸B、隐丹参酮和丹参酮IIA7 种化学成分含量的UHPLC 方法,为全面提升益心舒制剂的质量控制水平提供支持,也为全面比较不同益心舒制剂的质量控制水准奠定基础。
1 仪器与材料
超高效液相色谱(UPLC)Accuracy 系统,包括二元超高压溶剂系统、自动进样恒温样本管理器、二极管阵列检测器、Empower 3 色谱工作站,美国Waters 公司;NANO-pure Diamond Ro+纯水系统,美国Thermo Fisher Scientific 公司;KQ5200DE 型超声波仪,江苏昆山市超声仪器有限公司;Sartorius CP225D 电子天平,德国Sartorius 集团。
提取用甲醇,批号20160401,分析纯,北京益利精细化学品有限公司;乙腈,色谱纯,美国Fisher公司;水为超纯水。
对照品迷迭香酸(批号111871-201001,质量分数98.8%)、丹酚酸B(批号111562-201212,质量分数95.4%)、隐丹参酮(批号110852-200806,质量分数98.7%)、阿魏酸(批号110773-200611,质量分数≥99.0%)、丹参酮IIA(批号110766-200619,质量分数≥99.0%),购自中国食品药品检定研究院;对照品紫草酸(批号20216-201107)和洋川芎内酯I(批号20157-201703)购自南昌贝塔生物科技有限公司,HPLC 测定质量分数均大于98%。9 批益心舒胶囊,批号分别为20160812、20160814、20160815、20160901、20160910、20160912、20160913、20160914、20161002,3 批A厂家益心舒片,批号分别为20150301、20150303、20150403,由贵州信邦制药股份有限公司提供;B厂家益心舒片(颈复康药业集团有限公司,批号为730042)、益心舒颗粒(山东中泰药业有限公司,批号为17030215)、益心舒丸(昆明赛诺制药股份有限公司,批号为16091402)均为市售。不同益心舒制剂的规格及用法用量见表1。
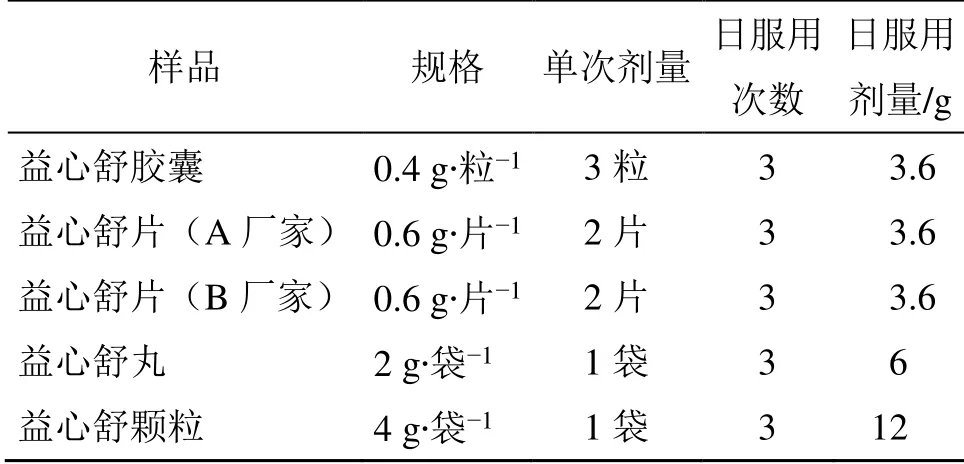
表1 不同益心舒制剂的规格及用法用量Table 1 Specifications,usage and dosage of different Yixinshu preparations
2 方法与结果
2.1 溶液的制备
2.1.1 供试品溶液的制备 取10 粒益心舒胶囊内容物,置于称量纸上,混合均匀,精密称取约0.5 g,(其他益心舒制剂以含有相等的药材投料量等比例折算,折算方法见表2),置于150 mL 具塞锥形瓶中,精密加入甲醇50 mL(不同制剂根据称样量按比例折算,见表2),称定质量,超声处理30 min,放置冷却至室温,用甲醇补足减失的质量,摇匀,溶液过0.22 μm 微孔滤膜,弃去初滤液,续滤液作为供试品溶液。
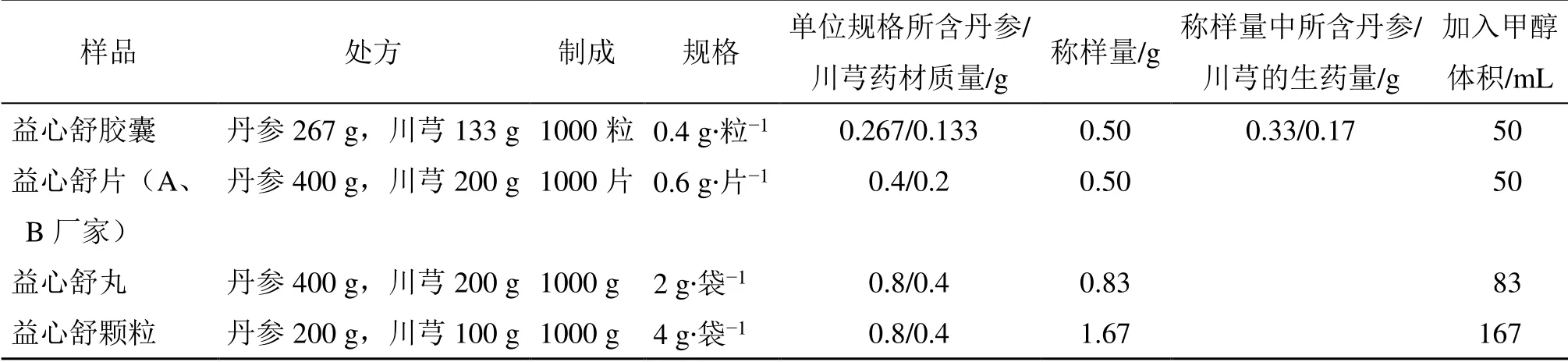
表2 不同益心舒制剂的称样量及加入甲醇体积计算Table 2 Weighting sample and methanol adding volume calculation of different Yixinshu preparations
取益心舒片10 片,置于研钵中研细,混合均匀,精密称取约0.5 g,置于150 mL 具塞锥形瓶中,精密加入甲醇50 mL,同法制备供试品溶液。
取益心舒丸1 袋,置于研钵中研碎,精密称取约0.83 g,置于250 mL 具塞锥形瓶中,精密加入甲醇83 mL,同法制备供试品溶液。
取益心舒颗粒1 袋,精密称取约1.67 g,置于250 mL 具塞锥形瓶中,精密加入甲醇167 mL,同法制备供试品溶液。
2.1.2 对照品溶液的制备 精密称取阿魏酸、迷迭香酸、紫草酸、洋川芎内酯I、丹酚酸B、隐丹参酮和丹参酮IIA对照品适量,分别加甲醇溶解制成含阿魏酸3.74 μg/mL、迷迭香酸110.0 μg/mL、紫草酸123.0 μg/mL、洋川芎内酯I 22.0 μg/mL、丹酚酸B 1.86 mg/mL、隐丹参酮121.0 μg/mL 和丹参酮IIA36.3 μg/mL 的对照品储备液。分别精密吸取各对照品储备液1 mL,加甲醇定容至10 mL,即得混合对照品溶液。
2.2 色谱条件
色谱柱为Waters Acquity HSS T3 柱(100 mm×2.1 mm,1.8 μm);流动相为0.5%甲酸水溶液-乙腈系统,色谱洗脱梯度:0~1 min,3%~4%乙腈;1~4 min,4%~18%乙腈;4~9 min,18%~42%乙腈;9~11 min,42%~63%乙腈;11~14 min,63%~73%乙腈;14~15 min,73%~100%乙腈;体积流量0.4 mL/min;检测波长:322 nm,阿魏酸;280 nm,迷迭香酸、紫草酸、洋川芎内酯I、丹酚酸B;265 nm,隐丹参酮、丹参酮IIA;进样量2 μL;柱温37 ℃;样品管理器温度4 ℃。混合对照品及样品的色谱图见图1。
2.3 方法学考察
2.3.1 线性关系考察 依次精密量取混合对照品溶液0.5、1.0、2.0、3.0、4.0、5.0 μL,按“2.2”项下色谱条件分别进样,记录各成分峰面积,以色谱峰峰面积为纵坐标(y),进样质量为横坐标(x)进行线性回归,结果见表3。可以看出,7 种成分在各自线性范围内线性关系良好,所有成分相关系数(r)均在0.999 5 以上。
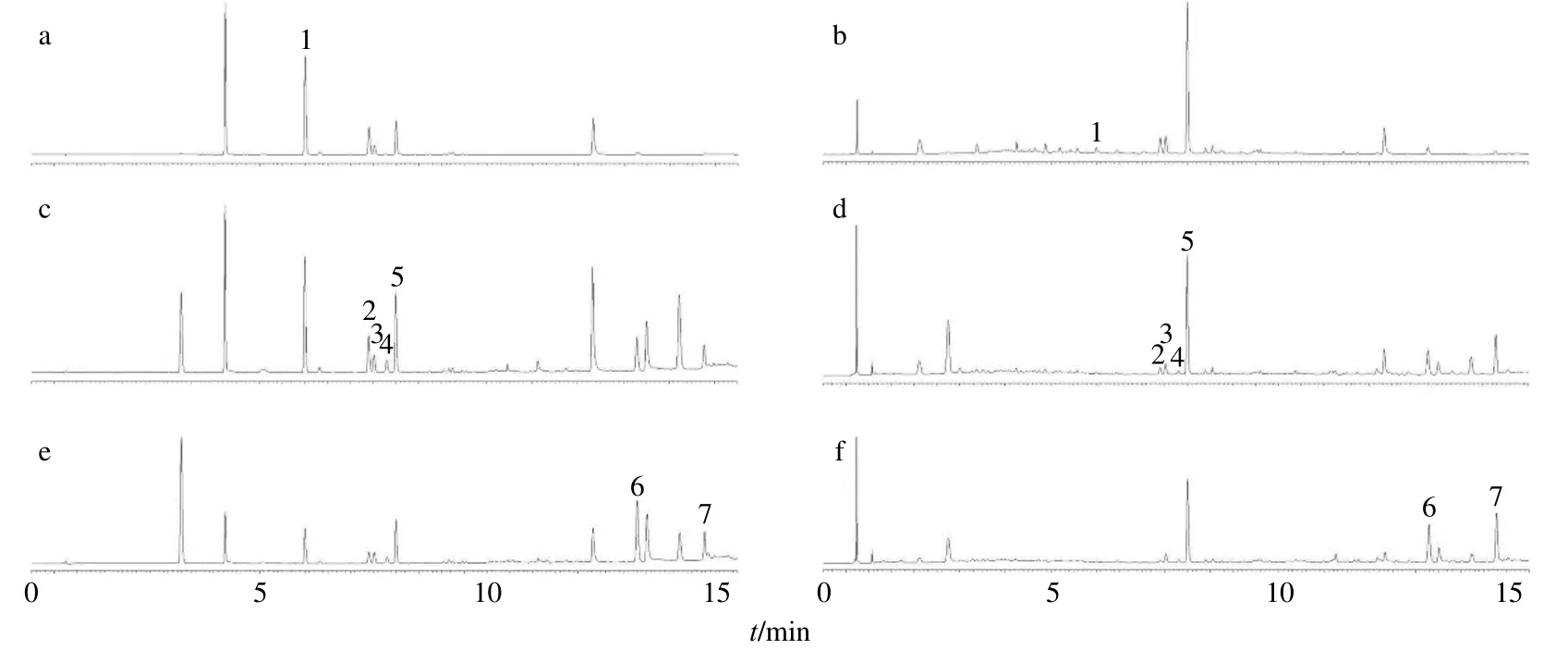
图1 3 个不同检测波长下混合对照品 (322 nm,a; 280 nm,c; 265 nm,e) 和样品-益心舒胶囊 (批号20160812,322 nm,b; 280 nm,d; 265 nm,f) 的UHPLC 图Fig.1 UHPLC of mixed reference substances (322 nm,a; 280 nm,c; 265 nm,e) and sample (batch 20160812,322 nm,b; 280 nm,d; 265 nm,f) at three different wavelengths

表3 线性关系考察结果Table 3 Investigation of linear relationship
2.3.2 精密度考察 精密量取混合对照品溶液,按“2.2”项下色谱条件连续进样6 次,记录各成分峰面积,计算6 次峰面积的RSD 值,结果见表4。7个待测成分峰面积的RSD 在0.45%~1.14%,表明仪器精密度良好。
2.3.3 稳定性考察 取益心舒胶囊(批号20160812)内容物约0.5 g,按“2.1.1”项下方法制备供试品溶液,分别于0、3、6、9、12、24 h 按“2.2”项下色谱条件进样,记录各成分峰面积,计算6 次峰面积的RSD 值,结果见表4。7 个待测成分峰面积的RSD 在0.35%~1.16%,表明供试品溶液在24 h 内稳定。
2.3.4 重复性考察 取同一批次益心舒胶囊(批号20160812)内容物6 份,每份约0.5 g,按“2.1.1”项下方法分别制备供试品溶液,按“2.2”项下色谱条件进样,记录各成分峰面积,以外标法计算各成分质量分数及6 份样品质量分数的RSD 值,结果见表4。7 个待测成分质量分数的RSD 在1.39%~2.46%,表明方法重复性良好。
2.3.5 加样回收率考察 精密称定已测定含量的益心舒胶囊(批号20160812)内容物6 份,每份约0.25 g,分别加入各对照品溶液适量(加入后待测物总量相当于样品中原有量的100%),按“2.1.1”项下方法制备供试品溶液,并按“2.2”项下色谱条件进样测定,记录各成分峰面积,以外标法计算含量并计算各成分的加样回收率及RSD 值,结果见表4。所测7个指标成分的平均加样回收率在97.56%~104.44%,RSD 值均小于3.72%,表明方法准确度良好。
2.4 样品测定及结果
分别精密称取不同益心舒制剂(益心舒片、益心舒丸研碎过筛),按“2.1.1”项下方法制得供试品溶液,按“2.2”项下色谱条件进样,记录各成分峰面积。各对照品储备液以适当比例稀释,按“2.2”项下色谱条件进样,记录峰面积。以外标法计算各成分含量。
2.4.1 9 批益心舒胶囊含量测定结果 9 批益心舒胶囊中7 种成分的含量测定结果如表5 所示。根据《中国药典》2020年版规定,益心舒胶囊中每粒含丹参以丹酚酸B 计不得少于1.0 mg,结果显示,本研究中所测定的所有样品均符合规定。检测的7 种成分平均RSD 为13.63%,其中最大为23.19%,最小为9.00%。
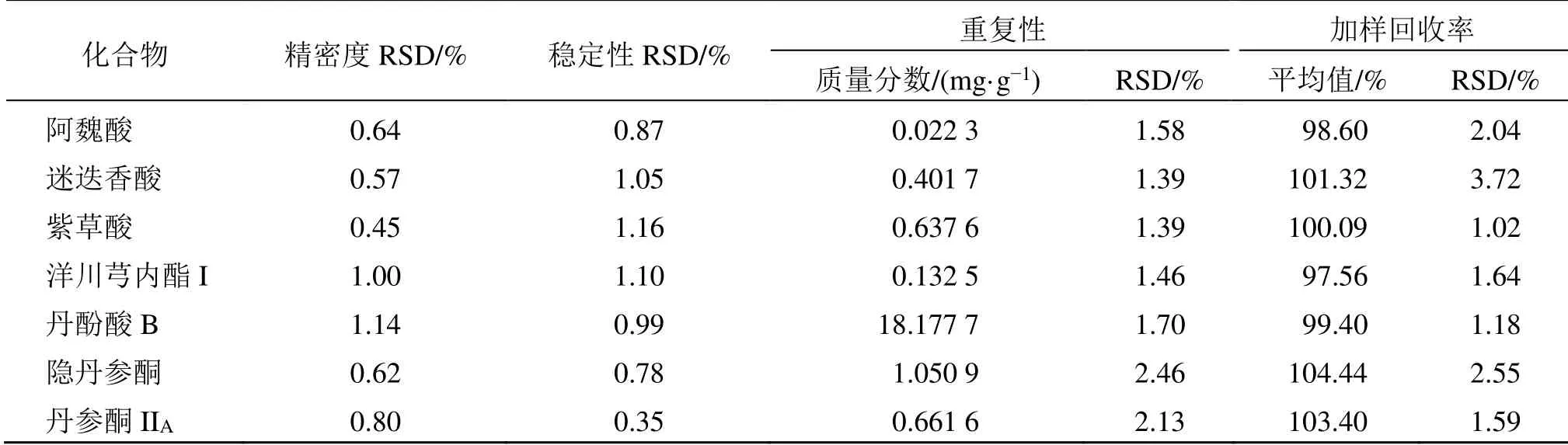
表4 精密度、稳定性、重复性和加样回收率考察结果 (n = 6)Table 4 Investigation of precision,stability,repeatability and average recoveries (n = 6)
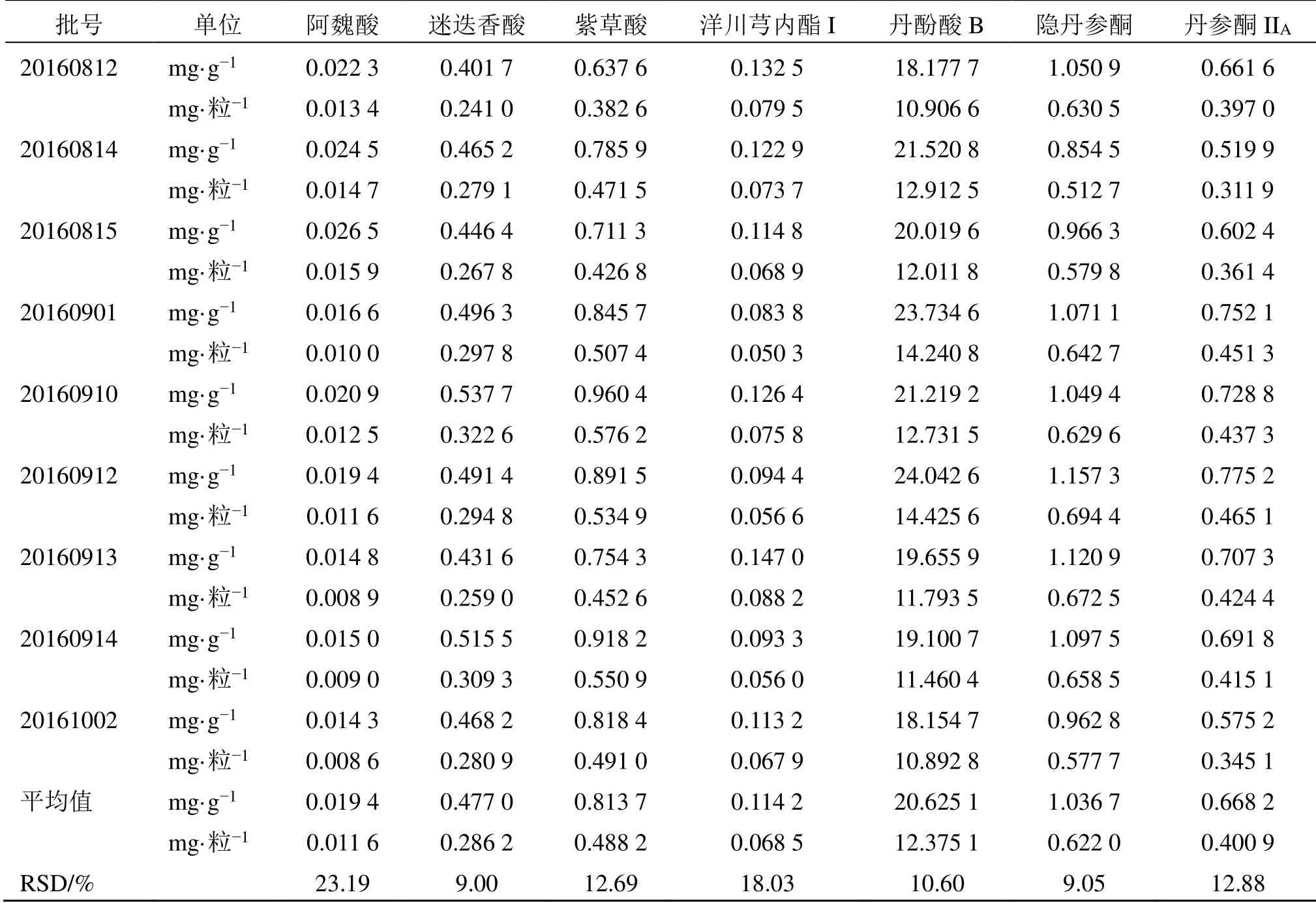
表5 9 批益心舒胶囊中7 种成分的含量测定结果Table 5 Content of seven components in nine batches of Yixinshu Capsules
2.4.2 不同厂家益心舒片中7 种成分的含量测定结果 益心舒片为多家产品,由7 家企业生产。不同厂家益心舒片的规格和服用剂量不同,为产品质量一致性比较增加了难度。本研究收集了多家企业的益心舒片样品,但由于部分企业产品执行的标准中工艺制法未公开,难以确定其生产时的投料量及制成片数,故本研究仅纳入2 家规格和用法用量与药典标准一致的益心舒片,对有关成分含量进行对比分析。结果见表6。根据《中国药典》2020年版规定,益心舒片每片含丹参以丹酚酸B 计不得少于1.5 mg,结果显示,本研究中所测定的所有样品均符合规定。然而本研究所考察的2 厂家生产的益心舒片中丹酚酸B 含量相差约一半,A 厂家3 批产品的平均值为10.859 7 mg/g,而B 厂家的含量达到了20.970 4 mg/g。A 厂家内部3 批次产品之间的RSD相对较小。
本研究比较了不同厂家生产的益心舒片中7 种化学成分的含量差异。为了能够更直观的反映差异程度,将各化学成分的质量分数转化为该成分含量平均值的相对百分当量,如图2 所示。A 厂家生产的益心舒片中7 种化学成分含量均低于2 厂家平均值,而B 厂家益心舒片高于平均值,其中,丹参所含的化学成分丹酚酸B、隐丹参酮和丹参酮IIA的含量差距较大,川芎所含的阿魏酸和洋川芎内酯I 含量差距相对较小。
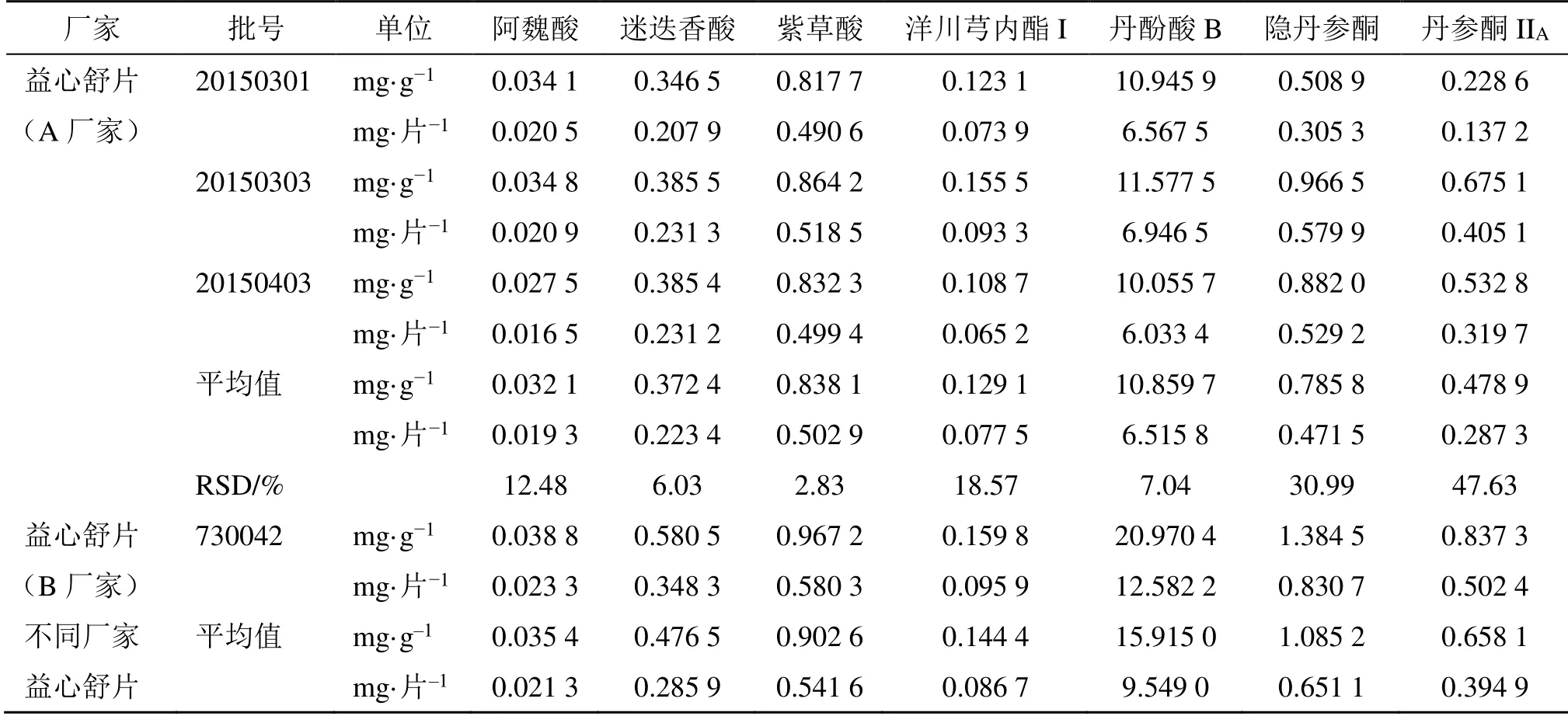
表6 不同厂家益心舒片中7 种成分的含量测定结果Table 6 Content of seven components in Yixinshu Tablets produced by different manufacturers
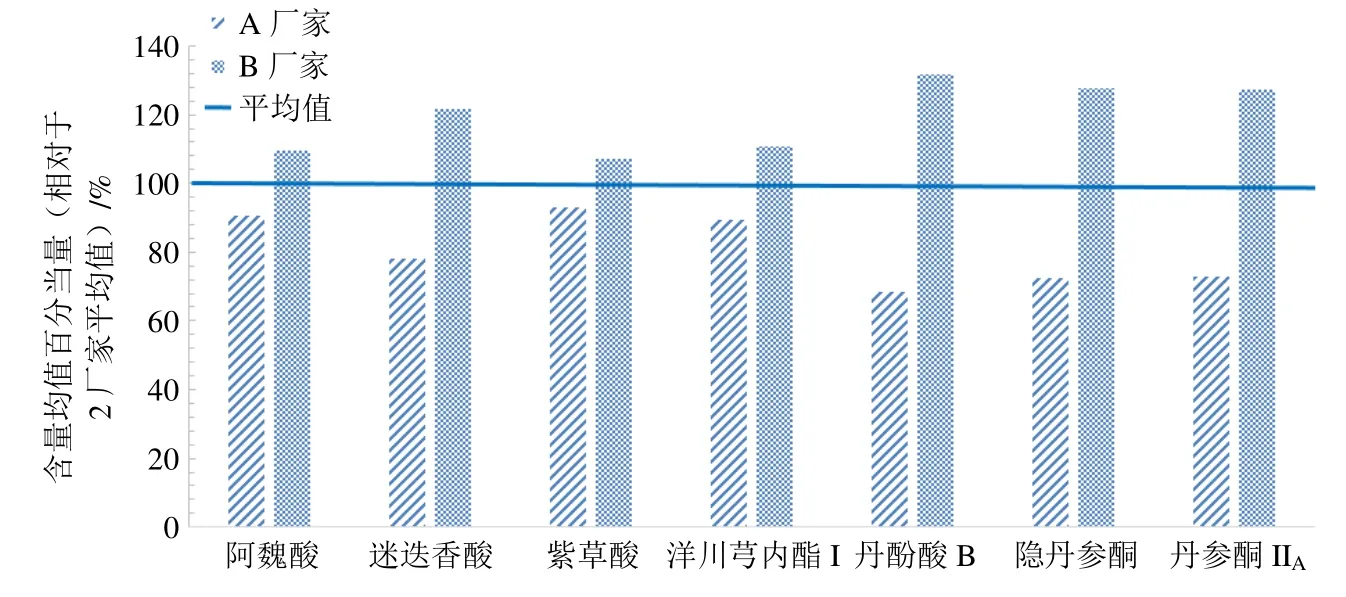
图2 不同厂家益心舒片中7 种化学成分的含量均值百分当量分布图Fig.2 Percent equivalent relative to average content distribution of seven chemical components in Yixinshu Tablets produced by different manufacturers
2.4.3 不同益心舒制剂中7 种成分的含量测定结果及比较分析 为全面比较不同益心舒制剂中化学成分的差异,综合研判益心舒制剂质量,本研究分别从成分含量及相对当量、成分日摄入量及相对当量、成分含量一致性3 个方面对其进行比较分析。不同益心舒制剂中7 种成分的含量测定结果见表7。根据《中国药典》2020年版规定,益心舒丸、益心舒颗粒中每袋含丹参以丹酚酸B 计不得少于3.0 mg,结果显示,本研究中所测定的样品符合规定。
比较不同益心舒制剂中7 种化学成分的质量分数当量(%,相对于益心舒胶囊),如图3 所示。通过比较可知,益心舒胶囊中药典规定指标性成分丹酚酸B 高于其他制剂,其他成分均稍低于其他制剂,其中阿魏酸相对更低。阿魏酸、洋川芎内酯I 的含量在益心舒丸中分布较高,此2 种成分均为川芎的特征成分;另外,由于辅料用量相对较大,益心舒颗粒中所含化学成分的含量低于其它剂型。
2.5 结果分析
2.5.1 不同益心舒制剂中7 种成分的日摄入量 经计算,不同益心舒制剂的日服用生药量是一致的,见表8。因此,本研究将7 种成分的质量分数转化为日摄入量(表9),以更好的比较不同益心舒制剂之间的差异。
以不同益心舒制剂中7 种化学成分的日摄入量当量(相对于益心舒胶囊)作图,如图4 所示。根据不同益心舒制剂日摄入量当量的柱形图分布可以看出,除洋川芎内酯I 外,益心舒颗粒中其他6 种成分的日摄入量均最高;洋川芎内酯I 的日摄入量在益心舒丸中分布最高。
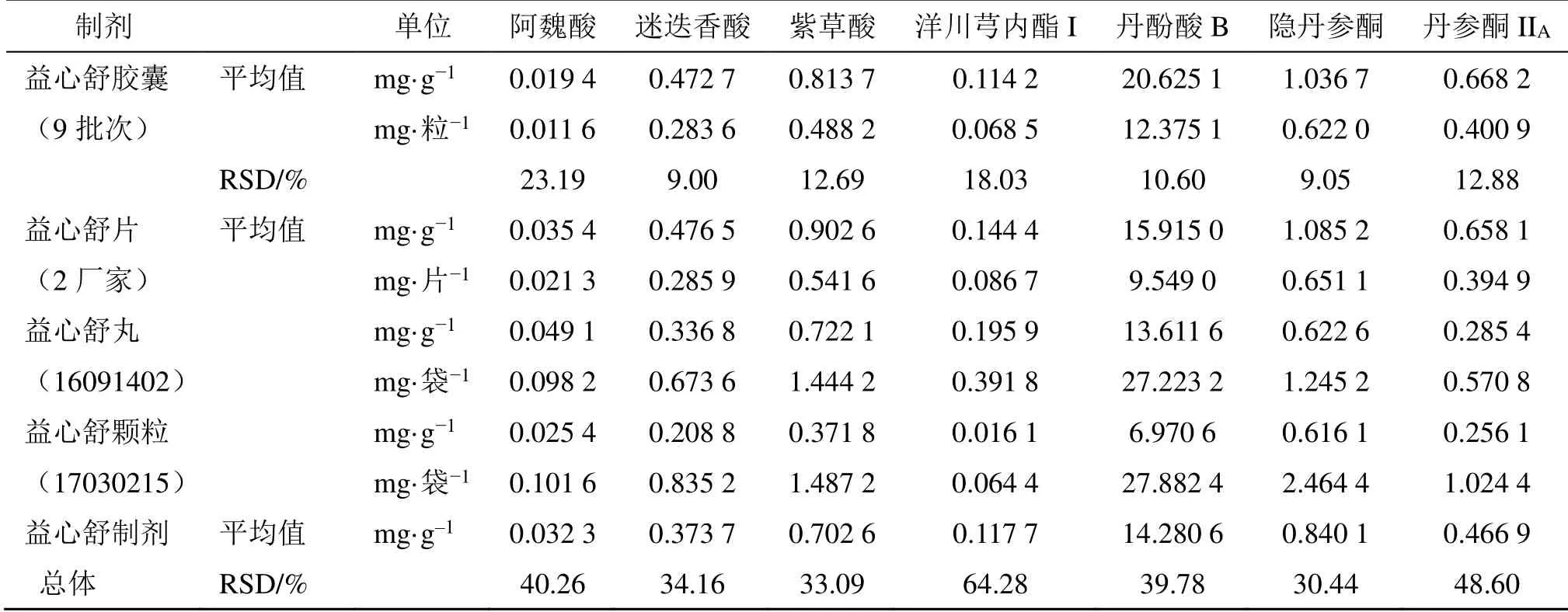
表7 不同益心舒制剂中7 种成分的含量测定结果Table 7 Content of seven components in different Yixinshu preparations
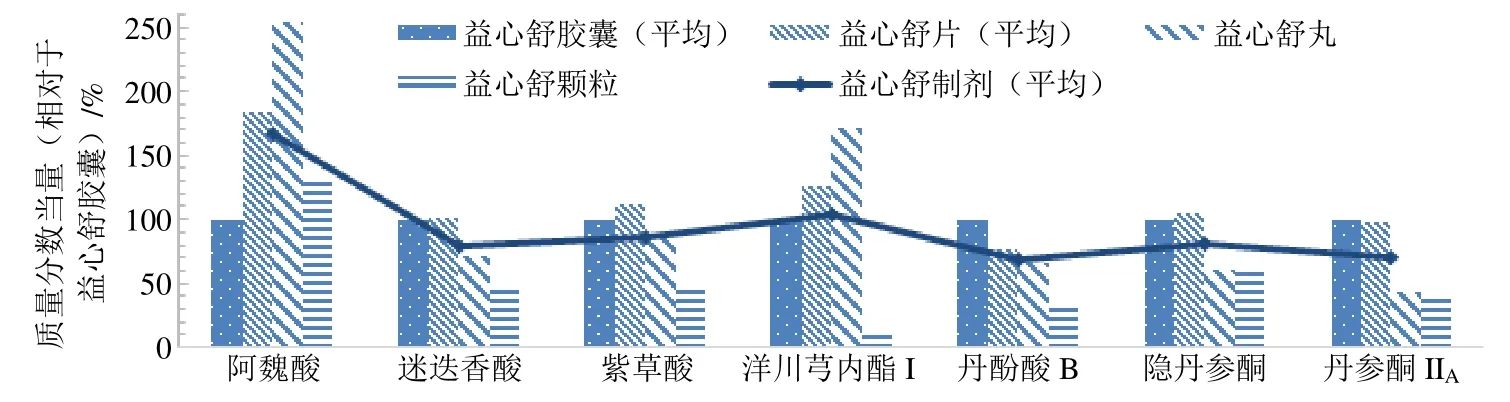
图3 不同益心舒制剂中7 种化学成分的质量分数当量分布图Fig.3 Mass fraction equivalent distribution of seven chemical components in different Yixinshu preparations
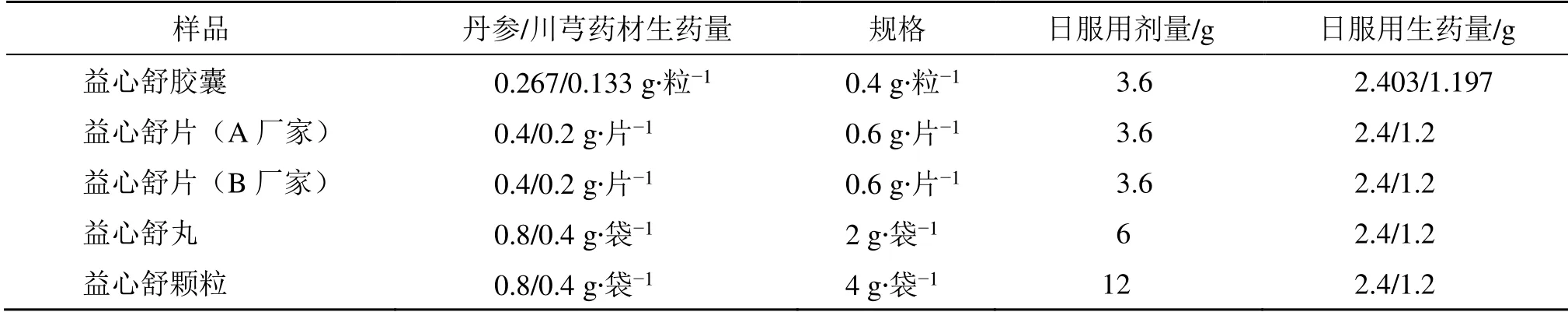
表8 不同益心舒制剂的日服用生药量Table 8 Daily intake dosage of crude medicinal materials of different Yixinshu preparations
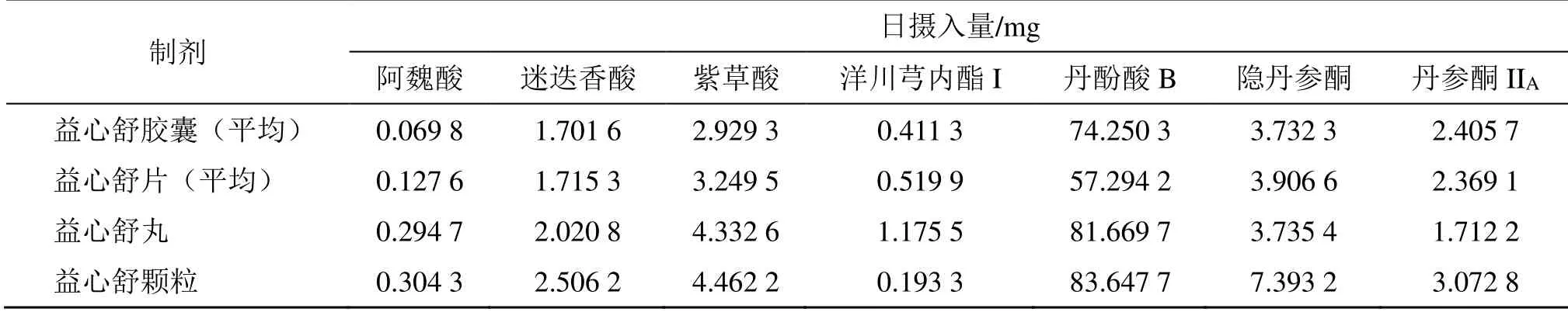
表9 不同益心舒制剂中7 种成分的日摄入量Table 9 Daily intake dosage of seven components in different Yixinshu preparations
2.5.2 益心舒制剂产品成分日摄入量离散性 从总体上计算并比较不同批次益心舒胶囊、不同批次益心舒片(A 厂家)、不同益心舒制剂(益心舒片中的成分含量以2 厂家的平均值计)中7 种成分日摄入量的RSD 差异,如图5 所示。可以看出,7 种化学成分日摄入量的RSD,9 批益心舒胶囊中大多在10%左右,仅有阿魏酸和洋川芎内酯I 偏高,约为20%。3 批A 厂家益心舒片除隐丹参酮和丹参酮IIA外,其余成分的RSD 均小于20%。不同益心舒制剂之间最小在20%,最大可高达70%。同一厂家不同批次的益心舒胶囊、益心舒片批间差异相对较好,但不同益心舒制剂中化学成分含量差异极为显著。
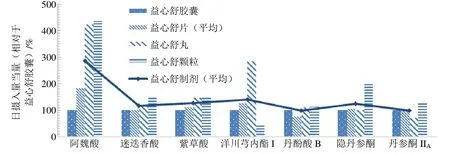
图4 不同益心舒制剂中7 种化学成分的日摄入量当量分布图Fig.4 Daily intake dosage equivalent distribution of seven chemical components in different Yixinshu preparations
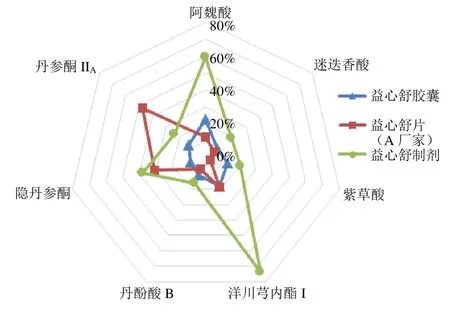
图5 不同批次益心舒胶囊、不同批次益心舒片 (A 厂家)、以及不同益心舒制剂中7 种化学成分日摄入量的RSD 雷达图Fig.5 RSD radar map of daily intake dosage of seven chemical components in different batches of Yixinshu Capsules,different batches of Yixinshu Tablets produced by manufacturer A and different Yixinshu preparations
以成分来看,不同批次益心舒胶囊和不同益心舒制剂中来自丹参药材的成分RSD 相对来说较小,而来自川芎药材中的阿魏酸和洋川芎内酯I 的RSD较大。A 厂家生产的3 批益心舒片中,酚酸类成分迷迭香酸、紫草酸及丹酚酸B 的RSD 仅不到10%,而同为丹参中所含成分的隐丹参酮和丹参酮IIA的RSD 却超过了30%,推测可能的原因与生产过程中工艺参数的控制有关。
3 讨论
在《中国药典》2020年版益心舒制剂标准的基础上,本研究进一步建立了同时检测益心舒制剂中阿魏酸、迷迭香酸、紫草酸、洋川芎内酯I、丹酚酸B、隐丹参酮和丹参酮IIA7 种成分含量的方法,为进一步提升益心舒制剂的质量控制水平奠定基础,也为不同批次产品之间、不同厂家之间及不同制剂之间的比较研究提供参考。
3.1 关于检测技术方法
本研究分别考察了超声法和回流法对各成分提取的影响,结果显示,经两种方法提取后的供试品溶液,各成分色谱峰高无明显差异,回流法提取的供试品溶液个别色谱峰还要稍低于超声法,且操作繁琐、耗时长。因此,本研究采用超声法进行提取。分别考察以50%、75%、100%甲醇为溶剂对提取的影响,结果表明,以100%甲醇进行提取更能兼顾到样品中多个色谱峰,50%、75%甲醇提取的样品峰高差异不大,低于100%甲醇。进一步比较了超声时间为15、30、45 min 时对结果的影响,发现30 min 基本可以实现将各个成分提取完全,继续延长时间,色谱峰高将不再发生明显变化。
采用PDA 检测器在190~400 nm 对提取后的益心舒胶囊样品进行紫外全波长扫描,结果显示,阿魏酸在322 nm 有最大吸收,迷迭香酸、紫草酸、丹酚酸B 在280 nm 有最大吸收,洋川芎内酯I 在277 nm 有最大吸收,隐丹参酮、丹参酮IIA在265 nm有最大吸收。在最大吸收波长处进行检测,各成分杂质干扰较少,各色谱峰分离较好,定量准确,重复性好。由于277 nm 与280 nm 十分接近,定量上无明显影响,故使洋川芎内酯I也在280 nm 下进行测定即可。综合考察后,本实验最终选择在322、280、265 nm 波长处分别检测益心舒制剂样品中的相关成分。
对甲醇-水、乙腈-水、乙腈-0.1%磷酸水溶液、乙腈-0.1%甲酸水溶液、乙腈-0.5%甲酸水溶液等作为流动相时对各成分分离及色谱峰峰形的影响进行了考察,结果显示,以乙腈-0.5%甲酸水溶液为流动相时,由于组分中含有较多的有机酸类成分,酸性条件可以起到抑制H+电离的作用,使色谱峰呈现出较好的峰形,且各色谱峰在该条件下均达到较好分离,因此本研究最终选择以乙腈-0.5%甲酸水溶液作为流动相。
同时,分别考察了Acquity BEH C18、Cortecs C18和Acquity HSS T3 色谱柱对分离的影响,结果显示,由于本研究所测定的7 种化学成分中含有较多的极性成分,同时还有隐丹参酮和丹参酮IIA2 个低极性成分,以Acquity HSS T3 柱作为色谱柱时,可以更好的增强极性成分的保留,同时减弱疏水性成分的保留,使极性与非极性成分达到较好的平衡,各色谱峰分离效果及峰形均最好。同时,由于HSS T3色谱柱在高水相条件下对较低pH 值的流动相有较好的耐受力,更适用于在本研究所建立的方法条件下使用。
3.2 关于测定结果分析
由于工艺、制法、剂型、规格、服用量等因素影响,不同益心舒制剂的质量难以简单的横向比较。本实验尝试通过成分含量、日摄入量、离散性多个维度的比较,较为综合的呈现不同批次、不同厂家、不同剂型益心舒制剂间的成分差异和质量特点。
同一厂家不同批次的产品,原料来源、制法与生产工艺均相对固定,成分含量波动区间相对较小,不同成分含量的差异主要源于原料波动和生产过程控制水平。不同批次的益心舒胶囊之间,成分含量的RSD 大部分在15%以内;同一厂家的3 批益心舒片之间,多数成分含量的RSD 在20%以内。
不同剂型的益心舒制剂,由于制法工艺及辅料添加量存在差异,导致成分间的质量分数差异更为悬殊。相对而言,胶囊剂、片剂辅料应用相对较少,制剂中多种化学成分的含量较高,有利于实现较小的日服用剂量,具有较好的便携性和顺应性;颗粒剂由于辅料占比相对较高,制剂中各类成分含量水平偏低,服用量较大,其优点是服用后吸收较快、作用迅速。
3.3 关于化学成分定量分析
中药化学成分复杂,药效作用多样。含量测定在不同的时间、空间以及使用不同的仪器时具有一定的可重复性,定量检测数据具有较好的可比性,尤其在信息化、大数据时代,基于含量测定的文献分析可以量化的比较中药质量变迁。
对于复方中药而言,多成分含量测定具有其它方法难以比拟的量化评估产品质量的优势。一方面,对于企业来说,多成分含量测定不仅可以作为企业的内控标准,用于产品的批间一致性评价研究,而且也可反映一定历史时期内用于生产的原料药材的质量变化,有助于进一步固定产地、厂家等,对更好的控制和保证药品质量具有重要意义;另一方面,多成分含量测定还可以用于不同企业之间药品质量的横向对比研究。
本研究借鉴中药化学全息理念策略[22],在当前技术条件下,拟尽可能多的实现对益心舒胶囊中化学成分的定量分析,但由于涉及的化学成分复杂,理化性质差异显著,难以以同一提取方法在同一色谱条件下进行检测,因此本实验重点探讨了其中有机酚酸类、内酯类、菲醌类成分的检测,该成药中所含的皂苷类、木脂素类等其它成分将在此后的研究中继续探讨。
3.4 关于中药一致性评价
近年来,药品集中招标采购成为我国医药市场竞争的关键环节。然而,招标过程中,需要在产品质量和疗效一致的前提下,才能通过价格机制形成有效竞争。近年来我国药监部门推行仿制药一致性评价,强调仿制药质量与疗效的一致性,取得了令人瞩目的成就。对于化学药品而言,其效应物质基础清晰,一致性评价过程中,只要通过药学等效性和生物等效性验证,实现体外药学指标、体内生物利用度一致,即在很大程度上可以保证彼此替代使用,满足现实需求。本研究也反映出,不同厂家中药产品之间物质基础差异显著,在临床实践中,中药所面临的产品质量和疗效不一致所带来的问题同样存在。因此,中药产品的质量一致性问题同样值得业界关注。
利益冲突所有作者均声明不存在利益冲突
