掺杂包覆提升高镍材料稳定性机理研究进展
2021-02-01王念举马洪运郭隆泉
王念举,马洪运,郭隆泉,周 江
(天津力神电池股份有限公司,天津 300384)
锂离子电池因其比容量高、安全性能较好、环境友好等优点已在消费类电子产品、新能源汽车及储能等领域得到广泛应用。特别是近年来,得益于国家新能源政策的推进,新能源汽车行业取得了快速发展。但是,续航里程不足等问题依旧是困扰着各大厂商的一大难题。对此,研究人员在不断开发研究提升锂离子电池能量密度的技术方案。从正极材料角度出发,高镍材料因其比容量高、电压平台高、倍率性能好、环境友好等优点迅速成为高比能量锂离子电池研制及应用的热点[1-2]。
然而,高镍材料的结构稳定性尤其是循环寿命及热稳定性是亟需解决的技术难点[3-4]。目前,掺杂或包覆技术被认为是最简单有效的改性方法。常用的掺杂或包覆元素包括Al、Zr、Ti、B、Mg、P、F、Ce等,这些元素对高镍材料的电化学稳定性均有较好的提升作用。本文综述了不同掺杂包覆元素对高镍材料稳定性的影响情况及其作用机理。
1 Al元素提升材料稳定性及其作用机理
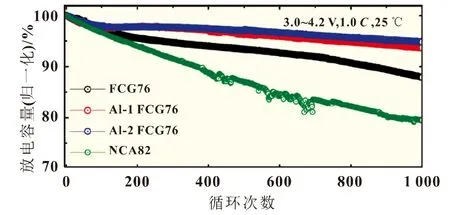
图1 高镍材料Li[Ni0.77Co0.09Mn0.14]O2(FCG76)、1%(摩尔分数)的Al掺杂(Al-1 FCG76)、2%的Al掺杂(Al-2 FCG76)及Li[Ni0.82Co0.14Al0.04]O2(NCA82)的循环寿命对比[5]
在高镍三元材料中,Al是最常用的一种掺杂包覆元素。Kim等[5]研究发现,Al掺杂高镍材料Li[Ni0.77Co0.09Mn0.14]O2后循环寿命显著提升,结果如图1所示。Al掺杂提升材料结构稳定性的作用机理包括:(1)Al掺杂可抑制锂镍混排度,提升材料结构稳定性,Kim等对XRD数据进行精修计算发现,FCG76、Al-1 FCG76、Al-2 FCG76 的 Li+/Ni2+混排度分别为2%、1.7%、1.5%。(2)Al掺杂可抑制循环过程中材料微裂纹的产生,维持材料机械结构稳定性,如图2所示。(3)Al-O键的键能高于Ni(Co、Mn)-O的键能,增强材料在嵌脱锂过程中本征机械结构的稳定性,从而提升材料的循环寿命[6]。

图2 全电池1 000次循环后材料的TEM图[5]
此外,快离子导体LiAlO2包覆也逐渐应用于高镍材料。Tang等[7]制备了γ-LiAlO2包覆的LiNi0.8Co0.1Mn0.1O2正极材料,Al3+掺杂和LiAlO2涂层较好的离子传导性能为Li+的传质构建了优异的传质结构,该材料10C下放电比容量高达135.2 mAh/g,展现了优异的倍率性能。
2 Zr元素提升材料稳定性及其作用机理
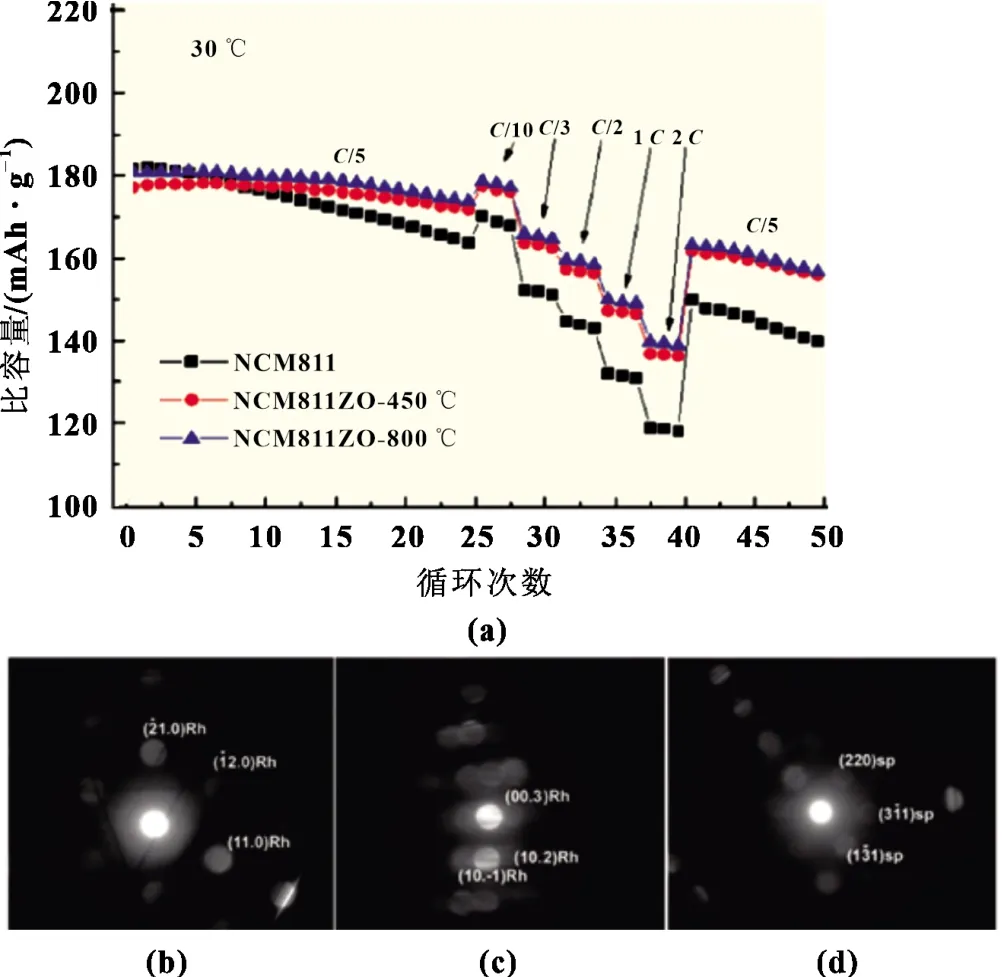
图3 (a)无Zr和有Zr(包含450和800℃两个煅烧温度)性能改善的NCM811循环寿命对比;(b)50次循环后800℃的Zr改性材料的纳米束电子衍射,仅存在层状结构的R-3m空间群;(c)50次循环后无Zr改性材料的纳米束电子衍射,存在层状结构的R-3m空间群;(d)50次循环后无Zr改性材料的纳米束电子衍射,存在立方尖晶石结构的Fd-3m空间群[8]
Florian Schipper等[8]研究发现,高镍三元材料Li-[Ni0.8Co0.1Mn0.1]O2(NCM811)在其表面包覆ZrO2和体相掺杂Zr后,ZrO2和Zr两者发挥了优异的协同作用,显著提升了材料的循环寿命,结果如图3(a)所示。Florian Schipper等认为Zr元素提升材料循环稳定性作用机理包括:在NCM811表面形成ZrO2包覆层可有效缓解正极材料与电解液之间的副反应;Zr元素体相掺杂会优先替代Ni位置,有利于降低Li+/Ni2+混排程度;ZrO2包覆及Zr掺杂协同作用可有效降低电荷转移阻抗以及抑制材料从层状结构向尖晶石相的转变[如图3(b)~(d)所示]。同时,S.Sivaprakash 等[9]认为Zr4+还能部分进入Li位,其“支柱效应”能维持Li+传输通道,随着嵌脱锂过程,Zr4+向材料表面迁移,抑制Ni3+向Ni2+转化反应,从而提升材料的结构稳定性。此外,Zr元素可提升材料的反应动力学速率以及锂离子固相传质系数,从而提升电池的倍率性能[10-11]。
3 Ti元素提升材料稳定性及其作用机理
Ti元素掺杂技术可以提升材料的结构稳定性,但是受掺杂量的影响显著。Zhang等[12]合成了三款Ti掺杂量不同的高镍材料Li1.05-xNi0.8Co0.1TixO2(x=0.0,0.005,0.01),其循环寿命如图4(a)所示。NCMT0.005材料循环稳定性优于未掺杂材料,但是NCMT0.01循环寿命变差。Ti元素的主要作用机理包括:(1)Ti3+的离子半径(0.067 nm)与 Ni2+半径(0.069 nm)、Li+半径(0.074 nm)相近,Ti可占据Li位及过渡金属位,适量的Ti掺杂可抑制Li+/Ni2+混排现象,从x=0.0到x=0.005时,XPS结果表明适量的Ti元素掺杂使得Ni2+氧化为Ni3+[如图4(b)所示],Ni2+/Li+混排度从4.4%降低至2.5%,有利于提高材料的循环性能[12-13]。(2)Zhang等[12]计算发现,Ti元素掺杂还可增加Li+传质层的层间距,经Ti4+掺杂后其间距由0.257 36增大至0.261 85 nm,有利于Li+的传输。但是,过多的Ti4+掺杂导致锂镍混排严重,从x=0.000 5增加到x=0.01时,Ni2+/Li+混排度从2.5%升高至5.4%,为维持电中性,过多的Ti4+的存在会导致Ni2+的增多,进一步提升锂镍混排度[13-14]。(3)Nurpeissova等[15]研究发现Ti元素掺杂可抑制高镍材料表面无电化学活性的NiO相形成,从而延长循环寿命。(4)Wu等[16]认为,Ti元素掺杂可提升H2-H3相变的可逆性[图5(a),(b)],从而抑制材料循环过程中微裂纹的产生[图5(c),(d)]。此外,Song等[17]也提出,Ti掺杂还有利于降低高镍材料阻抗的增长速度。
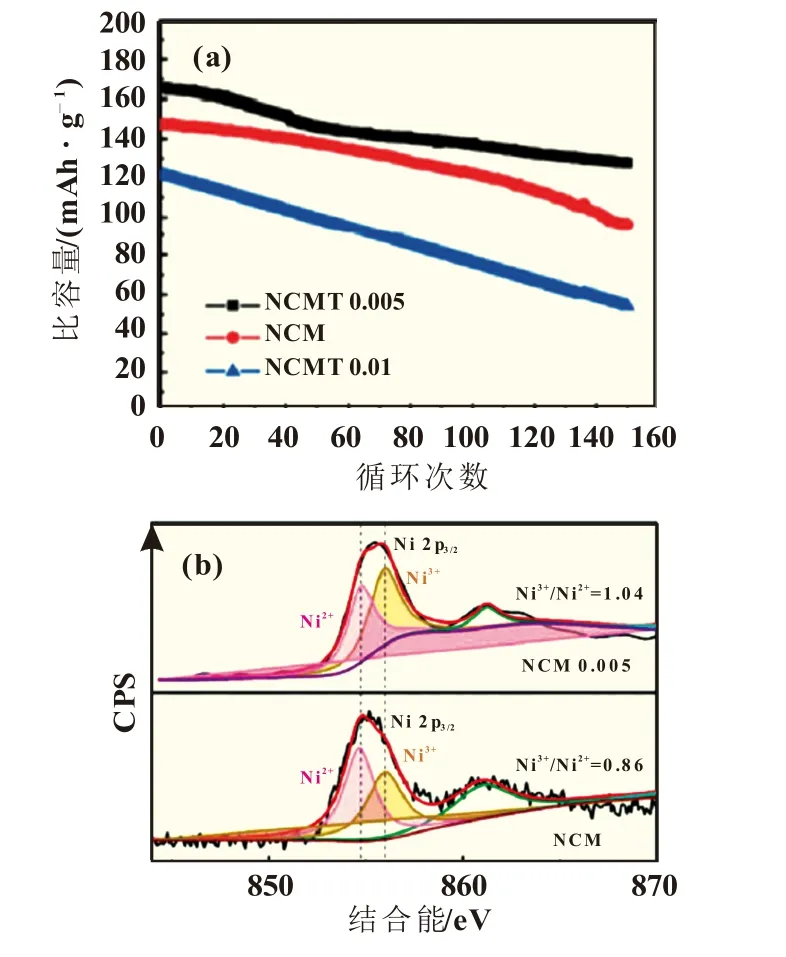
图4 (a)三款Ti掺杂量不同的高镍材料Li1.05-xNi0.8Co0.1TixO2(x=0.0,0.005,0.01)循环寿命;(b)Li1.05-xNi0.8Co0.1TixO2(x=0.0,0.005)两款材料XPS的Ni2p图谱[12]

图5 (a)未掺杂Ti材料循环的dQ/dV曲线;(b)掺杂5%(摩尔分数)Ti材料循环的dQ/dV曲线循环寿命;(c)未掺杂Ti材料循环30次后极片剖面的SEM图片;(d)掺杂5%(摩尔分数)Ti材料循环30次后极片剖面的SEM图[16]
4 Mg元素提升材料稳定性及其作用机理
Mg元素掺杂可提升材料的循环寿命[18-19]。Huang等[20]制备了LiNi0.6-xCo0.2Mn0.2MgxO2(x=0,0.01,0.03,0.05)材料,代号为:Mg-0,Mg-1,Mg-3,Mg-5。2.8~4.3 V循环100次后,容量保持率分别为79.33%、90.02%、89.94%和89.61%,表明Mg元素掺杂可提升材料的循环稳定性。Mg掺杂的作用机理包括:(1)如图6所示,Huang等采用XRD精修计算发现,四个样品的Li+/Ni2+混排度分别为5.18%、1.58%、1.77%和3.2%,Mg2+与Li+半径相近(Mg2+半径为0.072 nm,Li+半径为0.076 nm),Mg2+会占据3a、3b位,抑制Li+/Ni2+混排现象,降低Ni2+在锂层的占位数量,从而提升材料的结构稳定性[14,20]。(2)Huang等计算的四个样品的晶胞结构参数c/a分别为4.953 6、4.956 4、4.956 3和4.961 1,表明Mg掺杂有利于优化层状结构,有利于Li+迁移。(3)Mg-O键的解离能为394 kJ/mol,而Ni-O键的解离能为391 kJ/mol,引入Mg掺杂后提升了材料结构稳定性。(4)Mg并不参与电化学反应,但是Mg掺杂有利于提高材料的导电性[21];其次,Lv等以共沉淀法制备了Mg掺杂的LiNi0.83-Co0.12Mn0.05O2材料,经Mg改性后其1C放电比容量为199.7 mAh/g,与未改性时较为接近,循环200次后其容量保持率由74.0%提升至87.2%,展现了优异的循环性能。Liu等制备了Li(Ni0.8Co0.1Mn0.1)0.97Mg0.03O2正极材料,0.1C下放电比容量为226.1 mAh/g,0.5C循环350次后容量保持率为81%。


图6 (a)LiNi0.6-xCo0.2Mn0.2MgxO2(x=0,0.01,0.03,0.05)(Mg-0,Mg-1,Mg-3,Mg-5)样品的精修XRD数据[20]
5 B元素提升材料稳定性及其作用机理
B在高镍材料中是一种常用的性能改性元素。Kang-Joon Park等[22]在烧结过程中加入B2O3,制备了0.4%(摩尔分数)-B、1.0%(摩尔分数)-B掺杂的 Li[Ni0.90Co0.05Mn0.05]O2(NCM90)材料,与无B掺杂的材料对比发现,1.0%(摩尔分数)-B掺杂的55℃循环100次容量保持率提高15%,如图7(a)所示。B掺杂提升循环稳定性的机理包括:(1)B掺杂可改变表面能,影响一次颗粒的形貌,随着B掺杂量增加一次颗粒变得更细长,并沿径向分布,有利于放射状的一次颗粒与二次颗粒均匀接触,消除局部应力集中,有效吸收各向异性应变,降低颗粒循环后的开裂程度[23],从而提升循环稳定性,结果如图7(b)~(d)所示;(2)B-O键能(809 kJ/mol)均高于Mn-O键(402 kJ/mol)和Ni-O键(382 kJ/mol),B掺杂可提升材料的结构稳定性[24];(3)B掺杂可抑制循环过程中材料从层状结构快速转变为立方尖晶石结构,有利于维持高镍材料中层状结构的稳定[25];(4)B以聚硼阴离子形式存在于材料中,可有效抑制循环中SEI膜增厚的现象,从而降低极化,提升材料循环寿命[26]。Chen等制备了B改性的NCA材料Li[Ni0.8Co0.15Al0.05]-(BO3)x(BO4)yO2-3x-4y。B元素成功掺杂到材料内部,稳定了其层状结构,该材料展现了优异的循环性能。
6 其他一些元素提升材料稳定性及其作用机理
其他一些掺杂包覆元素也常常用于提升高镍材料的循环稳定性,例如P、F、Ce、La等。
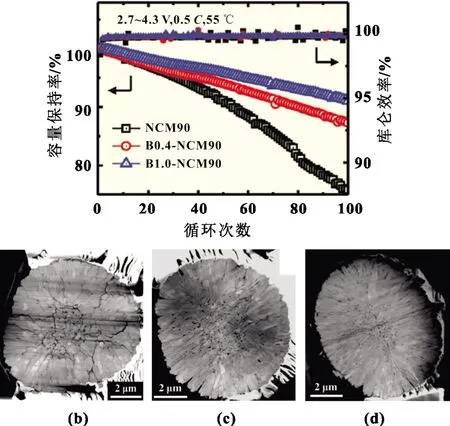
图7 (a)NCM90、0.4%(摩尔分数)-B、1.0%(摩尔分数)-B掺杂样品在55℃的循环寿命曲线;55℃循环100次后扫描透射电镜剖面图像:(b)NCM90;(c)0.4%(摩尔分数)-B掺杂样品;(d)1.0%(摩尔分数)-B掺杂样品[22]
P元素对高镍材料的改性主要采用包覆技术。包覆物质的研究主要集中于Li3PO4及氮氧磷锂化合物(LiPON)等快离子导体。Wang等[27]制备了LiPON包覆的浓度梯度Li-(Ni0.73Co0.12Mn0.15)O2材料,该材料常温循环1 000次后容量保持率为87.3%,比未包覆材料容量保持率高36.1%,Wang等认为其主要作用机理包括:(1)磷酸盐包覆可抑制正极材料与电解液之间副反应,从而提升材料循环稳定性;(2)PITT法测试结果显示,LiPON包覆材料的Li+扩散系数提高50%,包覆层可形成稳定的锂离子传质通道。Yan等[28]采用原子层沉积法(ALD)制备了Li3PO4包覆的LiNi0.76Mn0.14Co0.10O2材料,该材料在60℃下,0.5C循环200次之后容量保持率达到73.2%,而未改性材料的容量保持率仅为58.3%。其主要作用机理包括[28]:(1)600℃煅烧2 h后,Li3PO4包覆层可向内部扩散,充斥于二次颗粒的缝隙之间,可更有效地抑制一次颗粒与电解液之间的副反应;(2)Li3PO4包覆层抑制循环过程中二次颗粒裂纹的形成,稳定材料的机械结构;(3)Li3PO4包覆层降低正极材料活性位点与电解液的副反应,提升循环寿命;(4)Li3PO4包覆层可抑制材料脱嵌锂过程中的相变,从而提升材料结构稳定性。
F元素改性主要包括阴离子掺杂和氟化物包覆。Li等[29]认为适量的卤素尤其是F掺杂可促进高镍材料中相邻的Ni、Li位置互换,造成反位缺陷,形成一种稳定的八面体卤化物可维持层状结构的稳定,并且由于其与O原子的静电排斥,使得晶格参数c增大,有利于Li+的迁移。当F的掺杂量为1%时,该材料在1C下循环200次,容量保持率可达94%。除了掺杂外,F元素对三元材料的改性还可体现在包覆方面。Lee[30]等合成了AlF3包覆的LiNi0.8Co0.15Al0.05O2材料。氟化物相较于其他包覆材料,其最大的优点为氟化物可以抑制因HF攻击而导致过渡金属溶出的现象,避免了包覆物与HF反应导致包覆层脱落,降低电荷转移阻抗的上升。该材料与石墨负极组成全电池后,1C下循环1 000次后容量保持率为86.2%,具有优异的循环性能。
除了上述常见元素外,近年来Ce、La等稀有元素也常作为改性元素来提升高镍材料的电化学性能。Wu等[31]首先将Ce(NO3)3·6 H2O溶解于乙醇中,然后与NCM811材料进行混合,经研磨、干燥并于O2气氛下烧结制备了外层CeO2包覆,内层Ce掺杂的NCM811改性材料。该材料在2.75~4.5 V,0.2C循环50次后容量保持率由未改性时的89.8%提升至99.2%,循环性能明显提升。其作用机理包括:(1)Ce4+具有强氧化性,可将Ni2+氧化为Ni3+(Ce4++Ni2+→Ce3++Ni3+),从而有效缓解Li+/Ni2+混排现象;(2)CeO2包覆层可有效减少正极材料与电解液之间的副反应,抑制高电压下过渡金属的溶解,提高了材料的结构稳定性及循环性能;(3)Ce2O3的吉布斯自由能为-1 706.2 kJ/mol,而NiO和MnO2则分别为-211.7和-466.1 kJ/mol,因此Ce-O键键能更强,能维持Li+脱嵌过程中层状结构的稳定性,抑制O的溶出;(4)当烧结温度不低于500℃时,50次循环后,Ce改性材料的H3相强度未发生变化,而未改性材料的H3相消失,Ce增强了材料H3相的稳定性能,从而提升了容量保持率。
Wu等[32]还制备了La改性的NCM811材料(La-NCM811)。在高温下,La(NO3)3与NCM811表面的Ni及残余的Li生成类钙钛矿物质La2Ni0.5Li0.5O4包覆在NCM811表面,提高了材料的结构稳定性。同时,Ni以+3价存在,有效降低了Li+/Ni2+混排程度。经La改性后,其混排程度由原来的4.71%降低为2.94%。该材料在2.75~4.5 V,1C下初始放电比容量为194 mAh/g,循环200次之后容量保持率为81.4%。不仅如此,La3+具有较大的离子半径,掺杂时会导致Li层间距增大,有利于Li+传输,La2Ni0.5Li0.5O4也可作为优良的Li+传输导体,因此该材料同样具有优异的倍率性能。
除了 Ce、La之外,Nb[33-34]、Ga[35]等元素也逐渐开始用于三元高镍材料的改性研究中。Nb元素可以部分取代Li+位,降低Li+/Ni2+混排度,降低锂离子传质阻抗,稳定晶体结构,从而使得高镍材料的倍率和热稳定性提高[33]。Wu等[35]采用Ga3+部分取代LiNi0.8Co0.1Mn0.1O2材料中的Mn4+,发现Ga3+改性可以抑制材料的析氧副反应,降低Li+/Ni2+混排,减缓材料脱嵌锂过程中层状结构的坍塌,提升循环稳定性。
