聚电解质纳米粒子作为酶破胶剂载体的性能研究
2021-02-01孟玉玲郭丹丹张志伟刘开泉李丕武
孟玉玲,赵 菲,郭丹丹,张志伟,李 旭,刘开泉,李丕武
齐鲁工业大学(山东省科学院) 生物工程学院,济南 250353
长时间以来,我国增储上产的主要资源来自自然产能较低的低渗透油藏。但是其基本不能满足工业油流的标准,必须进行压裂改造后才可以进行有效的工业开发[1]。在典型的压裂操作中,高性能的压裂液应该在施工过程中保持高粘度,而结束施工后又能完全破胶[2]。这样就必须向压裂液中加入破胶剂(氧化剂或酶),降解聚合物从而降低粘度[3]。酶通常被用作破胶剂来降解瓜尔胶主链上甘露糖之间的醚键,然而,在高温环境中,酶容易变性,失去了催化活性,这限制了酶作为压裂液的破胶剂的应用[4-6]。
为了提供这些特性和保护酶破胶剂免受环境因素的影响,破胶剂可以封装在一个特殊的聚合物中,以实现控制释放和延迟断裂过程[7-11]。尽管封装破胶已经存在了一段时间,但大多数都是树脂类封装剂。由于树脂包被剂分布不均匀,且在破胶过程中有些树脂包被剂不会完全破裂或不破裂,造成压裂液不完全破胶,使返排受阻[12-14]。因此,采用了一种最初为药物输送应用开发的纳米粒子体系-聚乙烯亚胺(polyethylenimine ,PEI)-硫酸葡聚糖(dextran sulfate ,DS)聚电解质复合纳米粒子(polyelectrolyte composite nano-particles ,PECNPs),并对其控释行为进行了研究[15-17]。
PECNPs是在低浓度下阳离子包被剂PEI和阴离子包被剂DS通过静电交替吸附作用进行层层自组装形成的微胶囊结构,在混合过程中添加了带电的甘露聚糖酶分子,它会并通过静电和空间相互作用将其结合到微胶囊中,并且聚电解质纳米粒子外表面上的多余电荷有助于其胶体稳定性[18-20]。使用这种纳米微粒后,可以将破胶剂与压裂液均匀混合,在注入时不会马上释放出甘露聚糖酶。在一定时间后,表层的包被剂因地层温度和压力的改变破裂释放出甘露聚糖酶与压裂液反应,使压裂液开始破胶。
1 实验部分
1.1 酶的添加顺序对纳米粒子缓释性能的影响
制备0.4%w/w的瓜胶溶液,将配置好的溶液在600 rpm下再搅拌5 min,然后将搅拌速率降低到400 rpm又1 h,最后使该聚合物在200 rpm下再水合3 h。将pH调节至7。
将500 mL 0.4%w/w瓜尔胶置于30 ℃水浴锅中,待其温度稳定后分别与3.1 mL的不同类型的纳米粒子(见表1)均匀混合,混合后,用SNB-4数字粘度计测量压裂液的粘度变化。设置对照组,测量0.1 mL 25%w/w 游离酶与30 ℃的瓜尔胶溶液混合均匀后的粘度变化。比对不同类型纳米粒子的破胶效果。
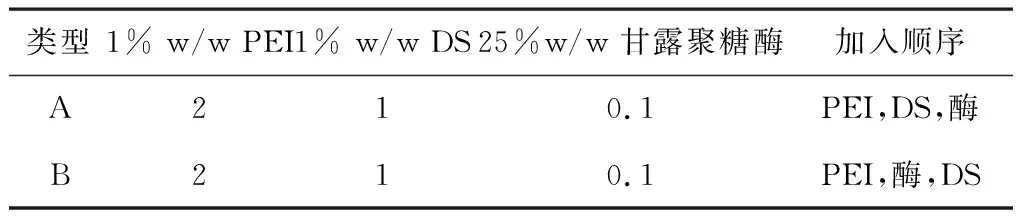
表1 纳米粒子体系在PEI、DS和甘露聚糖酶的添加顺序上的差异 mL
1.2 温度对纳米粒子缓释性能的影响
在典型配方中,将0.1 mL的25%w/w甘露聚糖酶溶液搅拌下逐滴添加2 mL 1%w/w的PEI(调节pH为7)水溶液,然后再将1 mL 1%w/w DS(调节pH为7)水溶液滴加到混合溶液中,再以600 rpm搅拌20 min。负载着25%w/w的甘露聚糖酶的纳米颗粒备用。
用SNB-4数字粘度计分别在测定30 ℃、50 ℃和70 ℃条件下纳米粒子与瓜尔胶混合均匀后的粘度变化,设置对照组,对比等量游离酶的破胶性能。
1.3 聚电解质纳米粒子的储存稳定性的测定
纳米粒子在储存5 d、10 d、15 d后,测试在30 ℃条件下纳米粒子的缓释性能。
1.4 聚电解质纳米粒子的粒径和Zeta电位的测量
为了进一步探究纳米粒子合成的机理,对其粒径和Zeta电位进行表征,使用Zeta电位和纳米粒径测定仪(马尔文公司)测量不同pH值的纳米粒子的平均粒径。用去离子水将纳米颗粒的样品稀释约40倍。记录的数据是通过检测90°角处的光散射得到的三个测量值的平均值。还使用同一仪器通过相分析光散射测量了这些样品的Zeta电位。将样品用1.0 mmol KCl溶液稀释约20倍。取每个样品的三个测量值的平均值。
2 结果与讨论
2.1 酶的添加顺序对纳米粒子缓释性能的影响
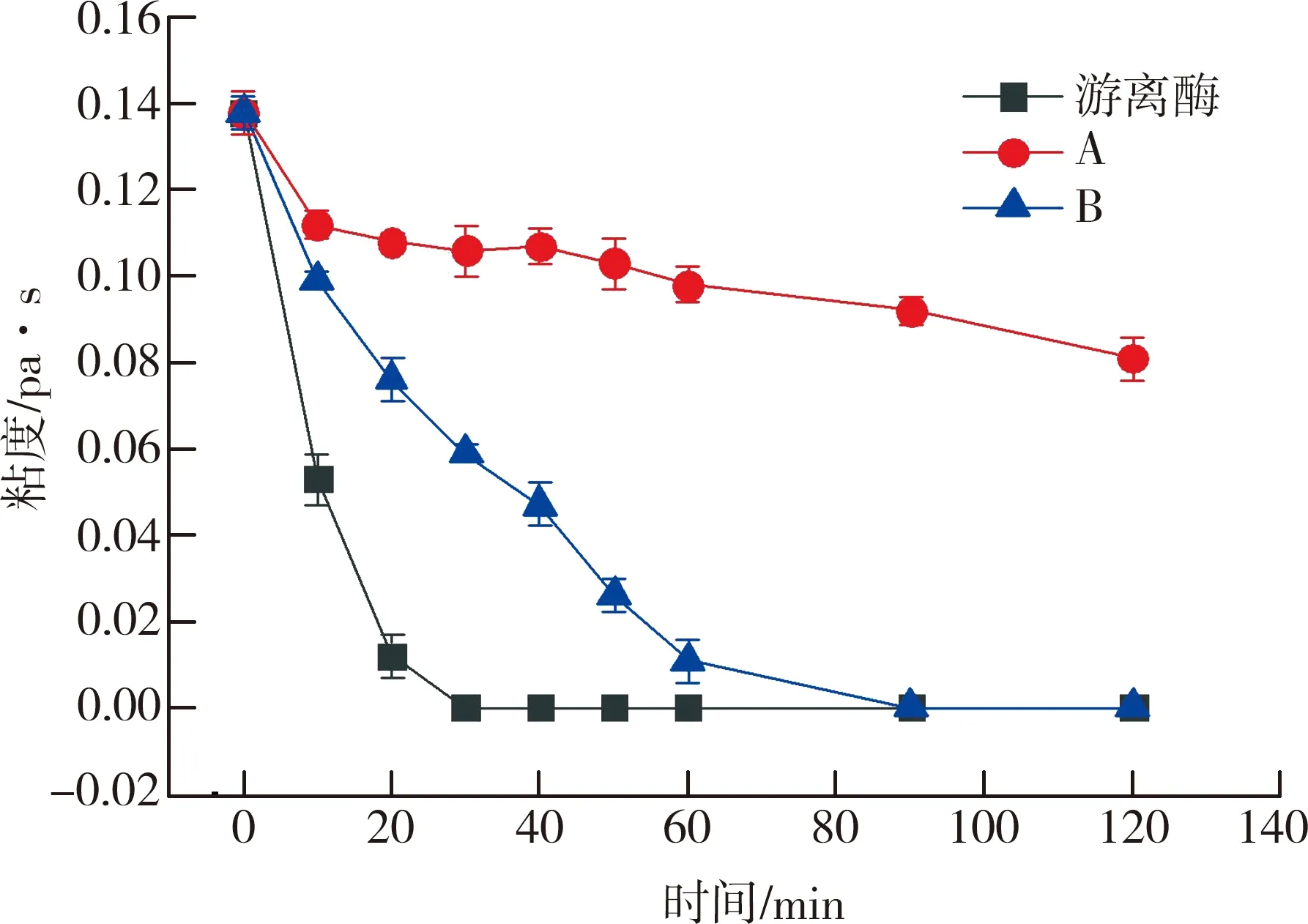
图1 不同类型纳米粒子破胶效果
从图1可以看出PEI-DS纳米粒子具有一定的缓释性能,在30 ℃条件下延长破胶时间大约为60 min。混合添加顺序对纳米粒子的形成有很大的影响,在添加DS之前先添加甘露聚糖酶,纳米粒子对酶分子的包封率高于将甘露聚糖酶添加到预先形成的PEE-DS纳米粒子中,差别几乎可以肯定是由于高分子量的酶分子无法插入到预先形成的PEI-DS颗粒中造成的,因此最后添加DS的添加顺序制成的纳米粒子的破胶效果最好。我们对类型B的纳米粒子进行了进一步的研究。
2.2 温度对纳米粒子缓释性能的影响
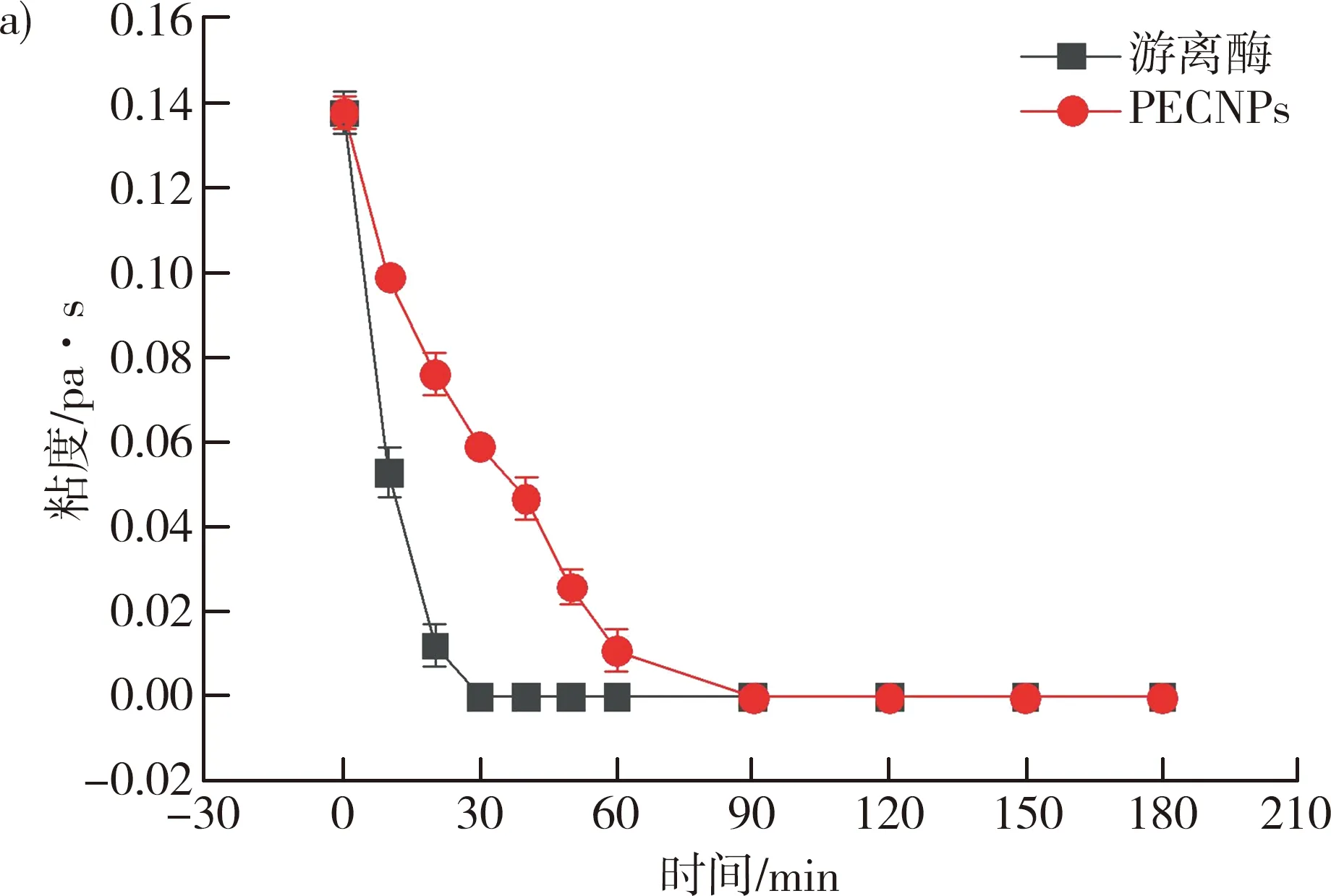
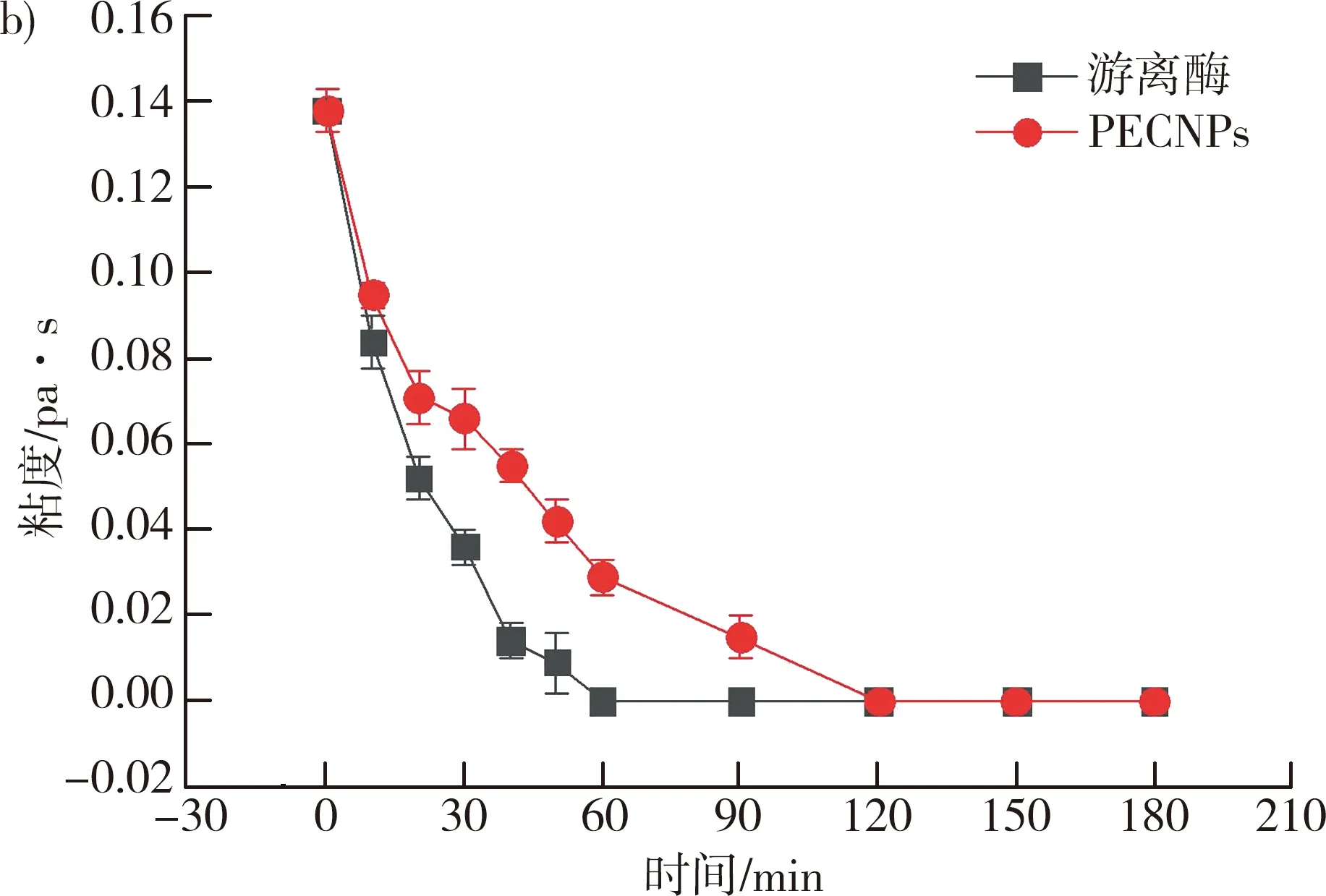
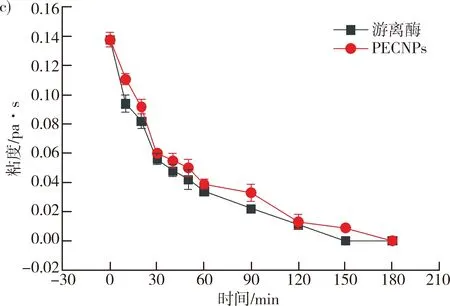
注: a)30 ℃下纳米粒子与游离酶的破胶效果对比;b)50 ℃下纳米粒子与游离酶的破胶效果对比;c)70 ℃下纳米粒子与游离酶的破胶效果对比。
30 ℃、50 ℃和70 ℃条件下纳米粒子和游离酶分别与瓜尔胶混合均匀后的粘度变化如图2所示,在30 ℃和50 ℃条件下,纳米粒子分别能延缓破胶时间约60 min,当温度达到70 ℃,破胶时间仅能延缓30 min。温度在一定程度上影响了纳米粒子的缓释性能。合适的温度是重要的因素,过高的温度会使纳米粒子结构遭到一定程度的破坏。
2.3 聚电解质纳米粒子的储存稳定性的测定

图3 不同储存时间的纳米粒子破胶效果
纳米粒子的储存稳定性如图3所示,储存10 d之后,彻底破胶时间稍微延长,储存15 d之后纳米粒子的破胶效果出现了明显的下降,由此我们推断,纳米粒子储存一段时间后酶的活性有所下降导致无法完成破胶任务,但是10 d之内对酶活性影响效果较小。
2.4 聚电解质纳米粒子的粒径和Zeta电位的测量

图4 纳米粒子粒径和Zeta电位随pH的变化
在pH范围(6.0~8.5)内测量了纳米粒子的大小和Zeta电位如图4所示。在测试范围内,包被甘露聚糖酶的PEI-DS纳米粒子的Zeta电位随着pH的升高而降低,而粒径在pH=7附近显示最大,然后随着pH的进一步升高而降低。这一现象推测是因为PEI上的电荷取决于pH。在PEI的等电点(10.8)时,PEI不带电并且不紧凑的缠绕。 随着pH值的降低,越来越多的仲胺基团被中和成-NH+-。这增加了PEI上的电荷密度,静电排斥导致聚合物形成更伸展的构型,从而增加了带电基团与DS或酶上负电荷相互作用的可能性。相反,随着pH值的升高并接近等电点,PEI的电荷更少且更紧凑,从而导致颗粒中的净正电荷的量减少和PEI之间的排斥力减小,从而减小了粒径。因此,环境pH是影响纳米粒子形成的重要的因素,并且随着环境pH升高,Zeta电位减小,纳米粒子的粒径减小。
3 结 论
实验制成的PEI-DS纳米粒子有一定的缓释性能,探讨了酶的混合顺序对聚电解质纳米粒子形成和缓释性能的影响,30 ℃条件下,在添加DS之前加入酶形成的纳米粒子可延长压裂液的破胶时间约为60 min。
甘露聚糖酶的适用温度在30~70 ℃,在现场使用的时候应注意地层温度对纳米粒子结构的影响,过高的温度会使纳米粒子结构遭到一定程度的破坏。纳米粒子储存至少10 d之内,纳米粒子的作用效果不会有很大的变化,实际应用中可对延长纳米粒子的储存稳定性进行进一步的研究。
另外,pH也是影响纳米粒子形成的重要的因素,纳米粒子的适用pH在6~8.5范围内,纳米粒子的粒径和电位会随着pH的升高而减小。
据作者所知,在油田行业中尚未有缓释甘露聚糖酶破胶剂的材料。 这种新型纳米粒子的引入也将有助于改善甘露聚糖酶破胶剂的较高温度和pH耐受性,在利用生物酶破胶剂提高低渗透油藏产量方面有着巨大的潜力。
