高中化学实验教学中科学素养的培养途径研究
2021-01-28张跃晖
张跃晖
(福建省永春第一中学 362601)
当前的教育观念较以往有很大的改变,不仅使学生掌握扎实的化学实验知识,而且越来越注重学生科学素养的提升,使学生认识到实验在化学学科以及问题研究中重要作用,自觉的养成良好的实验习惯,促使其终身受益.
一、注重传授实验技巧
科学素养包括了解科学的研究方法.高中化学实验教学中,为使学生掌握科学的研究方法应注重实验技巧的传授.教师可以结合具体的实验,为学生讲解实验技巧,使其掌握高效的研究方法,给其以后作相关的化学实验带来良好启发.如实验教学中可为学生讲解以下习题.
例1 实验中可使用无水FeCl3和氯苯(无色液体,沸点132.2℃)制备少量的无水FeCl2,并测定无水FeCl2的产率.
实验原理:
实验装置:如图1所示,检查器密性后,向三颈烧瓶A中加入16.76g无水FeCl3和22.5g氯苯.

图1
回答以下问题:
(1)装置C中装有____(填试剂名称)其作用为____.
(2)启动搅拌器,在约126℃条件下剧烈搅拌30min,物料变成黑色泥状.加热装置A最好选用____;
A.酒精灯 B.水浴锅 C.电磁炉 D.油浴锅
(3)继续升温,在128~139℃条件下加热2h,混合物颜色逐渐变浅,黏度降低.在步骤中加热温度已经接近或超过氯苯沸点,但氯苯实际上却非常小,原因为____.
(4)继续加热1h后冷却,在隔绝空气条件下过滤出固体,用洗涤剂多次洗涤所得固体,置于真空中干燥得到成品.若D中所得溶液恰好与25mL 2.0mol·L-1的NaOH溶液完全反应,则实验中FeCl2的产率约为____(保留三位有效数字).
解答该题需要明确实验原理,结合实验装置特点进行分析、解答.对于问题(1),由于FeCl2、FeCl3易水解,因此,实验中应加干燥装置,即,C中装无水氯化钙,以阻止水蒸气进入A中.(2)中为更好的控制温度应选D.(3)中认真观察实验装置可知,其含有球形冷凝管,具有冷凝回流液体的作用,会使氯苯冷凝、回流.(4)由化学方程式计算出FeCl2的产率约为97.0%.
二、讲解新颖实验例题
教学中应注重讲解新颖的实验例题,使学生亲身感受科学的研究过程,积累更多的经验与技巧.如教学中可讲解以下例题.
例2 为探究AgNO3溶液与Na2SO3溶液的反应设计实验进行探究,具体内容为:取4mL 0.1mol/L的AgNO3溶液,滴加5滴0.1mol/L的Na2SO3溶液,产生白色沉淀后,测得溶液的pH为5.继续滴加Na2SO3溶液,白色沉淀逐渐增多而后消失,测的混合溶液的pH为9.已知Ag2SO3为难溶于水的白色固体;Ag2SO4为微溶于水的白色固体;AgOH为白色固体,但常温下不稳定,容易分解产生棕褐色固体.
(1)测得0.1mol/L的Na2SO3溶液的pH=10,用离子方程式解释原因为____;
(2)实验猜想,①可能含有Ag2SO3;②可能含有Ag2SO4,理由为____;③可能含有AgOH.产生的白色沉淀放置一段时间后未发生明显变化,排除猜想③.
图2
测得沉淀C质量小于沉淀B,试剂1和试剂2分别是____、____,说明白色沉淀是Ag2SO3和Ag2SO4的混合物.

三、创设实验问题情境
在教学中教师需要注重创设相关的实验问题情境对学生进行训练,提高其运用所学实验知识解决实际问题的意识与能力.如训练时可设计如下问题.
例3从含有少量铁的铜银合金废料中回收银和铜,实验工艺如图3:
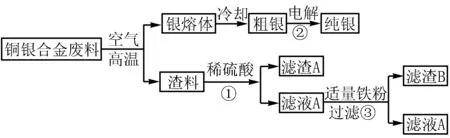
图3
下列说法正确的是( ).
A.粗铜溶于过量稀硝酸过滤、低温干燥得纯铜
B.电解时用粗铜作阴极,硝酸银溶液为电解质溶液
C.用稀硫酸处理渣料时主要发生了氧化还原反应
D.从滤液B中可以提出绿矾(FeSO4·7H2O)
由已知条件可知A的描述并不能得到纯铜,错误.粗铜为阳极,纯银为阴极,B项错误.由实验工艺可知渣料的主要成分为氧化铜还含有少量的氧化铁.两种物质均能和稀硫酸反应,但化合价并未发生变化,C项错误.滤液B中的溶质为硫酸亚铁,经过蒸发浓缩、降温结晶、过滤、洗涤、干燥可得到绿矾,D项正确.
