氯化过程中含氮消毒副产物生成特性
2021-01-20周冰洁
殷 盈,周冰洁,林 涛
(1.河海大学环境学院,江苏南京 210000;2.南京市给排水工程设计院有限公司,江苏南京 210000)
自20世纪70年代,三卤甲烷首次被Rook[1]从加氯消毒后的饮用水中检测出后,人们逐渐开始对DBPs广泛关注[2]。DBPs是指消毒剂与水中的化学成分反应,生成对人体有毒有害的物质。因此,饮用水领域的研究热点之一一直是关于消毒副产物的生成和控制。近年来,各国饮用水水质标准对常规含碳消毒副产物进行了日益严格的控制[3],且具有更高细胞毒性、基因毒性和遗传毒性的新兴含氮消毒副产物不断被检出[4-5]。含氮消毒副产物主要包括卤代乙酰胺类(HAcAms)、卤乙腈类(HANs)、卤代硝基甲烷类(HNMs)和非卤代的亚硝胺类(nitrosamines)。虽然其出厂水浓度一般为ng/L~μg/L,远低于常规含碳消毒副产物的浓度,但其危害远高于后者。三卤甲烷中三氯甲烷、二溴一氯甲烷的致癌风险浓度分别为350 000 μg/L和400 ng/L,而亚硝胺中二甲基亚硝胺仅为0.7 ng/L[6-7],含氮消毒副产物的去除显得尤为重要。但鉴于常规处理工艺难以去除消毒过程中产生的DBPs,因此,降低其在饮用水中的生成量成为控制DBPs的有效手段。其中,DBPs前体物的识别和削减最为重要[8]。
为考察不同类型有机物生成含氮消毒副产物的特性,本研究以长江流域某常规处理厂为对象,从有机物的分子量分布、亲疏水性、极性和带电性角度,分别采用超滤法、树脂固相萃取法和快速分析法,对原水中消毒副产物前体物进行分析,掌握DBPs前体物的性质,为水厂后续的控制技术针对性去除该类型有机物提供参考依据。
1 材料与方法
1.1 试验材料
本试验在以长江为水源地的某水厂进行。水厂采用混凝、沉淀、过滤、消毒的常规工艺。
试验期间长江水源水质情况如表1所示。

表1 试验原水水质Tab.1 Raw Water Quality for Experiment
试验水样取自该水厂各工艺单元出水,水样均用1 L棕色试剂瓶取得,取样后使待测水通过0.45 μm的玻璃纤维纸(GF/F,Whatman,英国),过滤以去除不溶性杂质,滤后水保存在4 ℃的环境下以待备用,直至加氯后测得其最大生成势。
1.2 N-DBPs的生成势及检测
Krasner法测定N-DBPs生成势[9]:加入一定体积标定后的次氯酸钠溶液(20 000 mg/L),控制需氯量满足Cl2(mg/L)=3×DOC(mg C/L)+7.6×NH3(mg N/L)+10(mg/L),再加入10 mmol/L的磷酸盐缓冲液,调节pH值为7.0,将样品密封保存于500 mL的棕色试剂瓶内,放置在暗光环境下的培养箱内,控制温度为25 ℃,反应24 h后,加入抗坏血酸终止氯化反应,并测定含氮消毒副产物浓度。
液液萃取-气相色谱-微电子捕获检测器进行N-DBPs:取100 mL消毒后的水样,加入10 g无水硫酸钠,使其振荡溶解,再加入10 mL萃取剂[(二氯乙腈(DCAN)和三氯硝基甲烷(TCNM)采用甲基叔丁基醚,二氯二酰胺(DCAcAm)采用乙酸乙酯,南京化学试剂有限公司];将样品置于旋涡混匀器(KS501IKA,德国)振荡萃取10 min,静置15 min等待分层;最后,加入无水硫酸钠脱水,控制温度为37 ℃,上层有机相氮吹至1 mL,用气相色谱仪(安捷伦7890B)检测。
1.3 有机物的分子量分级
超滤膜法测定水样中有机物分子量分布[10]:水样先通过0.45 μm(GF/F,Whatman,英国)微滤膜,再分别通过截留分子量为1 kDa和10 kDa的超滤膜(Millipore,美国),收集膜过滤后出水,并进行相应水质指标的测定。例如,N-DBPs生成势、DOC,通过差减法得到2个分子量区间(1~10 kDa和>10 kDa)有机物的N-DBPs生成势和DOC浓度。
1.4 有机物的亲疏水性分级
树脂固相萃取法测定水样中有机物的亲疏水性[11-12]:水样先通过0.45 μm微滤膜(GF/F,Whatman,英国),再用0.1 mmol/L的NaOH和HCl溶液控制pH值为7.0,将水样分别通过XAD-8和XAD-4树脂填料的SPE柱(Sigma,美国),2种树脂分别吸附强疏水性(HPO)和弱疏水性(TPI)有机物,不被吸附的为亲水性有机物(HPI),将2个DAX柱上的有机物用甲醇、0.1 mmol/L NaOH和0.1 mmol/L HCl进行淋洗,分别从柱中洗出疏水中性(HPON)、疏水酸性(HPOA)和疏水碱性(HPOB)有机物,之后将各部分水样分别进行相关水质指标,如N-DBPs生成势和DOC浓度的测定。
1.5 有机物的极性和带电性分级
快速分析法测定有机物的极性:水样先通过0.45 μm的微滤膜(GF/F,Whatman,英国),再以1 mL/min的滤速通过C18柱(Sigma,美国),树脂吸附非极性和弱极性有机物,不被吸附的为极性有机物。
带电性分级除填料更换为SCX树脂,除用于吸附带正电的有机物外,其余同极性分级。
2 结果与讨论
2.1 有机物DOC分子量与生成势的关系分析
采用超滤膜法对长江水源地进行有机物亲疏水性分级,试验结果如下。
由图1可知:在进行DCAN、DCAcAm和三氯硝基甲烷(TCNM)生成试验时,原水中DOC主要集中在MW>10 kDa和MW<1 kDa的组分中,浓度为1.4 mg/L和1.1 mg/L,占总DOC的41.2%和32.3%;而在1 kDa 图1 按分子量分类的DOC质量分布Fig.1 Mass Distributions of DOC Classified by Molecular Weights 由图2可知:从分子量分布规律上分析,DCAN、DCAcAm、TCNM主要以<1 kDa的小分子有机物和>10 kDa的大分子有机物同时生成的形式为主;其中,前体物中分子量>10 kDa的有机物生成DCAN、DCAcAm的浓度分别为4.5 μg/L和2.6 μg/L,其次是分子量<1 kDa的有机物,生成势分别为3.1 μg/L和1.5 μg/L,分子量为1~10 kDa的有机物生成势分别为1.6 μg/L和1 μg/L;而TCNM中,分子量<1 kDa的有机物生成势最高,为2.2 μg/L,其次是1~10 kDa的有机物,生成势浓度为0.5 μg/L,分子量>10 kDa的有机物生成势浓度为0.4 μg/L。 图2 N-DBPs前体物的分子量特性Fig.2 Molecular Weight Properties of N-DBPs Precursors 由图3可知:充分氯化后,DCAN、DCAcAm中分子量>10 kDa的有机物N-DBPs的单位生成势最高,该区间有机物的DCAN、DCAcAm单位生成势分别高达3.21 μg/(mg DOC)和1.86 μg/(mg DOC),占各自总单位生成势的41%和43%;其次是分子量<1 kDa的有机物,DCAN、DCAcAm的单位生成势分别为2.81 μg/(mg DOC)和1.36 μg/(mg DOC),约占各自总单位生成势的36%和31%;分子量为1~10 kDa的有机物两种N-DBPs的单位生成势分别为1.78 μg/(mg DOC)和1.11 μg/(mg DOC),占总生成势的23%和26%。分析原因为加氯后,部分已生成的DCAN水解为DCAcAm[13],即部分DCAN的前体物同时也是DCAcAm的前体物,两者具有相似的分子量分布特征。而充分氯化后,分子量<1 kDa的TCNM单位生成势最高,高达2 μg/L,约占TCNM总单位生成势的70%;分子量在1~10 kDa和>10 kDa的有机物TCNM单位生成势分别为0.56 μg/(mg DOC)和0.29 μg/(mg DOC),分别占TCNM总单位生成势的20%和10%。综上,3三种N-DBPs中分子量<1 kDa和>10 kDa的有机物单位DOC质量生成势分别为6.02、3.22 μg/(mg DOC)和2.29 μg/(mg DOC),远高于1~10 kDa的有机物,这两个区间的有机物生成N-DBPs的活性强,潜能大。 图3 不同分子量的N-DBPs前体物生成势分布Fig.3 Formation Potential Distributions of N-DBPs Precursors with Different Molecular Weights 在长江水源地中,一般以分子量<1 kDa和>10 kDa的有机物所占比例最大为主,且其单位生成潜能通常也为最大。因此,这两个区间有机物是N-DBPs的主要前体物。在常规处理工艺水厂中,大分子有机物的去除效果较理想,而小分子有机物的去除效果则较差。水厂在消毒前,应针对性地提高小分子有机物的去除效率,从而对出厂水中的N-DBPs进行更好的控制。 采用超滤膜法对长江水源地进行有机物亲疏水性分级,试验结果如下。 由图4可知:在DCAN、DCAcAm和TCNM试验中,原水中疏水中性和疏水碱性DOC组分占主导地位,浓度均为0.9 mg/L,占总DOC的26.5%;其次是亲水性组分,浓度为0.6 mg/L,占17.6%;过渡亲水性和疏水酸性的DOC含量差不多,约占14.7%。 图4 按亲疏水性分类的DOC质量分布Fig.4 Mass Distributions of DOC Classified by Hydrophility and Hydrophobicity 由图5可知:长江原水中的前体物以亲水性有机物生成DCAN、DCAcAm为主,生成势浓度依次为2.3、1.8 μg/L,疏水碱性有机物次之,生成势依次为2.3、1.2 μg/L;前体物以疏水中性有机物生成TCNM为主,生成势为1.2 μg/L,其次为亲水性有机物,生成势为1.1 μg/L。 图5 N-DBPs前体物的亲疏水性特性Fig.5 Hydrophilicity and Hydrophobicity of N-DBPs Precursors 由图6可知,充分氯化后,亲水性有机物生成DCAN、DCAcAm、TCNM的单位生成势最高,分别为3.83、3 μg/(mg DOC)和1.83 μg/(mg DOC)。因此,在长江水源地中,亲水性有机物的N-DBPs生成潜能最大,亲水性组分是N-DBPs的主要前体物。 图6 不同亲疏水性的N-DBPs前体物生成势分布Fig.6 Formation Potential Distributions of N-DBPs Precursors with Different Hydrophility and Hydrophobicity 在长江水源地中,N-DBPs前体物中亲水性有机物分布更为密集,且其单位生成潜能也最大,因此,该区间有机物是N-DBPs的主要前体物。水厂在消毒前应针对性地去除亲水性有机物,从而对出厂水中的N-DBPs进行更好的控制。 采用快速分析法对长江水源地进行有机物极性和带电性分级,试验结果如下。 由图7可知,原水极性组分占主导地位,在DCAN、DCAcAm和TCNM生成试验中,极性的DOC含量为2.4 mg/L,占70.6%,非极性组分浓度为1 mg/L,占总DOC的29.4%。 图7 按极性分类的DOC质量分布Fig.7 Mass Distributions of DOC Classified by Polarities 由图8、图9可知:充分氯化后,长江原水中前体物以非极性组分生成DCAN、DCAcAm为主,生成势分别为7.2 μg/L和4.2 μg/L,非极性有机物生成DCAN、DCAcAm的单位生成势为7.2 μg/(mg DOC)和4.2 μg/(mg DOC),高于极性有机物;而 TCNM中前体物虽以极性组分生成TCNM为主,含量为1.8 μg/L,但充分氯化后,非极性有机物的单位生成势仍高于极性有机物,含量为1.3 μg/(mg DOC)。因此,在长江水源地中,非极性有机物的生成潜能大,为N-DBPs的主要前体物,应优先考虑去除,从而使出厂水水质得以更好的控制。 图8 N-DBPs前体物的极性特性Fig.8 Polarity Properties of N-DBPs Precursors 图9 不同极性的N-DBPs前体物生成势分布Fig.9 Formation Potential Distributions of N-DBPs Precursors with Different Polarities 由图10可知,原水中非正电组分占主导地位,浓度为2.8 mg/L,占82.4%,带正电的DOC浓度为0.6 mg/L,占总DOC的17.6%。 由图11、图12 可知,长江原水前体物中带正电和非正电组分生成DCAN、DCAcAm的浓度相差不大,生成势分别为5、4.2 μg/L和3、2.1 μg/L,前体物中带正电的生成势略高于非正电的,而TCNM中,虽然前体物中非正电的组分生成势为2.2 μg/L,远高于带正电的,但充分氯化后,仍为带正电的前体物单位生成势较高。因此,在长江水源地中,带正电的有机物生成潜能大,应提高带正电的有机物的去除率,从而使出厂水水质得到更好的控制。 图10 按带电性分类的DOC质量分布Fig.10 Mass Distributions of DOC Classified by Electricity 图11 N-DBPs前体物的带电性特性Fig.11 Charge Characteristics of N-DBPs Precursors 图12 不同带电性的N-DBPs前体物生成势分布Fig.12 Formation Potential Distributions of N-DBPs Precursors with Different Charge Properties (1)长江原水中二氯乙腈(DCAN)的前体物浓度为9.2 μg/L,二氯乙酰胺(DCAcAm)的前体物浓度为5.1 μg/L,三氯硝基甲烷(TCNM)的前体物浓度为3.1 μg/L。 (2)长江水源中前体物主要以<1 kDa的小分子有机物和>10 kDa的大分子有机物、疏水中性或疏水碱性,以及极性的非正电组分占主导地位。 (3)氯化后,长江水源中生成DCAN、DCAcAm、TCNM的前体物中以<1 kDa的小分子有机物和>10 kDa的大分子有机物同时存在为主,生成DCAN、DCAcAm前体物主要以亲水性、带正电的非极性有机物潜能较高,生成TCNM前体物绝大部分是疏水中性、非正电的极性有机物潜能较高。由于前体物存在分子量减少而亲水性增强的特点[14],且水中大分子有机物去除效果较好,去除TCNM前体物可以考虑吸附、生物氧化的方法去除水中小分子的有机物,而去除DCAN、DCAcAm前体物则需重点关注非极性有机物,从而降低饮用水中消毒副产物的生成量。 (4)氯化后,N-DBPs的单位生成潜能以<1 kDa的小分子有机物和>10 kDa的大分子有机物,以及亲水性的非极性带正电有机物较高,单位生成潜能呈现同氯化DOC生成N-DBPs相似的趋势。研究其高效的去除方法,是目前去除消毒副产物领域研究的方向之一。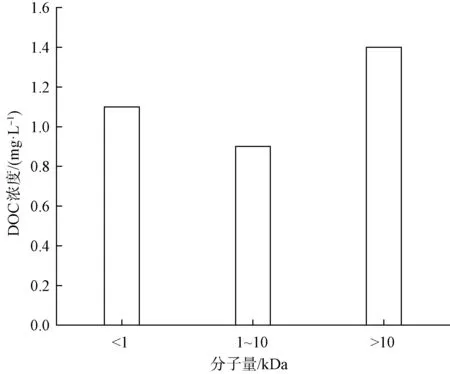


2.2 有机物DOC亲疏水性与生成势的关系分析
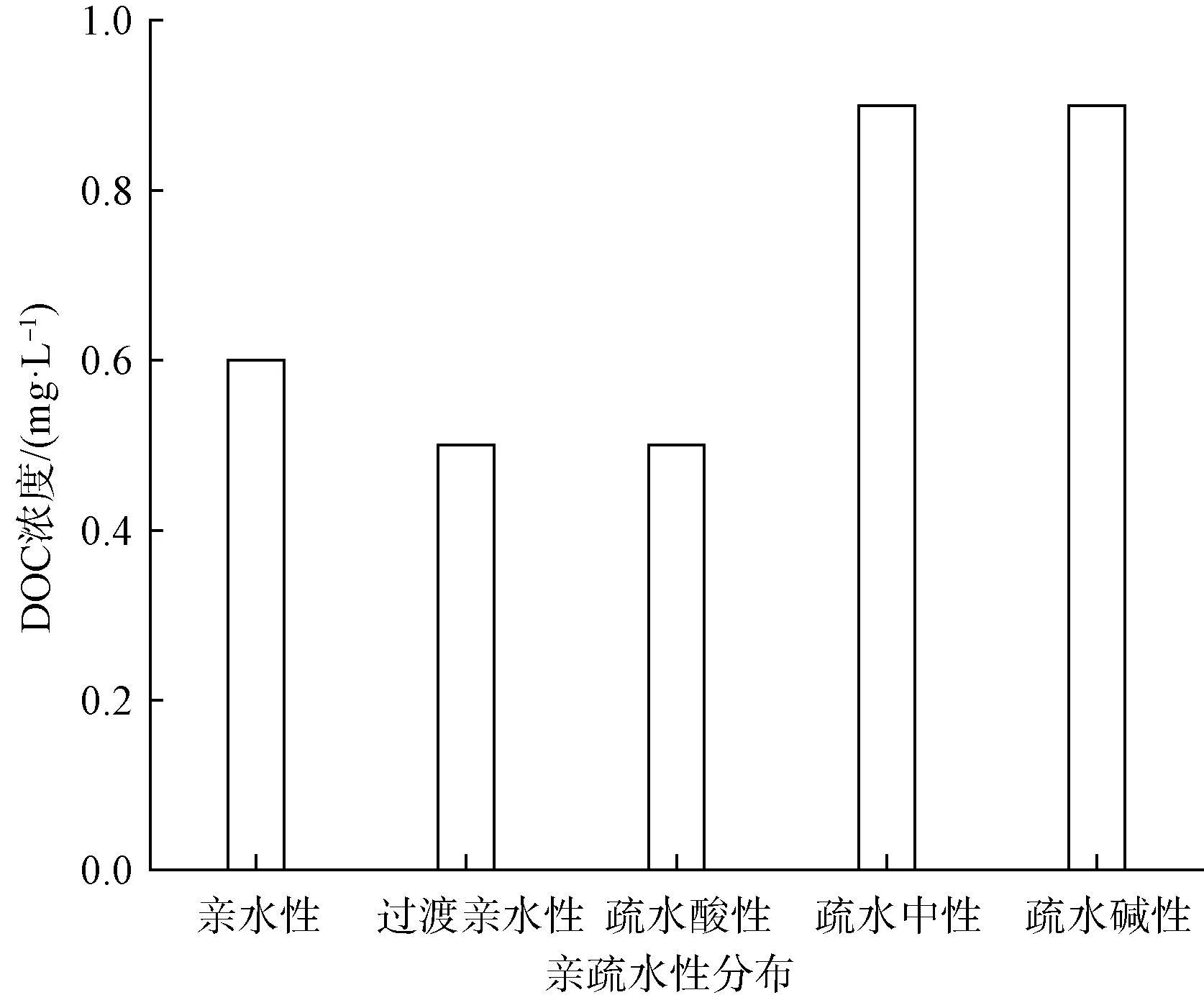


2.3 有机物DOC极性和带电性与生成势的关系分析






3 结论
