氧化石墨浆液逾渗转变过程的影响因素
2021-01-09朱皓楠刘丽艳
谭 蔚,朱皓楠,刘丽艳
氧化石墨浆液逾渗转变过程的影响因素
谭 蔚,朱皓楠,刘丽艳
(天津大学化工学院,天津 300350)
氧化石墨在去除所含金属离子杂质和添加金属离子改性的过程中遇到的浆液发生逾渗转变现象会导致固液分离过程终止,成为层状碳材料工业化生产及应用过程中亟待突破的瓶颈.为了调控氧化石墨浆液的状态,探究各因素对浆液逾渗转变阈值的影响,本文选择电导率变化率作为监控逾渗转变是否发生的指标,在对各因素进行初步筛选的基础上,采用正交试验法研究金属阳离子价态、溶液pH值和环境温度对氧化石墨浆液逾渗转变阈值的影响以及各因素间的交互作用.采用SEM、激光粒度仪、FT-IR等手段表征了氧化石墨浆液发生逾渗转变前后的形貌、尺寸及官能团种类数量等特征,进一步验证通过电导率变化率来描述结果的准确性.结果表明,金属阳离子价态、溶液pH值和环境温度对逾渗转变过程均有影响,其中金属阳离子价态是影响逾渗转变现象发生的首要因素,溶液pH值次之,而环境温度的影响最不显著.离子价态和溶液pH值之间存在交互作用,随着金属阳离子化合价的升高,氧化石墨逾渗转变过程受溶液pH值的影响逐渐减小.试验所得调控氧化石墨浆液最佳固液分离操作条件为三价金属阳离子(N3)、pH值1.41(P1)和35℃(T3).相关结果可为氧化石墨纯化和改性过程中涉及的浆液状态调控提供指导,利于后续的固液分离操作.
氧化石墨;逾渗转变阈值;金属阳离子;电导率;固液分离
氧化石墨浆液中常存在一些K+、Na+、Mn2+等金属离子,或为制备过程中引入的杂质离子或为功能修饰等目的而添加的离子[1-5].一定浓度的金属离子在氧化石墨浆液的固液分离过程中会导致浆液在悬浮状态和胶体状态之间转变,也称为逾渗转变.当氧化石墨浆液发生逾渗转变由悬浮状态转变为胶体状态之后无法进行固液分离操作.逾渗理论表明,无序体系中连通性的变化导致体系急剧相变、出现某种长程连通性,使体系的某些物理性质发生明显的变化[6]. Lux[7]通过观察多孔介质材料的电导率升高幅度来判断导电填料的体积分数是否达到逾渗转变阈值.通过测定炭黑在富填料相和连续相[8]中的浓度,确定了炭黑填充聚合物共混物的电导率变化进而确定体系的逾渗转变阈值.李华斌[9]研究了初始状态对单极记忆开关元件中逾渗导电通道形成的影响.橡胶硫化网络演变过程的逾渗阈值与诸多因素有关,包括橡胶种类或结构、硫化条件及硫化体系[9];通过调节溶剂用量、温度、聚苯胺含量等因素可以使共聚物聚苯胺溶液的逾渗转变阈值降低,使其在较低的添加量下达到较高的电导率[10].在各体系中,逾渗转变阈值的影响因素均较为复杂.
氧化石墨烯单体完成从分散体到组装体转变的过程中会受到氧化石墨烯的浓度、尺寸、溶剂、温度、pH值和金属离子等的影响[11],大量研究发现金属离子类型和价态、溶液体系的pH值和温度会影响氧化石墨水溶液的逾渗转变阈值.基于此,有研究表明采用富含电解质的纯化剂对氧化石墨进行纯化可以有效地抑制逾渗转变[5],不同价态离子的半径差别较大,对颗粒水化作用的抑制差别显著,影响逾渗转变阈值.溶液的pH值会影响氧化石墨溶液中金属离子存在形式和表面电荷,会导致氧化石墨表面的离子与其片层上的官能团间的络合方式发生变化,进而导致氧化石墨逾渗转变阈值变化.当溶液pH值为2时,可以将0.7mg/mL的石墨烯组装成单体,而当pH值调节到7或12[12]时,只能得到黑色的石墨烯分散体,而不是沉积物.另外,逾渗从根本上是一个热力学的现象,体系温度变化也会对逾渗转变阈值产生重要影 响[7].在粒子绝对密度不变的情况下,随着温度升高粒子的运动速度加快,长程连结性更容易产生.若能揭示这些因素对氧化石墨浆液体系发生逾渗转变过程的影响规律,将能控制体系的状态为实现固液分离奠定基础.本文以氧化石墨浆液的电导率变化率为指标,揭示金属阳离子价态、溶液pH值和体系温度对氧化石墨浆液逾渗转变阈值影响的规律,为氧化石墨的纯化及改性过程中浆液状态变化调控提供指导,便于进行后续固液分离操作.
1 材料与方法
本实验所用氧化石墨原料溶液源于山西煤化所,氧化石墨固相含量20g/L,实验中稀释10倍使用.采用元素分析仪分析氧化石墨原料的C、H、N、S、O元素的质量分数分别为65.00%、2.30%、0.72%、0.50%、31.50%.
1.1 逾渗转变阈值表征
根据逾渗理论及前期研究发现当氧化石墨浆液发生逾渗转变前后,浆液的电导率会发生突变.通过向氧化石墨浆液中加入金属离子,获得电导率随浓度变化的曲线,分析相邻浓度浆液电导率的变化率来确定浆液逾渗转变阈值,并采用TEM及宏观形貌判定浆液是否发生逾渗转变.
1.2 因素水平筛选及正交实验设计
影响氧化石墨浆液逾渗转变阈值的因素主要有金属阳离子价态(N)、溶液pH值(P)及环境温度(T)等,因素和水平范围如表1所示.然后选用表2所示正交表实验研究各因素对氧化石墨浆液逾渗转变阈值的影响,并探究金属阳离子价态、溶液pH值和环境温度三者之间可能存在的交互作用.设置误差列e1、e2、e3、e4,每组实验设置3次重复,取平均值.
表1 正交实验因素水平表
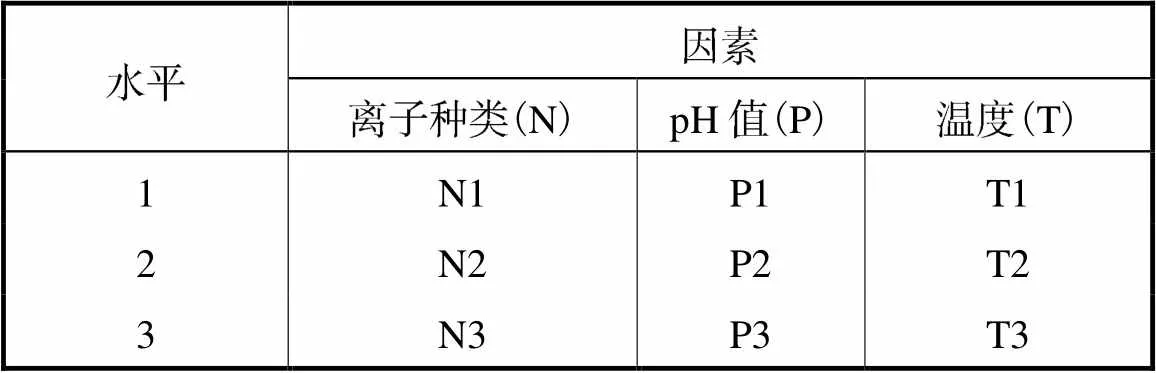
Tab.1 Orthogonal experimental factors
表2 正交表表头设计
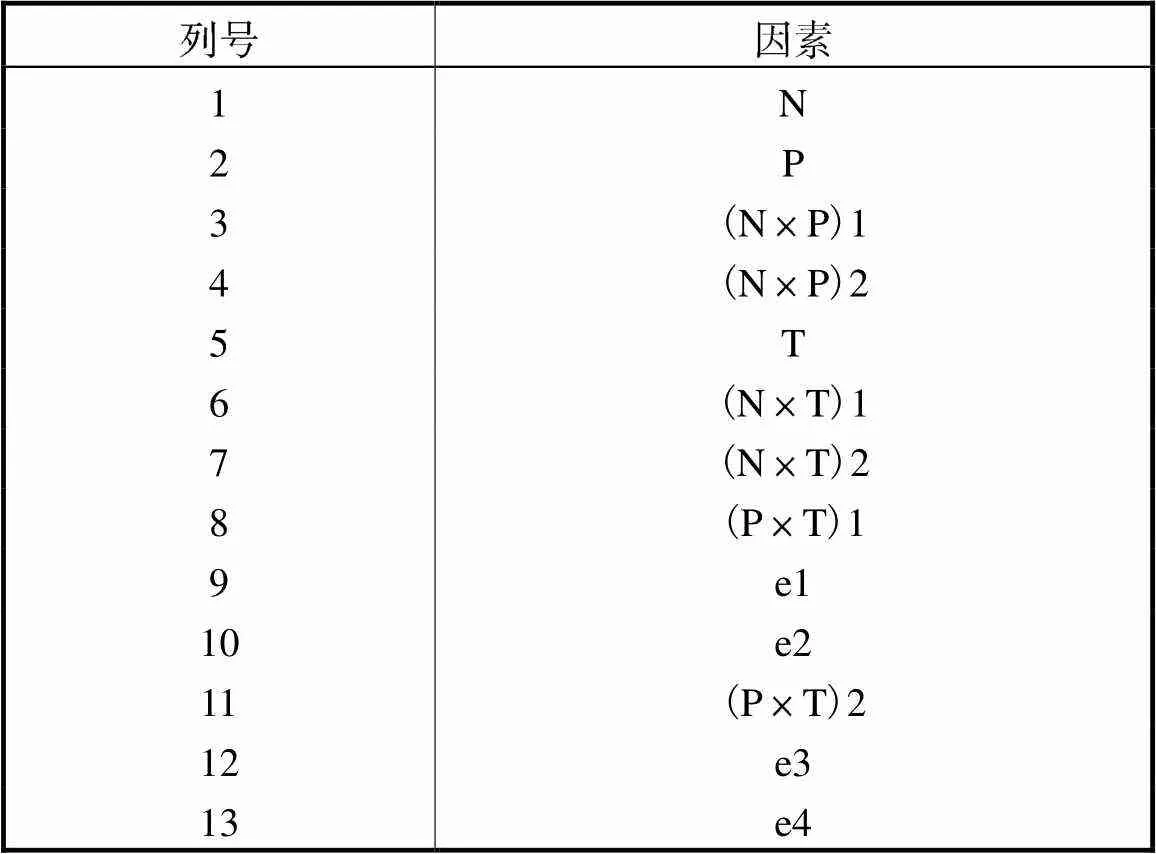
Tab.2 Orthogonal table header design
1.3 预测氧化石墨纯化过程中的逾渗转变阈值
通过正交实验确定最佳固液分离条件,预测含杂质原料可能发生逾渗转变现象的阈值,在该条件下对多种含杂质的氧化石墨浆液进行了纯化分离,测定电导率随过滤过程的变化曲线,使用ICP测定浆液中的金属杂质含量.将预测结果与实验结果对比,SEM、粒度、红外光谱等测试手段对氧化石墨状态及形貌进行表征.所用试剂及仪器见表3和表4.
表3 实验试剂
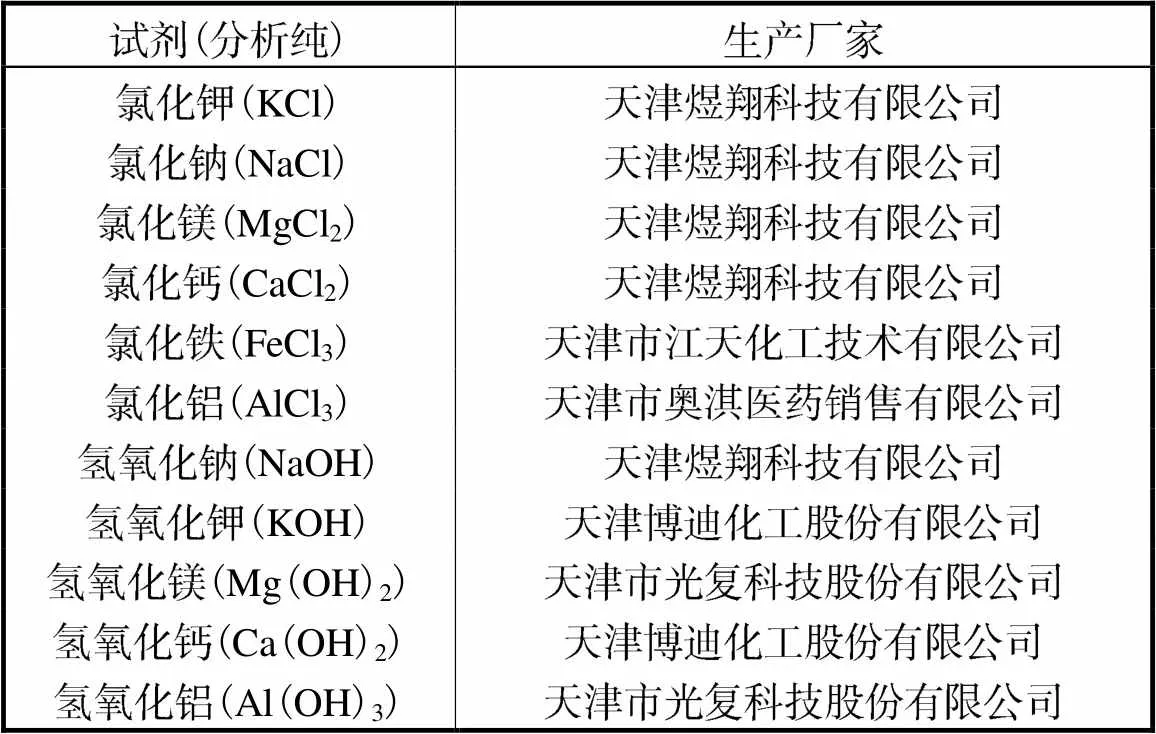
Tab.3 Experimental reagents
表4 实验所用仪器
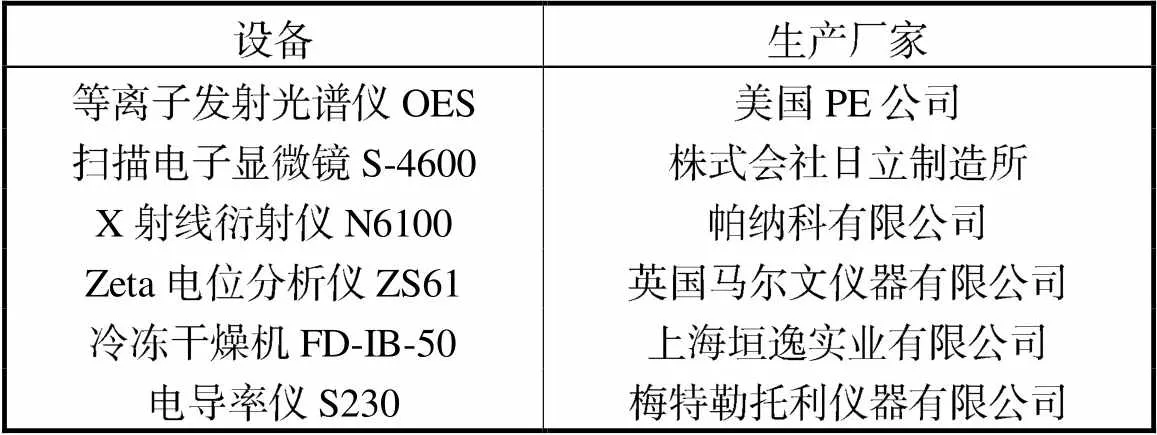
Tab.4 Instruments used in the experiment
2 结果与讨论
2.1 逾渗转变阈值表征
图1为氧化石墨溶液电导率与离子浓度的关系.根据式(1):
m=/(1)
式中:m代表摩尔电导率;代表溶液电导率;代表溶液的浓度.随着电解质浓度的增加,阳离子和阴离子浓度同步增加,电导率提高.若无逾渗转变现象发生,则氧化石墨浆液的电导率应沿图1中虚线变化呈现与浓度线性相关的规律[13-14].但是当钾离子浓度为8.322~8.591mmol/L区间时,氧化石墨浆液的电导率激增,该区域的电导率变化率明显高于其他区域.究其原因是形成了整体导电网络,而这也正是逾渗转变发生的标志.可以断定此时浆液中的离子浓度达到了逾渗转变阈值,选取突变的起始浓度值为逾渗转变阈值.通过对突变区域的浓度进行细分获得更窄的电导率突变浓度区域,如图1中小框图所示.通过多种表征手段对逾渗转变阈值前后的氧化石墨进行探究,验证电导率作为预测手段的准确性.
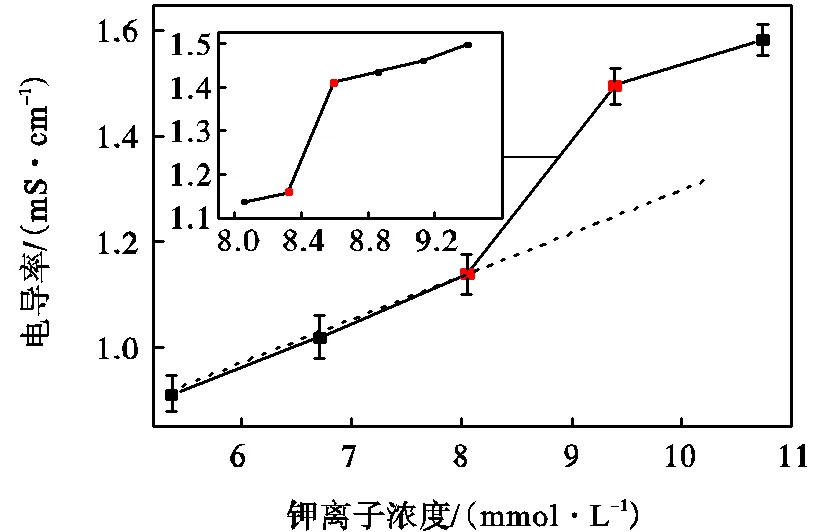
图1 电导率随离子浓度变化
通过分析该浓度范围的氧化石墨浆液TEM及宏观形貌(如图2所示),可以发现在该浓度范围的氧化石墨浆液由胶体状态转变为悬浮状态,内部的粒子相互接触成块,进而整体连结成为联通网络,结构方面的变化趋势与物性变化趋势相一致.

图2 逾渗前后氧化石墨TEM及宏观形貌
测定了氧化石墨粒度,为了表征逾渗阈值前后氧化石墨颗粒粒度分布的变化,在所测粒度范围0~70μm内,根据文献[15]将粒度较为均匀地划分为4个等级:粒径小于10.00μm为A级、10.00~22.91μm为B级、22.91~52.48μm为C级、大于52.48μm为D级.观察逾渗转变前后各区占比的变化情况,结果如图3所示.C、D区颗粒占比均在迅速增长,说明阈值前后,颗粒水化作用增强,扩散层的厚度减小,颗粒由于水化作用而发生黏着行为,打破之前的恒定状态并迅速增大,颗粒之间相互连结,逾渗转变现象发生.
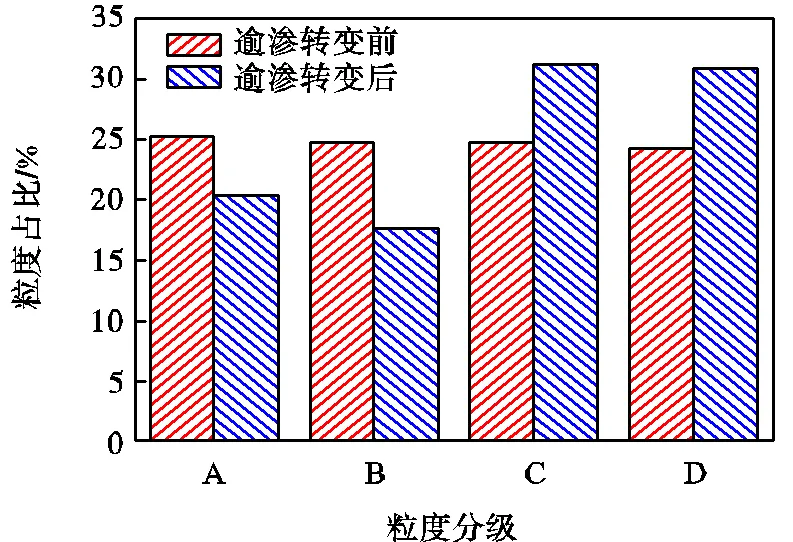
A:粒径<10.00μm;B:10.00μm≤粒径≤22.91μm;C:22.91μm<粒径≤52.48μm;D:粒径>52.48μm
观察发现逾渗转变阈值前后的氧化石墨浆液红外光谱如图4所示.由图可知,波数在1600cm-1和3400cm-1左右的两个峰值分别为羧基和羟基所代表的峰值,其位置相同,而波峰和波谷的差值即相对峰强降低,根据红外光谱半定量分析的原理即官能团种类相同而数量略有减少.氧化石墨片层表面的含氧官能团减少,与水分子的结合力减弱,氧化石墨的状态由胶体向悬浮液发生转变,即发生逾渗转变现象.
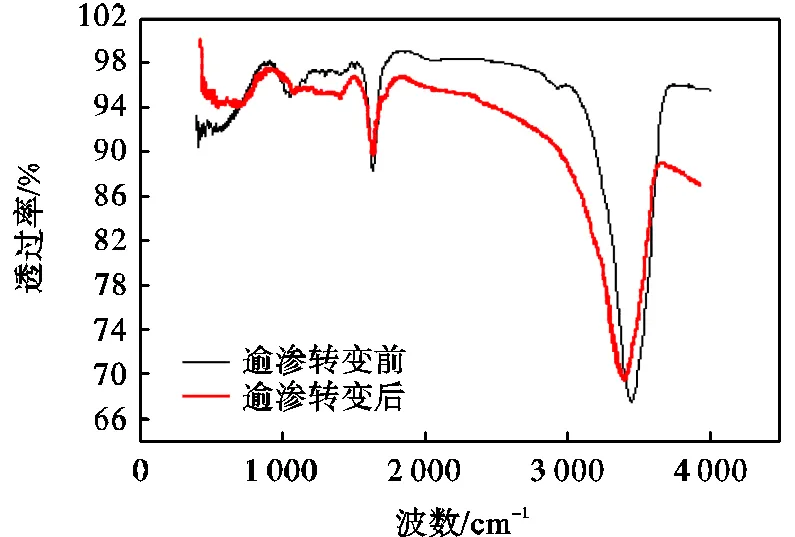
图4 氧化石墨红外光谱
图5为氧化石墨浆液的微观形貌图.逾渗转变前氧化石墨片层大且孔洞较多,容易剥离以包存液体,造成溶胀;随着外加离子的增多,逾渗转变现象发生,此时氧化石墨片层变得琐碎且堆叠交叉片层,孔洞变得平整.结合图6氧化石墨Zeta电位在逾渗阈值前后的变化可知,由于电解质的作用,影响了氧化石墨颗粒之间的相互作用,Zeta电位的绝对值降低,表面电位下降,影响扩散层的厚度,改变双电层结构,造成氧化石墨片层微观性质的差异[16-17].

图5 氧化石墨SEM图
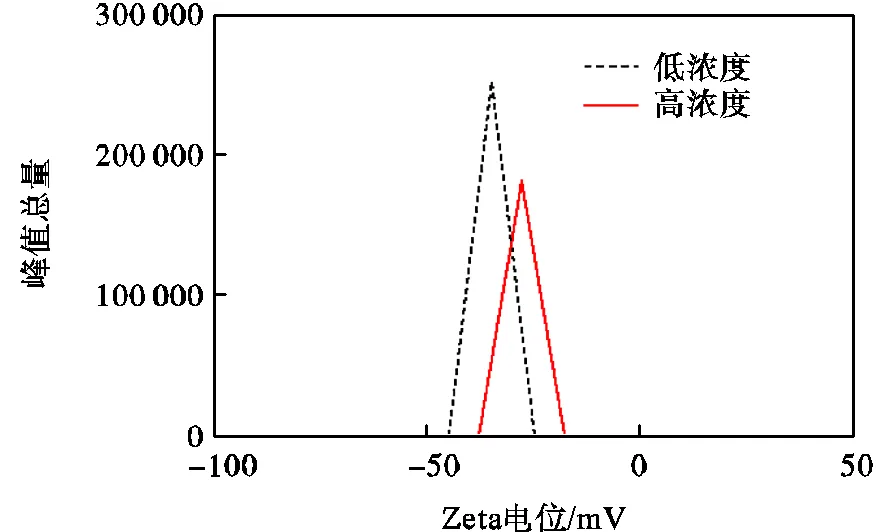
图6 氧化石墨Zeta电位图
综上,电导率作为预测指标,可以准确且显著地表征氧化石墨浆液的逾渗转变阈值,接下来的实验中皆以电导率变化率作为氧化石墨浆液体系是否发生逾渗转变的指标.所有试验数据重复3次.
2.2 因素水平筛选实验
2.2.1 离子种类及价态确定
为筛选适宜离子进行正交实验,测定了K+、Na+、Ca2+、Mg2+、Al3+和Fe3+对氧化石墨浆液电导率的影响,结果如图7~图9所示.
在相同离子浓度下,含Na+的氧化石墨浆液的电导率低于含K+的,这是由于Na+溶剂化作用较强,在水中迁移速度慢.但是二者的曲线趋势相近,且发生电导率突变所对应的浓度区间几乎重叠.外加二价的Ca2+、Mg2+以及三价的Al3+和Fe3+时也存在相同的现象,Ca2+的曲线在Mg2+下方,Al3+的曲线在Fe3+下方,且其发生突变的区间均重叠.这表明离子价态会显著影响氧化石墨浆液的逾渗转变,并且相同价态的影响类似,选取K+、Ca2+和Al3+作代表离子进行后续实验研究.
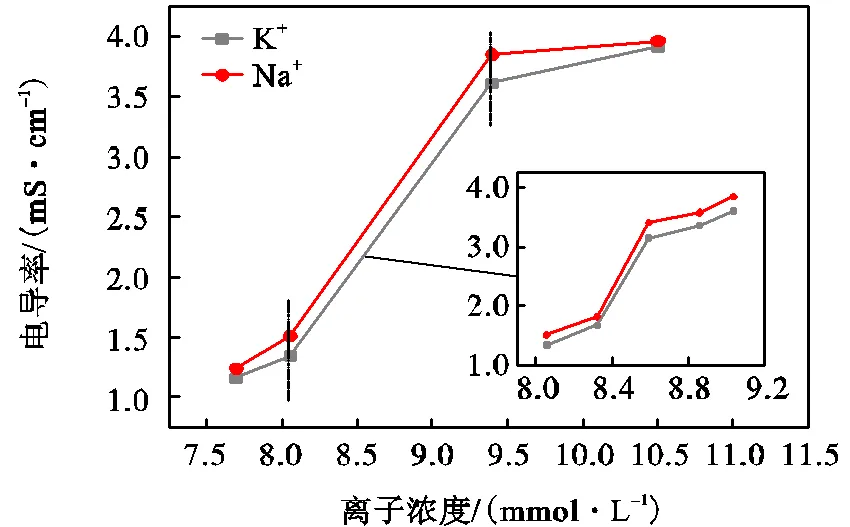
图7 氧化石墨浆液电导率随离子浓度变化(一价)
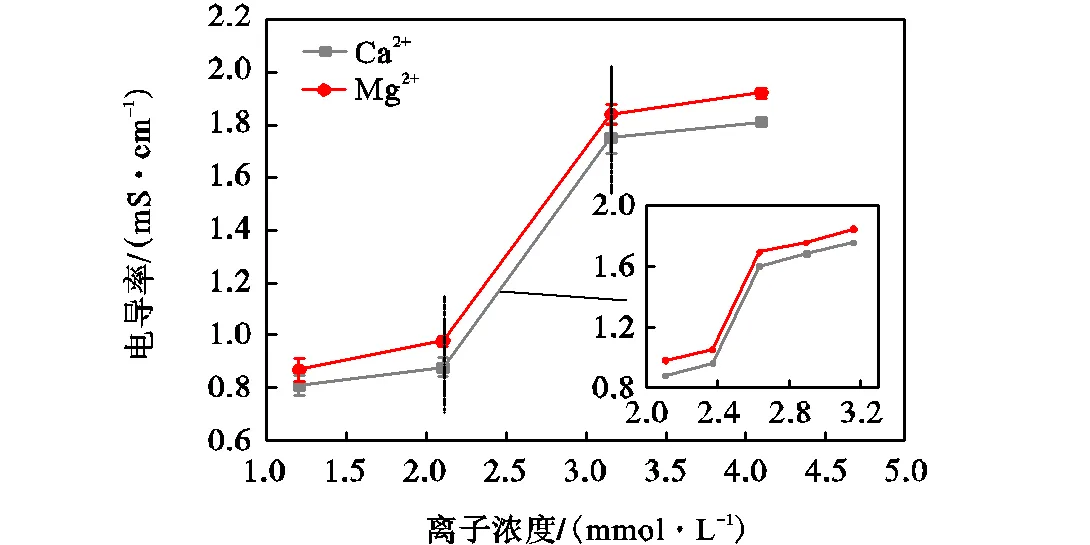
图8 氧化石墨浆液电导率随离子浓度变化(二价)
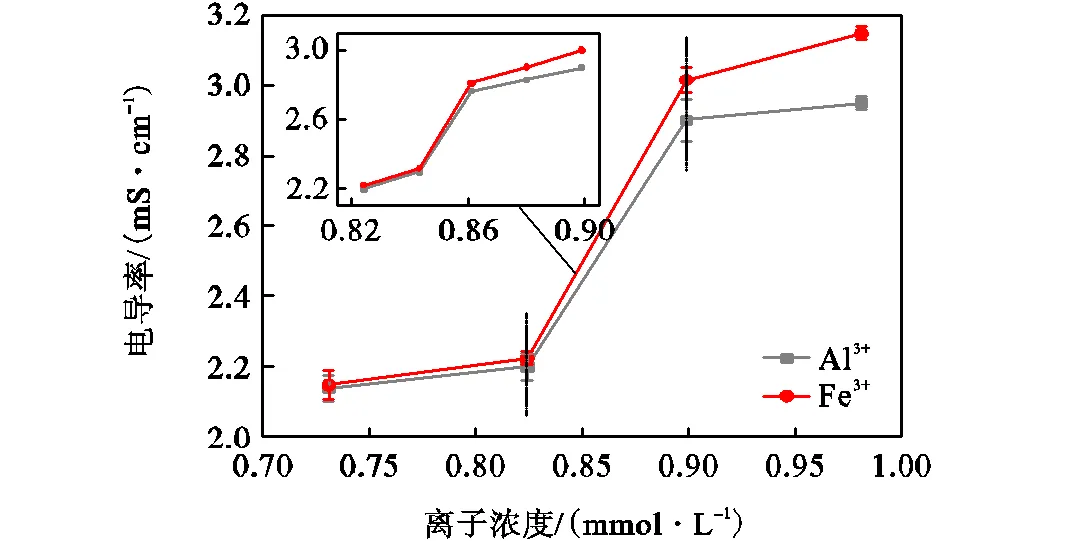
图9 氧化石墨浆液电导率随离子浓度变化(三价)
表5可见随着金属阳离子价态升高氧化石墨浆液的逾渗转变阈值逐渐下降.测定氧化石墨的XRD图谱,记录发生逾渗转变前后图谱的峰值所在位置,如表6所示.采用如下布拉格方程:
2sin=(2)
式中:代表晶面距离即层间距;为波峰角度的1/2,参数=1.计算氧化石墨层间距结果如表6所示,可见逾渗转变发生后,不但浆液中的氧化石墨颗粒之间出现长程连结,单个氧化石墨颗粒的层间距也发生了突变,水分子被锁住,无法进行固液分离,这与Liu等[18]的研究结果一致.
表5 氧化石墨浆液逾渗转变阈值
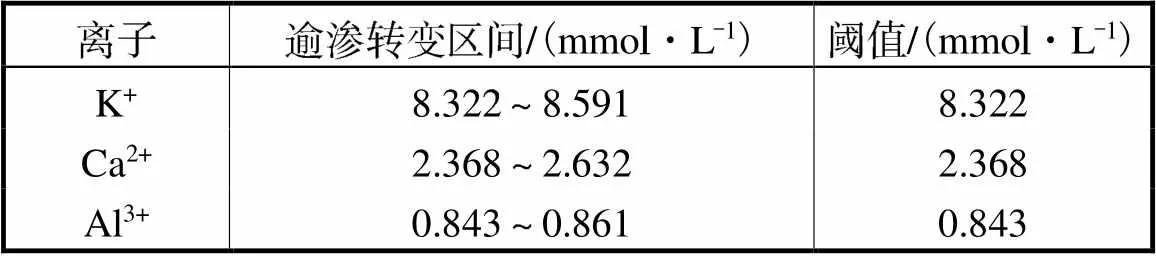
Tab.5 Percolation transition threshold of the GO slurry
表6 氧化石墨发生逾渗转变前后的层间距对比
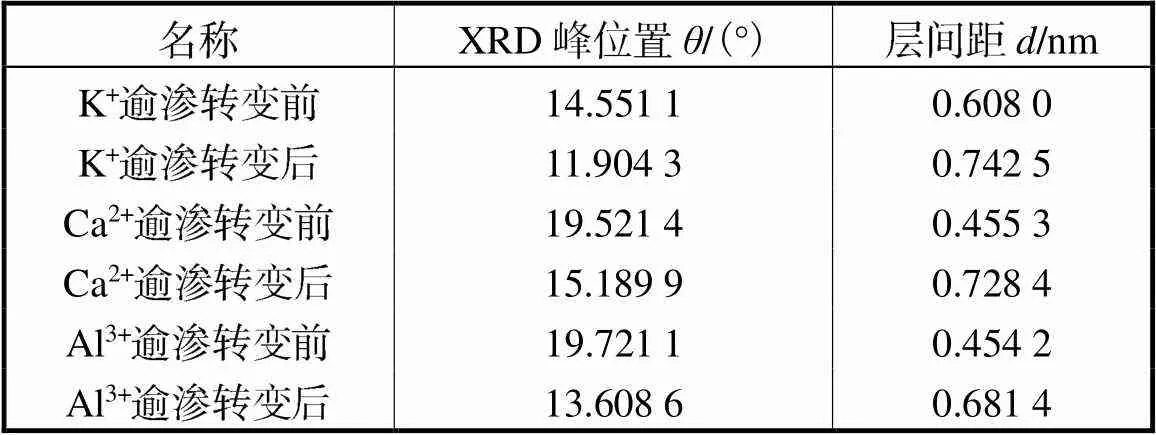
Tab.6 Comparison of the layer spacing of GO before and after percolation transformation
氧化石墨浆液的逾渗转变阈值随离子价态升高而降低,这是因为金属阳离子价态越高,相同浓度下所含正电荷数越多,更易形成联通网络.离子价态从一价到三价,其逾渗转变阈值从8.322mmol/L、2.368mmol/L 到0.843mmol/L不断降低.这是因为在氧化石墨层剥离临界斥力一定的条件下,高价态金属阳离子对颗粒之间的斥力和引力势能作用较明显,影响扩散层的厚度,从而改变双电层结构,对氧化石墨逾渗转变有较大作用.图10为添加不同价态金属阳离子后氧化石墨浆液的宏观形貌图.随着离子价态升高,其团聚的黑色弥散物变小,吸水量变少,说明高价态金属阳离子能更好地抑制氧化石墨颗粒溶胀,只需更少的金属离子即可使得浆液由胶体状态变为悬浮状态.从氧化石墨烯的传统胶体科学性质来看,这也与最近刊发的基于DLVO理论的氧化石墨烯胶体聚集和稳定性研究一致[19-21].

图10 含不同离子的氧化石墨浆液宏观形貌图(2g/L)
2.2.2 溶液pH值
氧化石墨水浆液本身呈酸性,稀释10倍后的pH值为2.92.本节选择了氧化石墨浆液原料中加入盐酸或氢氧化钾,加入去离子水稀释至10倍,调节稀释后的浆液pH值分别为1.01、1.41、2.92(原液)、4.92和9.96.浆液的电导率随钾离子浓度变化如图11所示.
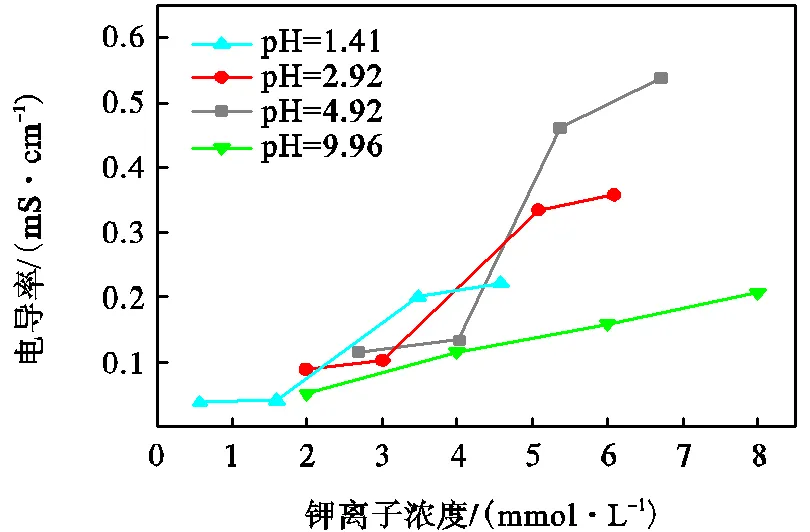
图11 不同浆液pH值条件下电导率随钾离子浓度变化
在钾离子浓度低于4.5mmol/L情况下,浆液的pH值越低,体系内H+浓度越高,导电能力更强,电导率就越高;同理当浆液的pH值越高,阳离子的碰撞几率变小,导电能力减弱,其电导率就越小.氧化石墨浆液逾渗转变阈值和阳离子总含量见表7.
表7 氧化石墨浆液逾渗转变阈值及阳离子浓度

Tab.7 Percolation transition threshold and cation content of the GO slurry
对比各组别的突变区间,当pH值为1.41、2.92和4.92时,逾渗转变阈值分别为2.55mmol/L、3.92mmol/L和4.75mmol/L,pH值显著影响体系内的阳离子存在状态,进而影响导电网络形成.大量的H+既影响氧化石墨颗粒自身的团聚,又强化了金属阳离子与氧化石墨间的相互作用,使得浆液在更低的金属阳离子浓度时就从胶体状态变为悬浮液状态.图12是氧化石墨浆液在不同pH 值条件下的形貌图,可见随着pH值降低,H+浓度和体系内的阳离子总量提高,宏观上表现的氧化石墨颗粒团簇变大,部分凝胶化,各叶脉之间接触,进一步交联形成网络,继而发生逾渗转变.

图12 氧化石墨浆液在不同pH值条件下的形貌图
当pH值达到9.96时,较高的OH-浓度,可影响阳离子的存在状态,导致层间斥力变化,氧化石墨颗粒易于团聚,颗粒内部的层间距不发生变化,浆液未发生逾渗转变.当pH值为1.01时,逾渗转变阈值达到了11.88mmol/L,与未处理的氧化石墨浆液差值过大,这说明由于外加OH-或H+可能会影响氧化石墨逾渗转变阈值.故在后续正交实验中选择外加适量酸、未处理和适量碱3个组别.
2.2.3 体系温度
稀释后的氧化石墨浆液在温度20℃、30℃、35℃、40℃和50℃条件下,其电导率随钾离子浓度变化的曲线,如图13所示.
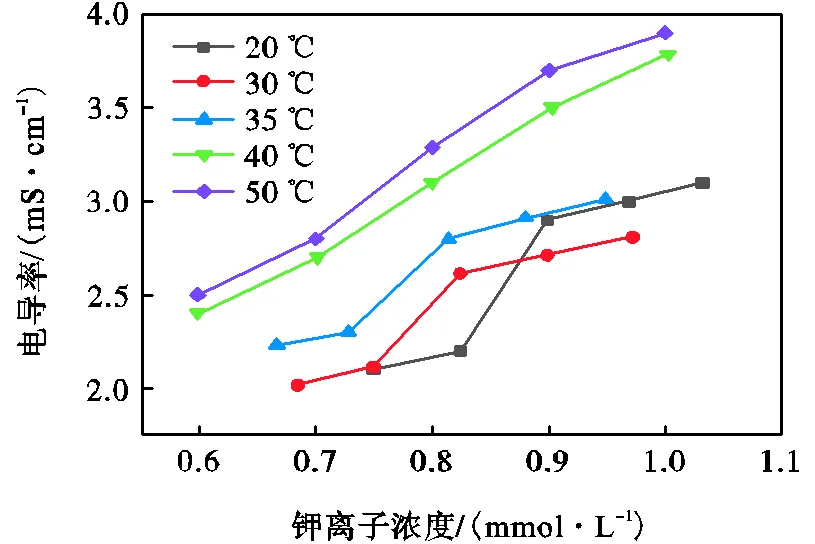
图13 不同温度下浆液电导率随钾离子浓度变化
由表8可见,当体系温度从20℃升至30℃时,氧化石墨浆液逾渗转变阈值明显减小,升高至35℃时,逾渗转变阈值基本不变.由图13可见,氧化石墨浆液电导率的绝对值随温度升高而上升.这是因为温度升高一方面使得浆液内粒子定向运动加快,粒子间碰撞更加频繁,其导电能力显著提升,逾渗转变阈值逐渐减小;另一方面,温度升高会使得颗粒间产生跳跃电导,导致氧化石墨浆液在较低的离子浓度区间发生逾渗转变.但是,当温度进一步升高,电导率随离子浓度变化趋缓,无法找到明显突变的区域,即逾渗转变阈值变得不明显或者逾渗转变没有发生.这可能是由于氧化石墨浆液在较高温度下,颗粒间及颗粒内部的交互作用过强;同时高温也会影响胶体的状态,导致其无法稳定存在.为了排除干扰,研究环境温度与其他因素的交互作用,只取20℃、30℃和35℃ 3个组别进行后续正交实验.
表8 不同温度下氧化石墨浆液逾渗转变阈值
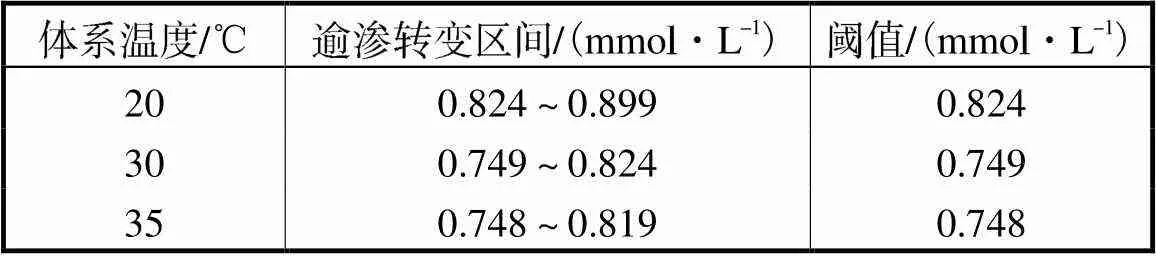
Tab.8 Percolation transition threshold of the GO slurry at different temperatures
2.3 正交实验
正交实验结果及各因素极差见下表9与表10所示.对于氧化石墨浆液逾渗转变阈值的影响大小依次为N>P>T,其中离子种类及价态对氧化石墨逾渗转变阈值的影响最为显著且远高于另外两因素.金属阳离子价态的不同代表其电子数的变化以及对颗粒水化作用抑制作用的区别,这对于氧化石墨浆液中形成导电网络的难易程度影响最大,直接导致逾渗转变阈值产生较大改变.选取最佳组成为N3P1T3,即当纯化剂价态最高、pH值1.41、温度35℃时,氧化石墨浆液的逾渗转变阈值最小,此时是保证能进行固液分离的最佳操作条件.
表9 正交实验方案及结果(略去空白列)
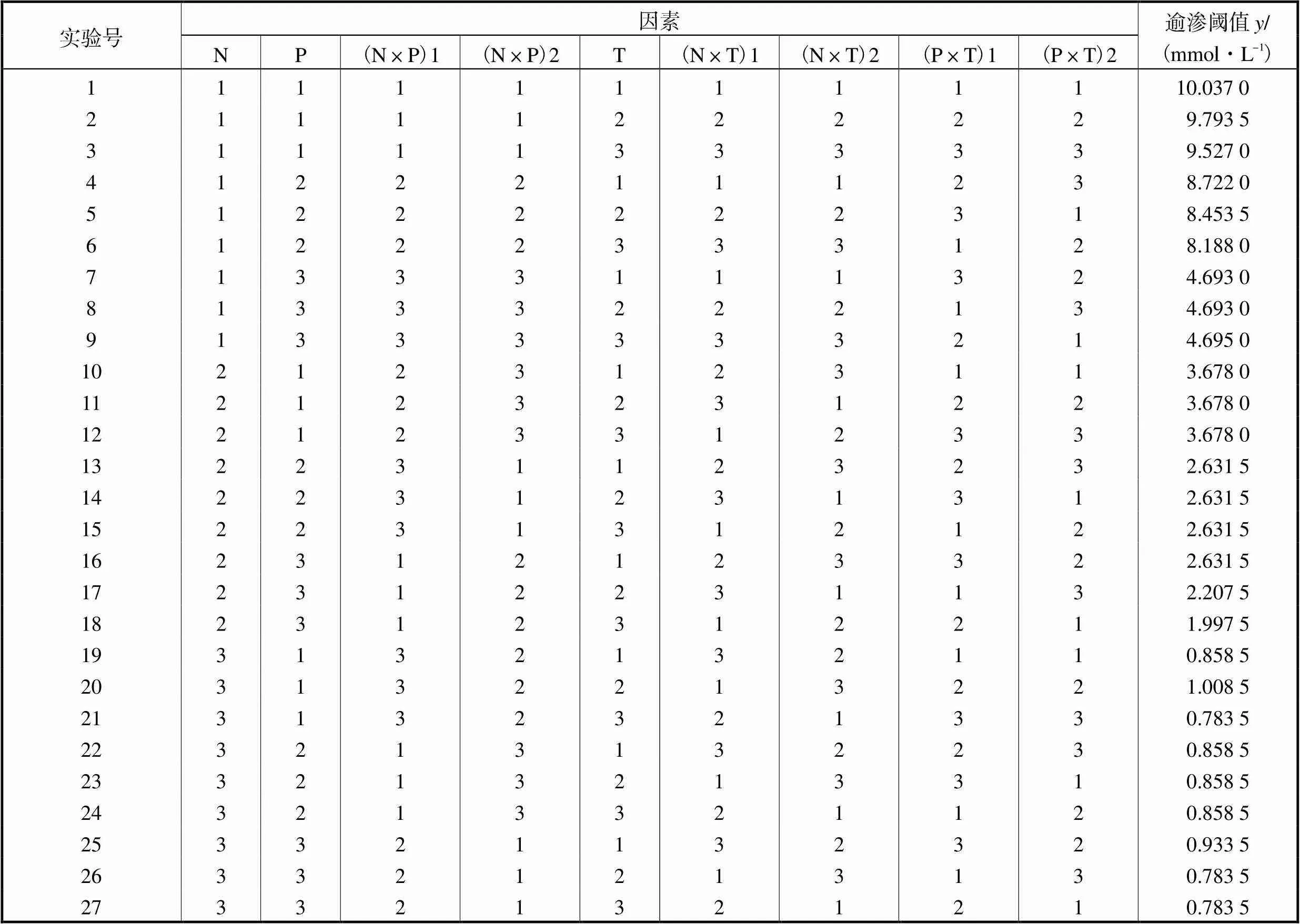
Tab.9 Orthogonal experimental scheme and results(blank columns omitted)
表10 氧化石墨逾渗转变阈值影响因素极差
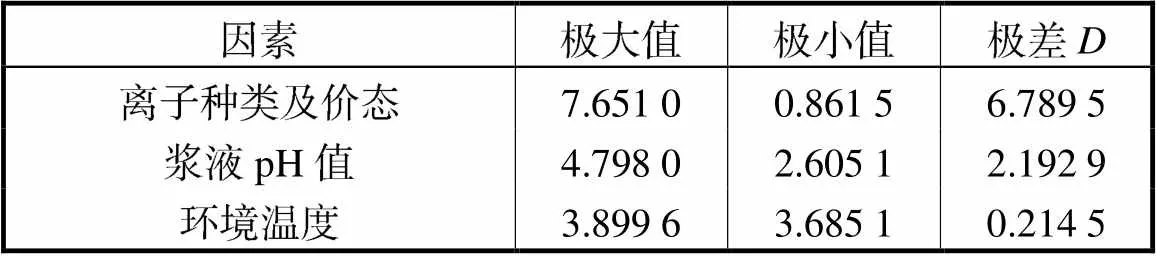
Tab.10 Range of the influencing factors of GO percolation transition threshold
表11分析各因素之间可能存在的交互作用, N×T、P×T列的值小于置信度=0.25所对应的临界值,故离子种类及价态与环境温度、浆液pH值与环境温度之间几乎不存在交互作用.而N×P列的值为290.1167,远大于临界值0.01,故其在置信度=0.01水平上显著.这表明离子种类及价态与浆液pH值的交互作用在95%的概率上显著.构建交互作用N×P的二元表以及二元图进一步分析.忽略环境温度的影响,摘取离子种类及价态与浆液pH值两个因素在各个水平所对应的逾渗阈值之和,如图14所示.图中的3条曲线并未平行,表明存在N×P交互作用,进一步印证显著性检验的结果.从图14中还可以发现,浆液pH值增大,逐步缓解了离子化合价升高而氧化石墨逾渗转变阈值降低的趋势,对一价金属阳离子影响的显著性高于对三价金属阳离子的影响.这是由于体系的pH值会影响浆液内氢键等作用力的大小,水可能与氧化石墨表面的含氧官能团通过氢键作用力形成大的分子团簇,外界分离作用力与氧化石墨颗粒之间的结合力达到动态平衡时发生逾渗转变,进而影响金属阳离子价态对逾渗转变的影响程度.同时孔隙溶液中OH-和H+浓度与抑制浆液内分子的扩散与膨胀有较好的相关性[12,22],故而对金属阳离子在浆液内形成联通网络造成影响,两者产生交互作用.
表11 正交实验方差分析
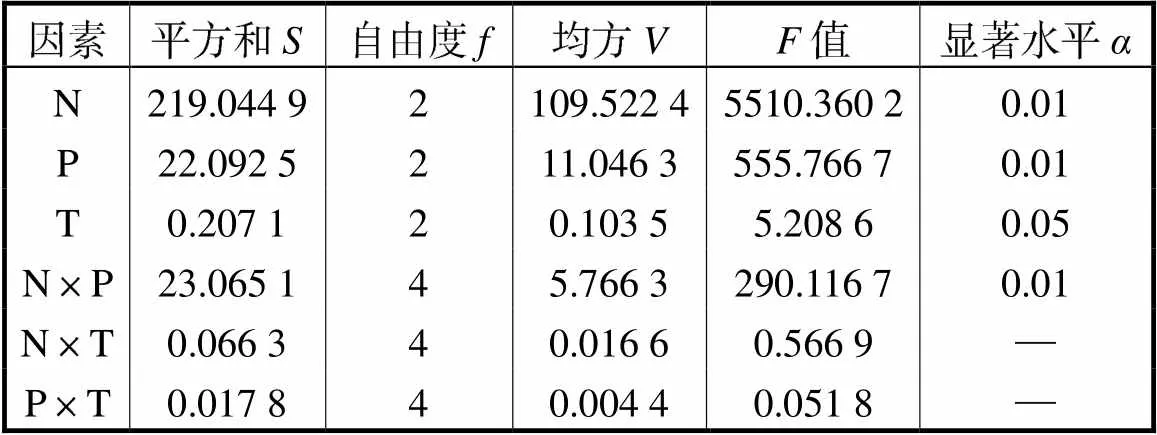
Tab.11 Analysis of variance of the orthogonal experiments
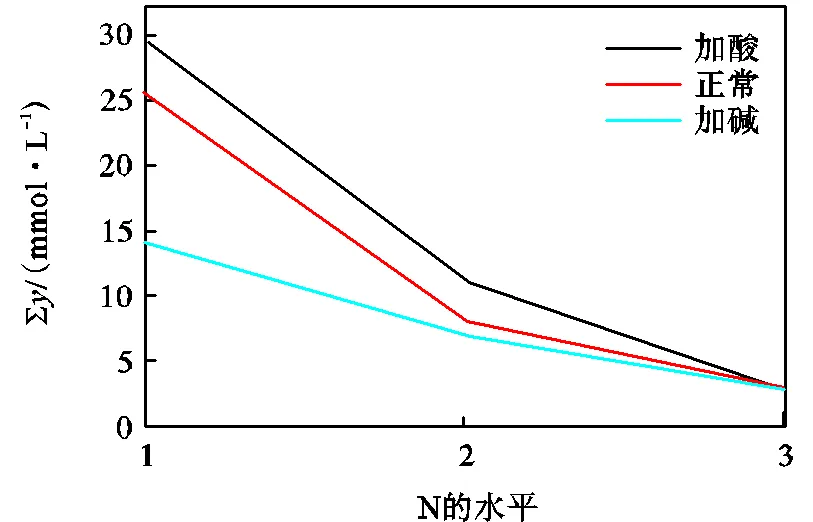
图14 交互作用N×P二元图
3 结 论
以浆液电导率变化率指示氧化石墨浆液逾渗转变过程,通过正交实验法研究了金属阳离子价态、环境温度和体系pH值对氧化石墨浆液逾渗转变阈值的影响以及因素之间的交互作用,并采用SEM、TEM、XRD、激光粒度仪、FT-IR等手段表征了氧化石墨浆液发生逾渗转变前后的形貌、结构、尺寸及官能团等信息,获得了如下结论.
(1)同价态金属阳离子所对应的氧化石墨逾渗转变阈值几乎相同;对氧化石墨逾渗转变阈值变化影响程度最大是金属阳离子的种类及价态,溶液pH值次之,环境温度影响程度最小.
(2)在一定范围内,随着金属阳离子价态的升高,氧化石墨浆液的逾渗转变阈值逐渐减小,随着溶液pH值减小,逾渗转变阈值减小,随着环境温度的升高,逾渗转变阈值缓慢减小;最佳过滤条件为三价金属阳离子,pH=1.41,温度35℃,与氧化石墨浆液纯化过程的逾渗转变阈值基本相同.
(3)金属阳离子价态与溶液pH值存在交互作用,当金属阳离子价态一定时,溶液pH值的减小使得氧化石墨逾渗转变阈值减小,对含一价金属阳离子的氧化石墨浆液的逾渗转变阈值影响最显著;随着金属阳离子化合价的升高,氧化石墨逾渗转变阈值受溶液pH值的影响减小,对三价金属阳离子的影响可以忽略.
[1] 谭 平. 功能化氧化石墨烯的制备及其吸附性能研究[D]. 广州:华南理工大学,2015.
Tan Ping. Preparation of Functionalized Graphene Oxide and Their Adsorption Properties Study[D]. Guangzhou:South China University of Technology,2015(in Chinese).
[2] 王 慧. 氧化石墨烯及其功能化改性材料富集水中重金属离子机理研究[D]. 长沙:湖南大学,2016.
Wang Hui. Application of Graphene Oxide and Its Functional Composites for Enrichment of Heavy Metal Ions from Aqueous Solution[D]. Changsha:Hunan University,2016(in Chinese).
[3] Klechikov A,Yu Junchun. Structure of graphene oxide membranes in solvents and solutions[J]. Nanoscale,2015,7(37):15374-15384.
[4] 韩军凯,冯奕钰,封 伟,等. 掺杂石墨烯制备方法新进展[J]. 天津大学学报:自然科学与工程技术版,2020,53(5):467-474.
Han Junkai,Feng Yiyu,Feng Wei,et al. Recent research progress in doped-graphene preparation[J]. Journal of Tianjin University:Science and Technology,2020,53(5):467-474(in Chinese).
[5] 魏晓兵,许鑫华,王丽红. 氧化石墨烯/分子印迹固相萃取材料的制备和表征[J]. 天津大学学报:自然科学与工程技术版,2017,50(10):1099-1104.
Wei Xiaobing,Xu Xinhua,Wang Lihong. Preparation and characterization of graphene oxide/molecularly imprinted solid phase extraction materials[J]. Journal of Tianjin University:Sceince and Technology,2017,50(10):1099-1104(in Chinese).
[6] 王俊峰. 逾渗模型的蒙特卡罗研究[D]. 合肥:中国科学技术大学,2013.
Wang Junfeng. Research on Percolation Models Based on Monte Carlo Simulation[D]. Hefei:University of Science and Technology of China,2013(in Chinese).
[7] Lux F. Models proposed to explain the electrical conductivity of mixtures made of conductive and insulating materials[J]. Journal of Materials Science,1993,28(2):285-301.
[8] 耿 浩,李金华,刘宣勇. 石墨烯在表面工程领域的研究进展[J]. 中国表面工程,2015,28(1):4-14.
Gen Hao,Li Jinhua,Liu Xuanyong. Research progress on graphene in surface engineering[J]. China Surface Engineering,2015,28(1):4-14(in Chinese).
[9] 李华斌. 橡胶硫化交联网络演变过程中的逾渗现象及其临界行为[D]. 青岛:青岛科技大学,2010.
Li Huabin. Percolation Phenomenon and Critical Behavior of the Crosslink Networks Evolution Process of Rubber Vulcanization[D]. Qingdao:Qingdao University of Science and Technology,2010(in Chinese).
[10] 贺热民,刘维锦. 溶液共混制备ABS/PANI导电复合材料的研究[J]. 工程塑料应用,2005,33(11):15-17.
He Remin,Liu Weijin. Study on preparation of ABS/PANI conducting composite by solution blending [J]. Engineering Plastics Application,2005,33(11):15-17(in Chinese).
[11] Lü W,Zhang C,Li Z,et al,Self-assembled 3D graphene monolith from solution[J]. J Phys Chem Lett,2015,6(4):658-668.
[12] Bai Y,Rakhi R B,Chen W,et al. Effect of pH-induced chemical modification of hydrothermally reduced graphene oxide on supercapacitor performance[J]. Journal of Power Sources,2013,233:313-319.
[13] Yun M H ,Yeon J W ,Hwang J ,et al. A calibration technique for an Ag/AgCl reference electrode utilizing the relationship between the electrical conductivity and the KCl concentration of the internal electrolyte[J]. Journal of Applied Electrochemistry,2009,39(12):2587-2592.
[14] Petrova T I,Kashinskii V I,Verkhovskii A E,et al. Investigation of the effect the concentration of phosphates in boiler water has on electrical conductivity and pH[J]. Thermal Engineering,2007,54(7):515-518.
[15] Yang Yonghui,Sun Hongjuan,Peng Tongjiang,et al. Synthesis and structural characterization of graphene-based membranes[J]. Acta Physico-Chimica Sinica,2011,27(3):736-742.
[16] Yoon K Y,An S J,Chen Yunshen,et al. Graphene oxide nanoplatelet dispersions in concentrated NaCl and stabilization of oil/water emulsions[J]. Journal of Colloid & Interface Science,2013,403(4):1-6.
[17] Mashayekhi H ,Ghosh S ,Du P ,et al. Effect of natural organic matter on aggregation behavior of C60 fullerene in water[J]. Journal of Colloid & Interface Science,2012,374(1):111-117.
[18] Liu L,Zhang R,Liu Y,et al. Effects of solvent molecules on the interlayer spacing of graphene oxide[J]. Transactions of Tianjin University,2018,24(6):1-8.
[19] Tang H,Zhao Y,Yang X,et al. New insight into the aggregation of graphene oxide using molecular dynamics simulations and extended Derjaguin-Landau-Verwey-Overbeek theory[J]. Environ Sci Technol,2017,51(17):9674-9682.
[20] Ye N,Wang Z,Wang S,et al. Aqueous aggregation and stability of graphene nanoplatelets,graphene oxide,and reduced graphene oxide in simulated natural environmental conditions:Complex roles of surface and solution chemistry[J]. Environ Sci Pollut R,2018,25(11):10956-10965.
[21] Wang M,Niu Y,Zhou J,et al. The dispersion and aggregation of graphene oxide in aqueous media[J]. Nanoscale,2016,8(30):14587-14592.
[22] Nixon P J,Page C L,Bollinghaus R,et al. The effect of a Pfa with a high total alkali content on pore solution composition and alkali silica reaction[J]. Magazine of Concrete Research,1986,38(134):30-35.
Factors Influencing the Percolation Transition Process of Graphite Oxide Slurry
Tan Wei,Zhu Haonan,Liu Liyan
(School of Chemical Engineering and Technology,Tianjin University,Tianjin 300350,China)
The percolation transition process of graphite oxide(GO) slurry involving the removal of metal ion impurities and modification by adding metal ions disrupts the solid-liquid separation process. This has become an urgent problem in the industrialized production and application of layered carbon materials. To adjust the state of the GO slurry,the factors influencing the percolation transition process of the slurry were investigated. In this study,the conductivity change rate was selected as the indicator of percolation transition. On the basis of the preliminary screening of various factors,orthogonal experiments were conducted to analyze the influence of metal cation valence,solution pH,and ambient temperature on the percolation transition threshold of the GO slurry. Moreover,the interaction between factors was analyzed. Scanning electron microscopy,laser particle size analysis,Fourier transform infrared spectroscopy,and other methods were used to characterize the morphology,size,and functional groups of the GO slurry before and after percolation transition and verify the accuracy of the results obtained using the conductivity change rate. The results showed that metal cation valence,solution pH,and ambient temperature affect the percolation transition threshold. Among them,metal cation valence was the most important factor influencing the percolation transition process,followed by solution pH. The effect of ambient temperature was the least significant. Meanwhile,the interaction between metal cation valence and solution pH was observed. With the increase in metal cation valence,the effect of solution pH on the percolation transition of GO gradually decreased. The optimal solid-liquid separation operating conditions for the controlled GO slurry obtained in the test were trivalent metal cations (N3),pH value 1.41 (P1),and 35℃(T3). The relevant results can provide guidance on how to control the state of the GO slurry during the purification and modification processes,which will improve the solid-liquid separation operations.
graphite oxide;percolation transition threshold;metal cation;electrical conductivity;solid-liquid separation
TQ028.5
A
0493-2137(2021)05-0533-09
10.11784/tdxbz202002039
2020-02-22;
2020-03-16.
谭 蔚(1965— ),女,博士,教授,wtan@tju.edu.cn.
刘丽艳,liuliyan@tju.edu.cn.
国家自然科学基金资助项目(21576188).
Supported by the National Natural Science Foundation of China(No. 21576188).
(责任编辑:田 军)
