论建模思想下的高中化学解题技巧
2021-01-04王燕
王 燕
(福建省莆田华侨中学 351115)
化学模型是对现实化学过程的抽象.解题教学中注重建模思想的应用讲解,使学生体会运用建模思想解题的具体过程,对深化学生理解,提高学生的解题水平与解题能力具有重要意义.
一、运用晶体模型思想解题
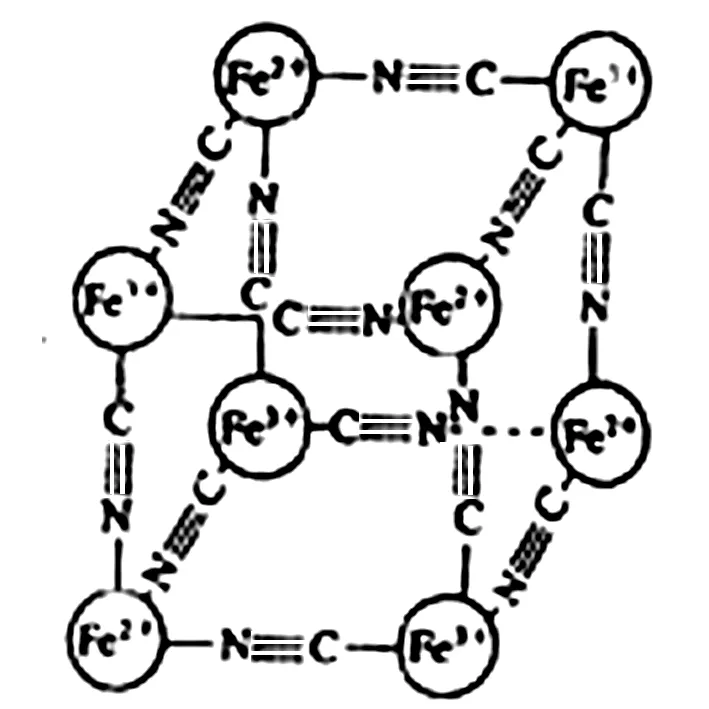
图1
例1分析化学常用X射线研究晶体结构,有一种蓝色晶体可表示为:[MxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,其晶体中的阴离子晶胞结构如图1所示,下列说法正确的是( ).
A.该晶体属于原子晶体
B.M的离子位于上述立方体的面心,呈+2价
C.M的离子位于上述立方体的体心,呈+1价
D.晶体的化学式为MFe2(CN)6,且M为+1价
解析A项该结构中存在阴、阳离子,因此,为离子晶体,错误.B项,由晶体结构模型可知,Fe2+、Fe3+分别占据立方体的顶点,其对应的个数为4×1/8=1/2,CN-位于立方体的棱上对应的个数为12×1/4=3,因此,M、Fe、CN-的个数比为x∶2∶6,则x+2+3=6,即,x=1,则该晶体的化学式为MFe2(CN)6,且M为+1价,错误.因为铁离子与亚铁离子的个数为4×1/8=1/2,相当于2个晶胞拥有1个M+,C项错误.经上述分析可知D项正确.答案为D.
解题技巧点拨回顾晶体模型,正确运用分摊法计算晶胞中含有的原子个数是解题的关键.
二、运用核外电子排布模型解题
例2科学研究表明:核外电子的能量不仅与电子所处的能层、能级有关,还与核外电子数目及核电荷数有关.氩原子与硫离子的核外电子排布相同(1s22s22p63s23p6).下列说法正确的是( ).
A.两粒子的1s能级上的电子能量相同
B.两粒子的3p能级上的电子离核的距离相同
C.两粒子的电子发生跃迁时,产生的光谱不同
D.两粒子都达8电子稳定结构,化学性质相同
解析由核外电子排布模型可知,A项,尽管具有相同的电子数,但核电荷数并不相同,因此电子能量并不相同.B项,在3p能级上,氩原子具有较大的核电荷数,对电子吸引力较大,因此,和原子核的距离较近,错误.C项,电子具有的能量不同,发生跃迁时产生的光谱不同,C项正确.D项,硫离子得到电子形成8电子稳定结构,但其失电子能力较强,两者的还原性并不同,D项错误.
解题技巧点拨准确把握核外电子排布模型中能量、数量规律是解题的关键,即,离核由近到远,电子能力由低到高.每层最多容纳2n2个电子,最外层不超过8个,第一层为最外层时不超过2个.
三、运用原电池模型思想解题
例3科学家发明了一种新型可控电池-锂水电池,工作原理如图2所示,以下说法错误的是( ).
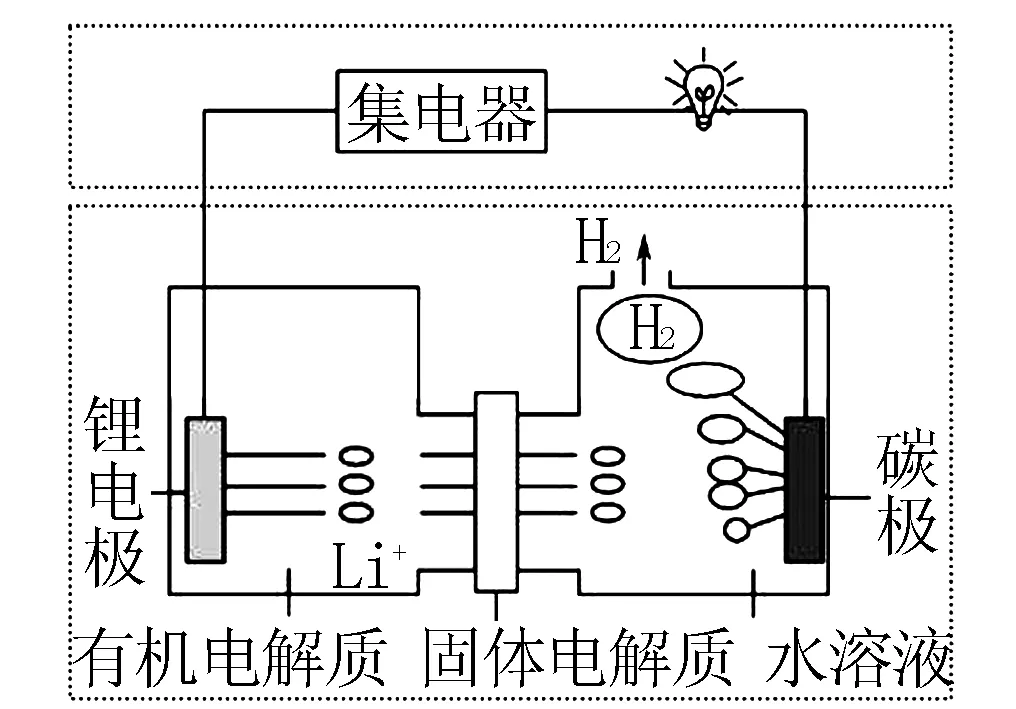
图2

B.有机电解质和水溶液不可以互换区域
C.标准状况下产生22.4L的氢气时正极消耗锂的质量为14g
D.该装置不仅可提供电能,还可得到清洁的氢气

解题技巧点拨原电池中发生的化学反应属于氧化还原反应,因此,认真观察图中内容,根据生成物,准确的判断正、负极,并根据电极反应方程式进行相关量的计算.
四、运用溶解平衡模型解题
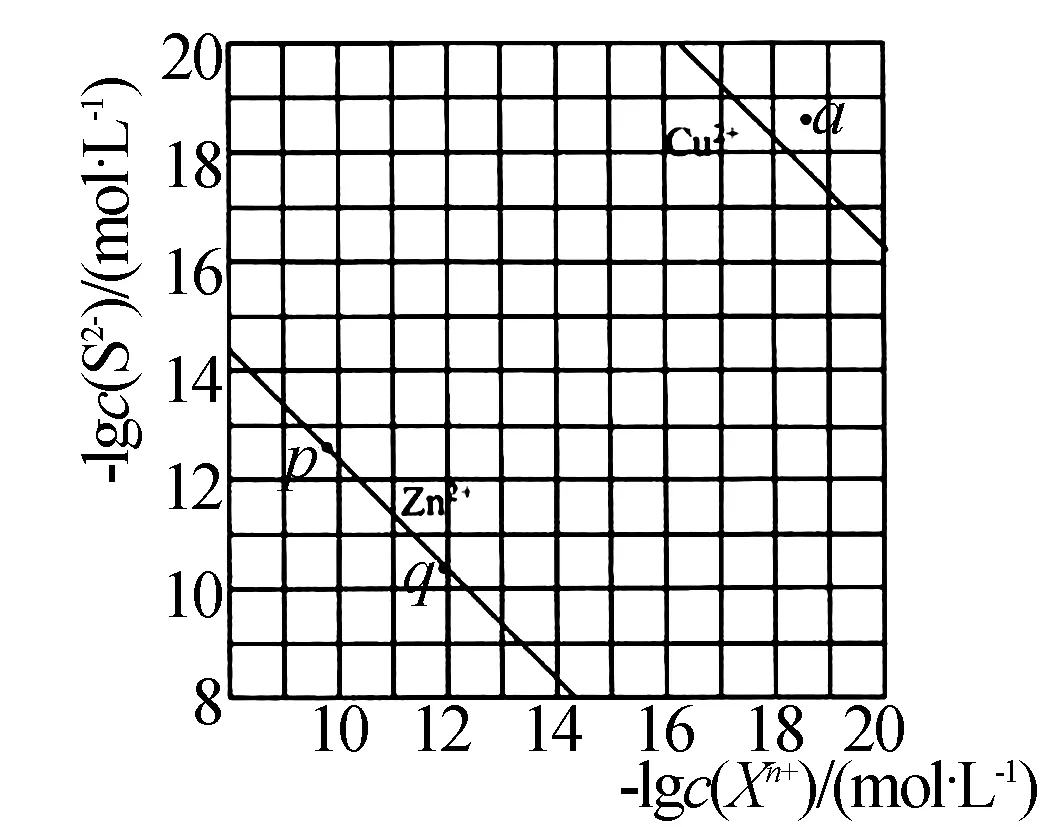
图3
例4 向废水中加入硫化物可依次获得CuS、ZnS纳米粒子.常温下,H2S的Ka1=1.3×10-7,Ka2=7.1×10-15,溶液中平衡时离子浓度关系如图3所示,以下说法错误的是( ).
A.Ksp(CuS)的数量级为10-37
B.a点对应的CuS溶液为不饱和溶液
C.向p点的溶液中加入少量NaS固体,溶液组成由p向q方向移动

解析根据溶解平衡模型以及图中内容可知,当c(Cu2+)=10-18mol/L时,c(S2-)=10-18.3,则Ksp(CuS)=c(Cu2+)×c(S2-)=10-36.3,数量级为10-37,A项正确.由A项可知,在a点的离子积浓度为10-37 解题技巧点拨认真审题,理解横轴与纵轴表示的含义.通过准确计算离子积浓度判断溶液是否达到饱和.根据溶解平衡常数计算结果判断化学反应进行的程度. 高中化学解题中运用建模思想可使学生少走弯路,提高解题效率,因此教学中应提高认识,做好高中化学常见模型知识的讲解与归纳,并为学生展示如何运用建模思想解答相关的化学习题,使其掌握运用建模思想解题的思路以及细节,提高其建模思想应用意识,指引其以后更好的解题.
