碎片化知识的整合与拓展
2020-12-31庄育兰
摘 要:文章对九年级教材中“铜及其化合物”的碎片化内容进行整合与拓展,在复习铜、氧化铜、硫酸铜和氢氧化铜的基础上,学习碱式碳酸铜。从宏观、微观、定性、定量、实验、模型等角度了解碱式碳酸铜,最后形成比较完整的“铜及其化合物”的价类关系图。
关键词:铜及其化合物;碱式碳酸铜;价类关系图;化学核心素养
中图分类号:G633.8 文献标识码:A 文章编号:2095-624X(2020)35-0087-02
一、内容分析
人教版九年级《化学》中有很多内容涉及铜及其化合物,但是零星散落在教材的各个角落。例如,绪言中提到“在翠绿色的孔雀石等铜矿石上面燃烧炭火,会有红色的铜生成”。第一单元课题1中引入化学变化和物理变化的区别时,进行的实验之一就是研磨硫酸铜晶体以及硫酸铜溶液和氢氧化钠反应。第二单元课题3中也提到“硫酸铜溶液等对过氧化氢的分解有催化作用”。第五单元课题1中验证质量守恒定律的实验之一就是铁和硫酸铜溶液的反应。第六单元课题1在讲述碳的化学性质时,进行了碳还原氧化铜的实验,并且详细阐述了该反应中失氧和得氧的变化。第八单元中讲到金属材料和金属的化学性质时,学生更加深入地了解到铜的金屬活动性顺序以及铜和氧气的反应、铁和硫酸铜的反应、铜和硝酸银的反应。第八单元中课后习题也介绍了“古代将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合后加热到800℃,得到一种外观似金子的锌和铜的合金”。
纵观《化学》上下册,铜及其化合物不仅是很好的教学素材,也是生活中很常见、很重要的物质,因此,笔者尝试将这些碎片化知识有机整合与适当拓展,期望能在丰富化学课堂的同时,提升学生的化学核心素养。
二、教学过程
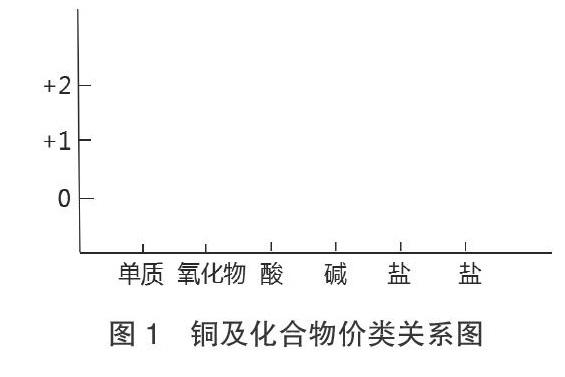
笔者用一系列图片引入铜元素,然后请学生将最常见的四种含铜物质——铜、氧化铜、硫酸铜、氢氧化铜的化学式填在价类关系图(如图1)的相应位置,并用箭头标出相互转化关系。完成价类关系图后,请学生按照所给试剂和实验仪器完成几个转化实验。
完成上述网络式的知识回顾后,接下来进行新物质——碱式碳酸铜的学习。首先展示碱式碳酸铜的资料卡片,请学生将碱式碳酸铜填写到价类关系图上,并标出转化关系。该教学设计的目的是让学生温故而知新,在复习前面含铜物质的性质的同时,展开新的含铜物质的学习。其次,笔者通过数字化实验探究碱式碳酸铜的分解产物,请学生通过观察实验和分析产物,书写化学方程式,并完善价类关系图。再次,根据生活常识引导学生思考碱式碳酸铜如何转化成硫酸铜,并且从微观角度进行解释。最后,对碱式碳酸铜定量分析,判断碱式碳酸铜的化学式,并且在解决该问题后,归纳化学式的测定方法,帮助学生建立宏微结合的解题模型。
三、教学思考
人教版初中化学每个单元的知识都承载着建立化学基本观念的功能,教师应充分挖掘知识背后隐藏的更有价值的观念。在中考复习时,教师更应超越具体的单元知识,以化学基本观念的视角统领复习内容[1]。
1.培养学生的变化观
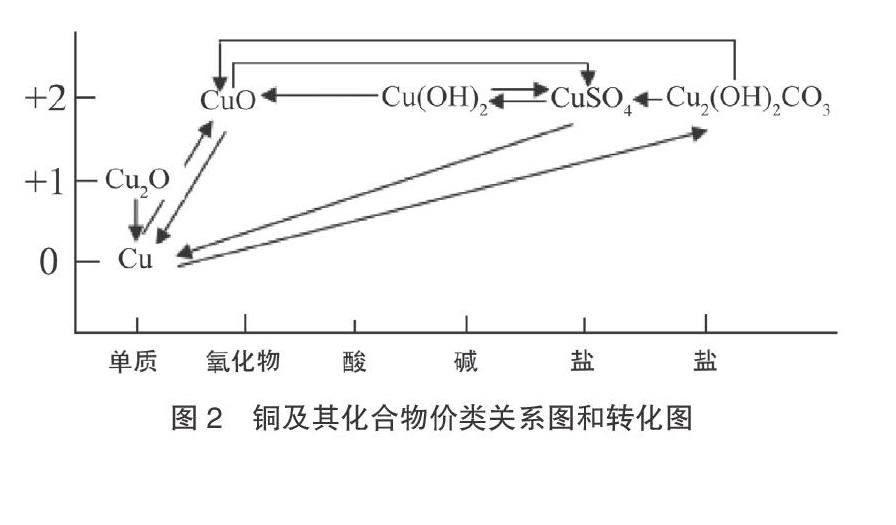
贯穿本节复习课的一条主线是铜及其化合物的价类关系图和转化图。从课前空白的价类关系图到一张比较完整的关系转化图(如图2),花费了整整一节课的时间,这应该是学生收获颇多的一节课。随着复习课内容的推进,学生一步一步完成转化图,一点一点回顾旧知,领悟新知,最后形成一张简单又丰富的铜及其化合物的关系转化图。在此过程中,既回顾了书本,复习了已有知识,又学习了几种新物质——Cu2(OH)2CO3和Cu2O。这比常态复习课中“默写化学方程式+习题讲解”的模式要更立体有趣。这样的复习形式学生听起来比较亲切,接受起来比较自然,而且便于学生更好地了解铜及其化合物之间的相互联系,因为世界上的物质都是相互关联的,不是简单的“1+1=2”,所以在日常教学中也要渗透这一点。
2.培养学生的微粒观
学生在新课学习中,已经能从离子角度认识中和反应等复分解反应。在笔者提问“如何将Cu2(OH)2CO3转化成CuSO4”时,笔者启发学生从微观角度思考Cu2(OH)2CO3的离子组成,在此基础上进行推导。在笔者的启发下,学生很快便理解上述转化的关键就是将OH-、CO32-和H+反应,生成CO2和H2O,所以应该使Cu2(OH)2CO3和酸反应,并且为了生成CuSO4,加入的酸必须是H2SO4。上述过程能更好地培养学生宏观辨识与微观辨析的学科素养。
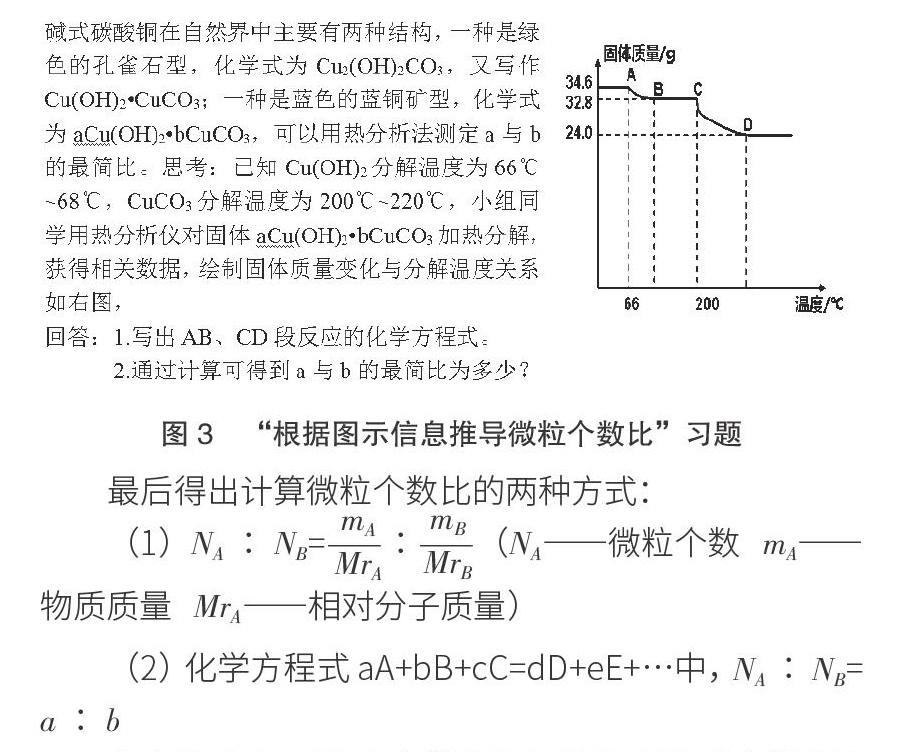
在进行碱式碳酸铜的化学式的定量分析时,笔者也注重宏微结合。借助于这样的习题(如图3),引导学生归纳计算微粒个数比的思路。
最后得出计算微粒个数比的两种方式:
(1)NA∶NB=—∶—(NA——微粒个数 mA——物质质量 MrA——相对分子质量)
(2)化学方程式 aA+bB+cC=dD+eE+…中,NA∶NB= a∶b
在介绍孔雀石型碱式碳酸铜和蓝铜矿型碱式碳酸铜的外观后,笔者也强调了它们的物理性质不同是因为它们的微观结构不同,也从微观本质解释了物质的结构决定物质的性质。
3.培养学生的实验观
初中阶段,硫酸铜、氢氧化铜和氧化铜是最具代表性的含铜化合物,为了突出这几种特征物质间的转化关系,使学生更好地了解它们的性质,笔者仅仅给学生提供了硫酸铜、稀硫酸和氢氧化钠三种物质,请学生自行设计实验并完成四个实验(如图4)。
在讨论实验方案时,产生了如下对话。
A学生:“Cu(OH)2既要生成CuSO4,又要生成CuO,怎么可能完成?”
B学生:“可以。先将生成的Cu(OH)2和H2SO4反应生成CuSO4,再将CuSO4和NaOH反应生成Cu(OH)2,
然后再加热Cu(OH)2生成CuO。”
C学生:“这样虽然可行,但是实验过程太复杂了,有没有简便些的实验过程?”
于是,教师建议:“第一次生成Cu(OH)2后,大家可以將试管中的蓝色絮状沉淀分一部分到另一个试管中,然后分别进行Cu(OH)2的两个实验。这样操作,就可以省去制取两次Cu(OH)2的麻烦,比较简单。”学生恍然大悟,纷纷感叹:“实验操作可以灵活些,在安全操作的前提下,可以进行一些简单创新。”
上述实验虽然仅仅是一组试管实验,但是学生在思考和操作的过程中,也感受到了与以往实验的不同,本实验也另辟蹊径地提高了学生的科学探究素养。
4.培养学生的发展观
近几年,随着科技的高速发展,化学实验中经常能看到数字化实验的身影,于是,笔者也当堂演示了数字化实验检验碱式碳酸铜分解产物。但是笔者也展示了传统实验,让学生通过观察两个实验,比较传统实验和数字化实验的优缺点。借此培养学生用辩证发展的眼光来看待如今的化学实验。
在介绍Cu2(OH)2CO3易和酸反应时,笔者也向学生提问:“家中铜制品表面的锈可以如何简单处理?”学生很快便回答:“和盐酸或稀硫酸反应。”笔者再追问:“家中有盐酸和稀硫酸吗?”学生答:“和白醋或醋精反应!”笔者希望化学的学习重在书本,但不局限于书本,化学必须走向生活,应用于生活中。
在复习书本上常见的铜及其化合物后,笔者重点介绍了碱式碳酸铜。碱式碳酸铜作为常见含铜化合物的拓展和延伸,能让学生用发展的眼光认识现在所学的物质。让学生知道学习书本上的物质是为了更好地认识没学过的物质。笔者也给学生介绍了碱式碳酸铜的两种结构,让学生了解随着学习的深入,以前的很多知识是有局限性的,所以需要不停地学习。
本节复习课的教学设计注重培养变化观、微粒观、实验观和发展观,但是碍于一节课的时长,有的内容并没有得到更深入的讨论,只能留作课后思考。九年级《化学》中像铜及其化合物这样的碎片化知识有很多,如碳及其化合物、钙的化合物等,若能对相关内容进行取舍,不求面面俱到,而是突出重点和适当扩展,相信能让复习课的课堂焕发出新的光彩。就像郑胤飞教授所说的:“我还是希望多给学生一点逻辑,多给学生一点化学味,多给学生一点文化,从而多给学生一点兴趣。”[2]
[参考文献]
[1]徐 丽.中考深度复习策略——基于化学基本观念有效架构“思维图谱”[J].中学化学教学参考,2017(5).
[2]郑胤飞.文化有根,课堂有魂[M].上海:上海教育出版社,2017:177.
作者简介:庄育兰(1981— ),女,江苏苏州人,中学一级教师,本科,化学教师,研究方向:化学教学。
